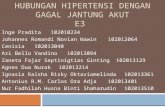
Skenario 5
-
Upload
ogie-silaen -
Category
Documents
-
view
98 -
download
1
Transcript of Skenario 5

Skenario
“Sering diare”
Tuan X, 35 tahun dibawa oleh istrinya ke Unit Gawat Darurat karena lemas dan hampir
pingsan. Setelah dianamnesis ternyata dari sehari sebelumnya Tuan X menderita diare dan
muntah-muntah. Menurut istrinya, bukan kali pertama kali ini suaminya menderita sakit seperti
ini. Istrinya yang saat ini sedang mengandung mengatakan, sejak di-PHK dari pekerjaannya
sebagai supir truk di Jakarta dan kembali ke kampung halamannya, sang suami menjadi sering
sakit-sakitan. Dalam 6 bulan terakhir di rasakan Tuan X makin kurus dan mudah terkena batuk
pilek.
Dari hasil pemeriksaan fisik antara lain didapatkan bercak putih di dalam mukosa mulut.
Dokter segera menyarankan Tuan X melakukan beberapa rangkaian pemeriksaan laboratorium.
1

Step 1
Step 2
1. Penyakit yang diderita Tuan X?
2. Etiologi dan patofisiologi dari penyakit Tuan X?
3. Pemeriksaan laboratorium?
4. DD?
5. Penatalaksanaan penyakit Tuan X?
6. Kapan dilakukan skrining untuk AIDS?
2

Step 3
1. AIDS
Factor resiko :
Berganti pasangan
Berhubungan tanpa menggunakan pengaman ,lebih sering pada orang homoseksual
Transfusidarah
Melakukan transfuse darah tanpa pengecekan terlebih dahulu, apakah darah yang
akan ditransfusi baik apa tidak
ASI
Pada ibu yang positif terkena AIDS
Narkotika
Pada narkotika biasanya dengan jarum suntik, menggunakan jarum suntik bergantian.
Fase :
Akut
Ditandai dengan demam, lemas
Kronis
Telah terjadi gejala opertunistik ,penurunan berat badan
Krisis
Berat badan menurun drastic, sering terkena infeksi
2. A. Etiologi
Karena virus HIV yang merupakan golongan retrovirus.
B. Patofisiologi
3

HIV menyerang CD4+ pada limfosit T dapat menurun kan imunitas
Fase HIV:
Fase terinfeksi
Fase akut
Gejala asimtomatik
Simtomatik
Lama infeksi bisa sampai lebih kurang 10 tahun, bila tidak diobati lebih kurang dari 2
tahun dapat mengakibatkan kematian.
HIV terdapat 2 tipe :
HIV tipe 1 HIV yang paling seringterjadi
HIV tipe 2 jarang terjadi, paling banyak terjadi di daerah afrika
Penularan HIV tipe 1:
Melalui mukosa
Jarum suntik/ transfusdarah
Jalur ibu anak
3. A. Pemeriksaan serologi :
a. Elisa
b. Western blot
B. pemeriksaan hematocrit lengkap
C. pemeriksaan penanda infeksi : LED
D. pemeriksaan CD4
4

4. Diare kronik
5. a. pemberian obat ARV
b. edukasi, konseling, medikamentosa
c. pengobatan terhadap infeksi
d. pengobatan suportif
e. perbaikan gizi
f. pengobatan simtom
g. pencangkokan sumsum tulang : harus cocok, agar mendapatkan limfosit T yang baru.
5

Step 4
1.
a. Infeksi HIV dimana virus bebas yang erinfeksi HIV masuk k eke tubuh
b. Gp120 menempelpada cd4 reseptor, virus menembus sel. Inti virus masuk
c. Envelop berfusidengan membrane sel plasma , membebaskan RNA virus
d. Terjadi reverse transcription
e. Integrasi dengan DNA kromosomsel host
f. Transkripsi, sel yang terinfeksiterpisah< DNA virus membaca dan mulai
pembentukan mRNA
g. Assembly, terjadi rangkaian ikatan protein virus
h. Partikel birus mulai budding
i. Virus yang immature bebas dan menginfeksi sel
6

j. Terjadi virus baru (matur)
Tidak hanya CD4 yang diserang, tetapi magrofag juga diserang oleh virus.Karena
pada magrofag terdapat reseptor agar gp 120 dan gp 41 dapat menempel. Pada awal
virus menyerang magrofag terlebih dahulu
Normal CXCR4
Sitokin IL-1 TH ikatanAGg-TCR dengankmpleks MHC kelas II
Magrofag
Interleukin 2 Magrofag (antigen)
CCR5
antigen
NK sel aktifasi
Humoral :
a. IL2b. BCGF ( B cell Growt Factor seltubuh)c. BCDF ( B cell differention factor)
Infeksimikroorganisme :
a. Bakterib. Jamurc. parasit
2. Setelah infeksi primer, terjadi replikasi virus dan viremia yang dapat dideteksi selama
sekitar 8-12 minggu. Virus tersebar secara luas di seluruh tubuh selama waktu ini,
termasuk organ limfoid. Respons imun terhadap HIV terjadi 1 minggu sampai 1 bulan
setelah infeksi, penurunan viremia plasma, dan kadar sel CD4Namun demikian,
respons imun tidak dapat mengatasi infeksi secara keseluruhan, dan sel yang
7

terinfeksi HIV menetap dalam kelenjar getah bening, Masa laten klinik dapat
berlangsung selama 10 tahun
Pada akhirnya, pasien akan menunjukkan gejala dan penyakit lainnya, seperti infeksi
oportunistik atau neoplasma. Saat tahap infeksi lanjut ini, virus dalam jumlah yang
banyak dapat dideteksi dalam plasma, dimana bila HIV ditemukan pada pasien
biasanya lebih virulen dan sitopatik dibandingkan bila virus ditemukan pada tahap
awal infeksi. Seringkali terjadi pergeseran dari monosit atau macrophage-tropic (M-
tropic) strain HIV-1 menjadi lymphocyte-tropic (T-tropic) mengiringi progresi
menjadi AIDS.
HIV memiliki beberapa mekanisme untuk menghindari dari respon imun
Diantaranya yang paling penting adalah :
kemampuan virus untuk bermutasi
mengubah antigenisitasnya
menghindar klirens antibodi
pembunuhan oleh sel T CD4
Infeksi persisten terjadi karena makrofag dan sel T CD4 memelihara virus sebagai
immune-privilage cell.
Fase infeksi :
AIDS adalah stadium akhir dalam suatu kelainan imunologikk dan klinis kontinum yang
dikenal sebagai”spektrum infeksi HIV”. Perjalanan penyakit dimulai saat terjadi
penularan pasien terinfeksi. Mungkin terdapat kofaktor lain dalam akuisisi yang perlu
diidentifikasi lebih lanjut. Setelah terinfeksi awal oleh HIV, pasien mungkin tetap
seronegatif selama beberapa bulan. Namun, pasien ini dapat menularkan selama periode
ini dan dapat memindahkan virus ke orang lain. Fase ini disebut window period(masa
jendela). Manifestasi klinis pada orang yang terinfeksi dapat timbul sedini 1 sampai 4
minggu setelah pejanan.
Infeksi akut terjadipada tahap serokonversi dari status antibodi negatif menjadi positif.
Sebagian orang mengalami sakit mirip penyakit virus dan mirip mononukleosis
8

infeksiosa yang berlangsung beberapa hari. Gejala mungkin berupa malaise, demam,
diare, limfadenopati, dan ruam makulopapular. Beberapa orang mengalami gejala yang
lebih akut, seperti meningitis dan pneuminitis. Selama periode ini, dapat terdeteksi HIV
dengan kadar darah perifer. Kadar limfosit CD4+ turun dan kembali ke kadar sedikit di
bawah kadar semula untuk pasien yang bersangkutan.
Dalam beberapa minggu fase infeksi akut pasien masuk ke fase asimtomatik. Pada awal
fase ini, kadar limfosit CD4+ umumnya sudah kembali mendekati normal. Namun, kadar
limfosit CD4+ umumnya menurun secara bertahap seiring dengan waktu. Selama fase
infeksi ini, naik virus maupunantibodi virus dapat ditemukan di dalam darah.
Pada fase simtomatik dari perjalanan penyakit hitung sel CD4+ pasien biasanya telah
turun dibawah 300 sel/ml. Dijumpai gejala-gejala yang menunjukan imunosupresi dan
gejala ini berlanjut sampai pasien menunjukkanpenyakit-penyakit terkait AIDS.
Fase transmisi:
9-11 jam
AB HIV –
HIV +
Fase infeksi:
AB HIV+
HIV +
Fase asimtomatik:
Pembesaran KGB
AB HIV +
HIV +
Fase AIDS
CD$ < 200
Tanda-tanda AIDS
9

MK : mayor ditandai penurunan berat badan.
Minor ditandai dengan ruam di kulit, mudah lelah, batuk, dan pembesaran limfa.
Fase akut : 3-11 minggu
Fase kronis : 7-10 tahun
Pada fase kronis sebagian sistem imun masih tersedia, menurun selama perjalanan
penyakit. Fase laten pada HIV.
Fase kritis : penurunan berat badan, limfosit T telah habis.
Reaksi auto antibodi tubuh menyerang sel normal, CD4 meningkat(700)
menyebabkan reaksi auto antibodi
Reaksi keganasan.
Gejala awal infeksi HIV (2-4 minggu setelah infeksi) akan menunjukkan gejala seperti
influenza atau mononukleosis infeksiosa dengan meningitis aseptik atau rash yang terjadi
3 bulan setelah infeksi. Gejala ini menghilang secara spontan setelah 2-3 minggu diikuti
dengan periode asimtomatik atau limfadenopati menyeluruh yang persisten yang dapat
terjadi selama bertahun-tahunSelama periode ini, virus bereplikasi dalam limfonodus.
Beberapa gejala penyakit dapat terjadi pada seluruh badan, Gejala khusus yang berkenaan
dengan infeksi HIV infeksi meliputi:
Sakittenggorakan
Infeksi candida di mulut
Kakuotot
Sakitkepala
Diare
Pembengkakan kelenjar limfe
10

Demam
Fatigue
Beberapa tipe rash, termasuk dermatitis seboroik
Infeksi jamur pada vagina
Klinikal manifestasi
CD4+ A B C
>500µL A1 B1 C1
200µL A2 B2 C2
<200µL A3 B3 C3
A3, B3, C1, C2, C3indikasi AIDS
A :asimtomatik, limfodenopati\
B :hrpes zoster
3. a.Elisamendeteksi AB HIV( adaatautidak)
b. westerm blot (-) tidakhiv , (+) HIV
untukmendeteksirantai protein pada DNA
c.rapid test didapatsetelah 20 menitdilakukantes
(+) diulangi, dilakukan 2x tes.
d.PCRDilakukanbilatessebelumnyatidakberhasil
Pemeriksaan infeksi HIV :
untuk mengetahui adanya infeksi .
11

untuk mengidentifikasi carir yang dapat menularkan infeksi kepada orang lain
(misalnya donor darah atau organ, wanita hamil, dan pasangan seksual) atau
untuk konfirmasi diagnosis AIDS.
Pemeriksaandeteksi HIV lainnya :
HIV juga dapat dideteksi dengan cara-cara seperti :
o pemeriksaan antigen
o amplifikasi gen-gen HIV (PCR)
Cara-cara ini terutama dipakai dalam riset.
12

Step 5
LO :
1. Diagnosis banding AIDS ?
2. Penatalaksanaan AIDS?
3. Kapan dilakukan skrining HIV?
13

Step 6
14

Step 7
1. Diagnosis banding AIDS ?
Agammaglobulinemia tipe Bruton X linked
Agammaglobulinemia X-linked (XLA), atau agammaglobulinemia Bruton, adalah
penyakit immunodeficiency kongenital disebabkan oleh mutasi pada gen yang berisi kode
tirosin kinase Bruton (BTK).
Penyakit ini pertama kali ditemukan oleh Bruton pada tahun 1952. BTK sangat
penting untuk pematangan sel pra-B dan diferensiasi menjadi sel B yang matang.Gen
cacat BTK telah dipetakan kelengan panjangkromosom Xpada pitaXq21.3 ke pita Xq22,
yang mencakup 37.5kb dengan 19 ekson membentuk 659 asam amino untuk
menyelesaikantirosin kinasesitosol BTK.
PATOFISIOLOGI
Dengan tidak adanya BTK, limfosit B tidak dapat berdiferensiasi atau matang.
Tanpa sel limfosit yang matang, antibody yang memproduksi sel plasma juga tidak ada.
Akibatnya, organ-organ retikuloendothelial dan organ-organ limfoid tempat dimana sel-
sel ini berproliferasi, berdiferensiasi dan disimpan kurang berkembang. Limpa, kelenjar
tonsil, kelenjar adenoid, plak Peyer di usus, dan kelenjar getah bening perifer dapat
mengecil atau tidak ada pada individu dengan Agammaglobulinemia X-linked (XLA).
Pengkodean protoonkogen untuk BTK telah dikloning dan telah ditentukan
genomnya, memungkinkan dapat melakukan suatu analisis mendalamtentang peranBTK
dan tanda-tanda molekul lain dari diferensiasi sel B.
Mutasi padamasing-masing 5domainBTK dapat menyebabkan penyakit, yang
paling umum adalah mutasi missense. Kebanyakan mutasi menyebabkan pemotongan
dari enzimBTK. Mutasi ini mempengaruhi residu dalam protein sitoplasmadan BTK
sangat bervariasi dan tersebar merata di seluruh molekul.Namun demikian, tingkat
keparahan penyakit tidak dapat diprediksi oleh mutasi spesifik. Sekitar sepertiga dari
mutasi titik mempengaruhi CGG, yang biasanya mengkode untuk residu arginin.
15

BTK diperlukan untuk proliferasi dan diferensiasi limfosit B. Pria dengan XLA
tidak mempunyai atau hampir tidak mempunyai limfosit B dan sel plasma. XLAadalah
penyakit kongenital yangdapat menyerang 1 dari 250.000 laki-laki. Perempuan
merupakan carrier yang tidak memiliki manifestasiklinis. Infeksi dimulai begituantobodi
imunoglobulin G(IgG) maternal telahdikatabolisme, biasanya sekitar usia 6 bulan.
DIAGNOSIS
Deteksi dan diagnosis dini sangat penting untuk mencegah morbiditas dan
mortalitas awal dari infeksi sistemik dan paru. Diagnosis dikonfirmasi oleh nilai
abnormal yang rendah atau tidak adanya limfosit B matang, serta ekspresi yang rendah
atau tidak adanya rantai μ berat pada permukaan limfosit. Sebaliknya,limfosit T kadarnya
meningkat. Penentu pokok XLA adalah tidak adanya asam BTK ribonukleat (RNA) atau
protein. Analisis molekuler spesifik dibuat oleh untai tunggal polimorfisme konfirmasi
(SSCP), analisis DNA langsung, denaturing elektroforesis gel gradien, atau reverse
transcriptase-polymerase chain reaction untuk mencari mutasi BTK. SSCP juga
digunakan untuk evaluasi prenatal, yang dapat dilakukan melalui pengambilan sampel
chorionic villus atau amniocentesis ketika seorang ibu diketahui sebagai carrier. IgG
tingkat kurang dari 100 mg / dL mendukung diagnosis.
Jarang sekali diagnosis dibuat pada orang dewasa di dekade kedua kehidupan
mereka. Hal ini diduga disebabkan oleh mutasi pada protein, bukan karena tidak lengkap.
EPIDEMIOLOGI
Frekuensi
Amerika Serikat
Frekuensi dar XLA adalah sekitar 1 kasus per 250.000 penduduk. Dua pertiga kasus
adalah keturunan, dan sepertiga dari kasus diyakini muncul dari mutasi baru.
Internasional
Insiden XLA seluruh dunia tidak berbeda jauh secara signifikan dengan Amerika Serikat.
16

Mortalitas /Morbiditas
Kebanyakan pria dengan X-linked agammaglobulinemia(XLA) hidup sampaiusia
40-an. Prognosisbaik jika pengobatan dimulai sejak dini, idealnya jika imunoglobulin
intravena G (IVIG) dimulai sebelum individu tersebut berusia 5 tahun. Bahkan dengan
pengobatan, pasien tetap dapat memiliki infeksi paru kronis, penyakit kulit, penyakit
radang usus (kolitis ulserativadan penyakit Crohn), dan komplikasisistem saraf pusat
akibat infeksi entero virus.
Ras
XLA tidak menunjukkan kecenderungan untuk ras tertentu. 2,6
Seks
AgammaglobulinemiaBruton adalah penyakit terkait-X, dengan hanya keturunan
laki-laki yang terpengaruh. Kebanyakan kasus diwariskan, namun, jarang penyakit ini
bermanifestasi sebagai konsekuensi dari mutasi spontan. Mutasi pada gen untuk gen Mu
berat (IGHM), gen imunoglobulin-alfa, dan lambda-5 gen dapat menyebabkan
agammaglobulinemia, dengan kurang dari 1%CD19ekspresisel B. Tidak ada perempuan
carrier terdapat manifestasi klinis dari mutasiBTK. 2,6
Usia
Bayi laki-laki menjadi terpengaruh oleh X-linked agammaglobulinemia(XLA)
ketika antibodi ibu menurun biasanya setelah usia4-6 bulan. Jika ibu telah diidentifikasi
sebagai pembawauntuk penyakit ini, chorionic villi sampling atau amniosentesis dapat
dilakukan untukmengumpulkan limfosit janin di dalam rahim. Saat lahir, sampel darah
dari tali pusat dapat diuji untuk penurunan CD19+sel B dan untuk peningkatan sel
Tmatangmelalui analisisfluorocytometric. Anak-anak biasanya memanifestasikan klinis
penyakit ini pada usia3-9 bulan dengan pneumonia,otitis media, selulitis, meningitis,
osteomielitis, diare, atau sepsis. Jarang terjadi kasus yang pada orang dewasa didekade
kedua mereka yang telah didiagnosa dengan bentuk lebih ringan XLA dianggap karena
mutasi bukan karena tidak adanya protein. 2,6
17

GEJALA KLINIK
Bayi laki-laki dengan X-linked agammaglobulinemia (XLA), atau
agammaglobulinemia Bruton, dapat muncul secara fisik lebih kecil dari bayi laki-laki
tanpa XLA karena pertumbuhan dan perkembangan tertunda dari infeksi berulang. 2,6
Pada pemeriksaan, kelenjar getah bening, amandel, dan jaringan limfoid lain
mungkin sangat kecil atau tidak ada. 2,6
Penyakit ini didiagnosis ketika bayi laki-laki berulang kali menjadi sakit dengan
infeksi sinopulmonary, otitis media, dan infeksi kulit stafilokokus dan konjungtivitis yang
tidak merespon baik terhadap terapi antibiotik. Infeksi parah mungkin terkait dengan
neutropenia. 2,6
Diare akibat Giardia, C jejuni, Shigella, dan infeksi Salmonella mungkin tanda
klinis XLA. 2,6
Pioderma gangrenosum - borok seperti dan selulitis dari ekstremitas bawah dapat
dilihat pada X-linked (Bruton) agammaglobulinemia 6
DIAGNOSIS DIFERENSIAL
Acrodermatitis Enteropathica
Ataxia-Telangiectasia
Atopic Dermatitis
Avitaminosis A
Common Variable Immunodeficiency
Severe Combined Immunodeficiency 6
LABORATORIUM
Dengan pengukuran kuantitatif IgG, IgM, imunoglobulin E (IgE), dan
imunoglobulin A (IgA) tingkat. Tingkat IgG harus diukur pertama, sebaiknya setelah usia
6 bulan, ketika tingkat penurunan. IgG ibu dibawah 100 mg / dL biasanya menunjukkan
agammaglobulinemia terkait-X (XLA). Deteksi IgG, IgA, IgM, IgE dan tingkat berkaitan
dengan usia. Biasanya, IgM dan IgA tidak terdeteksi. Semua tingkat berkurang pada pria
dengan XLA. 6
18

Setelah tingkat antibodi yang terdeteksi sebagai abnormal rendah, konfirmasi
dicapai dengan menggunakan analisis fluorocytometric penanda B-limfosit dan T-
limfosit. CD19 + sel B tingkat yang lebih rendah dari 100 mg / dL merupakan diagnostik
XLA. Pada analisis fluorocytometric, T-sel nilai (CD4 + dan CD8 +) biasanya
meningkat.6
Analisis lebih lanjut dapat dibuat dengan mendeteksi respon IgG terhadap sel T-
dependent dan sel T-independen antigen dengan pemberian imunisasi, seperti vaksin 23-
valent pneumokokus konjugasi (sel T-independen tanggapan) atau tetanus, difteri, dan H
influenzae tipe b imunisasi (T-sel yang tergantung respon). 6
PENATALAKSANAAN
Medika Mentosa
Tidak ada terapi kuratif ada untuk X-linked agammaglobulinemia (XLA), atau
agammaglobulinemia Bruton. Pengobatan untuk XLA adalah IVIG. Dosis tipikal adalah
400-600 mg / kg / bln diberikan setiap 3-4 minggu. Dosis dan interval dapat disesuaikan
berdasarkan respon klinis individu. Terapi harus dimulai pada usia 10-12 minggu.
Pemeliharaan tingkat IgG dari 500-800 mg / dL dianjurkan. Terapi harus dimulai pada
usia 10-12 minggu. Saat ini, tidak ada bukti mendukung bahwa salah satu merek tertentu
atau cara pemberian (IV vs SC) lebih baik dari yang lain. 2,6
Antibiotik, seperti amoksisilin dan amoksisilin / klavulanat, diberikan untuk
infeksi sinopulmonary umum.Seftriakson intravena dapat digunakan untuk infeksi kronis,
pneumonia, atau sepsis. Infeksi dengan Streptococcus pneumokokus, khususnya,
mungkin memerlukan seftriakson, sefotaksim, atau vankomisin. 2,6
Bronkodilator, inhaler steroid, dan tes fungsi paru teratur (setidaknya 3-4 kali
setahun) mungkin merupakan bagian yang diharuskan dari terapi selain antibiotik. 2,6
Manifestasi dermatologi kronis dermatitis atopik dan eksim dikendalikan dengan
lotion pelembab sehari-hari dan steroid topikal. 2,6
Suplementasi gizi dengan multivitamin dianjurkan.6
19

Perawatan Bedah
Intervensi bedah untuk X-linked agammaglobulinemia (XLA) dibatasi untuk
infeksi akut parah atau infeksi kronis tidak responsif. Prosedur yang paling umum
melibatkan mengobati pasien dengan otitis berulang dengan memasukkan tabung
tympanostomy dan mengobati pasien dengan sinusitis kronis dengan drainase bedah.6
Diet
Pasien dengan XLA harus mengikuti diet normal dan dilengkapi dengan
multivitamin. Tidak ada batasan diet khusus untuk XLA, meskipun diet rendah lemak
mungkin diperlukan untuk pasien dengan penyakit inflamasi usus6
Kegiatan
Pasien dengan XLA tidak memiliki keterbatasan fisik tertentu. Tidak merokok
atau tidak terpapar asap rokok sangat dianjurkan untuk pasien karena risiko peningkatan
infeksi sinopulmonary.6
PENCEGAHAN
Keluarga dengan gen bermutasi dapat dikenal sebelum lahir dievaluasi untuk
lebih mempersiapkan untuk perawatan bayi. Pengujian dilakukan melalui amniosentesis
atau pengambilan sampel chorionic villi. Setelah lahir, pengujian dilakukan pada darah
tali pusat.6
KOMPLIKASI
Komplikasi bagi penderita XLA termasuk infeksi sinopulmonary kronis, infeksi
enterovirus dari sistem saraf pusat, terjadinya peningkatan penyakit autoimun, dan infeksi
kulit.6
PROGNOSA
Pasien dengan XLA dapat hidup sampai akhir 40-an mereka. Prognosis baik
selama pasien didiagnosis dan diobati secara dini dengan terapi gamma globulin
intravena secara teratur sebelum gejala sisa dari infeksi berulang muncul.6
20

IVIG bertanggung jawab untuk meningkatkan tingkat ketahanan hidup, dengan
pengobatan awal sebaiknya sebelum pasien berusia 5 tahun.6
EDUKASI
Pasien dan keluarga mereka harus memahami sifat dari penyakit dan pentingnya
pengobatan dini. Identifikasi dan pengobatan infeksi yang umum diperlukan untuk
prognosis yang lebih baik.
Konseling genetik direkomendasikan untuk orang tua dan saudara perempuan
laki-laki yang terpengaruh. Karakterisasi molekuler dan deteksi pembawa informatif di
95% keluarga.6
Common Variable Immunodeficiency (CVI)
CVID adalah gangguan yang melibatkan berikut: (1) rendahnya tingkat sebagian
besar atau semua immunoglobulin (Ig), (2) kurangnya limfosit B atau sel plasma yang
mampu memproduksi antibodi, dan (3) seringnya terserang infeksi bakteri. Diagnosis
CVID dipakai untuk mereka yang memiliki disfungsi sel-B tak terdefinisi. 2,7
CVID mempunyai banyak ragam, baik dalam presentasi klinis dan dalam jenis
kekurangan. Meskipun penurunan kadar serum imunoglobulin G (IgG) dan
imunoglobulin A (IgA) yang khas, sekitar 50% dari pasien dengan defisiensi ini juga
telah mempunyai serum imunoglobulin M (IgM) yang tinggi dan disfungsi limfosit T.
Sekitar 20% dari mereka dengan CVID mengembangkan penyakit autoimun 2,7
PATOFISIOLOGI
Pada pasien dengan imunodefisiensi umum variabel(CVID), banyak kelainan
sistem kekebalan yang dilaporkan, yang paling umum yang rusak adalah pembentukan
antibodi. Beberapa pasien CVID mungkin memiliki cacat dalam kemampuan sel-
Tmembantu sel B, dan/atau B-sel respon terhadapT-sel. Secara umum jumlah sel B
cukup, namun terdapat cacat pada proses diferensiasi atau fungsi terminalnya. Cacat
tersebut berupa kegagalan sel B untuk berdiferensiasi menjadi sel plasma sehingga
21

pembentukan imunoglobulin kurang memadai jumlahnya atau berupa kelainan intrinsik
pada sel B sendiri2,7
EPIDEMIOLOGI
Frekuensi
Amerika Serikat
Prevalensi immunodeficiency variabel umum (CVID) adalah sekitar 1 kasus per 50.000
penduduk.7
Internasional
Prevalensi internasional mirip dengan yang di Amerika Serikat.7
Mortalitas / Morbiditas
Tingkat kelangsungan hidup 20-tahun adalah 64% untuk pasien pria dan 67%
untuk pasien wanita.Secara umum, tingkat kelangsungan hidup yang diharapkan untuk
pasien pria dan wanita adalah 92% dan 94% masing-masing.Kematian dapat terjadi
akibat berbagai penyebab.7
Ras
CVID tidak menunjukkan kecenderungan untuk ras tertentu.7
Seks
CVID sama mempengaruhi pria dan wanita.7
Usia
CVID dapat terjadi pada bayi, anak-anak, remaja, atau bahkan tahun-tahun 20-40
baya atau lebih tua. CVID dapat menjadi jelas setiap saat dari bayi sampai setelah dekade
keempat kehidupan. Puncak onset terjadi pada anak usia 1-5 tahun dan pada orang
berusia 16-20 tahun. Lebih dari dua pertiga pasien berusia 21 tahun atau lebih ketika
CVID didiagnosis.7
GEJALA KLINIS
Lima fenotipe klinis yang berbeda telah digambarkan untuk umum variabel
immunodeficiency (CVID):. Ada komplikasi, autoimunitas, infiltrasi limfositik
22

poliklonal, enteropati, dan keganasan limfoid. Dalam setiap pasien dengan riwayat medis
masa lalu dari CVID, 3 komplikasi harus diperhatikan: infeksi berulang, fenomena
autoimun, dan keganasan.2,7
Pasien dengan CVID sering memiliki riwayat infeksi berulang.
Infeksi yang berulang sering mempengaruhi saluran pernafasan atas dan bawah. Pasien
datang ke perhatian medis karena penyakit menular pada saat onset, yang paling umum
adalah otitis media, diare, pneumonia, dan sinusitis. Hampir semua memiliki infeksi akut
dan berulang.. 2,7
Diare persisten dan malabsorpsi disebabkan oleh infeksi Giardia lamblia terjadi
pada pasien dengan CVID. Gejala umumnya sembuh setelah pengobatan dengan
metronidazol. Etiologi infeksi dan autoimun adalah penyebab paling mungkin untuk diare
kronis parah. Keganasan pada saluran pencernaan tidak menyebabkan diare. 2,7
Anak-anak kecil mungkin sulit berkembang karena sering infeksi atau penyakit
saluran pencernaan. 2,7
DIAGNOSIS DIFERENSIAL
Bruton Agammaglobulinemia
Severe Combined Immunodeficiency 7
LABORATORIUM
Umum immunodeficiency variabel (CVID) dapat didiagnosis setelah terjadi cacat
pembentukan antibodi fungsional. Biasanya, pasien mengalami penurunan (tidak ada)
serum IgA dan IgG, kadang-kadangpenurunan kadar IgM serum tanpa adanya penyebab
lain yang dikenal defisiensi antibodi.7
Dibandingkan dengan pasien dengan X-linked agammaglobulinemia, pasien
dengan CVID umumnya memiliki lebih tinggi tingkat serum Ig. Kisaran referensi untuk
serum Ig bervariasi dengan usia pasien, dan hasil Ig harus dievaluasi atas dasar usia.7
Meskipun elektroforesis dan immunoelectrophoresis tidak diterima teknik untuk
kuantifikasi tingkat Ig, imunodifusi radial atau metode immunoturbidimetric tetap
berharga. 7
23

Mengukur tingkat mediator dan sitokin seperti IL-2, IL-4, IL-5, interleukin 6 (IL-
6), interferon gamma, dan tumor necrosis factor dalam supernatan kultur adalah alat lain
yang berguna. 7
Metode lain adalah pengukuran kadar Ig disekresikan dalam supernatan kultur.
Hitungan darah lengkap dan tes autoantibody dapat membantu juga. Anemia sekunder
untuk proses autoimun dapat dideteksi. Limfopenia parah dapat menunjukkan bahwa
pasien menderita penyakit imunodefisiensi parah gabungan atau primer sel T cacat. 7
PENATALAKSANAAN
Andalan pengobatan untuk immunodeficiency variabel umum (CVID) adalah Ig
terapi pengganti. Meskipun mahal, terapi penggantian Ig menghentikan siklus infeksi
berulang.2,7
Ig dapat diberikan intravena atau subkutan. Solusi imunoglobulin intravena 3-
12% (IVIG) dapat digunakan secara teratur untuk mempertahankan tingkat palung dari
400-500 mg / dL pada orang dewasa. Sebuah dosis 400-600 mg / kg setiap 2-4 minggu
biasanya dibutuhkan. Pada pasien dengan kerusakan paru-paru struktural, tingkat dosis
pemeliharaan 700-800 mg / dL diperlukan. 2,7
Larutan injeksi subkutan 16% immunoglobulin IV (SCIG) juga merupakan
pengobatan yang efektif pada pasien dengan akses intravena yang sulit. Seperti yang
diharapkan, volume yang diperlukan untuk mencapai tingkat endapan yang memadai jauh
lebih tinggi dengan SCIG dibandingkan dengan IVIG. Dosis 160 mg / kg / minggu
sebanding dengan dosis IVIG 400 mg / kg / bln. 2,7
Reaksi negatif terhadap Ig administrasi harus dipantau selama terapi. Reaksi yang
paling umum termasuk sakit punggung, mual, muntah, menggigil, demam, mialgia, dan
kelelahan. Efek samping terjadi dalam waktu 30 menit infus dan biasanya berlangsung
selama beberapa jam. Memperlambat laju infus selama beberapa menit sangat membantu
dalam mencegah gejala. Efek dapat diobati dengan antipiretik, diphenhydramine, dan /
atau kortikosteroid. Meskipun reaksi anafilaksis untuk IVIG jarang terjadi, pasien dengan
defisiensi IgA memiliki peningkatan risiko untuk efek ini. Jangka panjang akses
intravena tidak dianjurkan karena dapat meningkatkan risiko infeksi. 2,7
24

Transmisi agen infeksi selama infus telah menyebabkan masalah di masa lalu.
Meskipun tidak ada kasus infeksi HIV telah dikaitkan dengan Ig terapi, penularan virus
hepatitis C telah dilaporkan. Metode terbaru dari inaktivasi virus membantu mencegah
penularan. Metode-metode termasuk pengobatan dengan pelarut organik dan deterjen,
pasteurisasi, dan penyimpanan pada pH rendah. Di Amerika Serikat, produk Ig berasal
dari plasma manusia dikumpulkan, yang mengalami proses manufaktur yang mencakup
fraksinasi etanol dingin dan langkah inaktivasi virus. 2,7
Pada kebanyakan pasien, CVID respons yang baik dengan terapi Ig. Terulangnya
infeksi, gejala rematik, dan tingkat keparahan dan / atau kejadian penyakit autoimun
dikurangi. Penyakit gastrointestinal menunjukkan sedikit perbaikan dengan IVIG. Pada
beberapa pasien dengan penyakit autoimun yang berat, penggunaan bersamaan dari
steroid atau obat imunosupresif lainnya mungkin diperlukan. 2,7
Siklosporin A telah berhasil digunakan pada pasien dengan pneumonitis
interstisial limfoid dan CVID. Pemberian anti-CD20 antibodi monoklonal telah
digunakan untuk mengobati trombositopenia autoimun dan neutropenia. Studi yang
dilakukan untuk mengevaluasi efektivitas IL-2 administrasi dalam hubungannya dengan
polietilen glikol. Hasil awal penelitian in vitro menunjukkan peningkatan produksi Ig
oleh limfosit B. 2,7
Terapi antimikroba harus dimulai pada tanda pertama infeksi. Sebuah spektrum
sempit obat harus digunakan bila hasil sensitivitas tersedia. Penggunaan profilaksis
antibiotik harus dihindari karena peningkatan risiko infeksi jamur atau organisme resisten
lainnya. 2,7
Terapi khusus sering diperlukan untuk menargetkan sistem organ yang terlibat.
Misalnya, pasien dengan penyakit paru kronis sering mengembangkan penyakit saluran
napas obstruktif yang memerlukan pengobatan dengan kortikosteroid inhalasi dan obat
asma lain. 2,7
PENCEGAHAN
25

Karena setidaknya beberapa pasien CVID dapat menghasilkan titer antibodi
pelindung, orang harus mempertimbangkan masuknya vaksin polisakarida dalam
program imunisasi untuk mereka 2,7
KOMPLIKASI
Dalam setiap pasien dengan riwayat medis masa lalu dari immunodeficiency
variabel umum (CVID), 3 komplikasi berikut ini harus dipertimbangkan : berulang
infeksi, fenomena autoimun, keganasan.7
Kematian dapat terjadi. Penyebab umum kematian pada pasien dengan CVID
adalah limfoma. Penyebab lainnya adalah cor pulmonale sekunder terhadap infeksi paru
kronis, gagal hati yang disebabkan oleh hepatitis virus atau autoimun, kekurangan gizi
akibat penyakit saluran cerna, dan infeksi virus lainnya. Faktor yang terkait dengan
kematian termasuk rendahnya tingkat IgG, sel T kurang sensitif terhadap antigen, dan
persentase yang rendah sel B perifer.7
Komplikasi lainnya termasuk sinusitis kronis, trombositopenia autoimun yang
berat, dan anemia hemolitik.7
PROGNOSA
Prognosis tergantung pada adanya penyakit autoimun yang berat, infeksi berulang
yang menyebabkan kerusakan paru-paru struktural, dan perkembangan keganasan.7
Faktor utama lainnya dalam menentukan prognosis adalah tingkat kerusakan akhir
organ dan keberhasilan profilaksis terhadap infeksi di masa depan.7
Infiltrasi limfositik poliklonal adalah prediktor klinis yang terkait dengan risiko 5
kali lipat dari keganasan limfoid. 7
EDUKASI
Pasien dan keluarga mereka harus dididik tentang tanda-tanda awal infeksi
sehingga pengobatan agresif tidak ditunda.
Defisiensi Ig A selektif
26

Defisiensi IgA selektif adalah penyakit imunodefisiensi primer dan yang paling
umum dari kekurangan antibodi primer. Defisiensi IgA selektif didefinisikan sebagai
imunoglobulin serum tidak terdeteksi Tingkat (IgA) dengan nilai a <5 mg / dL (0,05 g /
L) pada manusia. Partial Defisiensi IgA selektif mengacu pada tingkat IgA terdeteksi
tetapi menurun yang lebih dari 2 standar deviasi di bawah normal sesuai usia 2,8
Defisiensi IgA selektif umumnya terkait dengan limfosit B normal di darah tepi,
CD4 yang normal + dan CD8 + T sel, dan, biasanya, neutrofil normal dan jumlah
limfosit. Anti-IgA autoantibodi dari IgG dan / atau IgE isotipe mungkin ada. Darah
perifer juga dapat dipengaruhi oleh cytopenias autoimun, misalnya, trombositopenia
autoimun, [3, 4] dan pasien mungkin memiliki fenomena autoimun lainnya. 2,8
IgA pertama kali diidentifikasi oleh Graber dan Williams pada tahun 1952;
sepuluh tahun kemudian, pasien pertama dengan IGAD digambarkan. 2,8
PATOFISIOLOGI
Defisiensi IgA selektif adalah penyakit immunodeficiency primer diduga akibat
dari kegagalan diferensiasi terminal di IgA positif sel B. 8
EPIDEMIOLOGI
Frekuensi
Amerika Serikat
Minimal, sebuah diperkirakan 250.000 orang telahDefisiensi IgA selektif di
Amerika Serikat. Dalam Amerika Afrika, prevalensi adalah 1 kasus per 6000 orang..8
Internasional
Faktor yang terkait dengan prevalensi Defisiensi IgA selektif termasuk riwayat
keluarga dan negara asal. Studi menunjukkan bahwa saudara-saudara memiliki tingkat
prevalensi 7,5% dari Defisiensi IgA selektif, yang merupakan 38 kali lipat lebih tinggi
dari donor yang tidak berhubungan. Prevalensi serologi dari Defisiensi IgA selektif
bervariasi 100 kali lipat di antara populasi8
Mortalitas / Morbiditas
27

IGAD lebih sering pada orang dewasa dengan penyakit paru kronis dari dalam,
sehat usia-cocok subyek kontrol .8
Ras
Defisiensi IgA selektif terjadipada orang Arabpada tingkat1 kasus per142
orang,pada orang putih pada tingkat1 kasus per500-700 orang, pada orang Amerika
Afrika pada tingkat 1 kasus per6000 orang, dan pada orang Asia pada tingkat 1 kasus per
14,840-18,500 orang8
Seks
Sebuah studi dari 7293 relawan Austria menunjukkan frekuensi yang lebih besar
dari SigAD pada pria dibandingkan pada wanita(0,19% vs 0,014%) dan frekuensi yang
lebih besar di bawah normal IgAserum(0,07-0,7 g / L) pada pria (2,66%) dibandingkan
pada wanita(0,93%). 8
Usia
Penyakit inidapat didiagnosis pada orang dari segala usia. Rata-rata serum IgA
meningkatkan tingkat0,2±0,06g / Lper dekade kehidupan.8
GEJALA KLINIS
Pasien datang dengan berbagai tanda berulang infeksi saluran pernapasan;
termasuk pembengkakan, nyeri, atau nyeri tekan pada palpasi pada sinus-sinus maksila
dan frontal; otorrhea kronis dan / atau membran timpani bekas luka atau berlubang dan
ketajaman pendengaran menurun atau bahkan ketulian; nasal discharge kronis, demam ;
produktif atau batuk produktif, dan dyspnea. Temuan GI mungkin termasuk perut
kembung, nyeri fokus untuk palpasi langsung (tanpa rebound), kram setelah makan, nyeri
menyebar, dan gerak peristaltik yang meningkat. 2,8
DIAGNOSIS DIFERENSIAL
Ataxia-Telangiectasia
28

Combined B-Cell and T-Cell Disorders
IgG subclass deficiency and/or specific polysaccharide antibody deficiency
Severe Combined Immunodeficiency
Wiskott-Aldrich Syndrome 8
LABORATORIUM
Imunoglobulin Kekurangan (IGAD) didefinisikan sebagai tingkat IgA serum tidak
terdeteksi. Di masa lalu, ini biasanya dikonfirmasi dengan metode imunodifusi tingkat
rendah radial (batas bawah deteksi adalah 50 mg / mL [5 mg / dL]). Namun, tes ini jarang
dilakukan dalam praktek saat ini, dan hasil yang biasanya dilaporkan sebagai <0,07 g / L
atau <0,05 g / L. Batas bawah deteksi berbeda, tergantung pada kepekaan metode yang
digunakan. Hal ini biasanya 0,05-0,1 g / L untuk nephelometry, 0,05 g / L (5 mg / dL)
untuk tingkat rendah piring imunodifusi radial, dan 0,0016 g / L untuk teknik inhibisi
hemaglutination. 8
PENATALAKSANAAN
Perawatan medis
Pendekatan terhadap pengobatan meliputi identifikasi kondisi komorbiditas;
langkah-langkah pencegahan untuk mengurangi risiko infeksi, dan prompt,perawatan
yang ketat, dan efektif infeksi. Bedah sinusendoskopi fungsional sering dapat membantu
meringankan obstruksi kronis dan drainase. Tabung tympanostomy juga dapat membantu
dalam mengurangi resiko penurunan pendengaran dan perkembangan bicara sekunder
cacat pada anak dengan otitis supuratif kronis yang berhubungan dengan defisiensi
antibodi.8
Perawatan Bedah
Beberapa pasien dengan sinusitis berulang memerlukan intervensi bedah untuk
drainase.8
PENCEGAHAN
29

Pencegahan primer untuk Defisiensi IgA selektif belum dikembangkan. Jika
dipertimbangkan obat sebagai penyebab IGAD, itu harus dihentikan.8
Pencegahan sekunder bergantung terutama pada vaksinasi untuk meningkatkan
IgG dan IgM spesifik. Dalam situasi di mana air murni dan didekontaminasi tidak dapat
dijamin, tindakan pencegahan seperti air minum mendidih dapat membantu mencegah
infeksi GI seperti giardiasis atau Cryptosporidiosis. Peran antibiotik profilaksis adalah
kontroversial karena mereka dapat meningkatkan bahaya infeksi dengan bakteri resisten
atau jamur.8
Pencegahan tersier meliputi (1) pengobatan antibiotik yang cepat untuk infeksi
saluran pernapasan, (2) identifikasi mikroba patogen diare dan pengobatan khusus, (3)
modifikasi diet untuk sindrom malabsorpsi, dan (4) menggunakan sel dicuci dan / atau
IgA miskin darah jika seluruh darah yang dibutuhkan, dan penyaringan untuk anti-
antibodi IgA jika reaksi terhadap produk darah terjadi (tidak rutin dilakukan).8
Sindroma DiGeorge (Hipoplasia Timus)
DiGeorge syndrome (DGS) sekarang dipahami sebagai hilangnya kromosom
22q11. Dr DiGeorge yang pertama kali menjelaskan DGS, pada tahun 1965. 2,9
Dr DiGeorge adalah orang pertama yang memberikan contoh-contoh klinis pada
manusia menunjukkan bahwa timus terlibat dalam fungsi kekebalan tubuh, kemudian
baru diketahui bahwa sistem kekebalan tubuh itu terdiri dari 2 elemen yang berbeda:
elemen (sel B) humoral dan diperantarai sel (sel T) elemen. Dia menggambarkan kasus
dari 4 bayi dengan hipoplasia thymus, hipoparatiroidisme , dan infeksi berulang. 2,9
PATOFISIOLOGI
DGS adalah hilangnya kromosom 22q11 dimana terdapat penghapusan 2-3 juta
pasang basa (Kb) pada lengan panjang kromosom 22. Daerah ini rawan mikrodelesi
karena kehadiran nonallelic, mengapit, rendah salinan sekuens DNA berulang di daerah,
yang mengarah pada tidak sama menyeberang antara dua 22s kromosom selama meiosis.
Penghapusan satu gen kritis atau gen bersebelahan beberapa diduga menjadi dasar dari
sindrom ini. Meskipun beberapa gen di daerah ini telah dipetakan, yang gen boleh
30

dihapus untuk menyebabkan sindrom ini masih belum diketahui. Gen TBX1 mungkin satu
gen penting di kawasan dihapus. Beberapa pasien memiliki penataan ulang kromosom
yang melibatkan kromosom 22.9
Mutasi pada gen TBX1 pada individu dengan fenotip DGS tapi tanpa mikrodelesi
22q11.2 telah ditemukan, menunjukkan bahwa gen ini adalah gen kritis. Hasil
penghapusan ini adalah cacat saat pengembangan yang melibatkan kantung faring ketiga
dan keempat yang disebabkan oleh cacat migrasi dari sel pial neural pada minggu
keempat embriogenesis. Bagian-bagian dari kepala, jantung dan leher, timus, dan
paratiroid ini berasal dari kantong faringeal9.
EPIDEMIOLOGI
Frekuensi
Amerika Serikat
Perkiraan DGS 1 per 2000-4000 pada populasi umum. Hal ini sering menjadi penyebab
bibir sumbing dan cacat jantung bawaan. 9
Internasional
Insiden DGS adalah sama seperti di Amerika Serikat. 9
Mortalitas / Morbiditas
Aspek jantung dari DGS mengarah pada morbiditas dan mortalitas terbesar. Cacat
jantung yang diamati dalam 74-80% dari pasien yang terkena. Hanya sebagian kecil
pasien mengalami infeksi berulang parah sekunder terhadap sel T immunodeficiency
karena hipoplasia thymus parah. Gagal tumbuh dapat diamati selama masa bayi awal
pada mereka dengan bibir sumbing dan kesulitan menelan. Komplikasi jangka panjang
mungkin termasuk ketidakmampuan belajar, keterbelakangan mental ringan, dan
gangguan kejiwaan. 9
Ras
Tidak ada kecenderungan ras atau etnis telah diidentifikasi. 9
Seks
31

Pria dan wanita tampaknya sama-sama terpengaruh. 9
Usia
Ini adalah kondisi bawaan, tetapi usia saat didiagnosis sangat tergantung pada
tingkat keparahan dan jenis cacat lahir. Jadi, orang dengan cacat jantung lebih serius,
hipokalsemia, atau keduanya pada periode neonatal. Infeksi berulang biasanya hadir pada
pasien lebih tua dari 3-6 bulan. Beberapa individu tanpa hipokalsemia yang memiliki
fungsi kekebalan tubuh normal, cacat jantung ringan, dan anomali wajah minimal tidak
dapat didiagnosis sampai anak terlambat. Keterlambatan diagnosis sampai dewasa terus
dilaporkan, terutama pada mereka dengan gejala ringan terisolasi. Diagnosis pada janin
dengan kelainan jantung bawaan harus ditawarkan kepada wanita hamil. 9
GEJALA KLINIS
Temuan pemeriksaan fisik bervariasi tergantung pada sistem organ yang terlibat.
Pasien biasanya memiliki karakteristik fasies, yang menjadi lebih jelas sebagai anak
tumbuh ke dekade kedua. Ini adalah lebih umum dan mudah dikenali pada anak-anak
putih. Retrognathia atau micrognathia, wajah panjang, jembatan hidung tinggi dan
luas, dan celah sempit palpebral adalah fitur umum.
o Malformasi paling umum adalah sumbing langit-langit sekunder. VPI tanpa
langit-langit dapat terjadi. Sumbing bibir, celah langit-langit, atau keduanya
mungkin ada.
o Fitur lainnya termasuk wajah sering gigi kecil, wajah menangis asimetris, dan
mulut turun-berbalik.
Temuan jantung mungkin ada, tergantung pada sifat dari lesi jantung.
Jari lentik mungkin ada.
Perawakan pendek dapat terjadi; jarang, pertumbuhan kekurangan hormon telah
dilaporkan.
Anomali GI seperti atresia esophagus dan atresia atau stenosis anal mungkin ada.
Polydactyly, anomali vertebralis telah terlihat dalam kasus yang jarang. 9
DIAGNOSIS DIFERENSIAL
32

Velocardiofacial Syndrome9
LABORATORIUM
Rekomendasi itu dulu untuk melakukan hibridisasi in situ fluorescent (IKAN)
untuk mendeteksi penghapusan 22q11.2 dalam hubungannya dengan analisis kromosom
standar untuk mendeteksi penyusunan ulang kromosom dan kelainan kromosom lainnya.
Namun, array genom hibridisasi komparatif (aCGH) adalah tes yang lebih baik dan harus
dilakukan bukan IKAN dengan analisis kromosom standar. CGH array akan mendeteksi
penghapusan 22q11.2 dan dapat mendeteksi delesi kromosom lain / duplikasi kromosom
jika penghapusan 22 klasik tidak ada. Hal ini juga dapat memberikan perbaikan dari
breakpoints. 9
PENATALAKSANAAN
Sebuah tim multidisiplin terbaik peduli untuk orang-orang ini, namun satu dokter
(biasanya dokter utama) perlu untuk memimpin dan memberikan rumah medis bagi
pasien. Para dokter utama harus memantau pertumbuhan dan perkembangan. Pendekatan
sistem demi sistem memberikan hasil terbaik. 9
Jantung: Konsultasikan ahli jantung yang diperlukan.
Imunologi: Konsultasikan imunologi jika limfopenia mutlak hadir. Ikuti saran
imunologi untuk imunisasi. Laporan terakhir menunjukkan bahwa pasien dengan
sindrom DiGeorge (DGS) yang secara klinik stabil dengan aman dapat mentolerir
vaksin hidup, termasuk campak, gondok, dan rubella (MMR) dan vaksin varicella.
Endokrin: Jika pasien ditemukan hypocalcemic, mulai suplementasi kalsium setelah
tes yang tepat (kalsium serum simultan dan tingkat hormon paratiroid serum) yang
diperoleh. Suplemen vitamin D mungkin menjadi perlu.
Gagal tumbuh: Feeding kesulitan dan gagal tumbuh yang umum pada pasien,
terutama pada mereka dengan bibir sumbing yang signifikan. Kadang-kadang,
penempatan tabung nasogastrik atau gastrostomy diperlukan untuk memberi makan
selama 6-12 bulan pertama kehidupan. Tabung ini menyediakan nutrisi yang cukup
untuk mencegah kegagalan pertumbuhan yang serius.
33

Masalah lain: Pasien dengan gangguan lain seperti gangguan perkembangan dan
psikosis, harus menerima perawatan yang tepat. 9
PENCEGAHAN
Evaluasi oleh ahli genetika klinis dan konseling genetik dianjurkan sebelum
membuat keputusan keluarga berencana. 9
PROGNOSA
Prognosis pada DiGeorge syndrome (DGS) sangat bervariasi. Ini sangat
tergantung pada sifat dan tingkat keterlibatan organ yang berbeda. Banyak orang dewasa
hidup lama, hidup produktif. 9
Sindroma Wiskott-Aldrich
Wiskott-Aldrich syndrome (WS) pertama kali dijelaskan oleh Wiskott pada tahun
1937 dan selanjutnya oleh Aldrich pada tahun 1954. Ini adalah gangguan terkait-X
immunodeficiency resesif ditandai oleh tiga serangkai berulang infeksi sinopulmonary
bakteri, eksim (dermatitis atopiclike), dan diatesis perdarahan akibat trombositopenia dan
disfungsi trombosit. Namun, hanya sepertiga pasien dengan sindrom ini memiliki triad
klasik. Hampir 90% pasien memiliki manifestasi dari trombositopenia pada presentasi,
20% hanya memiliki kelainan hematologi, 5% hanya memiliki manifestasi menular, dan
tidak hanya memiliki eksim. Gejala lain mungkin termasuk fenomena autoimun dan
keganasan.10
Wiskott-Aldrich syndrome terjadi pada laki-laki tetapi dapat terjadi pada wanita
ketika kromosom X yang berisi alel fungsional tidak aktif, meskipun ini jarang terjadi.
Mungkin ada beberapa genotipe reversi pada pasien dengan sindrom Wiskott-Aldrich. 10
PATOFISIOLOGI
Gen untuk protein sindrom Wiskott-Aldrich (WASP) terlokalisasi Xp11.22-23
dan terdiri dari 12 ekson yang mengkode asam amino 502 (53 kD) protein. WASP
merupakan protein sitosol diekspresikan pada semua garis keturunan sel hematopoietik
34

dan sangat penting untuk fungsi antibodi normal, tanggapan sel T, dan produksi
trombosit. Hal ini juga mengatur polimerisasi aktin, transkripsi, dan, selektif pasca-
transkripsi peran dalam efektor Th2 fungsi. Sekitar 300 mutasi telah ditemukan di seluruh
gen dan dapat termasuk substitusi pasangan basa, sisipan, dan penghapusan. Mutasi ini
dapat menghasilkan fenotipe klinis yang berbeda, termasuk klasik Wiskott-Aldrich
syndrome, terkait-X trombositopenia, trombositopenia intermiten, dan neutropenia. 10
Dalam studi in vitro dengan sel T, trombosit, fagosit, dan sel dendritik pasien
dengan sindrom Wiskott-Aldrich mengungkapkan cacat dalam pembentukan mikrovili,
filopodia, vakuola fagositosis, dan podosomes, masing-masing; struktur ini tergantung
pada reorganisasi cytoskeletal filamen aktin. Para peneliti juga mengidentifikasi mutasi
berbeda yang mengganggu protein mengikat Cdc42 dan Rac GTPases, antara mitra
mengikat lainnya, sebagian besar yang terlibat dalam regulasi dari sitoskeleton aktin
limfosit. The sitoskeleton aktin bertanggung jawab untuk fungsi seluler , seperti
pertumbuhan, endositosis, eksositosis sitokinesis. 10
EPIDEMIOLOGI
Frekuensi
Amerika Serikat
Kejadian diperkirakan Wiskott-Aldrich syndrome di Amerika Serikat adalah 1 dalam
250.000 kelahiran laki-laki hidup. 10
Internasional
Frekuensi pada populasi Eropa telah dilaporkan mirip dengan Amerika Serikat (1 dalam
250.000 kelahiran laki-laki hidup). Sebuah studi dari Swiss melaporkan kejadian
Wiskott-Aldrich syndrome adalah 4,1 kasus per 1 juta kelahiran hidup. Penelitian yang
sama juga meneliti prevalensi sindrom Wiskott-Aldrich di beberapa pendaftar nasional
(yaitu, Italia, Jepang, Swiss, Swedia) dan menemukan bahwa kondisi ini terjadi pada 2-
8,8% pasien dengan immunodeficiencies primer. Berbagai mirip telah didokumentasikan
dalam daftar nasional di Irlandia, juga. 10
35

Mortalitas / Morbiditas
Morbiditas dan mortalitas telah berangsur-angsur membaik dengan antibiotik
yang lebih baik, perawatan yang lebih baik mendukung, dan dengan transplantasi sel
induk. Hidup rata-rata telah meningkat dari 8 bulan pada pasien lahir sebelum tahun 1935
sampai lebih dari 6 tahun pada pasien yang lahir setelah tahun 1964. Dalam satu
rangkaian kasus, 94 pasien yang masih hidup berkisar di usia 1-35 tahun, dengan rata-rata
11 tahun; usia rata-rata pasien yang meninggal adalah 8 tahun. 10
Ras
Wiskott-Aldrich Syndrome telah dilaporkan pada individu keturunan Eropa,
Afrika, dan Asia, namun, kulit hitam dan Asia cenderung tidak terpengaruh. Salah satu
seri besar dari 301 kasus sindrom Wiskott-Aldrich dari 149 keluarga melaporkan bahwa 8
keluarga yang hitam dan 4 keluarga yang Chicano. Dari 40 keluarga yang keturunan
dijiplak di luar Amerika Utara, 38 beremigrasi dari Eropa. 10
Seks
Lebih dari 90% pasien yang terkena adalah laki-laki, tetapi perempuan pernah
dilaporkan dalam literatur. Wanita biasanya tidak memiliki riwayat keluarga. Dalam
beberapa kasus, perempuan telah terbukti memiliki inaktivasi nonrandom dari kromosom
X yang menyandang alel Wiskott-Aldrich sindrom fungsional. 10
Usia
Usia berkisar presentasi dari lahir sampai 25 tahun. Dalam salah satu review, usia
rata-rata dari presentasi adalah 21 bulan. Infeksi biasanya mulai pada masa bayi awal
setelah ibu imunoglobulin G (IgG) hilang selama 3 bulan pertama kehidupan. Frekuensi
infeksi biasanya meningkat dengan usia. Pasien sangat rentan terhadap organisme
dienkapsulasi. Eksim berkembang selama tahun pertama kehidupan dan menyerupai
klasik dermatitis atopik . Keganasan dapat terjadi pada anak tetapi lebih sering pada
orang dewasa yang terkena. Limfoma terjadi pada 26% pasien berusia 20 tahun dan lebih
tua. 10
36

PEMERIKSAAN FISIK
Perhatikan tanda-tanda perdarahan, infeksi, keganasan, dan atopi pada
pemeriksaan fisik. Umum pasien penampilan dan tanda-tanda vital yang penting. Ikuti
tinggi dan berat badan dari waktu ke waktu untuk memantau pembangunan yang tepat.
Pasien biasanya mengalami pertumbuhan yang normal untuk beberapa tahun pertama
kehidupan, bahkan dengan episode infeksi akut yang parah 10
Periksa kulit untuk bukti eksim. Wajah, kulit kepala, dan daerah lentur yang
paling sering terlibat. Infeksi dangkal atau mendalam seperti infeksi bakteri sekunder
(misalnya, impetigo, selulitis, furunkel, abses), herpeticum eksim, dan moluskum
kontagiosum yang umum. Juga memeriksa kulit untuk purpura (trombositopenia).
Kehadiran ekimosis ekstremitas bawah pada bayi (lihat gambar di bawah) yang belum
berjalan menunjukkan kelainan trombosit. Periksa untuk diare berdarah tanpa adanya
etiologi infeksi. Manifestasi lain mungkin termasuk hematemesis, melena, epistaksis, dan
hematuria. 10
Selama pemeriksaan kepala dan leher, diketahui adanya kelainan membran
timpani (misalnya otitis media) atau sinus dan selaput lendir (misalnya, infeksi sinonasal,
faringitis , sariawan ). Bayi yang lebih tua sering memiliki kejadian dramatis
meningkatkan otitis media, meskipun merespon dengan tepat terhadap antibiotik oral. 10
Pemeriksaan neurologis sangat relevan jika meningitis, limfoma SSP, atau
perdarahan intrakranial atau infeksi dianggap. 10
Vaskulitis kutan mungkin jarang terlihat sebagai edema hemoragik akut berulang
dari masa bayi. 10
DIAGNOSIS DIFERENSIAL
Agammaglobulinemia
Dermatitis Atopik
Bruton agammaglobulinemia
DiGeorge Syndrome
Histiocytosis
Parah Gabungan Immunodeficiency 10
37

LABORATORIUM
Klasik Wiskott-Aldrich sindrom dikaitkan dengan M imunoglobulin rendah (IgM)
dan Imunoglobulin G (IgG) tingkat, dengan normal ke tinggi imunoglobulin A (IgA) dan
imunoglobulin E (IgE) tingkat. Namun, bayi muda khususnya mungkin tidak
menunjukkan kelainan imunoglobulin klasik karena Wiskott-Aldrich syndrome terkait
dengan gesekan dalam fungsi imunologi. 10
Cacat antibodi spesifik yang paling mungkin sebagai respons terhadap antigen
polisakarida. Oleh karena itu, isohemagglutinins, IgM ditujukan terhadap antigen
golongan darah ABO, biasanya tidak ada; isohemagglutinins yang berkaitan dengan usia
dan tidak terdeteksi sampai bayi berusia lebih dari sekitar 6 bulan. IgG ditujukan terhadap
antigen pneumokokus unconjugated ditentukan postvaccination tetapi tidak diproduksi
oleh anak-anak sehat yang lebih muda dari 2 tahun. Respon antibodi T-tergantung untuk
tetanus, difteri, dan vaksin konjugasi Hib bervariasi dalam Wiskott-Aldrich syndrome.
Gesekan kekebalan pada respon antibodi terjadi pada pasien yang lebih tua. 10
PENATALAKSANAAN
Secara optimal, sel donor harus cocok dengan pasien di semua histokompatibilitas
6 utama (MHC) situs karena pertandingan tidak lengkap membawa risiko lebih tinggi
untuk komplikasi (terutama penyakit graft versus host [GVHD]) di Wiskott-Aldrich
Syndrome dibandingkan dengan pasien dengan sebagian immunodeficiency primer
lainnya penyakit. Terkait transplantasi sumsum tulang dari saudara telah berhasil di
hampir 90% pasien dengan sindrom Wiskott-Aldrich, dengan engraftment sel T, sel B,
dan trombosit penuh. 10
Karena pasien dengan sindrom Wiskott-Aldrich memiliki beberapa derajat
imunitas diperantarai sel, pasien harus menerima rezim preparatif terapi imunosupresif,
biasanya siklofosfamid, busulfan, dan, mungkin, iradiasi total tubuh, untuk
memungkinkan sel-sel donor untuk menanamkan. Baru-baru fludarabine rejimen berbasis
penyejuk myeloablative telah dikembangkan dengan hasil yang menjanjikan dari
engraftment baik dan rendah toksisitas terkait pengobatan. Dalam rahim transplantasi
tidak menjadi pilihan karena kebutuhan untuk imunosupresi pretransplant. 10
38

Terapi gen diharapkan menjadi tersedia di masa mendatang karena penelitian
pada tikus yang menjanjikan. Satu studi berhasil ditransfer gen WASP menjadi sel induk
hematopoietik, menggunakan WASP yang mengandung vektor lentiviral, dikombinasikan
dengan iradiasi tidak mematikan. Studi lain murine menunjukkan bahwa ekspresi
transgen WASP dapat berhasil mempertahankan jangka panjang pada penerima dan
bahwa adalah dikaitkan dengan perbaikan signifikan cacat bermigrasi. Tahap I dan II
studi klinis mulai segera di beberapa negara Eropa untuk menilai keamanan dan
kemanjuran ini vektor lentiviral di Wiskott-Aldrich Syndrome. Meskipun gen WASP
diklona , identitas yang tepat dan fungsinya tidak sepenuhnya dipahami, yang
menyebabkan kekhawatiran bahwa overekspresi WASP dapat menyebabkan penyakit
klinis. 10
Manajemen infeksi termasuk antibiotik dan mungkin intravena imunoglobulin G
(IVIG). Keputusan untuk menggunakan antibiotik profilaksis dan / atau IVIG dibuat
kasus per kasus, berdasarkan insiden dan keparahan infeksi pada pasien.
Postsplenectomy, antibiotik profilaksis adalah wajib, meskipun pasien yang menjalani
splenektomi tetap pada resiko besar untuk sepsis meskipun profilaksis. Imunisasi adalah
wajib dengan Hib konjugasi polisakarida dan vaksin pneumokokus dan vaksin
meningokokus dengan tak terkonjugasi. 10
Pasca pajanan profilaksis untuk varicella ditunjukkan. Varicella-zoster immune
globulin diberikan dalam waktu 48 jam jika mungkin, meskipun mungkin berlaku sampai
96 jam pasca pajanan. Di luar waktu itu, asiklovir dianjurkan selama masa inkubasi.
Pasien dengan eksim parah berada pada risiko untuk kedua infeksi diseminata varicella-
zoster dan herpeticum eksim. Perawatan yang tepat untuk kedua adalah lisan asiklovir. 10
Mengelola perdarahan akut dengan transfusi trombosit dan eritrosit penuh. Semua
produk darah harus leukosit bebas dan disaring untuk menghindari transmisi virus
sitomegalo (CMV), selain skrining rutin untuk human immunodeficiency virus (HIV) dan
virus hepatitis. Meminimalkan paparan sel alogenik pada pasien untuk siapa
membendung pemulihan sel direncanakan penting karena eksposur tersebut menambah
tingkat penolakan korupsi. Trombosit memiliki kelangsungan hidup lebih pendek pada
sindrom Wiskott-Aldrich dari pada orang sehat. Episode berulang perdarahan yang
signifikan telah dikelola oleh splenektomi ketika pemulihan kekebalan bukanlah pilihan.
39

Splenektomi adalah prosedur kontroversial karena meningkatkan risiko infeksi dengan
organisme dienkapsulasi. 10
Mengobati eksim dengan konvensional krim pelembab topikal dan steroid topikal.
Susu dan lain alergen makanan potensial dapat dihilangkan dari diet pada percobaan
dasar untuk mengamati untuk perbaikan. Eksim sering bertambah dan berkurang tanpa
pemicu yang jelas, meskipun beberapa pasien terlihat memperbaiki selama terapi
antibiotik. Rinitis alergi dan asma diperlakukan dengan cara yang sama seperti pada
individu imunokompeten. Herpeticum eksim diobati dengan acyclovir oral. 10
Mengelola anemia hemolitik autoimun (AIHA) dan gangguan autoimun lain pada
individu imunokompeten. Menariknya, dosis tinggi IVIG tidak mungkin memiliki
manfaat dalam AIHA atau trombositopenia kekebalan tubuh. 10
PERAWATAN BEDAH
Intervensi bedah mungkin diperlukan untuk komplikasi perdarahan. Splenektomi
merupakan pilihan untuk pasien yang trombositopenia berat dan perdarahan sering hidup
berdampingan dan untuk siapa membendung pemulihan sel tidak dianggap. Namun,
splenektomi menciptakan resiko tambahan untuk sepsis yang fatal luar biasa dan
meninggalkan pasien pada risiko komplikasi lanjutan untuk keganasan. 10
KOMPLIKASI
Komplikasi dari perdarahan dan infeksi sekarang telah menurun karena
pengenalan yang lebih baik dan intervensi pengobatan dini. 10
PROGNOSIS
Rata-rata usia hidup pasien dengan sindrom Wiskott-Aldrich pada tahun 1994
adalah 11 tahun, sedangkan kematian selama tahun 1960 terjadi dalam waktu 4 tahun.
Kajian yang lebih mutakhir menunjukkan usia rata-rata kelangsungan hidup berada di
sekitar 15 tahun. Prospek untuk pasien yang berhasil ditransplantasikan jauh lebih tinggi.
Penyakit Granulomatosa Kronis
40

Penyakit Granulomatosa kronis (CGD) merupaka kelainan bawaan sel fagositik,
hasil dari ketidakmampuan fagosit untuk menghasilkan anion superoksida bakterisida (O 2 -). Hal ini menyebabkan berulang mengancam nyawa infeksi bakteri dan jamur. 14
Penyakit granulomatosa kronis sekarang diketahui disebabkan oleh cacat dalam
nikotinamida adenin dinukleotida fosfat (NADPH), mengurangi bentuk, kompleks enzim
oksidase fagosit. Penyakit granulomatosa kronis mengacu pada karakteristik granuloma
yang berkembang sebagai respon terhadap peradangan kronis. 14
PATOFISIOLOGI
Penyakit granulomatosa kronis yang disebabkan oleh cacat dalam oksidase
NADPH fagositik, yang bertanggung jawab untuk memproduksi O 2 -. Ini anion
superoksida kemudian diubah menjadi oksidan reaktif yang relatif bakterisida, seperti
hidroksil radikal - peroksida, hidrogen (H 2 O 2), anion peroxynitrite (ONOO -) (OH), dan
oxyhalides (Hox -, di mana X adalah bagian yang paling umum klorin). Anion
superoksida dihasilkan dengan mentransfer elektron dari NADPH berkurang menjadi
molekul O 2 dalam menanggapi rangsangan fisiologis, seperti fagositosis. Reaksi ini
diperantarai oleh NADPH oksidase fagosit atau dikenal sebagai oksidase fagosit (Phox).14
Sistem Phox adalah enzim kompleks NADPH oksidase yang terdiri dari 5
komponen protein. Glikoprotein 91 (gp91) dan protein 22 (p22) membentuk b dan
subunit dari membran terikat heterodimer disebut sebagai flavocytochrome b558. Protein
47 (p47), protein (P67), dan protein 40 (p40) ada bersama sebagai komponen sitosol dari
Phox. Komponen yang terikat membran (gp91 dan p22) dan sitosol (p47, P67, dan p40)
berkumpul di membran phagolysosome dalam menanggapi rangsangan inflamasi seperti
fagositosis. Kompleks enzim dirakit mengangkut elektron dari NADPH sitosol melewati
membran ke molekul oksigen di dalam phagolysosome untuk menghasilkan radikal
superoksida dan lebih beracun lainnya, seperti hidrogen peroksida dimediasi oleh
superoksida dismutase dan Hox. 14
Cacat molekul yang paling umum pada penyakit granulomatous kronis adalah
mutasi pada gen (sitokrom B, b subunit) CYBB yang terletak pada kromosom X dan yang
mengkodekan untuk gp91 (subunit b sitokrom b558). Sindrom yang dihasilkan biasa
disebut X-linked granulomatosa penyakit kronis (X-CGD). Gp91 kekurangan
41

menyumbang 50-70% dari semua kasus penyakit granulomatosa kronis. Lebih dari 350
mutasi pada gen CYBB diketahui, dan sejauh ini, semua yang unik untuk setiap keluarga.
Data dari analisis menunjukkan bahwa pembawa mutasi de novo terjadi pada sekitar 10%
kasus. 14
Mutasi kedua yang paling umum terjadi pada gen pada kromosom 7 NCF1 yang
mengkodekan untuk p47. Mutasi ini adalah bentuk paling umum resesif autosomal dari
penyakit, terhitung 20-40% dari semua kasus penyakit granulomatosa kronis. Tidak
seperti CYBB yang memiliki lebih dari 350 mutasi, mutasi NCF1 sangat kekal untuk
penghapusan tunggal di lebih dari 90% pasien. 14
Mutasi pada gen NCF2 (yang mengkode P67) dan CYBA (yang mengkode p22)
jarang terjadi, terhitung kurang dari 10% dari semua kasus penyakit granulomatosa
kronis. Kedua hasil mutasi pada bentuk resesif autosomal penyakit granulomatosa kronis.
Sekitar 95% dari mutasi tersebut di atas mengakibatkan tidak lengkap atau tingkat sangat
berkurang dari protein yang terkena. Dalam 5%, tingkat normal protein cacat yang
dihasilkan. The 4 bentuk penyakit yang disebut sebagai X91 (X-linked, gp91), A22
(autosomal, p22), A47, dan A67 CGD. The + superscript, -, atau o ditambahkan untuk
menunjukkan tingkat normal, penurunan tingkat, atau tidak lengkap dari subunit yang
terkena. 14
Kurang dari 10% pasien memiliki bentuk X-linked varian dari CGD (X91 -), yang
memiliki perjalanan klinis yang relatif ringan. Sebagian besar pasien ini memiliki tingkat
rendah tetapi terdeteksi flavocytochrome b588, dan fagosit mereka dapat menghasilkan
sejumlah terukur superoksida. Cacat pada p47 juga tampaknya dikaitkan dengan
kekurangan enzimatik dan klinis kurang pentingnya daripada yang diamati dalam bentuk
lain. Diagnosis di masa dewasa tidak jarang pada pasien dengan aktivitas Phox sisa. 14
EPIDEMIOLOGI
Frekuensi
Amerika Serikat
42

Insiden pasti penyakit granulomatosa kronis tidak diketahui. Analisis data yang diajukan
ke registri nasional menunjukkan bahwa kejadian penyakit granulomatosa kronis di
Amerika Serikat adalah sekitar 1 kasus per 200,000-250,000 populasi (sebanyak 20
pasien dengan penyakit granulomatosa kronis yang lahir setiap tahun), tanpa ras jelas
atau etnis kegemaran. 14
Internasional
Survei dari Belanda dan bagian lain dunia menunjukkan frekuensi sekitar 1 kasus di
220,000-500,000 populasi. 14
\
Mortalitas / Morbiditas
Sebuah studi rinci tentang riwayat alami penyakit granulomatosa kronis tidak
tersedia. Data registri menunjukkan bahwa kedua angka kesakitan dan angka kematian
tertinggi pada pasien dengan bentuk X-linked penyakit. Sejumlah besar pasien di registri
meninggal selama dekade kedua dan ketiga kehidupan, meskipun beberapa selamat di
luar dekade keempat. Sekitar 80% pasien masih hidup di 5 tahun setelah mereka masuk
dalam registri. Bahkan di era modern perawatan untuk penyakit ini, data sporadis
menunjukkan kelebihan potensi dalam mortalitas pada individu yang berusia 10-30
tahun. 14
Ras
Tidak ada predileksi ras dikenal. 14
Seks
Sekitar dua pertiga kasus diwariskan sebagai X-linked cacat, dan sisa kasus diwariskan
dalam mode resesif autosomal. Dari 368 pasien dari 318 segala suku dilaporkan ke
registri penyakit granulomatosa kronis, 316 (86%) adalah laki-laki. 14
Usia
Meskipun sebagian besar dari individu yang terkena hadir dengan infeksi pada
anak usia dini, beberapa laporan menggambarkan pasien yang terkena gejala yang
43

menjadi lambat ini. Penyakit granulomatosa kronis mungkin tidak terdiagnosis pada
beberapa pasien karena mereka memiliki fenotip klinis ringan. 14
PEMERIKSAAN FISIK
Uraian awal anak dengan penyakit granulomatosa kronis yang ditandai sebagai
yang mengalami limfadenopati, hepatosplenomegali, kegagalan pertumbuhan, dan
stigmata dari infeksi kulit kronis. 14
Temuan fisik yang diamati kurang umum sekarang daripada sebelumnya karena
kebanyakan pasien diidentifikasi dan dirawat di awal masa bayi atau masa kanak-kanak. 14
Pasien yang terinfeksi kadang-kadang hadir tanpa gejala khas infeksi (yaitu,
demam, leukositosis). 14
DIAGNOSIS DIFERENSIAL
Bruton agammaglobulinemia
Variabel umum Immunodeficiency
Melengkapi Kekurangan
Manusia Infeksi Virus Immunodeficiency
Hyperimmunoglobulinemia E (Ayub) Sindrom
Leukosit Adhesi Defisiensi
Parah Gabungan Immunodeficiency
Wiskott-Aldrich Syndrome 14
LABORATORIUM
Tes-tes berikut diindikasikan pada penyakit granulomatosa kronis (CGD):
Nitroblue tetrazolium (NBT) tes
Uji standar untuk aktivitas oksidase fagositosis adalah tes NBT. Para NBT
senyawa tidak berwarna dikurangi menjadi formazan biru oleh aktivitas sistem
enzim Phox. Beberapa versi dari tes ada; masing-masing memiliki kelebihan dan
kekurangan.
Dihydrorhodamine (DHR) tes
44

Prenatal diagnosis
Diagnosis prenatal untuk saudara kandung dari pasien yang terkena dapat dicapai
dalam satu dari dua cara. Ketika mutasi yang tepat diidentifikasi pada anak yang
terkena dampak, chorionic villus biopsi dapat dilakukan untuk mendapatkan DNA
yang cukup untuk mengidentifikasi janin yang terkena. Sebagai alternatif,
polimorfisme yang berulang dinukleotida terkait dengan gen CYBB mungkin
berguna dalam diagnosis prenatal X-CGD. 14
PENATALAKSANAAN
Profilaksis antimikroba, pengobatan dini dan agresif dari infeksi, dan interferon-
gamma merupakan landasan terapi saat ini penyakit granulomatosa kronis (CGD). sel
induk hematopoietik transplantasi (HSCT) dari antigen leukosit manusia (HLA)-yang
kompatibel donor dapat menyembuhkan granulomatosa kronis penyakit. Namun,
pendekatan ini penuh dengan morbiditas yang signifikan secara klinis dan risiko hingga
kematian. HSCT tetap merupakan modalitas terapi yang kontroversial dalam penyakit ini,
bahkan ketika sel induk dari donor saudara kandung yang cocok tersedia. 14
o Interferon-gamma sekarang direkomendasikan sebagai terapi seumur hidup untuk
profilaksis infeksi pada penyakit granulomatosa kronis. 14
Kuratif pendekatan (HSCT) 14
HSCT adalah modalitas terapeutik kuratif hanya saat ini tersedia untuk penyakit ini.
Sedikitnya 24 pasien yang telah menjalani HSCT untuk penyakit granulomatosa kronis
dilaporkan Registry Bone Marrow Transplant Internasional Pusat Internasional Darah
dan Sumsum Penelitian Transplantasi (CIBMTR). Laporan kasus beberapa HSCTs
berhasil dipublikasikan dalam literatur. [10]
Karena kurangnya transplantasi dilakukan sampai saat ini, penilaian bermakna dari
kemungkinan hasil yang sukses setelah HSCT pada penyakit granulomatosa kronis tidak
dapat dibuat.
Transplantasi dengan sumsum tulang saudara cocok atau darah tali pusat mungkin
akan paling berhasil jika dilakukan pada masa bayi atau anak usia dini, ketika risiko
kematian akibat infeksi atau penyakit graft versus host adalah minimal. Namun, bahkan
dalam situasi seperti ini, resiko kecil tapi terbatas kematian dari HSCT dicatat. Risiko ini
45

telah menyebabkan keengganan di kalangan dokter yang merawat dalam
merekomendasikan atau menggunakan prosedur terapeutik.
Terapi gen 14
Terapi gen untuk penyakit granulomatosa kronis yang menarik untuk berbagai
alasan. Cacat genetik yang tepat biasanya dapat diidentifikasi. Sel-sel yang tidak
memiliki produk gen fungsional dan prekursor mereka dapat diakses dalam darah atau
sumsum tulang. Karena pembawa X-CGD jarang bergejala, kecuali kurang dari 10% dari
fagosit mengekspresikan gen normal untuk gp91, koreksi stabil hanya 5-10% dari fagosit
beredar mungkin cukup untuk secara substansial meningkatkan hasil klinis.
Kerugian utama dari penyakit granulomatosa kronis sebagai penyakit kandidat untuk ter
api gen adalah bahwa sel-sel gen yang dimodifikasi tidak memiliki keuntungan
selektif lebih rusak sel inang. Hal ini karena gen Phox diperlukan hanya dalam fagosit
tersembuhkan dibedakan.
Hasil yang dipublikasikan dari terapi gen pada penyakit granulomatosa kronis
berasal dari penelitian hewan, dalam studi in vitro sel berasal dari sumsum tulang
manusia, dan laporan transfer angkat ex vivo dimodifikasi sel ke pasien manusia. Sebuah
laporan pada dua pasien yang menjalani berkurang intensitas pengkondisian transplantasi
dan transfer gen menyebabkan peningkatan dalam aktivitas yang menghasilkan
superoksida fagosit. [11] Jangka panjang tindak lanjut penelitian yang diperlukan untuk
mendokumentasikan keamanan dari penyisipan gen dan kemungkinan efek merusak.
Dengan teknik saat ini, sementara sebagian koreksi dari cacat fagosit dapat dibuat
sebagai tambahan untuk terapi medis infeksi akut atau kronis. Namun, koreksi signifikan
secara klinis tahan lama penyakit granulomatosa kronis dengan terapi gen menunggu
diperbaiki metode untuk transfer gen, menargetkan sel-sel induk hematopoietik, dan
pengendalian ekspresi genetik. Ketika masalah ini diselesaikan, terapi gen aman praktis
akan menjadi pilihan perawatan untuk penyakit granulomatosa kronis.
PROGNOSIS
Prognosis untuk pasien dengan penyakit granulomatosa kronis telah meningkat
selama 2 dekade terakhir. Meskipun tidak ada studi formal tentang sejarah alami dari
penyakit ini telah dilakukan, durasi kelangsungan hidup saat ini rata-rata untuk pasien
46

dengan penyakit granulomatosa kronis diperkirakan sekitar 20-25 tahun, dengan angka
kematian sebesar 2-3% per tahun. Angka kematian tertinggi adalah pada anak usia dini.
Penyebab biasa kematian adalah infeksi. Namun, penyakit granulomatosa kronis
memiliki heterogenitas klinis yang signifikan dalam tingkat keparahan penyakit pada
pasien yang terkena. .
Kandidiasis Mukokutaneus Kronis
Kandidiasis mukokutan kronis (CMC) mengacu pada sekelompok heterogen
gangguan yang ditandai oleh infeksi superfisial berulang atau persisten pada kulit,
membran mukosa, dan kuku dengan organisme Candida, biasanya Candida albicans
Gangguan ini terbatas pada permukaan kulit,dengan kecenderungan sedikit untuk
sistemik diseminasi. CMC tidak mewakili penyakit tertentu, melainkan presentasi
fenotipik spektrum kekebalan, endokrinologik, dan gangguan autoimun. Fitur pemersatu
dari gangguan heterogen terganggu diperantarai sel kekebalan terhadap spesies Candida.
Gambar di bawah menggambarkan CMC pada kuku. 16
Menebal, terfragmentasi, hiperkeratotik kuku dan kulit eritematosa periungual.
Courtesy of Walter Reed Army Medical Center.
PATOFISIOLOGI
Candida albicans adalah ragi oportunistik yang merupakan bagian dari flora
normal pada saluran pencernaan, kulit, dan selaput lendir. Jamur bisa ada di ragi,
(pseudohyphal) miselium, atau fase chlamydospore. Penyakit invasif adalah jarang,
namun ketika itu terjadi, biasanya berhubungan dengan elemen miselium. Beberapa
faktor tuan rumah adalah penting dalam mempertahankan terhadap infeksi oleh
organisme candida. Sehat, kulit utuh yang terus desquamates dan melahirkan kembali
47

biasanya merupakan penghalang awal yang efektif. Sistem kekebalan tubuh utuh sangat
penting untuk menjaga ini organisme oportunistik di teluk. 16
CMC dikaitkan dengan cacat dalam imunitas diperantarai sel yang baik mungkin
terbatas terhadap antigen Candida atau menjadi bagian dari kelainan kekebalan yang
lebih umum. Data terakhir menunjukkan perubahan dalam produksi sitokin sebagai
respon terhadap antigen Candida. Perubahan ini termasuk interleukin menurun 2 dan
interferon-gamma level (T H 1 sitokin) dan peningkatan interleukin 10 tingkat dalam
beberapa studi. [1, 2] Pasien yang kekurangan kekebalan sel-T (misalnya, mereka dengan
sindrom defisiensi imun berat gabungan atau DiGeorge Sindrom) atau pasien dengan
sangat terganggu fungsi sel T (misalnya, pasien dengan AIDS) rentan terhadap infeksi
candida kronis. Cacat dalam imunitas humoral tidak umum diamati pada pasien dengan
CMC, dan pasien dengan defisiensi antibodi tidak terlalu rentan terhadap kandidiasis. 16
EPIDEMIOLOGI
Mortalitas / Morbiditas
CMC tidak terkait dengan tingkat kematian yang tinggi karena infeksi kandida
invasif disebarluaskan jarang terjadi. Dalam CMC yang terisolasi, prognosisnya baik,
namun morbiditasnya signifikan terkait dengan kulit kronis dan persisten, kuku, dan
infeksi selaput lendir candida. Risiko dari aneurisma mikotik, walaupun rendah, tetap
dapat menjadi kemungkinan yang nyata. [4] Dalam sebuah subset dari pasien, thymoma
ganas atau kanker rongga mulut dan saluran pencernaan dapat terjadi. Pasien dengan
distrofi polyendocrinopathy-kandidosis-ectodermal autoimun (APECED) memiliki
morbiditas yang signifikan dari endokrinopati atau penyakit autoimun lainnya terkait
dengan kondisi ini. Beberapa kasus pneumonia Pneumocystis carinii pada pasien dengan
CMC dilaporkan dalam literatur. 16
Ras
Tidak ada predileksi rasial dilaporkan untuk CMC, meskipun APECED yang paling
umum di Finlandia, Sardinia, dan populasi Yahudi Iran. 16
Seks
48

Rasio laki-perempuan untuk CMC sama. 16
Usia
CMC biasanya memanifestasikan pada masa bayi atau anak usia dini (60-80% kasus),
dengan usia rata-rata onset 3 tahun. Onset tertunda atau orang dewasa penyakit ini
dilaporkan dan dapat dikaitkan dengan timoma, myasthenia gravis, dan kelainan sumsum
tulang. 16
GEJALA KLINIS
Pasien datang dengan infeksi kandida superfisial berulang atau berkelanjutan dari
rongga mulut (sariawan) atau daerah intertriginosa atau periorificial. Bayi sering hadir
dengan sariawan bandel, dermatitis popok candida, atau keduanya. Skala yang lebih luas
dari lesi kulit dan kuku menebal dan merah, bengkak jaringan periungual dapat mengikuti
infeksi ini. 16
Kandidiasis sistemik dan dermatitis jamur invasif, meskipun jarang, biasanya
terjadi pada bayi prematur, terutama yang dengan berat lahir sangat rendah. 16
Infeksi candida yang berulang dan tahan api, yang mencirikan CMC, harus
dibedakan dari pertumbuhan berlebih lebih umum dan pengobatan responsif Candida
yang terjadi dalam pengaturan terapi antibiotik sistemik, lokal / sistemik pengobatan
kortikosteroid, atau hiperglikemia pada penderita diabetes mellitus. 16
PEMERIKSAAN FISIK
CMC didiagnosa berdasarkan temuan pemeriksaan fisik, pemeriksaan kalium
klorida (KOH), kultur jamur, dan riwayat infeksi kandidiasis berulang dan tahan api.
Pemeriksaan oral dapat mengungkapkan plak putih atau sariawan cheilitis angular
perlèche. Keterlibatan oral dapat menjalar sampai ke esofagus, tetapi penjalaran ini
sangat jarang. 16
Kuku dapat menebal, terfragmentasi, dan berubah warna, dengan edema dan
eritema yang signifikan dari jaringan periungual sekitarnya, simulasi clubbing (lihat
gambar pertama di bawah). 16
49

Lesi kulit lebih sering adalah acral dan ditandai dengan eritematosa,
hiperkeratotik, plakat serpiginous (lihat gambar kedua di bawah). 16
Kulit kepala mungkin terlibat dengan plak hiperkeratotik serupa, yang dapat
mengakibatkan jaringan parut alopecia (lihat gambar ketiga di bawah). 16
Menebal, terfragmentasi, hiperkeratotik kuku dan kulit eritematosa periungual.
Courtesy of Walter Reed Army Medical Center.
Berkulit hiperkeratotik plak pada dan di sekitar hidung.
Courtesy of Walter Reed Army Medical Center.
Berkulit hiperkeratotik plak pada alis, dahi kulit kepala, dan.
Courtesy of Walter Reed Army Medical Center.
Sebuah subset dari pasien CMC memiliki infeksi noncandidal berulang atau berat,
termasuk dari jamur patogen virus, bakteri, dan lainnya. Beberapa pasien dengan CMC
50

memiliki tingkat rendah zat besi serum dan penurunan toko besi, kemungkinan
berhubungan dengan penyerapan zat besi menurun. Pengganti besi harus dimulai pada
pasien ini. Beberapa pasien dilaporkan telah membaik setelah terapi besi parenteral.
Beberapa klasifikasi ada untuk CMC. Para penulis mengkategorikan CMC berdasarkan
hubungannya dengan kondisi lain. 16
CMC tanpa endokrinopati16
o Kategori ini terdiri dari spektrum presentasi klinis.
o Warisan mungkin autosomal resesif atau dominan, tetapi banyak kasus sporadis.
o Onset adalah di masa kecil, dan tidak terkait endokrin atau gangguan autoimun
yang diamati.
CMC dengan endokrinopati16
o CMC dapat terjadi sebagai bagian dari sindrom autoimun polyendocrinopati tipe 1
( Pewarisan Mendel Online di Man # 240300 ), juga dikenal sebagai APECED. [6]
APECED ditandai oleh minimal 2 dari berikut: CMC, hipoparatiroidisme, dan
penyakit Addison. Gangguan autoimun lainnya dapat berhubungan, seperti,
diabetes tipe 1, tiroiditis autoimun, penyakit Graves, alopecia areata, vitiligo,
hipogonadisme, sirosis bilier, hepatitis, idiopatik purpura thrombocytopenic,
dan anemia pernisiosa.
APECED diwariskan dalam mode resesif autosomal dan biasanya
bermanifestasi awal di masa kecil. Hal ini disebabkan oleh mutasi pada gen
regulator autoimun (Aire) pada 21q22.3, yang mengkode protein yang
memainkan peran penting dalam membangun dan memelihara toleransi di
timus. [7]
Sebuah penelitian baru menemukan bahwa pasien APECED memiliki cacat
reseptor-mediated internalisasi Candida, yang menyebabkan perubahan
Candida spesifik respon imun. [6]
Kandidiasis sering manifestasi pertama APECED, muncul sebelum usia 5
tahun dalam banyak kasus, diikuti oleh manifestasi dari endokrin lainnya dan
kondisi nonendocrine, termasuk ectodermal displasia. Ectodermal displasia
manifestasi termasuk gigi enamel hipoplasia dan distrofi kuku diadu.
Keratopati dan kalsifikasi dari membran timpani juga dapat terjadi.
51

Sebuah tinjauan 2006 dari 18 pasien APECED ditemukan kandidiasis pada
semua pasien sebagai gejala menyajikan, dan peneliti menyimpulkan bahwa
distrofi ectodermal biasanya hanya terjadi sebagai fenomena sekunder. [7]
Tidak ada korelasi ada antara keparahan endocrinopathy dan tingkat
keparahan infeksi candida. Perawatan dari endocrinopathy mendasari biasanya
tidak meningkatkan infeksi candida.
o CMC dapat berhubungan dengan penyakit tiroid. Sebuah CMC dominan
autosomal yang terkait dengan penyakit tiroid telah dipetakan ke 2p. [8]
CMC dengan timoma 16
o Pasien dalam subkelompok ini biasanya hadir setelah dekade ketiga kehidupan.
o Pasien-pasien ini mengalami peningkatan risiko myasthenia gravis dan kelainan
sumsum tulang.
CMC dengan kondisi lain 16
o CMC dapat dilihat pada pasien dengan sindrom hyperimmunoglobulin e.
o Kandidiasis oral rekuren tidak jarang pada pasien dengan infeksi HIV.
ETIOLOGI
CMC terjadi pada kelompok heterogen pasien dengan spektrum yang luas dari disregulasi
imun, mulai dari Candida spesifik imunitas menurun menjadi cacat kekebalan tubuh yang
lebih luas. 16
DIAGNOSIS DIFERENSIAL
Kandidiasis, Cutaneous
Kandidiasis, mukosa
DiGeorge Syndrome
Parah Gabungan Immunodeficiency 16
LABORATORIUM
52

Ketika seorang pasien menyajikan dengan kulit manifestasi dari CMC, studi berikut
harus dilakukan:
o Mengorek dari situs yang terinfeksi tersuspensi dalam 10-20% KOH dan
mikroskopis diperiksa. Kehadiran sel ragi dan pseudohifa menegaskan diagnosis.
Noda jamur, seperti E hitam chlorazol noda atau Parker biru-hitam tinta, dapat
ditambahkan untuk menyoroti organisme.
o Organisme candida tumbuh baik pada media kultur beberapa. Mereka tumbuh
sebagai ragi pada agar Sabouraud dengan kloramfenikol dan cycloheximide C
albicans juga. Tumbuh pada medium uji dermatofit tetapi tidak menunjukkan
perubahan karakteristik warna merah dermatofit.
o Skrining tes laboratorium untuk disfungsi endokrin CMC terkait termasuk
glukosa darah atau tes hemoglobin glikosilasi, tes fungsi tiroid, fungsi hati tes,
serum evaluasi elektrolit, pengujian kortikotropin, dan nilai kortisol serum.
Pertimbangkan jumlah sel darah lengkap, untuk layar untuk leukopenia, dan tes
HIV. Tes skrining lainnya endokrin yang dapat dianggap termasuk follicle-
stimulating hormon, hormon luteinizing, prolaktin, testosteron, paratiroid-
stimulating hormone, kalsium, fosfat, magnesium, dan uji synacthen pendek.
Lakukan tes awal dan tahunan tindak lanjut untuk layar untuk endocrinopathy
terkait. 16
Tes lainnya
Hasil dari tes imunitas selular, seperti uji tusuk-dengan antigen Candida, mungkin
negatif. In vitro proliferasi limfosit biasanya dikurangi untuk ekstrak C albicans. 16
Kekurangan imunoglobulin G subclass telah dilaporkan pada beberapa pasien
dengan CMC, yang memiliki predisposisi terhadap infeksi saluran pernapasan.
Imunoglobulin terisolasi A dan kekurangan imunoglobulin M juga telah dilaporkan,
selain satu kasus agammaglobulinemia lengkap. 16
Pada pasien dengan infeksi berulang lainnya, studi kekebalan tubuh harus
dipertimbangkan. 16
Jika kecurigaan klinis untuk APECED tinggi, analisis genetik dari gen Aire dapat
konfirmasi. 16
53

Baru, anti-interferon-1 antibodi yang ditemukan menjadi sangat spesifik untuk
APECED dan mendahului munculnya CMC, menunjukkan tes diagnostik yang penting
baru. 16
Temuan histologis
Rutin hematoxylin dan eosin bernoda bagian lesi kandidiasis superfisial
mengungkapkan pustula subcorneal. Lesi granulomatosa CMC menunjukkan
hiperkeratosis dan parakeratosis, dengan kulit campuran padat menyusup mengandung
limfosit dan sel plasma. Noda asam Schiff atau perak periodik spesimen biopsi kulit
dapat membantu mengidentifikasi organisme dalam stratum korneum dan dermis. 16
PENATALAKSANAAN
Manajemen bisa sulit, dan kekambuhan umum terjadi setelah penghentian terapi.
Terapi topikal tidak biasanya efektif pada pasien dengan CMC. Pengobatan keterlibatan
oral pada CMC bisa dibantu dengan terapi dengan clotrimazole troches atau larutan
nistatin oral. Pengobatan jatuh menjadi 3 kategori utama: agen anti jamur, terapi
imunologi, dan terapi kombinasi. 16
Terapi antijamur sistemik adalah terapi utama CMC. Ini dapat digunakan sendiri
atau dalam kombinasi dengan agen imunomodulator. Kelemahan dari terapi antijamur
sistemik termasuk risiko efek samping atau toksisitas, kegagalan untuk memperbaiki
defisiensi imun yang mendasari, kambuh setelah penghentian terapi, dan resistensi anti
jamur untuk beberapa agen antijamur. 16
Terapi imunologi telah diajukan dalam upaya untuk memperbaiki defisiensi imun
yang mendasari pada orang dengan CMC. Pengobatan yang paling sering diteliti adalah
penggunaan transfer factor. Transfer factor adalah protein bebas sel diekstrak dari
limfosit T Candida-imun donor. Meskipun mekanisme yang tepat belum diketahui, telah
ditunjukkan untuk mentransfer tertunda-jenis reaksi hipersensitivitas terhadap pasien
yang sebelumnya anergic untuk uji kulit candida. 16
2. Penatalaksanaan AIDS ?
54

PrinsipART
Prinsip pengobatan antiretroviral atau ART secara umum adalah sebagai berikut:
TujuanPengobatanARV:
1) Mengurangi laju penularan HIV di masyarakat
2) Memulihkan dan/atau memelihara fungsi imunologis (stabilisasi/peningkatanselCD4)
3) Menurunkan komplikasi akibat HIV
4) Memperbaiki kualitas hidup ODHA
5) Menekan replikasi virus secara maksimal dan secara terus menerus
6) Menurunkan angka kesakitan dan kematian yang berhubungan dengan HIV
Manfaat ART
Antiretroviral merupakan suatu revolusi dalam perawatan ODHA. Terapi dengan
antiretroviral atau disingkat ARV telah menyebabkan penurunan angka kematian dan kesakitan
bagi ODHA. Manfaat terapi antiretroviral adalah sebagai berikut:
1) Menurunkan morbiditas dan mortalitas
2) Pasien dengan ARV tetap produktif
3) Memulihkan sistem kekebalan tubuh sehingga kebutuhan profilaksis infeksi
oportunistik berkurang atau tidak perlu lagi
4) Mengurangi penularan karena viralload menjadi rendah atau tidak terdeteksi, namun
ODHA dengan viralload tidak terdeteksi, namun harus dipandang tetap menular
5) Mengurangi biaya rawat inap dan terjadinya yatim piatu
6) Mendorong ODHA untuk meminta tes HIV atau mengungkapkan status HIV-nya
secara suka rela
Pengetahuan Dasar Penggunaan ARV
ART atau antiretroviral sampai saat ini merupakan satu-satu obat yang memberikan
manfaat besar dalam pengobatan ODHA. Namun penggunaan ARV menuntut adherence dan
kesinambungan berobat yang melibatkan peran pasien, dokter atau petugas kesehatan,
pendamping dan ketersediaan obat. Beberapa hal khusus yang harus diperhatikan dalam
55

penggunaan antiretroviral adalah sebagai berikut:
1) Replikasi HIV sangat cepat dan terus menerus sejak awal infeksi, sedikitnya
terbentuk sepuluh milyar virus setiap hari, namun karena waktu paruh(halflife) virus
bebas(virion) sangat singkat, maka sebagian besar virus akan mati. Walau ada
replikasi yang cepat, sebagian pasien merasa tetap sehat tanpa ART selama
kekebalan tubuhnya masih berfungsi dengan baik.
2) Replikasi yang terus menerus mengakibatkan kerusakan sistem kekebalan tubuh
semakin berat, sehingga semakin rentan terhadap infeksi oportunistik (IO), kanker,
penyakit saraf, kehilangan berat badan secara nyata (wasting) dan berakhir dengan
kematian.
3)Viralload menunjukkan tingginya replikasi HIV sehingga penurunan CD4
menunjukkan kerusakan sistem kekebalan tubuh yang disebabkan oleh HIV.
4) Nilai viral load menggambarkan progresivitas penyakit dan risiko kematian.
Pemeriksaan secara berkala jumlah CD4 dan viral load (jika memungkinkan) dapat
menentukan progresivitas penyakit dan mengetahui syarat yang tepat untuk memulai
atau mengubah rejimen ART.
5)Tingkat progresivitas penyakit pada ODHA dapat berbeda-beda. Keputusan
pengobatan harus berdasarkan pertimbangan individual dengan memperhatikan
gejala klinik, hitung limfosit total dan bila memumgkinkan jumlah CD4.
6) Terapi kombinasi ART dapat menekan replikasi HIV hingga di bawah tingkat
yangtidak dapat dideteksi oleh pemeriksaan yang peka(PCR). Penekanan virus
secara efektif ini mencegah timbulnya virus yang resisten terhadap obat dan
memperlambat progresivitas penyakit. Jadi tujuan terapi adalah menekan
perkembangan virus secara maksimal.
7) Cara paling efektif untuk menekan replikasi HIV secara terus menerus adalah
memulai pengobatan dengan kombinasi ARV yang efektif. Semua obat yang
dipakai harus dimulai pada saat yang bersamaan pada pasien yang baru. Pada pasien
yang tidak pernah diterapi, tidak boleh menggunakan obat yang memiliki resistensi
silang dengan obat yang pernah dipakai.
8) Terapi kombinasi ARV harus menggunakan dosis dan jadual yang tepat.
56

9) Prinsip pemberian ART diperlakukan sama pada anak maupun dewasa,
walaupun pengobatan pada anak perlu perhatian khusus.
10)Walaupun viral load tidak terdeteksi, ODHA yang mendapat ART harus tetap
dianggap menular.Mereka harus dikonseling agar menghindari seks yang tidak
aman, atau penggunaan NAPZA suntik yang dapat menularkan HIV atau patogen
menular lain.
11)Untuk menghindari timbulnya resistensi, ART harus dipakai terus menerus dengan
kepatuhan (adherence) yang sangat tinggi, walaupun sering dijumpai efek samping
ringan.
12)Pemberian ART harus dipersiapkan secara baik dan matang dan harus
digunakan seumur hidup.
13)Disamping ART,makai nfeksi oportunistik harus pula mendapat perhatian dan harus
diobati.
Memulai ART pada ODHA Dewasa
A. Prasyarat
Sebelum memulai ART, sebaiknya tersedia layanan dan fasilitas khusus karena terapi
yang rumit dan biaya tinggi, perlu pemantauan yang intensif:
Layanan tersebut terdiri dari:
1)Layanan konseling dan pemeriksaan sukarela(VoluntaryCounselingAnd
Testing/VCT) untuk menemukan kasus yang memerlukan pengobatan dan layanan
konseling tindak-lanjut untuk memberikan dukungan psikososial berkelanjutan.
2)Layanan konseling kepatuhan untuk memastikan kesiapan pasien menerima
pengobatan oleh konselor terlatih dan meneruskan pengobatan (dapat
diberikan melalui pendampingan atau dukungan sebaya).
3) Layanan medis yang mampu mendiagnosis dan mengobati penyakit yang sering
berkaitan dengan HIVserta infeksi oportunistik.
57

4) Layanan laboratorium yang mampu melakukan pemeriksaan laboratorium rutin
seperti pemeriksaan darah lengkap dan kimia darah. Akses ke laboratorium
rujukan yang mampu melakukan pemeriksaan CD4 bermanfaat untuk
memantau pengobatan.
5) Layanan kefarmasian untuk ODHA untuk memberikan ARV termasuk menjamin
ketersediaan ARVdan obat infeksi oportunistik serta penyakit terkait lain yang
efektif, bermutu, terjangkau dan berkesinambungan. Layanan Kefarmasian harus
mampu meningkatkan kepatuhan pasien dalam menggunakan ARV (adherence)
B. Penilaian Klinik
Sebelum memulai terapi, perlu dilakukan hal-hal sebagai berikut:
1) Penggalian riwayat penyakit secara lengkap
2) Pemeriksaan fisik lengkap
3) Pemeriksaan laboratorium rutin
4) Hitung limfosit total (Total Lymphocite Count/TLC) dan bila mungkin
pemeriksaan CD4.
Penilaian klinis yang mendukung adalah sebagai berikut:
1) Menilai stadium klinis infeksi HIV
2) Mengidentifikasi penyakit yang berhubungan erat dengan HIV di masa lalu
3) Mengidentifikasi penyakit yang terkait dengan HIV saat ini yang membutuhkan
pengobatan
4) Mengidentifikasi pengobatan lain yang sedang dijalani yang dapat
mempengaruhi pemilihan terapi
C. Riwayat Penyakit
Pertanyaan tentang riwayat penyakit meliputi:
58

1) Kapan dan dimana diagnosis HIV ditegakkan
2) Kemungkinan sumber infeksi HIV
3) Gejala dan keluhan pasien saat ini
4) Riwayat penyakit sebelumnya, diagnosis dan pengobatan yang diterima
termasuk infeksi oportunistik
5) Riwayat penyakit dan pengobatan TB termasuk kemungkinan kontak dengan TB
sebelumnya
6) Riwayat kemungkinan infeksi menular seksual (IMS)
7) Riwayat dan kemnugkinan adanya kehamilan
8) Riwayat penggunaan ART termasuk riwayat rejimen untuk PMTCT sebelumnya
9) Riwayat pengobatan dan penggunaan kontrasepsioral pada perempuan
10)Kebiasaan sehari-hari dan riwayat perilaku seksual
11)Riwayat penggunaan NAPZA suntik
D. Pemeriksaan Fisik
Pemeriksaan fisik yang dilakukan meliputi:
1) Berat badan,tanda vital
2)Kulit:herpe
szoster,sarkomaKaposi,dermatitisHIV,pruriticpapulareruption(PPE),dermatitissaborik
berat,jejassuntikan(needletrack)ataujejassayatan
3) Limfadenopati
4) Selaputlendirorafaringeal,kandidiasis,sarkomakaposi,hairyleukiplakia,HSV
5) Pemeriksaanjantung,parudanabdomen
6) Pemeriksaan sistemsarafdanototrangka;keadaankejiwaan,berkurangnya
fungsimotorisdansensoris
7) Pemeriksaanfundusmata:retinitisdanpapiledema
8) Pemeriksaansalurankelamin/alatkandungan
59

E. PemeriksaanPsikologis
SebelummemulaiterapiARV,perludilakukanpemeriksaanpsikologisdengan tujuan:
1) Untukmengetahuistatusmental
2) Menilaikesiapanmenerimapengobatanjangkapanjangatauseumurhidup
F. Pemeriksaan Laboratorium
Pemeriksaan laboratorium yang harus dilakukan sebelum memulai terapi
denganantiretroviraladalah:
1) Pemeriksaan serologi untuk HIV dengan menggunakan strategi 2 atau
strategi3sesuaipedoman
2) LimfosittotalatauCD4(jikatersedia)
3) Pemeriksaan darah lengkap (terutama HB) dan kimia darah (terutama
fungsihati)danfungsiginjal
4) Pemeriksaankehamilan
G. PemeriksaanTambahan
Adabeberapapemeriksaantambahanyangdiperlukansesuairiwayatpenyakit
danpemeriksaanklinisyaitu:
1) Fototoraks
2) Pemeriksaanurinrutindanmiksroskopik
3) Serologi virus hepatitis C(HCV) dan virus hepatitis B(HBV) tergantung
padaadanyapemeriksaandansumberdaya
Pemeriksaan HIV harus dilakukan oleh teknisi yang terlatih di laboratorium
yangmenjalankanprogramjaga mutu.Hasilpemeriksaansebaiknyajuga
menyebutkanjenis pemeriksaanyang dipakaiuntukmenegakkandiagnosis
berdasarkanpedomanWHO.Bilatimbulkeraguan,pemeriksaanharusdiulang
60

dilaboratoriumrujukan.
Jikamemungkinkan,profilkimiadarahdiperiksameliputi:
1) Kreatinin serum dan/atau ureum darah untuk menilai fungsi ginjal pada awal
2) Glukosadarah
3) SGOT/SGPT untuk mengetahui kemungkinan adanya hepatitis serta
memantauadanyakeracunanobat
4) Pemeriksaanlain bila perlusepertibilirubinserum,lipidserumdanamilase serum
H. PersyaratanLain
1) Sebelum mendapat ART, pasien harus dipersiapkan secara matang dengan
konseling kepatuhan yang telah baku, sehingga pasien paham
benarakanmanfaat,carapenggunaan, efeksampingobat,tandabahaya
laindansebagainyayangterkaitdenganART
2) Pasien yang mendapat ART harus menjalani pemeriksaan untuk
pemantauansecaraklinisdenganteratur
Indikasi ART
ODHA dewasa seharusnya segera mulai ART mana kala infeksi HIV telah ditegakkan
secara laboratories disertai salah satu kondisi berikut:
1. SecaraklinissebagaipenyakittahaplanjutdariinfeksiHIV:
2. InfeksiHIVstadiumIV,tanpamemandangjumlahCD4
3. InfeksiHIVstadiumIIIdenganjumlahCD4<350/mm3
4. InfeksistadiumIatauIIdenganjumlahCD4<200mm3
Artinya bahwa ART untuk penyakit stadium IV (kriteria WHO disebut AIDS
klinik)tidakseharusnya tergantung padajumlahCD4.Untukstadium III,bila
tersediasaranapemeriksaanCD4akansangatmembantu untukmenentukan saatpemberiaan
61

terapiyanglebihtepat.Tuberkulosis parudapattimbulpada tahapan dengan jumlah CD4 berapapun,
bila jumlah CD4 tersebut dapat terjagadenganbaik(misalnya>350/mm3),
makaterapidapatditundadengan meneruskan pemantauan pasien secara klinis. Nilai ambang
untuk kondisi Stadium III adalah 350/mm3 karena pada nilai nilai dibawahnya biasanya
kondisi pasien mulai menunjukkan perkembangan penyakit yang cepat
memburukdansesuaidenganpedomanyangada.Bagipasiendalamstadium Iatau II,maka jumlah
CD4<200/mm3 merupakan indikasi pemberian terapi. Apabilatidakada
saranapemeriksaanCD4,makayangdigunakansebagai
indikatorpemberianterapipadainfeksiHIVsimptomatikadalahjumlahlimfosit total 1200/mm3
atau kurang (misalnya pada stadium II). Sedangkan pada pasien asimptomatik jumlah limfosit
total kurang berkorelasi dengan jumlahCD4.Namun biladalamstadium simptomatik
baruakanbermanfaat sebagai petandaprognosisdanharapanhidup.
Pemeriksaan viral load (misalnya dengan menggunakan kadar RNA HIV-1
dalamplasma)tidakdianggapperlusebelumdimulainyaARTdan tidak direkomendasikan oleh
WHOsebagai tindakanrutinuntuk memandupengambilankeputusanterapikarenamahaldan
pemeriksaannyarumit. Diharapkanpadamasamendatangdapatberkembangcarapemeriksaanviral
load yang lebih terjangkau sehingga cara memantau pengobatan tersebut dapat diterapkan
secara luas.Perlu diperhatikan bahwa sistem pentahapan infeksiHIVmenurutWHObagi
orangdewasatersebutdikembangkanpada beberapatahunyanglaludanmemilikiketerbatasan
tetapimasihbermanfaatuntukmembantumenetapkanindikatorsaatmemulaiterapi.
Bila tersediapemeriksaan CD4Stadium IV : tanpa memandang jumlahCD4
StadiumIII :denganjumlah CD4<350/mm3sebagaipetunjuk Stadium Iatau IIdengan jumlahCD4<200/mm3bBila tidaktersedia saranapemeriksaan CD4StadiumIV : tanpa memandang jumlahlimfosittotalStadiumIII :tanpa memandang jumlahlimfosittotal
StadiumII, denganjumlahlimfosittotal<1200/mm3c
Tabel:SaatmemulaiterapipadaODHAdewasa
62

Keterangan:
a. CD4dianjurkan digunakan untukmembantu menentukan mulainya terapi.
ContohTBparudapatmunculkapansajapadanilaiCD4berapapun dan
kondisilainyangmenyerupaipenyakityangbukandisebabkanolehHIV.
b. NilaiyangtepatdariCD4diatas200/mm3
dimanaARTharusdimulaibelumdapatditentukan.
c.Jumlahlimfosittotal >1200/mm3 dapatdipakaisebagaipenggantibila pemeriksaan
CD4 tidak dapat dilaksanakan dan terdapat gejala yang berkaitan
denganHIV(Stadium IIatauIII).Halinitidakdapatditerapkan
padaODHAasimtomtatik. Makabilatidakadapemeriksaan CD4,ODHA
asimptomatik (stadium I)tidakbolehditerapi karena padasaatinibelum
adapetandalainyangterpercayadidaerahdengansumberdayaterbatas.
FarmakologiARV
Pengertian
Antiretroviral (ARV) adalah obat yang menghambat replikasi Human
Immunodeficiency Virus (HIV). Terapi dengan ARV adalah strategi yang secara
klinispalingberhasilhinggasaatini. TujuanterapidenganARVadalahmenekan replikasi HIV secara
maksimum, meningkatkan limfosit CD4 dan memperbaiki
kualitashiduppenderitayangpadagilirannyaakandapatmenurunkan morbiditas danmortalitas.
Seperti obat-obat antimikroba lainnya maka kompleksitas antara pasien,patogendan
obatakanmempengaruhiseleksiobatdan dosis.Karakteristik pasienakan
mempengaruhifarmakokinetikobat. Karakteristikmikrobameliputi
mekanismekerja,polakepekaan,dan resistensi.Farmakodinamikobatmerupakan
integrasihubunganantara kepekaanmikrobadenganfarmakokinetikpasien.Untuk menjamin
tercapainya targetterapi,interaksifarmakodinamik antaraantimikroba
dantargetmikrobaharustercapai.
PenggolonganARV
63

AdatigagolonganutamaARVyaitu
A. Penghambatmasuknyavirus; enfuvirtid
B. Penghambatreversetranscriptaseenzyme
B.1Analognukleosida/nukleotida (NRTI/NtRTI)
analognukleosida
analogthymin:zidovudin(ZDV/AZT)danstavudin(d4T)
analogcytosin:lamivudin(3TC)danzalcitabin(ddC)
analogadenin:didanosine(ddI)
analogguanin:abacavir(ABC)
analognukleotidaanalogadenosinmonofosfat:tenofovir
B.2.Nonnukleosida(NNRTI)
nevirapin(NVP)
efavirenz(EFV)
C.Penghambatenzimprotease(PI)ritonavir(RTV)
saquinavir(SQV)
indinavir(IDV)dannelfinavir(NFV)
MekanismekerjaARV
Penghambatmasuknyavirus
(Fusion/EntryInhibitors)
Penghambat Enzim
Protease / Protease
Inhibitor
64

Penghambat reverse
Transcriptase
NNRTI dan NRTI
Gambar:MekanismeKerjaARV
A. Penghambatmasuknyaviruskedalamsel
Bekerja dengan cara berikatan dengan subunit GP41 selubung glikoprotein virus
sehingga fusi virus ketarget seldihambat. Satu-satunya obatpenghambat fusi ini
adalahenfuvirtid.
B. ReverseTranscriptaseInhibitor(RTI)
1. Analognukleosida(NRTI)
NRTI diubah secara intraseluler dalam 3tahap penambahan 3gugus fosfat) dan
selanjutnyaberkompetisidengannaturalnukleotidamenghambatRT sehingga
perubahanRNAmenjadiDNAterhambat.Selainitu NRTIjugamenghentikan
pemanjanganDNA.
2. Analognukleotida(NtRTI)
MekanismekerjaNtRTIpadapenghambatanreplikasiHIV samadenganNRTItetapi
hanyamemerlukan 2tahapan prosesfosforilasi.
3. Nonnukleosida(NNRTI)
Bekerjanya tidakmelalui tahapan fosforilasi intraseluler tetapi berikatan langsung
denganreseptorpadaRT dantidakberkompetisidengannukleotidanatural.Aktivitas
antiviralterhadapHIV-2tidakkuat.
65

C. Proteaseinhibitor(PI)
Protease Inhibitor berikatan secara reversible dengan enzim protease yang
mengkatalisa pembentukan protein yang dibutuhkan untuk proses akhir pematangan
virus.Akibatnyavirusyangterbentuktidakmasukdantidakmampumenginfeksisellain.
PIadalahARVyangpotensial.
FarmakokinetikARV
Konsepfarmakokinetik
Absorpsiobatyangdberikanperoral tidaklengkapatauterhambatdanobatakan mengalami
metabolisme lintas pertama sehingga bioavaibilitas (F) obat akan lebih
rendahdibandingkandenganobatyangdiberikansecaraintravena.Distribusiobat akan
dipengaruhi olehkelarutan dalam lemak danikatan dengan protein plasma. Volume
distribusi (Vd)menggambarkan distribusi obatdalam kompartemen tubuh. Obatyang
terutama terdistribusi di plasma akan mempunyai Vd yang relatif kecil dan
konsentrasinya tinggidiplasma.Obatyangterdistribusiluaskeberbagaikompartemen
tubuhakanmempunyaiVdyangbesardankonsentrasinya relatifrendahdiplasma.Vd diperlukan
untuk menghitung loading dose. Loading dose dapat digunakan untuk
mencapaikonsentrasiterapidengansegera.
Metabolisme obatumumnya terjadi dihatiyang menyebabkan perubahan kimia obat
sehingga obat mudah untuk dieliminasi dari tubuh. Obat yang di metabolisme oleh
sistemP450 akanberkompetisi denganobat-obatyangjugadimetabolisme olehsistem ini. Obat
atau zat yang mempengaruhi P450 apakah menginduksi atau menghambat
akanmenyebabkan kecepatanmetabolismeobatyangdimetabolismeolehsistemP450
terganggu.
Eliminasiobatumumnyamelaluiginjal,walauada jugayangmelaluiekskresiempedu.
66

Klirens/Clearence (Cl)obatmenggambarkan banyaknya darahpersatuanwaktuyang
dibersihkan dariobattersebut.Tanpamembedakan ruteeliminasi,kecepataneliminasi obat
dari tubuh dinyatakan sebagai waktu paruh obat. Waktu paruh obat dapat digunakan
untuk menentukan kondisi steady state yaitu suatu kondisi
dimanakonsentrasiobatkonstankarenapemberianobatyangterusmenerus/berulang. Kondisi
initercapaisetelahlebihkurang5waktuparuhobat.Setelahmencapaikondisisteady
statemakapemberiandosisberikutnyatidakakanmengubahkonsentrasi obatkecuali
biladosisobatatauparameterfarmakokinetikberubah.
No Obat K
epekaanIVa,
K
Fb Vdc T½d CI/Fe Dosis
dosis/
hari)
Cmax/Cminf
A NRTI
1 Abacavir 0.07– 5.8 83 0,86 1,5 49,8 300(2) 10,7/0,04
2 Didanosin 0,01– 10 40 0,83 1,4 26,9 200(2) 4/0,02
3 Lamivudin 0,002 –15 86 1,3 5 23,1 150(2) 7,5/0,22
300(1)
4 Stavudin 0,009 -4 86 0,53 1,4 34 40(2) 4/0,004
5 Tenofovir 0,04– 8,5 40 1,2 17 35,7 300(1) 1,13/0,2
6 Zalcitabin 0,03– 0,5 85 0,53 2 12 0,75(3) 0,05/0,001
7 Zidovudin 0,01– ,048 64 1,6 1,1 112 200(3) 2/0,2
B NNRTI
1 Efavirenz 0,0017–
0,025
43 10,2 48 10,3 600(1) 12,9/5,6
2 Nevirapin 0,010 –0,1 50 1,21 25 2,6 200(2) 5,5/3,0
C PI
1 Loponavir 0,004 –0,07 ? 0,74 5,5 6,5 400(2) 15,4/8,8
2 Ritonavir 0,0038–
0,154
60 0,41 3,5 8,8 600(2) 16/5
3 Nelfinavir 0,009 –0,06 ? 2 2,6 37,4 750(3) 5,6/0,7
4 Saquinavir 0,001 –0,03 12 10 3 80 1200(3) 0,4/0,15
Tabel: ParameterFarmakokinetikARV
67

Keterangantabel
a. IV : invitro
b. F : bioavaibilitasc. Vd : volumedistribusid. T1/2 : waktuparuheliminasie. Cl/F : clearence/bioavaibilitasf. C konsentrasimaksimal/konsentrasi minimaldiplasma.g. MIC50 : konsentrasi hambatan minimum untuk menghambat pertumbuhan 50%
virus
III.2.5 Efeksampingumum
Efeksampingobat adalahsalahsatu penyebabmorbiditas,dirawatnyapasiendan
mortalitas.Hal tersebutjugaberpengaruhpadakepatuhanpasienterhadaprencana
terapi.Karenaitu pendeteksiandiniefeksampingadalahhalkritisdandalamhalini
apotekerdapatikutberperan.
GOLONGA
N
EFEKSAMPING
NRTI Laktatasidosisdanhepatotoksik
NtRTI Toksisitasginjal
NNRTI Hepatotoksisitasdanrash
PI Gangguan metabolik ganda (insulin resistensi,
hiperlipidemia,
Tabel:EfekSampingUmumAntiretroviral
68

NO EFEKSAMPING OBAT TANDAKLINIS MANAJEMEN
1 Hepatitisakut NVP,EFV
(jarang),
ZDV, ddl, d4T,RTV
Jaundice, pembesaran hati,
gejala GIT(mual,muntah, diare, nyeriperut, lemah, anoreksia)
- Bila
mungkin,monitortransaminaseserum, bilirubin,
-Stop ARV sampaigejalahilang.2 Pankreatitisakut ddl,d4T M
ual,muntahdannyeriperut-Monitor amilase
pankreatik-Stop ARV, tukar
denganobat baru3 Laktatasidosis SemuaNRTI L
elahdanlemahmenyeluruh,
gejala GIT,hepatomegali,
-StopARV-Berikan terapi
penunjang-Tukarobatbaru
4 Reaksi
Hipersensitivitas
ABC ABC:demam,lelah,mialgia,
gejalaGIT, faringitis, batuk, dispnea (dengan
-Stop ARV sampai
gejalahilang,jangan diberiABCatauNVP
-Bila gejala hilang,
segeramulaidengan
NVP NVP:gejalasistemik,demam
mialgia, atralgia,hepatitis,
eosinofilia 5 Neuropati perifer
Berat
ddl,d4T, 3TC
Nyeri, kesemutan, tangan
dankaki kebal,bagian ujung tubuh hilangrasa,lemahotot, tidakadarefleks
- Stop NRTI yangdicurigai,
ganti dengan NRTI
lain yangtidak
menyebabkan neurotoksisitas misalnyaZDV,ABCTabel:Efeksampingumumyangmemerlukanpemutusanobat
69

InteraksiARV
Interaksiobat–obatyangsignifikanmenyebabkan penggunaanklinisARVmenjadi rumit.
Beberapa interaksi menguntungkan tetapi beberapa mungkin berbahaya. Karena itu
pengetahuan mengenai interaksi obat ARV penting untuk tenaga
kesehatanyangbersangkutan.
Secaraumum,efavirenz,nevirapin,amprenavirdan tipranaviradalahinduktor metabolisme
obat,sedangkandelavirdindanproteaseinhibitoradalahpenghambat
metabolismeobat.RitonaviradalahpenghambatsitokromP450 3Ayangpotensial dan
sekarangterutamadigunakanuntuk meningkatkansecarafarmakokinetikPI lainnya.
Karenaitumakakombinasiritonavirdenganlopinavir(Kaletra)diformulasikan.
InteraksijugaterjadidiantarasesamaNRTIdan denganobatlain. Sebagaicontoh,
zidovudindanstavudindifosforilasiolehenzimkinaseyangsama,sehingga terjadi
antagonisme baiksecara invitromaupun invivosehingga kombinasi kedua ART
tersebutdihindari. Konsentrasi Zidovudin ditingkatkan olehflukonazol, interferon-B,
metadon, valproat, simetidin, imipramindantrimetoprim. Zidovudin karena
berinteraksisecara farmakokinetik,pemberianbersamazidovudindengangansiklovir
sebaiknyadihindarikarenadapat menimbulkaninteraksifarmakodinamikyang
menyebabkanterjadinyaneutropeniapada beberapapasien.Didanosindapat
berinteraksisecarafarmakodinamikdenganbeberapaobat; cisplatin,isoniazid,
metronidazol,nitrofurantoin, ribavirin,stavudin,vinkristin, danzalcitabin
menyebabkanneuropatiperifer.Sedangandenganetanol,lamivudindan pentamidin didanosin
dapat menimbulkan pankreatitis. Didanosin menyebabkan penurunan absorbsi dapson,
indinavir,itrakonazol,ketokonazol,pirimetamin,rifampin dan trimetoprim.
Interaksi yang potensial terjadi antara obat antituberkulosis terutama Rifampisin dengan
PI. Interaksi ini menyebabkan penurunan konsentrasi PI secara nyata,
sehinggarifampisintidakdiberikanbersamadenganPI. Saquinafir,ritonaviratau
efavirenzdapatdianjurkanuntukpengobatanHIVpadapasiendengantuberkulosis.
70

Pengguna kontrasepsi oral yang mengandung etinil estradiol sebaiknya tidak
diberikanritonavirkarenaritonavirmempercepatmetabolismedan eliminasietinil
estradiolsehinggadapatmenurunkanefekkontrasepsi.
Obat herbal , Hypericum perforatum (Saint John’s wort) adalah inhibitor yang
potensial,sehinggadikontraindikasikanpadapemberianPIdanNNRTI.
Zidovudin
(ZDV,AZT,Retrovir®)
Sediaandalambentuktablet 300mgdankapsul100mg,sirup10mg/ml,suntikan
IV10mg/ml
Dosis300mglewatoral tiap12jamdenganatautanpamakan. Sediaan
kombinasiDuviralmengandungZDV300mg/3TC150mg/tab. DosisDuviral1tablet peroral
tiap12jam
Efeksamping: mual/muntah, sakitkepala,kembung, anemia,neutropenia, mialgia,
miopati,artralgia,peningkatantransaminase.
Pemberianbersamamakananmengurangimual.
Perhatian:monitorhematokrit,leukosit,tesfungsihati.
Didanosin(ddI,Videx®)
Bentuk sediaan tablet salut enterik yang dapat diberikan sebagai dosis tunggal
Dosis:>60kg,400mgperoralsekalisehari
Dosis:<60kg,250mgperoralsekalisehari
Efek samping : diare, neuropati perifer, pankreatitis, enzim transaminase dan
neuropatiperifer.
71

Perhatian:
9Obatdiberikantidakbersamamakanan.
9Monitorfungsihati,amilase/lipase,
9Hati-hatipemberianbersamadenganobatyangmenyebabkanpankreatitis.
Stavudin
(d4T,Zerit®)
Bentuksediaankapsul:15,20,30,40mg,larutan 1mg/ml
Dosis:>60kg,40mgperoraltiap12jamdengan/tanpamakanan.
Dosis:<60kg,30mgperoraltiap12jam
Efeksamping:neuropati perifer,peningkatan enzimtransaminase, laktatasidosis,
gejalasalurancerna,danlipoatrophy.
Perhatian:Tidakamandigunakandengandidanosin.
Lamivudin
(3TC,Hiviral®)
Bentuksediaantablet:150mg/300mg(HIV),100mg(hepatitisB)
Dosis: 150mgperoraltiap12jamatau300mgperoralsekalisehari<50kg:2mg/kg
peroraltiap12jamdengan/tanpamakanan.
Obatinimerupakanobatyangsangatdapatditoleransi,tapimudahterjadiresistensi.
ObatinidapatdigunakanuntukhepatitisB.
Abacavir
(ABC,Ziagen®)
Sediaantablet:300mg
Dosis:300mgtiap12jamdengan/tanpamakanan,atau600mgsekalisehari.
72

Efeksamping:mual,muntah,diare,nyeriperut,danreaksihipersensitivitas(5%)
Perhatikan tanda-tanda alergi:demam, mualataulelah,denganatautanparuam.
Janganpernahdiulangijika terjadialergikarenabisatimbulshokanafilaksis.
Informasikansecararincimengenaikemungkinandantandaalergidan lakukan
monitoringketatterhadapreaksihipersensitivitas.
Nelfinavir
Sediaantablet250mg.
Dosis tiap 12 jam 1250 mg (5 tablet) dimakan bersama makanan atau sesudah makan.
MetabolismemelaluijalurP4503A4.
Efeksamping: diareseringtimbulsetelahdosisawal,dalambentukintermitendan
biasanyatidakdisertaidengankeluhanyanglain. Diaretersebutmemberikanrespon
yangbaikterhadaploperamide,bisadicobadengan kalsiumkarbonate.
TenofovirDF(Viread)
Sediaantablet245mg
Dosis:245mglewatoral sekalisehari denganatautanpamakanan.
Efeksamping:Fanconissyndromedengandisertairenaltoksisitas.
ObatinidapatdigunakanuntukhepatitisB.Kurangidosis ketikadigunakandengan tenofovir.
Efavirenz
(EFV,Sustiva®,Stocrin®)
73

Bentuksediaankapsul:50,100,200,600mg
Dosis: 600mgperoralsekaliseharidengan/tanpamakanan
74

Efeksamping: susunansarafpusat(SSP):mimpiburuk, susahkonsentrasi,pusing, insomnia,
ruam.Gejala SSPbiasanya terjadi,tapi akanmembaik dalam 7-14hari; T1/240-
55jam;CYP3Ainducer.
Perhatian:Jangandiberikanpadawanitahamilkarenamenimbulkanteratogenik.
Nevirapine
(NVP,Viramune®)
Bentuksediaantablets:200mg
Dosis:200mgperoralsekalisehari 14hari,lalu200mgdengan/tanpamakanan Efeksamping:
ruam yang berat, demam, gangguan saluran cerna, peningkatan
transaminase
Perhatian:Pemberian200mgdosistunggal untuk2minggupertamamengurangi
kemungkinan alergi; periksa fungsi hati tiap 2 minggu untuk 2 bulan pertama,
selanjutnyatiapbulanuntuk3bulanberikutnya.
Saquinavir
(SQV-HGC,Invirase®;SQV-SGC,Fortovase®FTV) Bentuksediaansoft-
gelkapsul(Fortovase®)200mg Hard-gelkapsul(Invirase®)200mg.
Dosis:FTV1200mgperoraltiap8jamdenganmakananatauFTV1000mg/
RTV100tiap12jam.Efeksamping: padasaluranpencernaan,nyeriabdominal,ruam.
Enfuvirtide(T-20)
Amino-acidsyntheticpeptideinhibitsHIV-1gp41
Dosis:90mg2kalisehari(subkutan).
Efek samping: Reaksi pada tempat suntikan, diare, nausea, sakit kepala, reaksi
hypersensitivitas (jangandiberikan lagibilaadagejalahipersensitivitas.)
Kaletra(lopinavir+ritonavir)
75

Sediaan tabletyangmengandunglopinavir200mgdanritonavir50mg,sedangkan
kapsulmengandunglopinavir133mgdanritonavir33mg.
Dosissatukalisehari untukpasien yangbarupertama kalimenerima terapiARV atau dua
kali sehari untuk penderita yang telah menggunakan ARV sebelumnya. Kaletra dapat
diminum dengan atau tanpa makanan. Anak-anak berusia 6bulan
sampai12tahundapatdiberiKaletra dengan dosissesuaidenganberatbadan.
Efeksampingyangpalingumumadalah defekasiabnormal,lelah-lemah,diare,mual
danmuntah.Anak-anakseringmengalamiruam.
76

Efeksampinglainhepatitis,pancreatitis,hyperlipidemia,diabetes,lipodistropi.
Obat yang perlu dihindari diberikan bersama kaletra karena dapat menimbulkan
interaksi adalah cisaprid,rifampin,ergotamine,astemizol,terfenadin,bepridil,
vorikonazol.
PenggunaanRasionalAntiretroviral
Pengertian
Penggunaanobat dikatakanrasionalbilapasienmenerimaobatyangsesuaidengan
kebutuhannya untukperiodewaktuyangadekuatdenganhargayangpalingmurah untuknyadan
masyarakat.(WHO,1985).Secarapraktis,penggunaanobatdikatakan
rasionalbilamemenuhikriteria:
1. Tepatdiagnosa
2. Tepatindikasipenyakit
3. Tepatpemilihanobat
4. Tepatdosis
5. Tepatcarapemberianobat
6. Tepatintervalwaktupemberian
7. Tepatlamapemberian
8. Waspadaterhadapefeksamping
9. Tepatpenilaiankondisipasien
10.Tepatinformasi
11.Tepatdalammelakukanupayatindaklanjut
12.Tepatpenyerahanobat(dispensing)
13.Kepatuhanpasien
RejimenARVLiniPertamabagiODHAdewasa
77

RejimenARVLini-PertamabagiODHAdewasasebagaiberikut:
ZDV+3TC+NVP
Toksisitas utama yang dapat terjadi padapemberian rejimen ARVlini-pertama ini
adalah: intoleransi gastrointestinal dari ZDV, anemia,netropenia; hepatotoksisitas
NVP,danruamkulitberat
RejimenARVLini-Kedua
RejimenARVlini-keduabagiODHAdewasa/remajadiberikanpadakegagalanterapi
padarejimenlini-pertama,sebagaiberikut:
TDFatauABC + ddl + LPV/ratauSQV/r
Catatan:
a. Dosisddlharusdikurangimenjadi250mgbiladiberikanbersamaTDF.
b. LPV/rdanSQV/rmemerlukancoldchain(Coldchainadalahsemacamcontainer
untukmembawaobat/vaksinyangharusdalamkeadaansuhusekitar50C)
AlasanMenggantiARV
AdakemungkinanperlumenggantiARV baik yangdisebabkankarenatoksisitasatau
kegagalanterapi.
Toksisitas
Toksisitasterkaitdenganketidakmampuan untukmenahanefeksampingdariobat, sehingga
terjadi disfungsi organ yang cukup berat. Hal tersebut dapat dipantau secara
klinis,baikdarikeluhan ataudarihasilpemeriksaan fisikpasien, ataudari
hasilpemeriksaanlaboratorium,tergantungdari macamkombinasiobatyangdipakai
78

dansaranapelayanankesehatanyangada.
KegagalanTerapi
Kegagalanterapidapatdidefinisikansecaraklinis denganmenilaiperkembangan
penyakitsecaraimunologisdenganpenghitunganCD4, dan/atausecaravirologist
denganmengukurviral-load.
Penilaianklinis perkembanganpenyakitharusdibedakandengansindrompemulihan
kekebalan (immuno reconstitution inflammatory syndrome / IRIS), yaitu keadaan
yangdapatmunculpadaawalpengobatanARV. Sindromini ditandaiolehtimbulnya
infeksioportunistikbeberapaminggusetelahART dimulaisebagaisuaturespon inflamasi
terhadap infeksi oportunistik yang semula subklinik.Keadaan tersebut
terjaditerutamapadapasiendengangangguankebalantubuhyang telahlanjut.
Kembalinyafungsiimunologidapatpula menimbulkangejalaatipikdariinfeksi
oportunistik.
PilihanRejimenARVPadaKegagalanTerapidariObatLiniPertamapadaODHADewasa
Pada kegagalan terapi dianjurkan untuk mengganti semua rejimen lini pertama
denganrejimenlinikedua.Rejimenlinikeduapenggantiharusterdiridariobatyang
kuatuntukmelawangalur/strain virusdansebaliknya palingsedikitmengandung 3 obatbaru,
satuatauduadiantaranya darigolongan yang baruagar keberhasilan terapi meningkat dan
risiko terjadinya resistensi silang dapat ditekan serendah mungkin.
Biladipakai (d4TatauAZT)+3TCsebagai rejimen linipertama, resistensi silang nukleosida
akanmembahayakan potensikeduakomponen nukleosida darirejimen lini kedua, terutama
pada kegagalan virologis yang telah lama. Pada situasi demikian, perlu membuat pilihan
alternatif secara empiris dengan pertimbangan untukmendapatkan
dayaantiviralyangsekuatmungkin.Denganadanyaresistensi
silangdarid4TdanAZT,makarejimenlinikeduayangcukupkuatadalahTDF/ddl atau ABC/
ddl. Namun ABC dapat memberi risiko terjadi hipersensitifitas dan
79

harganyamahal.Lagipula,koresistensi padaAZT/3TCdapatjugaterjadiresistensi
terhadapABC.TDFdapatdiperlemaholeh adanyamutasimultipeldari analog
nukleosida(NAM= nucleosideanaloguemutation)tetapiseringmasihmemilikidaya
antiviralmelawangalurvirusyangresistenterhadapnukleosida.Sepertihalnyaddl,
TDFdapatdiberikandengandosissekalisehari.TDFdapatmeningkatkankadarddl dan oleh
karenanya dosis ddlharus dikurangi bila kedua obat tersebut diberikan bersamaan,
agarpeluangterjadinyatoksisitasakibatddldapatdikurangi, misalnya
neuropatidanpankreatitis.
Olehkarenapotensiyangmenurundarihampirsemuajenisnukleosida linikedua,
makadidalamrejimen linikedualebihbaikmenggunakan suatujenisPI(protase inhibitor)
yangdiperkuat olehritonavir(ritonavir-enhanced PIatauRTV-PI), seperti
lopinavir(LPV)/r,saquinavir(SQV)/ratauindinavir(IDV)/r.PI yangdiperkuatdengan
ritonavirlebihkuatdaripadanelfinavir(NFV)saja.
IDV/r memiliki efek samping yang berat pada ginjal tetapi perlu dipertimbangkan
sebagaisuatualternatifkarenapotensinya.PerandanketersediaanATV/rdi negara
berkembangsaat inibelumdapatdipastikan.
PadakegagalanterapirejimenyangmengandungPI, pilihanalternatifpenggantinya tergantung
dari alasan awal memilih rejimen PI tersebut, dibandingkan memilih rejimen yang
mengandung NNRTI. Biladiduga adaresistensi NNRTI atauinfeksi HIV-2 maka pilihan
rejimen menjadi sulit karena tergantung dari kendala yang dihadapi oleh masing-
masing individu ODHA,kemampuan melaksanakan pemeriksaan resistensi obat
secara individual dan ketersediaan obat ARV. Kegagalan
terapiatasrejimentigaNRTIlebihmudahdiatasikarenaduagolongan obatterpenting (NRTI
danPI),masih dapat digunakan. Suatu alternatif RTV-PI + NNRTI
dengan/tanpaNRTI,misalnyaddldan/atauTDFdapatdipertimbangkanbilatersedia.
80

Kegagalanatas Digantidengan
d4TatauAZT
+
3TC
+
NVPatauEFV
TDFatauABC
+
ddla
+
LPV/ratauSQV/rb
81

Bagan: RejimenARVlinikeduabagiODHAdewasabiladijumpai
kegagalan terapipadarejimenlinipertama
Keterangan:
a. Dosisddlharusdikurangidari400mgmenjadi250mgbiladiberikanbersama denganTDF
b. LPV/rdanSQV/rmemerlukancoldchain.NFVdapatdipertimbangkansebagai
suatualternatifdinegaraberkembang.
IndikasiuntukMenggantiatauMenghentikanART
Menggantirejimenakibattoksisitasobat dapatdilakukandenganmengganti
menggantisatuataulebihobatdari golonganyangsamadenganobatyangdicurigai
mengakibatkantoksisitas.
Mengganti terapi akibat kegagalan untuk hal ini sebaiknya ada kriteria khusus
untukpenggantian terapimenjadi rejimen yangbarusecara keseluruhan (masing- masing
obatdalam kombinasi diganti dengan yangbaru)ataupenghentian terapi
penggantian,ataupenghentiandilakukanbila:
1. ODHA pernah menerima rejimen yangsamaseklai tidak efektif lagi,misalnya
monoterapiatauterapidenganduanukleosida(NRTI).
2. Viralloadmasihterdeteksisetelah4-6bulanterapi,ataubilaviralloadmenjadi
terdeteksikembalisetelahbeberapabulantidakterdeteksi.
3. JumlahCD4terusmenerusturunsetelahditesduakalidenganintervalbeberapa minggu.
4. Infeksioportunistikatauberatbadanmulaimenurunsecaradrastis. Haliniharus
dibedakandenganimmunereconstitutionsyndrome/ sindrompemulihankembali
kekebalan.
82

ARTuntukKelompokTertentu
BayidanAnak
WalaupunperjalananpenyakitinfeksiHIVdanpenggunaan ARTpadaanakadalah
serupadenganorangdewasa,tetqpiada beberapapertimbangankhususyang
dibutuhkanuntukbayi,balitadananakyangterinfeksiHIV.
Sistemkekebalanbayimulaidibentukdan berkembangselamabeberapatahun pertama.
Bila bayi tertular HIV dalam masa kehamilan dan persalinan maka gejala klinis,
jumlahCD4danviralloadberbedadenganorangdewasa. Efekobatjugaberbeda selama
transisi dari bayi keanak. Oleh karena itudibutuhkan perhatian khusus tentang
dosisdantoksisitas padabayidananak. Kepatuhan berobat padaanak
menjaditantangantersendiri.
IbuHamil
Padaibu hamilyangtelahmenggunakanARVsebelumkehamilannyamaka
penggunaanARVharusditeruskan(ARVLini-Pertama).
JikaibuhamilternyatapositifHIVdanbelumpernahmendapatkanARV,maka:
•j i k akondisi s angibu l e mah/buruk :
dapatsegeradiberikanARVLini-Pertama
•j i k akondisi s angibubaik/norm a l :
tidak disarankan untuk memulai ARV pada triwulan pertama karena mual atau
muntahyangseringterjadipadaawalkehamilandapatmempengaruhi kepatuhan
pengobatan.
PasienKoinfeksiTuberkulosis–HIV
83

PasienyangsudahmemulaiARVdanterkenaTBaktifharusmenyesuaikanrejimen
ARTagarcocokdenganpengobatan TB. SetelahterapiTBselesai,rejimenART
dapatditeruskansepertisemulaatau diubah,tergantungpadastatusklinis dan
imunologispasien.
PenggunaNapzaSuntik(IDUs)
ARVdiberikansekalisehari.
DapatterjadiinteraksiantararejimenARVdenganmetadon(kadarmetadonturun).
ProfilaksisPascapajanan
Profilaksispascapajananadalahpengobatanantiretroviraljangka pendek untuk
menurunkankemungkinanterjadinyainfeksipascapajanan,baikdi tempatkerjaatau
melaluihubunganseksual. Risikoterpajan karenatertusukjarumdancaralainnya dapat
terjadi pada lingkungan dengan sarana pencegahan terbatas dan angka
pajananinfeksiHIVcukuptinggipadakelompoktertentu.
Ketersediaan profilaksis pascapajanan dapat mengurangi risiko penularan HIV
ditempat kerja pada petugas kesehatan. Selain itu ketersediaan profilaksis
pascapajanan pada petugas kesehatan dapat meningkatkan motivasi petugas
kesehatan untukbekerja dengan orangyangterinfeksi HIVdandiharapkan dapat
membantupemahamantentangadanyarisikoterpajandenganHIVditempatkerja.
ResistensiObat
JikaARTtidakdilaksanakan dengan baik,HIVdapatmengalami mutasigenatau
mengubahstrukturkimiasertastrukturgenetiknyasehinggaresistenatau tidaklagi
mempanolehobatARV.
84

Secara umum resistensi obat ARV meningkat bila ARV diberikan sebagai obat tunggal.
NamunhalinitidakberartibahwaODHAtidakdapatminumobatARVitu lagi. Resistensi
akan timbul lebih lambat bilaviralload rendah danCD4 masih
tinggi.Sebaliknya,HIVakanlebihcepatresistenbilaviralloadtinggi.
Asuhan Gizi
Asuhan gizi merupakan komponen penting dalam perawatan individu yang terinfeksi HIV.
Mereka akan mengalami gangguan pertumbuhan dan penurunan berat badan dan hal ini
berkaitan dengan kurang gizi. Penyebabnya multifaktorial antara lain karena anoreksia,
gangguan penyerapan sari makanan pada saluran cerna, hilangnya cairan tubuh akibat diare dan
muntah, dan gangguan metabolisme. Jika seseorang dengan HIV mempuyai status gizi yang baik
maka daya tahan tubuh akan lebih baik sehingga menghambat memasuki tahap AIDS.
Asuhan gizi dan terapi gizi bagi ODHA sangat penting bagi mereka yang mengkonsumsi
ARV. Makanan yang dikonsumsi mempengaruhi penyerapan ARV dan obat infeksi
opoortunistik dan juga sebaliknya, sehingga mmerlukan pengaturan diet seperti obat ARV
dimakan ketika saat lambung kosong.
Prinsip gizi medis pada ODHA ialah tinggi kalori tinggi protein (TKTP) diberikan secara
oral, juga kaya vitamin meneral dan cukup air. Berdasarkan beberapa penelitian, pemberian
stimulan nafsu makan, seperti megestrol acetate dan human recombinant growth hormone dapat
memberikan kenaikan berat badan dan pertumbuhan.
Seiring dengan berkembangnya penyakit, akan terjadi penurunan berat badan yang sangat
drastis (drastic wasting) dan terhambatnya pertumbuhan anak. Berkurangnya cadangan protein
dapat diatasi dengan meningkatkan intake asam amino, terutama threonine dan methionine.
Bayi yang lahir dari ibu HIV tidak boleh diberi ASI ibunya, sehingga bayi diberikan
pengganti air susu ibu (PASI). Namun dalam keadaan tertentu dimana pemberian PASI tidak
memungkinkan dan bayi akan jatuh ke dalam kurang gizi, ASI masih dapat diberikan dengan
cara diperas dan dihangatkan terlebih dahulu pada suhu di atas 66OC untuk membunuh virus
HIV.
Rekomendasi terkait menyusui untuk ibu dengan HIV adalah sebagai berikut :
85

1.Menyusui bayinya secara eksklusif selama 4-6 bulan untuk ibu yang tidak terinfeksi atau
ibu yang tidak diketahui status HIV-nya.
2.Ibu dengan HIV positif dianjurkan untuk tidak memberikan ASI dan sebaliknya
memberikan susu formula (PASI) atau susu sapi atau kambing yag diencerkan.
3.Bila PASI tidak memungkinkan disarankan pemberian ASI eksklusif selama 4-6 bulan
kemudian segera dihentikan untuk diganti dengan PASI.
PROGNOSIS
Viremia plasma dan hitung limfosit CD4 sesuai usia dapat menentukan resiko perjalanan
penyakit dan komplikasi HIV. Prognosis yang buruk pada infeksi perinatal berhubungan dengan
terjadinya encephalofati, infeksi, perkembangan menjadi AIDS lebih awal, dan berkurangnya
jumlah limfosit CD4 yang cepat. Tanpa terapi, kurang lebih 30% bayi yang terinfeksi
berkembang menjadi gejala klinis berat kategori C atau kematian dalam 1 tahun kehidupan.
Dengan terapi yang optimal angka mortalitas dan morbiditas menjadi rendah.(2)
2.7 PENCEGAHAN
Edukasi dan konseling pasien yang terdeteksi terinfeksi HIV. Infeksi HIV yang muncul
pada wanita biasanya karena pengguna obat-obatan dan pasangan seksual laki-laki yang resiko
tinggi. Sehingga dibutuhkan pendidikan seks yang baik dan sehat. Konseling juga jangan hanya
membahas tentang modifikasi stress namun juga memodifikasi perubahan gaya hidup melalui
pesan-pesan budaya dan religi.
Perlu dilakukan uji tapis serologis bagi darah pendonor dan pengawasan serta perlakuan
yang lebih ketat bagi bahan-bahan yang berasal dari darah, terutama yang akan diberikan pada
anak yang perlu mendapat transfusi atau pemberian bahan yang berasal dari darah berulang-
ulang atau daerah dengan prevalensi HIV yang tinggi.
Program pendidikan kesehatan reproduksi untuk remaja, perlu dipikirkan strategi
penerapannya di sekolah dan akademi dan untuk remaja yang berada di luar sekolah.
Transmisi vertical dapat dicegah dengan memberikan terapi antiretrovirus pada ibu selama
kehamilan dan memberikan profilaksis pada bayinya yang baru lahir. Wanita hamil yang
terinfeksi HIV sebaiknya diberikan terapi kombinasi 3 (tiga) obat. Terapi kombinasi dapat
membuat supresi virus.
86

3. Kapan dilakukan skrining HIV?
Skrining HIV mempunyai makna melakukan pemeriksaan HIV pada suatu populasi tertentu, sementara uji diagnostik HIV berarti melakukan pemeriksaan HIV pada orang-orang dengan gejala dan tanda yang konsisten dengan infeksi HIV. CDC menyatakan bahwa infeksi HIV memenuhi seluruh kriteria untuk dilakukan skrining, karena: 11 1. Infeksi HIV merupakan penyakit serius yang dapat didiagnosis sebelum timbulnya gejala.
2. HIV dapat dideteksi dengan uji skrining yang mudah, murah, dan noninvasif.
3. Pasien yang terinfeksi HIV memiliki harapan untuk lebih lama hidup bila pengobatan dilakukan sedini mungkin, sebelum timbulnya gejala.
4. Biaya yang dikeluarkan untuk skrining sebanding dengan manfaat yang akan diperoleh serta dampak negatif yang dapat diantisipasi. Di antara wanita hamil, skrining secara substansial telah terbukti lebih efektif dibandingkan pemeriksaan berdasarkan risiko untuk mendeteksi infeksi HIV dan mencegah penularan perinatal.
Saat ini terdapat kontroversi mengenai kapan harus memulai terapi ARV. Ada pendapat yang mengatakan bahwa menunda terapi, lebih baik dibandingkan bila memulai terapi ARV sesegera mungkin.22 Penundaan terapi ARV dimaksudkan untuk menghindari efek toksik obat, menyiapkan cadangan obat bila terjadi resistensi kelak, dan menghindari ketidaknyamanan pasien yang menerima banyak obat untuk jangka panjang.23 Di sisi lain, pengobatan ARV lebih awal diperkirakan dapat menjaga fungsi sistem imun dan mengurangi risiko transmisi virus.24 Suatu studi kohort mengenai pelaksanaan program PMTCT di Ukraina oleh Thorne dkk25 (2000 - 2006) pada 3.356 wanita hamil, yang 21% di antaranya pernah atau sedang memakai narkoba suntik. Kebanyakan dari mereka didiagnosis HIV saat kunjungan antenatal dan perbandingan antara klien yang didiagnosis saat trimester pertama dan trimester kedua meningkat, dari 47% pada tahun 2000/2001 menjadi 73% di tahun 2006/2007 (p < 0,001). Persentase wanita yang tidak menerima profilaksis antiretroviral sama sekali menjadi berkurang, dari 18% di tahun 2001 menjadi 7% di tahun 2007 (p < 0,001). Angka bedah sesar (sectio caesarean-SC) elektif relatif stabil, sekitar 34%. Angka transmisi HIV dari ibu ke anak berkurang dari 15,2% di tahun 2001 (interval kepercayaan 95%; 10.2–21.4) menjadi 7,0% di tahun 2006 (interval kepercayaan 95%; 2.6–14.6). Sesudah dilakukan penyesuaian terhadap berbagai macam faktor perancu disimpulkan bahwa penularan HIV dari ibu ke anak berkurang 43% dengan SC elektif dibandingkan persalinan pervaginam dan 75% dengan profilaksis zidovudin dibandingkan tanpa profilaksis. Penelitian oleh Kitahata dkk26 (2005) membandingkan antara pengidap HIV asimtomatik yang mendapat terapi ARV lebih awal (dalam waktu 6 bulan) dengan pengidap HIV yang menunda terapi ARV pada subkelompok yang dibagi berdasarkan kadar CD4 351-500 sel/mm3 dan CD4 > 500 sel/mm3. Di masing-masing subkelompok tersebut, diperbandingkan lagi antara pemberian ARV pada saat kadar CD4 masih di atas nilai tersebut (kelompok yang memulai terapi ARV lebih awal) dengan pemberian ARV pada saat kadar CD4 di bawah nilai tersebut (kelompok yang menunda terapi ARV). Hasilnya, pada tiap subkelompok, risiko meninggal pada pengidap HIV yang menunda pemberian ARV meningkat sebesar 69% dan 94%. Pada anak, diagnosis HIV dan pemberian ARV lebih awal mengurangi mortalitas sebesar 75% dan progresivitas HIV sebesar 75%.27
87

Manfaat yang didapat dari memulai terapi ARV lebih awal harus diimbangi dengan antisipasi terhadap efek samping obat yang mungkin terjadi. ARV yang baru yang lebih poten memiliki efek samping yang lebih sedikit, dan tidak perlu diminum sesering mungkin dapat meningkatkan kepatuhan berobat sehingga dapat menekan perkembangan virus pada tingkat yang rendah. Selain itu, memulai terapi pada kadar CD4 tinggi dapat menurunkan risiko terjadinya efek toksik terkait ARV, seperti neuropati, anemia, dan insufisiensi ginjal.26 a. Model Skrining
Menurut UNAIDS/WHO terdapat empat jenis model skrining HIV, antara lain:28 1. Pemeriksaan dan konseling HIV (voluntary counselling and testing)
Pemeriksaan HIV yang didorong oleh kemauan klien untuk mengetahui status HIV-nya ini masih dianggap penting bagi keberhasilan program pencegahan HIV. Konseling pra tes dapat dilakukan secara individu maupun berkelompok. UNAIDS/WHO mendukung penggunaan uji cepat sehingga hasilnya dapat diketahui segera dan dapat ditindaklanjuti langsung dengan konseling pasca tes baik untuk yang HIV positif maupun HIV negatif.2. Pemeriksaan HIV diagnostik, diindikasikan pada pasien dengan tanda dan gejala yang sejalan dengan penyakit-penyakit yang terkait HIV atau AIDS, termasuk pemeriksaan terhadap tuberkulosis sebagai pemeriksaan rutin.28 Pada pemeriksaan ini, pasien sebaiknya diberikan informasi yang cukup sehingga pasien dapat memutuskan apakah setuju untuk dilakukan pemeriksaan HIV atau tidak. Untuk keadaan di mana pasien tidak dalam posisi memberikan persetujuan, seperti pasien psikiatrik atau pasien yang tidak sadar, pemeriksaan dapat dilakukan bila hasilnya bermanfaat bagi pasien. Jika ini terjadi, harus ada usaha untuk mengkomunikasikan hasil pemeriksaan kepada pasien dan memberitahukan hasil tersebut dengan konseling. 3. Pemeriksaan HIV dengan inisiatif dari tenaga kesehatan (Provider-Initiated Testing and Counseling -PITC) dilakukan pada pasien yang: - Sedang menjalani pemeriksaan terhadap penyakit menular seksual (PMS) di klinik umum atau khusus infeksi menular seksual (IMS). - Sedang hamil, untuk mengatur pemberian antiretroviral untuk mencegah transmisi dari ibu ke bayi. - Dijumpai di klinik umum atau puskesmas di daerah dengan prevalens HIV yang tinggi dan tersedia obat antiretroviral, namun tidak memiliki gejala. Dalam model ini, dibutuhkan mekanisme rujukan yang jelas untuk mendukung sistem perujukan ke pelayanan konseling pascates HIV bagi semua pasien yang diperiksa, yang menekankan pada pencegahan dan pemberian dukungan medis serta psikososial bagi pasien yang hasil tesnya positif HIV. Pada pemeriksaan jenis ini, juga dilakukan konseling sebelum pemeriksaan, hanya saja tidak penuh seperti pada pemeriksaan jenis VCT di atas. Informasi minimal yang harus diketahui pasien pada saat melakukan informed consent adalah: - Manfaat pemeriksaan tersebut secara klinis dan untuk pencegahan. - Hak untuk menolak. - Pelayanan tindak lanjut yang ditawarkan. - Bila hasilnya positif, diberikan pemahaman untuk mengantisipasi keharusan untuk menginformasikan kepada siapa saja yang berisiko yang mungkin tidak sadar bahwa mereka terpajan dengan HIV. Pada pemeriksaan yang sifatnya ditawarkan oleh tenaga medis, misalnya untuk tujuan diagnosis, atau untuk mengetahui status HIV-nya. Selain itu tenaga medis juga dapat menawarkan pemeriksaan HIV kepada wanita hamil untuk memberikan profilaksis
88

antiretroviral untuk mencegah transmisi HIV dari ibu ke bayi. Konseling pada situasi ini harus diperbanyak agar bisa sedikit ”memaksa” ibu untuk mengikuti program PMTCM. Meski demikian, dalam semua kondisi tersebut, pasien tetap memiliki hak untuk menolak. 4. Skrining HIV wajib UNAIDS/WHO mendukung diberlakukannya skrining wajib bagi HIV dan penyakit yang dapat ditransmisikan lewat darah bagi semua darah yang ditujukan untuk transfusi atau pengolahan produk darah lainnya. Skrining wajib dibutuhkan sebelum dilakukannya prosedur-prosedur yang berkaitan dengan pemindahan cairan atau jaringan tubuh, seperti inseminasi buatan, graft kornea, dan transplantasi organ. UNAIDS/WHO tidak mendukung pemberlakuan skrining wajib pada tingkat pelayanan kesehatan individu atau umum. Pemeriksaan sukarela sepertinya dapat mengubah perilaku untuk menghindari penularan HIV ke orang lain. Menyadari bahwa beberapa negara membutuhkan pemeriksaan wajib HIV untuk tujuan imigrasi dan beberapa negara lainnya melakukan pemeriksaan wajib untuk perekrutan dan pemantauan kesehatan tentaranya, UNAIDS/WHO merekomendasikan agar pemeriksaan tersebut dilakukan hanya bila diiringi dengan konseling baik bagi yang hasilnya positif maupun negatif dan sistem perujukan ke pelayanan medis dan psikososial bagi mereka yang mendapat hasil positif.28,29 Menyadari pentingnya menghubungkan orang yang positif HIV ke pusat layanan pencegahan, pengobatan, dan perawatan, UNAIDS dan WHO pada bulan Mei 2007 merilis panduan operasional PITC di tempat pelayanan kesehatan. Panduan ini sejalan dengan keputusan UNAIDS/WHO mengenai pemeriksaan HIV dan merekomendasikan agar seluruh VCT dilengkapi dengan PITC di seluruh tempat pelayanan kesehatan di tingkat epidemi meluas, dan fasilitas kesehatan spesialistik (seperti klinik TB, klinik antenatal, dan klinik infeksi menular seksual) di daerah dengan tingkat epidemi rendah atau terkonsentrasi.
89

Tahun 2006, CDC merekomendasikan pemeriksaan diagnostik dan skrining HIV menjadi suatu pemeriksaan rutin di seluruh sarana pelayanan kesehatan dengan tetap menjaga hak pasien untuk menolak serta menjamin hubungan tenaga kesehatan dan pasien yang kondusif. Rekomendasi ini ditujukan untuk seluruh sarana pelayanan kesehatan, termasuk ruang gawat darurat rumah sakit, ruang rawat inap, klinik infeksi menular seksual, tuberkulosis, klinik bagi penyalahgunaan zat, klinik umum, serta pelayanan kesehatan tingkat primer. Tujuan dari rekomendasi CDC ini adalah untuk meningkatkan jumlah skrining HIV pada pasien di seluruh tempat layanan kesehatan, termasuk ibu hamil; mengembangkan program deteksi dini terhadap HIV; mengidentifikasi dan melakukan konseling terhadap orang yang belum diketahui status HIV-nya serta merujuknya ke tempat pelayanan kesehatan; dan lebih jauh lagi untuk mengurangi transmisi HIV perinatal di Amerika Serikat. Latar belakang rekomendasi CDC adalah sebagai berikut: Diperkirakan 1/4 dari satu juta orang dengan HIV/AIDS di Amerika Serikat tidak menyadari bahwa mereka telah terinfeksi. Hal ini berarti terdapat 250.000 orang yang dapat menularkan HIV kepada pasangannya secara tidak sadar. Dengan adanya skrining HIV sebagai pemeriksaan rutin dalam pelayanan medis, akan lebih banyak orang mengetahui status HIV-nya.31
Orang-orang dengan HIV dapat menerima pengobatan untuk HIV, sehingga dapat memperbaiki kualitas hidup mereka sekaligus memperpanjang umur mereka, jika HIV didiagnosis lebih dini. Saat ini, kebanyakan orang mengetahui infeksi HIV setelah munculnya gejala (dalam suatu studi terhadap orang yang terinfeksi HIV, 65% orang melaporkan bahwa mereka pertama kali diperiksa HIV karena penyakit yang mereka derita).31
Banyak orang yang setelah mengetahui status HIV-nya mengubah perilaku berisiko mereka untuk mengurangi penularan HIV. Pemeriksaan HIV rutin dapat melindungi pasangan dari orang yang sebenarnya mengidap HIV namun tidak mengetahui status HIV-nya. Teorinya, infeksi baru HIV dapat dikurangi 30% setiap tahunnya jika seluruh orang dengan HIV mengetahui status HIV mereka dan mulai mengadopsi perilaku untuk mengurangi penularan HIV.31
Pemeriksaan HIV rutin dapat mengurangi stigma terkait pemeriksaan HIV yang didasarkan pada pengetahuan atau persepsi dari para tenaga kesehatan mengenai risiko terkait HIV/AIDS.31
Persyaratan mengenai perlunya konseling pra-tes dan informed-consent tertulis tidak cocok untuk diberlakukan di instalasi gawat darurat atau tempat pelayanan kesehatan yang sibuk lainnya.31 Oleh karena itu, CDC merekomendasikan bahwa konseling pencegahan tidak perlu dimasukkan ke dalam program skrining HIV di sarana pelayanan kesehatan. Konseling pencegahan sangat disarankan bagi orang-orang yang berisiko tinggi terinfeksi HIV pada keadaan di mana perilaku berisiko tersebut dinilai secara rutin (misalnya di klinik IMS) namun tidak perlu dihubungkan dengan pemeriksaan HIV.11
Selain itu, CDC berpendapat bahwa pertama, pemeriksaan HIV berdasarkan penilaian risiko tidak efektif, khususnya dalam usaha pencegahan HIV melalui transmisi seksual. Kedua, strategi universal, seperti yang sudah diterapkan terhadap wanita hamil dan darah donor, terbukti efektif. Ketiga, kebanyakan orang yang sudah mengetahui bahwa mereka terinfeksi HIV akan mengurangi perilaku berisiko mereka.32 Isi rekomendasi CDC adalah sebagai berikut:
90

Latar belakang rekomendasi CDC adalah sebagai berikut: Diperkirakan 1/4 dari satu juta orang dengan HIV/AIDS di Amerika Serikat tidak menyadari bahwa mereka telah terinfeksi. Hal ini berarti terdapat 250.000 orang yang dapat menularkan HIV kepada pasangannya secara tidak sadar. Dengan adanya skrining HIV sebagai pemeriksaan rutin dalam pelayanan medis, akan lebih banyak orang mengetahui status HIV-nya.31
Orang-orang dengan HIV dapat menerima pengobatan untuk HIV, sehingga dapat memperbaiki kualitas hidup mereka sekaligus memperpanjang umur mereka, jika HIV didiagnosis lebih dini. Saat ini, kebanyakan orang mengetahui infeksi HIV setelah munculnya gejala (dalam suatu studi terhadap orang yang terinfeksi HIV, 65% orang melaporkan bahwa mereka pertama kali diperiksa HIV karena penyakit yang mereka derita).31
Banyak orang yang setelah mengetahui status HIV-nya mengubah perilaku berisiko mereka untuk mengurangi penularan HIV. Pemeriksaan HIV rutin dapat melindungi pasangan dari orang yang sebenarnya mengidap HIV namun tidak mengetahui status HIV-nya. Teorinya, infeksi baru HIV dapat dikurangi 30% setiap tahunnya jika seluruh orang dengan HIV mengetahui status HIV mereka dan mulai mengadopsi perilaku untuk mengurangi penularan HIV.31
Pemeriksaan HIV rutin dapat mengurangi stigma terkait pemeriksaan HIV yang didasarkan pada pengetahuan atau persepsi dari para tenaga kesehatan mengenai risiko terkait HIV/AIDS.31
Persyaratan mengenai perlunya konseling pra-tes dan informed-consent tertulis tidak cocok untuk diberlakukan di instalasi gawat darurat atau tempat pelayanan kesehatan yang sibuk lainnya.31 Oleh karena itu, CDC merekomendasikan bahwa konseling pencegahan tidak perlu dimasukkan ke dalam program skrining HIV di sarana pelayanan kesehatan. Konseling pencegahan sangat disarankan bagi orang-orang yang berisiko tinggi terinfeksi HIV pada keadaan di mana perilaku berisiko tersebut dinilai secara rutin (misalnya di klinik IMS) namun tidak perlu dihubungkan dengan pemeriksaan HIV.11
Selain itu, CDC berpendapat bahwa pertama, pemeriksaan HIV berdasarkan penilaian risiko tidak efektif, khususnya dalam usaha pencegahan HIV melalui transmisi seksual. Kedua, strategi universal, seperti yang sudah diterapkan terhadap wanita hamil dan darah donor, terbukti efektif. Ketiga, kebanyakan orang yang sudah mengetahui bahwa mereka terinfeksi HIV akan mengurangi perilaku berisiko mereka.32 Isi rekomendasi CDC adalah sebagai berikut:
91

Skrining infeksi HIV11
92

o Di seluruh tempat pelayanan kesehatan, skrining terhadap infeksi HIV dilakukan secara rutin terhadap seluruh pasien yang berusia 13-64 tahun. Para petugas kesehatan harus mulai menginisiasi dilakukannya skrining kecuali prevalens infeksi HIV yang tidak diketahui < 0,1%. Bila tidak terdapat data mengenai prevalens HIV, petugas kesehatan harus memulai menginisiasi skrining HIV secara sukarela sampai didapatkan hasil prevalens < 1 per 1000 pasien yang diskrining.
93

o Seluruh pasien yang akan memulai terapi TB diskrining terhadap HIV secara rutin.
94

o Seluruh pasien yang mencari pengobatan PMS, termasuk seluruh pasien yang mengunjungi klinik PMS, diskrining secara rutin setiap kali kunjungan untuk keluhan baru, tanpa memperhatikan apakah pasien diketahui atau dicurigai memiliki perilaku berisiko tertular HIV.
95

Skrining Ulangan11 o Petugas kesehatan harus memeriksa orang-orang yang berisiko terinfeksi HIV minimal setiap tahun. Orang-orang berisiko terinfeksi HIV di antaranya adalah pengguna narkoba suntik dan pasangan seksualnya, pekerja seks, pasangan dari orang yang terinfeksi HIV, laki-laki yang berhubungan seksual dengan laki-laki serta pasangan heteroseksual yang pasangan seksualnya pernah berhubungan seksual dengan satu atau lebih pasangan seksual lain sejak pemeriksaan HIV terakhir. o Petugas kesehatan harus mendorong pasien dan calon pasangan seksualnya untuk melakukan pemeriksaan HIV sebelum memulai hubungan yang baru. o Skrining ulangan terhadap orang yang tidak memiliki perilaku berisiko tertular HIV harus didasarkan pada penilaian klinis. o Bila belum terdapat hasil tes HIV terbaru, setiap orang yang darah atau cairan tubuhnya menjadi sumber penularan HIV terhadap petugas kesehatan harus diinformasikan dan diperiksa HIV pada saat terjadi paparan. Persetujuan dan Informasi Pre-tes11 o Skrining harus dilakukan secara sukarela dan sepengetahuan pasien bahwa akan dilakukan pemeriksaan HIV. HTA Indonesia_ 2010_Skrining HIV di Rumah Sakit Dalam Upaya Pencegahan Penyebaran HIV 28
96

o Pasien harus diberi informasi secara lisan atau tulisan bahwa dia akan diperiksa status HIV-nya kecuali bila pasien menolak (opt-out testing). Informasi tersebut harus mencakup penjelasan mengenai infeksi HIV dan arti dari hasil tes nantinya, serta pasien juga harus diberi kesempatan untuk bertanya dan menolak dilakukannya pemeriksaan. Dengan pemberitahuan seperti itu, persetujuan dilakukannya skrining HIV harus diikutsertakan pada waktu dilakukannya informed-consent secara umum untuk tindakan medis atau pemeriksaan skrining lainnya Tidak direkomendasikan adanya lembar persetujuan terpisah untuk pemeriksaan HIV. o Materi informasi yang diberikan harus mudah dimengerti dan tersedia dalam bahasa yang digunakan setempat. o Bila pasien menolak dilakukannya pemeriksaan HIV, catat di dalam rekam medik. Uji Diagnostik untuk Infeksi HIV11 o Setiap pasien dengan tanda dan gejala yang konsisten dengan infeksi HIV atau infeksi oportunistik AIDS harus diperiksa HIV. o Para klinis harus selalu mewaspadai adanya infeksi HIV akut pada setiap pasien dengan sindrom klinis yang sesuai dan memiliki perilaku berisiko tinggi. Bila dicurigai terdapat sindrom retroviral akut, pemeriksaan RNA plasma harus dilakukan bersama dengan pemeriksaan antibodi HIV untuk mendiagnosis infeksi akut HIV. o Pasien atau orang yang merawat pasien harus diberitahukan secara lisan bahwa akan direncanakan pemeriksaan HIV dan implikasi dari hasil positif atau negatif tes tersebut, serta tetap memberikan kesempatan untuk bertanya dan menolak tes tersebut. Dengan informasi semacam itu, persetujuan pasien pada saat menyetujui tindakan perawatan medis secara umum dianggap sudah cukup untuk menyetujui dilakukannya pemeriksaan HIV.
Menurut CDC, semua wanita hamil harus menjalani skrining HIV sejalan dengan rekomendasi terhadap remaja dan dewasa. Skrining HIV dianjurkan untuk dimasukkan sebagai bagian dari pemeriksaan rutin prakonsepsi, untuk memberi peluang bagi semua wanita untuk mengetahui status HIV sebelum konsepsi. Selain itu, skrining pada awal kehamilan berguna bagi wanita yang terinfeksi HIV serta anaknya untuk dilakukan intervensi yang sesuai (misalnya pemberian antiretroviral, penentuan jadwal persalinan bedah sesar, dan penghindaran menyusui). Rekomendasi ini ditujukan bagi klinisi yang merawat wanita hamil dan HTA Indonesia_ 2010_Skrining HIV di Rumah Sakit Dalam Upaya Pencegahan Penyebaran HIV 29
97

neonatus serta pembuat kebijakan kesehatan yang bertanggung jawab pada populasi ini.11 b. Metode, Cara, dan Target Skrining
CDC merekomendasikan untuk melakukan pemeriksaan HIV secara rutin untuk setiap orang berusia 13-64 tahun yang datang ke sarana pelayanan kesehatan meskipun tanpa gejala. Selain itu, CDC juga merekomendasikan agar pemeriksaan HIV dimasukkan dalam pemeriksaan rutin antenatal bagi wanita hamil.11 Sementara pemeriksaan wajib HIV lebih ditekankan untuk dilakukan pada donor darah dan organ. Pemeriksaan wajib HIV juga dapat dilakukan pada bidang perekrutan tentara atau tenaga kerja imigran.28,29 Panduan WHO mengenai PITC tahun 2007 menyebutkan bahwa metode ini dapat diterapkan pada wilayah dengan tingkat epidemiologi HIV yang berbeda-beda, yaitu daerah dengan epidemi HIV yang rendah, daerah dengan tingkat epidemi HIV yang terkonsentrasi, dan daerah dengan tingkat epidemi yang meluas. Yang dimaksud dengan epidemi yang rendah adalah infeksi HIV hanya ditemukan pada beberapa individu dengan perilaku berisiko (WPS, pengguna narkoba suntik, laki-laki berhubungan seks dengan laki-laki); angka prevalensinya tidak melebih 5% pada subpopulasi tertentu. Sementara itu, yang dimaksud dengan tingkat epidemi yang terkonsentrasi adalah infeksi HIV telah menyebar di subpopulasi tertentu, namun tidak ditemukan di populasi umum. Hal ini menunjukkan aktifnya hubungan antara risiko dengan subpopulasi; angka prevalensi pada subpopulasi melebihi 5%, namun tidak sampai 1% pada wanita hamil. Kemudian, yang dimaksud tingkat epidemi yang meluas adalah infeksi HIV telah ditemukan pada populasi umum, dengan prevalensi pada wanita hamil melebihi 1%.33 Pada semua tingkat epidemi, PITC direkomendasikan untuk dilakukan kepada orang dewasa, remaja, atau anak dengan gejala dan tanda klinis yang sesuai dengan infeksi HIV; anak yang terpapar HIV atau anak yang lahir dari ibu yang HIV positif; anak dengan pertumbuhan suboptimal atau malnutrisi, di daerah dengan epidemi yang meluas, yang tidak membaik dengan terapi yang optimal; serta pria yang menginginkan untuk dilakukan sirkumsisi sebagai pencegahan penularan HIV.33 Pada daerah dengan epidemi yang meluas, PITC direkomendasikan untuk diterapkan kepada pasien rawat inap dan rawat jalan, termasuk pasien TB; pelayanan kesehatan antenatal, persalinan dan post partum; pelayanan infeksi menular seksual; pelayanan kesehatan untuk populasi yang berisiko; pelayanan kesehatan untuk anak usia dibawah 10 tahun; pelayanan kesehatan untuk HTA Indonesia_ 2010_Skrining HIV di Rumah Sakit Dalam Upaya Pencegahan Penyebaran HIV 30
98

remaja; pelayanan pembedahan; dan layanan kesehatan reproduksi, termasuk keluarga berencana.33 Untuk daerah dengan tingkat epidemi yang rendah atau terkonsentrasi, PITC dapat dipertimbangkan untuk diaplikasikan pada tempat pelayanan infeksi menular seksual; pelayanan kesehatan untuk populasi paling berisiko; pelayanan antenatal, persalinan, dan pascamelahirkan; serta pelayanan untuk TB.33 Panduan nasional Inggris tahun 2008 tentang pemeriksaan HIV merekomendasikan pemeriksaan HIV secara rutin kepada orang-orang berikut:34 1. Semua pasien yang datang ke sarana pelayanan kesehatan di mana HIV, termasuk infeksi primer HIV, menjadi salah satu diagnosis banding.
2. Semua pasien yang didiagnosis dengan infeksi menular seksual.
3. Semua partner seksual dari laki-laki atau wanita yang diketahui HIV positif.
4. Semua laki-laki dengan riwayat berhubungan seksual dengan laki-laki
5. Semua wanita partner seksual dari laki-laki yang berhubungan seks dengan laki-laki.
6. Semua pasien dengan riwayat penggunaan narkoba suntik.
7. Semua laki-laki dan wanita yang diketahui berasal dari negara/daerah dengan prevalensi HIV yang tinggi (>1%).
8. Semua laki-laki dan wanita yang berhubungan seksual di luar atau di dalam Inggris dengan pasangan yang diketahui berasal dari negara/daerah dengan prevalensi HIV yang tinggi.
Mengenai skrining HIV pada wanita hamil, Society of Obstetricians and Gynecologists of Canada (SOGC) pada tahun 2006 mengeluarkan panduan skrining sebagai berikut:35 1. Semua wanita hamil harus ditawarkan untuk mengikuti skrining HIV dengan konseling yang memadai. Pemeriksaan harus bersifat sukarela. Skrining harus dipertimbangkan sebagai salah satu bagian dari standar pelayanan antenatal, meskipun klien tetap wajib diinformasikan mengenai manfaat dan risiko pemeriksaan ini serta hak mereka untuk menolak. Mereka tidak boleh diperiksa tanpa sepengetahuannya.
2. Konseling pre-tes dan keputusan pasien mengenai pemeriksaan ini harus didokumentasikan di dalam rekam medik pasien.
3. Pasien yang menolak untuk dilakukan skrining tetap berhak mendapatkan pelayanan antenatal yang optimal. HTA Indonesia_ 2010_Skrining HIV di Rumah Sakit Dalam Upaya Pencegahan Penyebaran HIV 31
99

4. Pasien sebaiknya ditawarkan untuk skrining HIV pada kunjungan pertama ke pelayanan antenatal.
5. Pasien yang hasil tesnya negatif dan berperilaku risiko tinggi harus dites ulang setiap trimester.
6. Wanita hamil yang tidak pernah menerima pelayanan antenatal dan tidak diketahui status HIV-nya harus ditawarkan untuk mengikuti pemeriksaan HIV ketika masuk RS untuk melahirkan. Wanita yang berisiko tinggi mengidap HIV dan tidak diketahui status HIV-nya harus diberikan profilaksis saat persalinan. Profilaksis HIV harus diberikan pada bayi baru lahir.
7. Wanita hamil yang hasil tesnya positif selanjutnya ditangani oleh dokter yang berpengalaman dalam menatalaksana wanita hamil yang positif HIV.
Review oleh Volmink dkk36 (2009) menyebutkan bahwa pemberian antiretroviral (ARV) dapat menurunkan transmisi HIV dari ibu ke anak melalui tiga cara yaitu, (1) menurunkan tingkat replikasi virus sekaligus menurunkan viral load pada wanita hamil, (2) melalui pemberian ARV pra-paparan kepada bayi melalui plasenta, (3) pemberian ARV pasca paparan pada bayi yang telah lahir. Dengan demikian, pemberian ARV pada masa perinatal menurunkan risiko transmisi HIV dari ibu ke bayi. Pada populasi yang tidak mendapatkan ASI, pemberian zidovudin jangka panjang pada masa antenatal dan intrapartum serta kepada bayi setelah lahir menurunkan 66% risiko infeksi HIV pada bayi saat berusia 18 bulan. Lalu bagaimana dengan pemeriksaan HIV di gawat darurat (GD)? Systematic review yang dilakukan oleh Rothman dkk37 (2003) mendukung implementasi skrining HIV di GD. Hal ini didasarkan pada pandangan bahwa infeksi yang tidak terdeteksi mencerminkan hilangnya peluang untuk memberikan pengobatan yang memadai bagi pengidap HIV serta mencegah penularan kepada orang lain. Dan GD dapat menjadi suatu tempat untuk mendeteksi HIV oleh karena banyak pengidap HIV yang tanpa gejala dan berperilaku risiko tinggi yang mendatangi GD. Penelitian oleh Kelen dkk38 (1995) menyimpulkan bahwa program pemeriksaan HIV berbasis GD terhadap populasi berisiko tinggi dapat mendeteksi orang-orang yang belum terdiagnosis HIV dalam jumlah yang signifikan. Rekomendasi CDC juga menyarankan untuk dilakukannya pemeriksaan HIV di GD.11 Memperluas skrining HIV ke tempat pelayanan kesehatan seperti gawat darurat akan memberikan manfaat yang besar. Penularan HIV dapat berkurang sebagai akibat pengurangan perilaku berisiko bagi orang yang menyadari bahwa mereka terinfeksi HIV serta berkurangnya viral load pada pasien yang mendapat terapi ARV.39 HTA Indonesia_ 2010_Skrining HIV di Rumah Sakit Dalam Upaya Pencegahan Penyebaran HIV 32
100

Suatu survei dilakukan pada tahun 1995 di Inggris terhadap para dokter bedah mengenai pemeriksaan antibodi HIV terhadap pasien bedah. Hasilnya beragam. Dari 50 (62,5%) dokter yang mengembalikan kuesioner, 66% berpendapat bahwa mereka menghendaki agar hal tersebut dijadikan pemeriksaan wajib terhadap pasien bedah, meskipun banyak dari mereka juga berpandangan bahwa hal tersebut hanya penting dilakukan terhadap pasien yang dianggap berisiko tinggi. Delapan puluh empat persen responden percaya bahwa cara tersebut dapat melindungi mereka selama mengerjakan operasi. Empat puluh delapan persen responden setuju untuk dilakukan pemeriksaan meski tanpa persetujuan pasien. Hasil tersebut mengungkapkan bahwa dokter bedah setuju diberlakukannya pemeriksaan antibodi HIV terhadap pasien yang akan menjalani operasi dengan keyakinan bahwa hal tersebut dapat melindungi mereka dari terpapar infeksi sewaktu melakukan pembedahan.40 Tampaknya kebijakan skrining HIV rutin terhadap pasien yang akan menjalani pembedahan sangat didukung oleh para tenaga kesehatan itu sendiri.41 Fournier dan Zeppa42 (1989) mengungkapkan bahwa alasan untuk melakukan skrining HIV rutin pada pasien pembedahan antara lain: (1) mengetahui status HIV memungkinkan dokter bedah bekerja sehati-hati mungkin untuk menghindari terjadinya infeksi; (2) manfaat pada pasien, yaitu infeksi HIV dapat mempengaruhi rasio risk-benefit dari suatu prosedur; dan (3) diketahuinya status HIV pasien tidak akan berpengaruh terhadap bagaimana pasien ditangani. Namun, mereka juga mengungkapkan alasan keberatan untuk menerapkan skrining HIV rutin, antara lain: (1) oleh karena risiko pada prosedur yang sifatnya individual rendah, diketahuinya status HIV tidak berarti mengurangi risiko penularan; (2) pelayanan terhadap pasien bisa dipengaruhi secara negatif; (3) ada kemungkinan hasil positif palsu dan; (4) standar etika dari otonomi, privasi, dan informed-consent tidak selalu diterapkan dalam pemeriksaan HIV. Mengenai cara pemeriksaan, panduan Eropa tahun 2008 mengenai pemeriksaan HIV/AIDS merekomendasikan pemeriksaan antibodi HIV-1, HIV-2, dan antigen HIV-1 p24. Sampel untuk pemeriksaan lebih disukai bila diambil dari darah vena, namun bila pungsi vena tidak memungkinkan, sampel dapat di ambil dari tempat lain, seperti darah hasil cukit kulit, cairan mulut atau urin. Hati-hati jika menggunakan uji cepat karena uji cepat tidak memeriksa antigen p24 sehingga dapat memberikan hasil negatif palsu. Pemeriksaan viral load juga tidak direkomendasikan sebab dapat memberikan hasil positif palsu.43 Untuk donor darah dan organ, WHO mewajibkan untuk skrining terhadap HIV.28 Indonesia sendiri sejak tahun 1992 telah melakukan skrining terhadap HIV pada setiap kantong darah yang diperoleh dari donor.10 Metode skrining yang dapat dilakukan terbagi menjadi tiga, tergantung jumlah spesimen donor darah yang terkumpul. Bila spesimen yang terkumpul mencapai 30 perminggu, metode yang digunakan adalah uji rapid; bila spesimen yang terkumpul mencapai 30-60 HTA Indonesia_ 2010_Skrining HIV di Rumah Sakit Dalam Upaya Pencegahan Penyebaran HIV 33
101

perminggu, metode yang digunakan adalah aglutinasi; sedangkan bila spesimen yang terkumpul lebih dari 60 sampel perminggu, metode yang digunakan adalah ELISA.44 Saat ini PMI hanya melaksanakan 2 metode skrining, yakni uji rapid bila spesimen yang terkumpul di bawah 60 perminggu dan ELISA dengan bila spesimen yang terkumpul di atas 60 perminggu. Penelitian mengenai dampak dari pemberlakukan skrining HIV terhadap darah donor pernah dilaporkan di Mozambik. Mozambik merupakan sebagai salah satu negara dengan prevalens HIV tertinggi di wilayah subsahara Benua Afrika, mencapai 16,7% pada tahun 2007. Pada tahun 2005, 121 bank darah di Mozambik telah memberlakukan skrining HIV terhadap darah donor sejumlah 76.663 kantong darah. Dari jumlah tersebut, 47.823 (62,4%) kantong darah diperiksa dengan uji cepat sementara sisanya diperiksa dengan ELISA, namun hasilnya tidak diketahui. Dari jumlah yang diperiksa dengan uji cepat tersebut, sebanyak 4.304 kantong darah (9%) berpotensi terinfeksi HIV. Dengan asumsi bahwa 50% transfusi dilakukan pada anak-anak oleh karena infeksi malaria, pemberlakukan skrining HIV terhadap darah donor dapat menghindari infeksi sebanyak 6.521 kasus pada anak dan 2.152 pada dewasa. Pan American Health Organization pada tahun 2008 mengeluarkan panduan pemeriksaan HIV
menggunakan kombinasi antara uji cepat dengan ELISA. Panduan tersebut berisi tiga macam
algoritme pemeriksaan HIV, dengan penggunaannya pada kondisi yang spesifik. Algoritme
pertama yaitu dengan pemeriksaan HIV secara serial untuk diterapkan pada daerah dengan
prevalens HIV < 5%. Algoritme kedua juga melakukan pemeriksaan HIV secara serial, hanya
saja pemeriksaan ini untuk diterapkan di daerah dengan prevalens HIV > 5% atau terhadap
sasaran pemeriksaan yang memiliki perilaku berisiko tinggi. Pemeriksaan serial yaitu
memeriksakan sampel dengan satu reagen yang sangat sensitif, kemudian sampel yang reaktif
pada pemeriksaan awal diperiksa kembali dengan reagen kedua yang sangat spesifik. Algoritme
ketiga merupakan pemeriksaan HIV secara paralel, yaitu memeriksakan sampel dengan dua
reagen yang berbeda secara bersamaan. Algoritme ketiga ini diusulkan untuk diterapkan pada
keadaan semisal kunjungan pertama wanita hamil ke klinik layanan antenatal, yang
membutuhkan keputusan cepat apakah akan melakukan intervensi untuk mencegah penularan
HIV ke anaknya. Kondisi lain yang memungkinkan diterapkannya strategi pemeriksaan secara
paralel yaitu pada keadaan gawat darurat, kecelakaan kerja, dan kekerasan seksual.
Alat Pemeriksaan dan Besaran Biaya Skrining Untuk melakukan pemeriksaan HIV, spesimen yang disukai adalah darah vena. Pengambilan sampel selain darah vena harus dihindari kecuali pungsi vena sulit atau tidak mungkin dilakukan. Bila sampel diambil dari sumber selain darah vena, misalnya darah dari ujung jari, cairan mulut, atau urin, harus dilakukan pengambilan sampel darah bila hasilnya reaktif atau indeterminat.43 Alat skrining ELISA generasi keempat yang secara bersamaan mampu memeriksa antibodi HIV-1, antigen p24 HIV-1, dan antibodi HIV-2 direkomendasikan untuk digunakan sebagai alat skrining HIV di klinik infeksi menular seksual di Eropa. Sensitivitasnya mencapai 99,78-100% sementara spesifisitasnya mencapai 99,5-99,93%.43
102

Pemeriksaan amplifikasi asam nukleat (HIV-1 viral load) tidak direkomendasikan sebagai
metode skrining diagnostik oleh karena hanya sedikit manfaat yang bisa diperoleh dengan
mendeteksi infeksi primer HIV serta adanya kemungkinan hasil positif palsu. Pemakaian uji
cepat HIV harus hati-hati mengingat uji ini tidak memeriksa antigen p24 HIV-1 dan dapat
memberikan hasil negatif palsu pada masa infeksi primer HIV atau AIDS lanjut.34,43 Ilustrasi
pembiayaan skrining antibodi dan antigen HIV pada darah donor di Indonesia di tahun 2008
adalah sebagai berikut. Bila terdapat sekitar 1,7 juta kantong darah yang dites dan masing-
masing kantong darah membutuhkan biaya US$ 3, sehingga biaya total yang diperlukan adalah
sekitar US$ 5,1 juta (sekitar Rp 48,45 miliar).
103

DAFTAR PUSTAKA
104