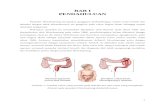
Hirschprung disease
-
Upload
william-sulistyono -
Category
Documents
-
view
33 -
download
5
description
Transcript of Hirschprung disease
BAB IPENDAHULUANPenyakit Hirschsprung atau disebut juga kongenital megakolon adalah penyakit yang disebabkan karena kegagalan dari migrasi ganglion pada kolon selama masa kehamilan. Hal ini menyebabkan bagian distal kolon, dengan panjang yang bervariasi, tidak dapat berelaksasi. Penyakit Hirschsprung lebih sering mengenai daerah rektosigmoid dari colon, tetapi dapat juga mengenai seluruh kolon, dan dalam jumlah kasus yang sedikit juga dapat mengenai usus halus (Kessmann, 2006).Penyebab utama dari gangguan ini adalah faktor genetik. Pada populasi umum kejadian penyakit Hirschsprung diperkirakan 1 per 5000 kelahiran hidup. Kejadian penyakit Hirschsprung ini bervariasi antar etnis. Populasi Asia memiliki angka kejadian paling tinggi yaitu 2,8 per 10.000 kelahiran hidup. Di masa lalu diduga kejadian timbulnya penyakit ini juga cukup banyak namun tidak terdiagnosis (under diagnosis), disebabkan karena kurangnya pemahaman masyarakat awam tentang gejala dini penyakit ini (fk.ugm.ac.id).Penyakit ini biasanya dapat dikenali sejak bayi, tapi beberapa pasien baru datang dengan keluhan konstipasi berat yang menetap di kemudian hari. Gejalanya berupa kesulitan defekasi, nafsu makan yang rendah, berat badan yang kurang dan distensi abdomen yang bertambah berat. Diagnosis yang cepat dan tepat penting untuk mencegah komplikasi, seperti enterokolitis dan ruptur kolon. Biopsi isap rektum dapat mendeteksi adanya hipertrofi dari trunkus saraf dan tidak adanya ganglion pada submukosa kolon, dan memastikan diagnosis penyakit Hirschsprung. Kurang lebih sepertiga dari penderita penyakit Hirschsprung berkembang menjadi Hirschsprung dengan enterokolitis, dimana merupakan penyebab utama kematian pada penyakit Hirschsprung. Dengan terapi yang tepat, mayoritas pasien dapat hidup normal tanpa komplikasi lain (Kessmann, 2006)BAB IITINJAUAN PUSTAKA2.1. KOLON DAN CANALIS ANALIS2.1.1. Anatomi2.1.1.1. KolonIntestinum crassum terdiri dari caecum, appendix vermiformis, colon, rectum, dan canalis analis. Colon terbagi menjadi colon ascendens, colon transversum, dan colon sigmoid (Moore, 2002).Colon ascendens melintas dari caecum ke arah kranial pada sisi kanan kavitas abdominalis menuju hepar, dan membelok ke kiri sebagai flexura coli dextra. Colon ascendens terletak di retroperitoneal. Peritonium di sebelah kanan dan kiri colon ascendens membentuk fossa paracolica. Colon ascendens dan flexura coli dextra mendapat suplai darah dari melalui arteri ileocolica dan arteri colica dextra dan peredaran darah balik melalui vena ileocolica dan vena colica dextra. Saraf untuk colon ascendens berasal dari plexus mesentericus superior (Moore, 2002).Colon transversum merupakan bagian intestinum crassum yang terbesar dan paling mobile. Bagian ini melintasi abdomen dari flexura coli dextra ke flexura coli sinistra, dan membelok ke arah kaudal menjadi colon descendens. Flexura coli sinistra terletak pada bagian kaudal ren sinister. Mesocolon transversum merupakan mesenterium yang paling mobile, sehingga letak colon transverum dapat berubah - ubah. Biasanya colon transversum tergantung ke bawah sampai setinggi anulus umbilicali, bahkan pada orang yang tinggi dan kurus colon transversum dapat sampai ke pelvis. Colon transversum mendapat suplai darah terutama dari melauli arteri colica media dan peredaran darah balik melalui vena mesenterica superior. Saraf untuk colon transversum berasal dari plexus mesentericus inferior (Moore, 2002).
Gambar 2.1 : Anatomi kolonColon descendens melintas secara retroperitoneal dari flexura coli sinistra ke fossa iliaca sinistra, kemudian berubah menjadi colon sigmoid. Pada lintasannya ke kaudal, colon melewati tepi lateral ren sinister. Colon sigmoideum, bagian usus yang berbentuk huruf S dengan panjang yang bervariasi, menghubungkan colon descendens dengan rectum. Colon sigmoid meluas dari tepi pelvis sampai ke segmen sacrum ketiga untuk berubah menjadi rectum. Permulaan rectum ditandai dengan hilangnya taenia coli. Rectosigmoid junction terletak kira - kira 15 cm dari anus. Pendarahan arterial colon descenden disuplai oleh arteri coli sinistra dan arteri sigmoidea superior. Vena mesenterica superior membawa darah balik dari colon descenden dan colon sigmoideum. Persarafan simpatis colon descenden dan colon sigmoideum berasal dari truncus simpaticus bagian lumbal dan plexus hipogastrikus superior. Sedangkan persarafan parasimpatisnya berasal dari nervi splanchnici pelvici (Moore, 2002).Rekum berawal mulai dari ventral vertebra S3 lalu mengikuti lengkung os sacrum dan os coccygis, dan berakhir di sebelah ventrocaudal ujung os coccygis dan beralih menjadi canalis analis. Bagian akhir rectum yang melebar ialah ampulla recti yang menopang dan menyimpan massa tinja sebelum dikeluarkan sewaktu defekasi. Rectum berbentuk S dan memiliki tiga lengkung yang tajam sewaktu mengikuti lengkung sakrokoksigeal. Bagian akhir rectum membelok tajam ke dorsal (lengkung anorektal) untuk beralih menjadi canalis analis. Pada masing masing dari ketiga bagian cembung yang terjadi karena lengkung - lengkung tersebut terdapat pelipatan (plica transversa recti) yang terdiri dari lapis mukosa dan submukosa dan hampir seluruh lapis otot sirkular dinding rectum (Moore, 2002).Persarafan rektum dan anus berasal dari cabang anterior saraf sakralis ke 2, 3, dan 4. Persarafan preganglion ini membentuk 2 saraf erigentes yang memberikan cabang langsung ke rektum dan berlanjut sebagai cabang utama ke pleksus pelvis. Di dalam rektum, serabut saraf ini berhubungan dengan pleksus ganglion Auerbach. Persarafan simpatik berasal dari dalam ganglion lumbal ke 2, 3, 4, dan pleksus praaorta. Persarafan ini bergabung pada kedua sisi membentuk pleksus hipogastrikus di depan vertebral lumbal 5 dan berlanjut ke arah posterolateral sebagai perserafan presakral yang bersatu dengan ganglion pelvis pada kedua sisi (Kartono, 2010).2.1.1.2. Sfingter AnalSfingter anal terdiri dari otot polos dan otot lurik yang membentuk saluran anal. Otot polos sfingter anal interna terletak secara instrinsik pada dinding usus dan menempati dua pertiga distal saluran anal, sebagian besar terletak pada bagian distal dari linea dentata. Otot tersebut merupakan penebalan dari muskulus sirkular yang diperkuat oleh muskulus longitudinal pada bagian luarnya. Sfingter anal merupakan lingkaran otot yang memanjang dan mengelilingi katup anal (anal valves) sampai orifisium anal (Kartono, 2010).
Gambar 2.2 : Anatomi Rektum dan Canalis Anais2.1.2. EmbriologiPerkembangan saluran cerna dibagi menjadi dua tahap besar, yaitu (1) pembentukan tabung usus (gut tube) dan (2) pembentukan masing - masing organ dengan sel - selnya yang khusus (Pratignyo, 2014).Gastrulasi adalah tahap awal pembentukan organ yang multiseluler. Pada mamalia fase fase gastrulasi menyebabkan terbentuknya tiga lapisan, yaitu endoderm, mesoderm, dan ektoderm. Endoderm akan membentuk tabung saluran cerna yang terdiri dari sel epitel dan sel parenkim hati dan pankreas. Mesoderm akan membentuk mesenkim termasuk otot polos dan stroma. Sedangkan ektoderm akan membentuk SSSC yang mengatur motilitas usus (Pratignyo, 2014).
Gambar 2.3 : Lempeng mudigah trilaminerEktoderm terbagi menjadi tiga jenis sel, ektoderm terluar, tabung neural (neural tube), dan krista neural. Krista neural yang tumbuh di bagian dorsal neural tube kelak akan berdiferensiasi membentuk organ - organ yang lebih dewasa seperti melanosit, medula kelenjar adrenal, dentin gigi, saraf simpatis dan parasimpatis dari saraf tepi (Pratignyo, 2014).
Gambar 2.4 : Embryonic plateUntuk berdiferensiasi menjadi organ organ yang lebih dewasa itu, nantinya sel KN perlu bermigrasi ke tempat lain. Kerusakan gen akan mengganggu proses migrasi sel - sel KN tersebut, sehingga dapat mengakibatkan gangguan pembentukan dari organ tersebut di kemudian hari (Pratignyo, 2014).KN terletak di sepanjang sumbu badan embryo (embryonal axis). Pada masa embriologi, awalnya KN tumbuh bersama SSP dalam TN, tetapi kemudian memisahkan diri. Dengan adanya transformasi epiteliomesenkimal, maka sel ini dapat bermigrasi mengikuti jalur yang ditentukan kemudian menetap dan berdiferensiasi menjadi berbagai organ yang lebih dewasa. Penetuan jalur migrasi sepertinya ditentukan oleh molekul yang bersifat promotor dan reduktor (Pratignyo, 2014).Dalam perkembangan fetus manusia, sel - sel KN mulai muncul dalam esofagus yang sedang berkembang pada usia gestasi 5 minggu dan terus bermigrasi ke arah anal kanal secara kraniokaudal pada usia 5 - 12 minggu kehamilan. KN pertama kali membentuk pleksus myenterikus di sebelah luar lapisan otot sirkuler, selanjutnya terbentuk jaringan mesenkim otot longitudinal, sehingga pleksus myenterikus berada di antara dua otot seperti sandwich (Pratignyo, 2014).Setelah petumbuhan secara kraniokaudal terhenti, bersamaan dengan itu neuroblas bermigrasi menyebrangi lapisan otot sirkuler menuju submukosa pada usia 12 - 16 minggu kehamilan membentuk pleksus submukosa dengan pola perkembangan kraniokaudal yang sama (Pratignyo, 2014).Tidak adanya sel ganglion pada penyakit Hirschprung dihubungkan dengan kegagalan migrasi dari sel - sel KN. Semakin dini terjadinya gangguan migrasi mengakibatkan semakin panjang segmen usus yang aganglionik (Pratignyo, 2014).2.1.3. FisiologiPersarafan simpatik dan parasimpatik pada rektum dan saluran anal didapat melalui ganglion pleksus Auerbach dan Meissner, yang akan mengatur peristalsis dan tonus sfingter anal internal. Serabut saraf simpatik merupakan inhibitor dinding usus dan motor sfingter anal internal, sedangkan serabut saraf parasimpatis merupakan motor dinding usus dan inhibisi dari sfingter. Sistem saraf parasimpatik juga merupakan persarafan sensorik untuk rasa atau sensasi distensi rektum (Kartono, 2010).Saat keadaan istirahat, lumen saluran anal akan menutup akibat puborectal sling yang terletak di sebelah kranial dari katup anal (linea dentata) dan oleh tonus istirahat dari sfingter anal eksterna dan interna. Peningkatan tekanan pada bagian kranial saluran anal akan di deteksi oleh reseptor regangan pada sleeve and sling complex. Peristalsis yang kuat akan menimbulkan regangan pada sleeve and sling. Untuk menghambat gerakan peristalsis tersebut, diperlukan kontraksi yang kuat yang harus dibantu secara sadar untuk menimbulkan kontraksi sling dan sfingter anal eksternal. Mekanisme sleeve and sling dapat membedakan antara gas, benda padat, benda cair, maupun gabungan, juga dapat mengeluarkan salah satu tanpa mengeluarkan yang lain. Setelah menilai isi, sling akan mengubah bentuk bolus sehingga dapat melalui anus (Kartono, 2010).Sfingter anal internal merupakan bagian akhir otot pendorong yang secara aktif mengeluarkan feses atau udara melalui anus. Serabut otot ini, terdiri atas gabungan otot sirkular dan longitudinal yang membantu peristalsis di saluran anal sampai ke orifisium. Bagian longitudinal membantu peristalsis di seluruh saluran anal sampai ke orifisium. Bagian longitudinal membantu peristalsis di seluruh saluran anal sampai ke orifisium (Kartono, 2010).
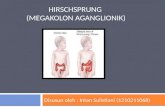
2.2. PENYAKIT HIRSCHSPRUNG2.2.1. DefinisiPenyakit Hirschsprung adalah gangguan perkembangan yang ditandai dengan hilangnya ganglion pada bagian distal kolon sehingga menyebabkan obstruksi fungsional (Wagner, 2014).
Gambar 2.5 : Kolon pada penderita Penyakit Hirschsprung
2.2.2. EpidemiologiDi Amerika Serikat penyakit Hirschsprung mengenai kurang lebih 1 per 5400 7200 kelahiran hidup. Sedangkan insiden di seluruh dunia sekitar 1 kasus per 1500 7000 kelahiran hidup (Wagner, 2014).Penyakit Hirschsprung lebih sering pada anak laki laki dibandingkan dengan anak perempuan. Risiko penyakit Hirschsprung pada saudara penderita Hirschsprung segmen pendek sekitar 3 5 % anak laki laki dan 1 % anak perempuan. Risikonya semakin besar (12,4 33 %) pada anak yang memiliki saudara penderita penyakit Hirschsprung pada seluruh segmen colon (total colon) (Kessmann, 2006).Delapan gen telah diketahui berhubungan dengan penyakit Hirschsprung. Penyakit Hirschsprung berhubungan dengan gen yang terikat dengan multiple endocrine neoplasia tipe II A (medullary carcinoma, tumor tiroid, dan tumor adrenal). Sindrom Down (trisomi 21) merupakan kelainan kromosomal yang paling banyak berhubungan dengan penyakit ini, sekitar 10% dari penderita (Kessmann, 2006).2.2.3. PatofisiologiUsus manusia dipersarafi oleh tiga pleksus saraf, yaitu pleksus submukosal (Meissner), pleksus mienterikus (Auerbach), dan pleksus submukosal (Henle). Semua pleksus ini berintegrasi dan mengatur usus dalam semua aspek termasuk absorbsi, sekresi, pengaturan aliran darah, dan motilitas (Wagner, 2014).Motilitas usus normal utamanya dibawah kontrol sinyal instrinsik dari enteric nervous system (ENS) yang besifat parasimpatik. Otot halus pada usus berkontraksi dan berrelaksasi dibawah kontrol enteric ganglia. Aktivasi dari ENS menyebabkan relaksasi otot halus pada usus, yang dimediatori oleh nitrit oxide dan neurotransmiter enterik lainnya (Wagner, 2014).Refleks motilitas normal terdapat pada rektum distal. Adanya bolus yang membuat distensi rektum akan membuat kontraksi rektum di atas bolus, dan sebaliknya membuat relaksasi rektum di bawah bolus. Refleks ini murni pada intestin sendiri. Bila refleks ini tidak ada, berarti terjadi abnormalitas atau tidak terdapat sel sel ganglion intramural (Kartono, 2010).Dengan tidak adanya sel sel ganglion, sistem saraf ekstrinsik mengakibatkan kenaikan inervasi intestin. Sistem kolinergik dan adrenergik menunjukkan kenaikan inervasi dua sampai tiga kali lipat pada kolon aganglionik. Diperkirakan sistem eksitasi adrenergik mendominasi fungsi inhibisi pada segmen aganglionik, sehingga menciptakan kenaikan otot polos. Inervasi kolinergik bertambah nyata dalam segmen aganglionik dan mendominasi eksitasi (Kartono, 2010).Pada penderita penyakit Hirschprung bagian kolon paling distal sampai pada bagian usus tertentu, yang berbeda ukuran penampangnya, tidak mempunyai ganglion parasimpatik intramural. Bagian kolon aganglionik ini tidak dapat mengembang sehingga tetap sempit dan mengganggu proses defekasi. Sehingga kolon proksimal akan mengembang karena timbunan feses dan menjadi megakolon.2.2.4. Klasifikasi Hirschprung segmen pendek (Hirschprung kasik), daerah aganglionik terbatas dari rektum sampai sigmoid. Hirschprung segmen panjang, dengan daerah aganglionik meluas melebihi sigmoid. Kolon aganglionik total, jika aganglionosis mengenai seluruh kolon. Aganglinosis universal, jika aganglionosis mengenai seluruh kolon dan hampir seluruh usus halus
Gambar 2.6 : Persentase panjang kolon yang terkena pada penyakit Hirschsprung2.2.5. Gambaran KlinisManifestasi klinis penyakit Hirschsprung yang khas biasanya terjadi pada masa neonatus cukup bulan dengan keterkambatan pengeluaran mekonium pertama, kemudian diikuti dengan distensi abdomen dan muntah hijau atau fekal, yang mirip tanda obstruksi setinggi ileum atau lebih distal (Kartono, 2010).Pada lebih dari 90% bayi normal, mekonium pertama keluar dalam waktu 24 jam pertama, namun pada mayoritas penyakit Hirschsprung, lebih dari 90% kasus, mekonium pertama keluar setelah 24 jam pertama. Berdasarkan penelitian oleh Darmawan Kartono pada 123 penderita penyakit Hirschsprung didapatkan bahwa 93,5% mekonium pertama dikeluarkan setelah 24 jam, dan hanya pada 6,5% pasien (8 orang) yang dapat mengeluarkan mekonium pada 24 jam pertama (Kartono, 2010).Distensi abdomen merupakan gejala penting lainnya pada penyakit Hirschsprung. Berdasarkan penelitian oleh Swenson pada tahun 1973 ditemukan tanda distensi abdomen pada 87,1% kasus penyakit Hirschsprung neonatal. Disrensi abdomen merupakan manifestasi obstruksi usus letak rendah dan dapat disebabkan karena kelainan lain seperti atresi ileum (Kartono, 2010).Muntah berwarna hijau sering terjadi pada penyakit Hirschsprung. Hal ini disebabkan oleh obstruksi usus, yang dapat pula terjadi pada kelainan lain dengan gangguan pasase usus, seperti pada atresia ileum, enterokolitis nekrotikans neonatal, atau peritonitis intrauterine (Kartono, 2010).Penyakit Hirschsprung yang disertai dengan enterokolitis dapat menunjukkan gambaran klinis distensi abdomen yang diikuti diare berupa feses cair bercampur mukus dan berbau busuk dengan atau tanpa darah dan umumnya berwarna kecoklatan (Kartono, 2010).2.2.6. Diagnosis2.2.6.1. RadiologisPemeriksaan foto polos abdomen dan khususnya pemeriksan barium enema merupakan pemeriksaan diagnostik terpenting untuk mendeteksi penyakit Hirschsprung pada neonatus (Kartono, 2010).Foto polos abdomenPenyakit Hirschsprung pada neonatus cenderung menampilkan gambaran obstruksi letak rendah. Daerah pelvis terlihat kosong tanpa udara. Gambaran obstruksi usus letak rendah juga dapat ditemukan pada penyakit lain seperti atresia ileum, sindrom sumbatan mekonium, atau keadaan sepsis karena enterokolitis nekrotikans neonatal (Kartono, 2010).Foto polos abdomen juga dapat menyingkirkan diagnosis lain seperti peritonitis intrauterin atau perforasi gaster. Pada foto polos abdomen neonatus, distensi usus halus dan distensi usus besar tidak selalu mudah dapat dibedakan. Pada pasien bayi dan anak gambaran d istensi kolon dan gambaran massa feses terlihat lebih jelas (Kartono, 2010).Foto enema bariumPemeriksaan enema barium harus dikerjakan pada neonatus yang mengalami keterlambatan pengeluaran mekonium yang diikuti distensi abdomen dan muntah hijau, walaupun pada pemeriksaan colok dubur didapatkan gejala dan tanda - tanda obstruksi usus telah mereda atau menghilang. Tanda - tanda klasik radiografik yang khas pada penyakit Hirschsprung adalah :
Gambar 2.7 : Foto radiologi enema barium1. Segmen dilatasi.2. Segmen transisi, daerah perubahan dari segmen sempit ke segmen dilatasi. Segmen transisi dibagi menjadi 3, yaitu Abrupt (tampak perubahan mendadak dari segmen sempit ke segmen dilatasi) Cone (bentuk seperti kerucut) Funnel (bentuk cerobong, dimana perubahan dari segmen sempit ke segmen dilatasi terlihat sangat gradual).3. Segmen sempit dari sfingter anal dengan panjang tertentu.Selain itu dapat juga didapatkan gambaran permukaan mukosa yang tidak teratur yang menunjukkan proses enterokolitis. Dapat juga terlihat gambar garis garis lipatan melintang (transverse fold), terutama jika larutan barium mengisi lumen kolon dilatasi yang berada dalam keadaan kosong (Kartono, 2010).Foto Retensi BariumBarium yang teretensi dalam waktu 24 - 48 jam setelah enema merupakan tanda penting penyakit Hirschsprung, terutama pada masa neonatal. Harus dibedakan antara retensi barium karena penyakit Hirschsprung dengan kasus obstipasi kronik non penyakit Hirschsprung. Gambaran barium pada penyakit Hirschsprung tampak membaur dengan feses ke arah proksimal dalam kolon berganglion normal, sedangkan pada kasus obstruksi kronik non penyakit Hirschsprung, barium akan lebih mengumpul di daerah distal, di daerah rektum dan sigmoid (Kartono, 2010).2.2.6.2. Patologi AnatomiSwenson pada tahun 1955 melakukan pemeriksaan patologi anatomi pertama untuk penyakit Hirschsprung. Swenson melakukan biopsi dengan cara mengeksisi seluruh tebal dinding rektum, sehingga pleksus mienterikus dapat diperiksa. Tidak adanya ganglion dalam spesimen biopsi membuktikan diagnosis penyakit Hirschsprung, sedangkan adanya ganglion akan menyingkirkan diagnosis penyakit Hirschsprung. Kerugian prosedur biopsi oleh Swenson ini secara teknik relatif sulit dan membutuhkan anestesi umum, selain itu dapat menyebabkan inflamasi dan jaringan fibrosis yang dapat mempersulit pembedahan selanjutnya (Kartono, 2010).Biopsi Seluruh Tebal Dinding RektumBiopsi seluruh tebal dinding rektum dilakukan dengan mengambil dua lapis muskulus, yaitu lapis muskulus sirkular dan lapis muskulus longitudinal. Oleh karena itu teknik ini ideal untuk mendeteksi sel ganglion Auerbach beserta serabut sarafnya. Akan tetapi prosedur biopsi ini harus dikerjakan dengan anestesi umum dan terdapat kemungkinan timbul komplikasi perdarahan, infeksi, dan fibrosis perirektal. Biopsi seluruh tebal dinding rektum dikerjakan hanya bila hasil pemeriksaan klinis, radiologis, dan biopsi isap diragukan. Swenson tidak menganggap biopsi seluruh tebal dinding rektum suatu pemeriksaan yang rutin untuk menegakkan diagnosa penyakit Hirschsprung (Kartono, 2010).Biopsi isap rektumBiopsi isap mukosa dan submukosa rektum menggunakan alat Rubin atau Noblett dapat dikerjakan lebih sederhana, aman dan tanpa menggunakan anestesi umum. Pada pemeriksaan ini, spesimen biopsi dilakukan potongan serial dan pewarnaan hematoksilin dan eosin. Diagnosis penyakit Hirschsprung ditegakkan bila tidak ditemukan sel ganglion Meissner dan ditemukan penebalan serabut saraf. Junis dkk melaporkan akurasi pemeriksaan ini 100%. Andrassy dkk juga melaporkan pemeriksaan teknik ini pada 30 pasien berumur kurang dari satu tahun juga menghasilkan akurasi 100% juga, tanpa adanya hasil false possitive atau false negative (Kartono, 2010).Pewarnaan Histokimia AsetilkolinesterasePada penderita penyakit Hirschsprung terdapat peningkatan aktivitas asetilkolinesterase pada serabut saraf dalam lamina propria dan muskularis mukosa. Penemuan ini diikuti dengan tidak ditemukannnya sel ganglion dengan pewarnaan Kamovsky dan Roots yang mempermudah terlihatnya penebalan serabut saraf. Pewarnaan untuk asetilkolinesterase dengan teknik yang sama sangat membantu menemukan sel ganglion di submukosa atau di lapisan muskularis (Kartono, 2010).Pewarnaan ImunohistokimiaPewarnaan histokimia asetilkolinesterase pada sediaan potong beku memang membantu penegakan diagnosis, tapi butuh pengalaman dalam interpretasinya dan perdaharan mukosa yang mungkin terjadi dapat mempersulit pemeriksaaan (Kartono, 2010).2.2.6.3. ManometriPada tahun 1949 Swenson melakukan penelitian patofisiologi untuk pertama kalinya pada pasien megakolon. Pengukuran dilakukan dengan memasukkan balon kecil dengan kedalaman yang berbeda - beda dalam rektum dan kolon. Dari penelitian ini didapatkan bahwa kontraksi yang terjadi dalam segmen aganglionik tidak ada hubungannya dengan kontraksi dalam kolon proksimal yang berganglion normal (Kartono, 2010).Penelitian manometri pada penyakit Hirschsprung memberikan hasikan hasil sebagai berikut :1. Dalam segmen dilatasi terdapat hiperaktivitas dengan aktivitas propulsif yang normal.2. Dalam segmen aganglion tidak terdapat gelombang peristalsis yang terkoordinasi. Motilitas normal digantikan oleh kontraksi yang tidak terkoordinasi dengan intensitas dan kurun waktu yang berbeda - beda.3. Refleks inhibisi antara rektum dan sfingter anal internal tidak berkembang. Refleks relaksasi sfingter anal internal setelah distensi rektum tidak terjadi, bahkan terdapat kontraksi spastik. Relaksasi spontan tidak pernah terjadi.Pemeriksaan elektromanometri ini dapat membantu diagnosis dan hanya dikerjakan bila hasil pemeriksaan klinis, radiologis, dan histologi meragukan, misalnya pada kasus yang asimtomatik atau penyakit Hirschsprung ultra pendek, yang menurut beberapa ahli lebih tepat disebut sebagai akalasia rektal. Banyak peneliti melaporkan bahwa manometri anorektal lebih sulit dilakukan pada neonatus karena keterbatasan sensitivitas alat dan sangat diperlukan pengalaman dari operator yang melakukan (Kartono, 2010).Berdasarkan pengalaman, Darmawan Kartono tidak pernah melakukan elektromanometri, karena disamping tidak tersedianya peralatannya, diagnosis penyakit Hirschsprung pada umumnya dapat ditegakkan berdasarkan riwayat penyakit, pemeriksaan klinis, dan pemeriksaan radiologis. Bila diagnosis masih diragukan, selama memungkinkan pasien diobservasi dan dilakukan pemeriksaan radiologis ulang pada 1 - 2 bulan kemudian (Kartono, 2010).2.2.7. Diagnosis BandingBila kita menemukan neonatus dengan gejala dan tanda hambatan passase usus letak rendah, maka diagnosis penyakit Hirschprung harus kita pikirkan. Walaupun keadaan ini dapat diakibatkan juga oleh hambatan mekanis seperti atresia setingi ileum atau lebih rendah, stenosis anal, dan ileus mekonium. Gangguan motilitas usus yang mengakibatkan obstruksi letak rendah juga dapat memberi gambaran mirip penyakit Hirschprung, seperti prematuritas enterokolitis nekrotikans, sepsis dengan keseimbangan elektrolit, hipotiroidisme, dan obstipasi psikogenik.Atresia IleumPada gambaran klinis atresia ileum, abdomen mengalami distensi mirip penyakit Hirschprung. Mekonium pada umumnya tidak keluar spontan, karena terperangkap di dalam ileum di distal atresia dan di kolon. Bila mekonium diusahakan keluar dengan irigasi, mekonium yang keluar jumlahnya sedikit, kering, berbutir - butir dan berwarna hijau muda. Pada pemeriksaan foto polos abdomen terlihat tanda - tanda obstruksi usus letak rendah, dan foto enema barium memperlihatkan gambaran kolon mikro.Sumbatan MekoniumMekonium yang terlalu pekat atau lengket di daerah kolon distal dapat mengakibatkan sindrom sumbatan mekonium (meconium plug syndrome). Sindrom ini diduga akibat kekurangan tripsin atau akibat kelainan mobilitas kolon tanpa kelainan sel ganglion. Pada foto polos abdomen terlihat pelebaran seluruh usus tanpa disertai bayangan kalsifikasi dan tanpa bayangan busa sabun dalam lumen usus seperti pada ileus mekonium atau enterokolitis nekrotikans.Atresia RektalAtresia pada kolon lebih sering dijumpai pada daerah rektum atau sigmoid. Bila letak atresia dekat dengan anus, maka diagnosis dapat ditegakkan dengan pemeriksaan colok dubur, dimana atresia akan teraba di ujung jari. Akan tetapi sebaiknya tetap dilakukan pemeriksaan enema barium karena lumen yang menuju sigmoid terlalu kecil, sehingga tidak dapat teraba oleh jari. Pemeriksaan rektoskopi juga dapat dilakukan untuk diagnosis.Enterokolitis Nekrotikans NeonatalSekilas gejala dan tanda enterokolitis nekrotikans neonatal (ENN) mirip dengan penyakit Hirschprung. Diagnosis ENN perlu dipikirkan pada neonatus dengan stres perinatal atau dengan faktor predisposisi lainnya. Pada ENN, neonatus mengalami gangguan pasase usus menyeluruh karena traktus gastrointestinal mengalami hipoksia, ulserasi, dan gangguan fungsiPeritonitis IntrauterinPeritonitis intrauterin atau sering disebut sebagai peritonitis mekonium, disebabkan oleh kontaminasi mekonium intraperitoneal sebagai akibat dari perforasi gastrointestinal semasa kehidupan intrauterin. Perforasi dapat terjadi sejak awal kehamilan sampai menjelang atau sesudah persalinan. Mekonium yang keluar dari traktus intestinal dan masuk ke dalam intraperitoneal akan mengalami kalsifikasi, terutama bila perforasi terjadi pada awal masa kehamilan. Manifestasi klinis ditentukan oleh umur janin saat terjadinya perforasi, penyebab perforasi, dan proses penyembuhan.Perforasi usus intrauterin dapat (1) sembuh total tanpa manifestasi klinis, (2) terjadi atresia intestinal tanpa diikuti tanda - tanda peritonitis, (3) tanda obstruksi usus disertai tanda - tanda peritonitis.2.2.8. PenatalaksanaanPembedahan merupakan satu-satunya cara penyembuhan pada penyakit Hirschsprung, berupa pengangkatan segmen usus aganglion, yang diikuti dengan pengembalian kontinuitas usus. Teapi medis hanya dilakukan untuk persiapan bedah. Prosedur bedah pada penyakit Hirschsprung terbagi menjadi bedah sementara dan bedah definitif (Kartono, 2010) .Tindakan Bedah Sementara Sebelum prosedur bedah definitif dilakukan, terlebih dahulu dilakukan tindakan bedah sementara yang bertujuan untuk dekompresi terhadap tekanan abdomen yang meningkat. Dekompresi ini dapat dilakukan dengan pembuatan kolostomi pada kolon paling distal yang bergangion normal. Tindakan ini bertujuan untuk untuk menghilangkan obstruksi usus dan mencegah enterokolitis yang merupakan penyebab utama kematian pada penyakit Hirschsprung (Kartono, 2010).Tindakan bedah definitif dapat langsung dikerjakan tanpa kolostomi, jika dekompresi secara medis berhasil. Indikasi kolostomi 1. Pasien Neonatus. Tindakan bedah definitif langsung tanpa kolostomi dapat menimbulkan banyak komplikasi dan kematian. Kematian dapat mencapai 28,6%. Kematian ini disebabkan oleh kebocoran anastomosis dan abses dalam rongga pelvis.2. Pasien anak dan dewasa yang terlambat terdiagnosis. Kelompok pasien ini memiliki kolon yang sangat terdilatasi, yang sudah terlalu besar untuk dianastomosiskan dengan rektum melalui bedah definitif. Dengan kolostomi, Kolon yang sudah terdilatasi akan mengecil kembali setelah 3 sampai 6 bulan pasca kolostomi. Sehingga anastomosis pada bedah definitif akan lebih mduah dikerjakan dan memberi hasil yang lebih baik.
Gambar 2.8 : Kolostomi3. Pasien dengan enterokolitis berat dan dengan keadaan umum yang buruk. Kolostomi dilakukan untuk mencegah komplikasi pasca bedah definitif, dengan kolostomi pasien akan cepat mencapai perbaikan keadaan umum.
Pada pasien yang tidak termasuk dalam kategori 1 , 2, dan 3 diatas dapat langsung dilakukan tindakan bedah definitif (Kartono, 2010).Tindakan Bedah DefinitifTindakan bedah definitif untuk menangani penyakit Hirschsprung telah dilakukan oleh Swenson dan Bill sejak tahun 1948. Saat itu mereka mengembangkan prosedur rektosigmoid yang dilanjutkan dengan prosedur pull through atau tarik terobos melalui abdomino perineal. Selain prosedur Swenson, beberapa prosedur lain juga sudah dikembangkan masing-masing oleh Duhammel, Soave dan Rehbein, dengan tujuan mengurangi komplikasi dan memperbaiki keberhasilan fungsional (Kartono, 2010).
Gambar 2.9 : Perbandingan prosedur bedah definitifProsedur SwensonSwenson memperkenalkan prosedur rektosigmoidektomi dengan preservasi sfingter anal. Anastomosis dilakukan langsung di luar rongga peritoneal. Pembedahan ini disebut sebagai prosedur rektosigmoidektomi dilanjutkan dengan pull through abdominoperineal. Prosedur ini merupakan prosedur bedah definitif pertama yang berhasil untuk penanganan pasien Hirschsprunng. Pada masa pascabedah ditemukan beberapa komplikasi seperti kebocoran anastomosis, stenosis, inkontinensi, enterokooitis, dan lain lain (Kartono, 2010).Enterokolitis pascabedah dapat merupakan proseslanjut dari enterokolitis prabedah. Pada prosedur Swenson ini, enterokolitis diduga terjadi karena spasme puntung rektum yang ditinggalkan (anal sphincter tightness). Sebenarnya sisa rektum yang ditinggalkan merupakan segmen aganglionosis sebagai preservasi sfingter untuk mencegah inkontinensia. Prosedur ini dikenal sebagai prosedur Swenson I (Kartono, 2010).Untuk mengurangi spasme sfingter anal, Swenson melakukan sfingterektomi parsial posterior Pada tahun 1964, dimana puntung rektum ditinggalkan 2 cm pada bagian anterior dan 0,5 cm pada bagian posterior.Prosedur ini dikenal sebagai prosedur Swenson II. Sayangnya, prosedur tersebut tidak mengurangi spasme sfingter anal dan tidak pula mengurangi komplikasi enterokolitis pasca bedah, justru angka kebocoran pada prosedur Swenson II lebih tinggi dari Swenson I. Hal ini dikarenakan pada prosedur Swenson II terdapat ketegangan anastomosis di bagian posterior (Kartono, 2010).
Prosedur DuhamelPada tahun 1956, Duhamel memperkenalkan prosedur bedah definitif dengan rektum yang dipertahankan. Kolon yang berganglion normal di proksimal ditarik melalui retrorektal transanal dan dilakukan anastomosis kolorektal ujung ke sisi pada bagian posterior dari rektal (Kartono, 2010).Pada prosedur Duhamel yang asli, anastomosis kolon proksimal dilakukan pada sfingter anal internal, hal ini dinilai kurang baik karena sering terjadi stenosis, inkontinensi, dan pembentukan fekaloma dalam puntung rektum yang ditinggalkan terlalu panjang. Sehingga dikembangkan berbagai modifikasi untuk mengatasi masalah masalah di atas (Kartono, 2010).Prosedur SoaveSoave membuat prosedur bedah yang berbeda dengan dua prosedur bedah dari Swenson dan Duhamel. Soave melakukan pendekatan abdominoperineal dengan membuang lapisan mukosa rektosigmoid dari lapisan seromuskular. Kemudian dilakukan penarikan kolon berganglion normal keluar anus melalui selubung seromuskular rektosigmoid. Prosedur ini disebut juga pull through endorektal. Setelah 21 hari, sisa kolon yang diprolapskan dipotong. Boley pada waktu yang hampir bersamaan melakukan prosedur pull through endorektal persis seperti prosedur Soave dengan anastomosis langsung tanpa kolon yang diprolapskan lebih dulu. Teknik ini dilakukan untuk mencegah retraksi kolon bila terjadi nekrosisbagian kolon yang diprolapskan (Kartono, 2010).Prosedur RehbeinPada dasarnya prosedur Rehbein merupakan prosedur State, berupa reseksi anterior yang diekstensi ke distal sampai dengan pengangkatan sebagian besar rektum. Reseksi segmen aganglion yang mencakup sigmoid kemudian dilanjutkan dengan anastomosis ujung ke ujung yang dikerjakan intra abdominal ekstraperitoneal. Dalam prosedur ini puntung rektum aganglion yang ditinggalkan masih cukup panjang sehingga sering didapatkan obstipasi residif (Kartono, 2010).Prosedur Bedah Definitif melalui LaparoskopiBeberapa tahun terakhir penangan penyakit Hirschsprung pada anak usia dini berkembang dari dua atau tiga tahap rekonstruksi (multi stage procedure) menjadi prosedur satu tahap (single stage procedure). Telah dilaporkan oleh banyak pusat bedah mengenai pengalaman melakukan pull through kolon primer single stage. Prosedur single stage ini dikerjakan dengan teknik laparoskopik. Keuntungan prosedur single stage ini dibandingkan dengan prosedur multi stage adalah (1) angka morbiditas lebih kecil, (2) tidak memerlukan kolostomi, (3) masa rawat lebih singkat, dan (4) biaya rumah sakit lebih murah. Dengan perkembangan prosedur bedah minimal, prosedur Swenson, Duhamel, dan Soave dapat dikerjakan dengan bedah laparoskopi (Kartono, 2010).Kesulitan bedah laparoskopik di antaranya : (1) pada prosedur Duhamel, dengan endostapler puntung rektum tidak terpotong tuntas , sehingga terjadi pouchitis, (2) Anus bayi yang masih kecil tidak muat untuk stapler sehingga menyulitkan, (3) biaya mahal, (4) waktu yang dibutuhkan lebih lama (Kartono, 2010).Prosedur Soave Single Stage TransanalTeitelbaum, dkk. setelah berhasil melakukan teknik pull through laparoskopik, mereka mengembangkan prosedur Soave single stage transanal. Menurut merka prosedur ini dapat menekan biaya rumah sakit, mengurangi risiko kerusakan struktur pelvis, insidens perdarahan intraperitoneal dan adhesi rendah, dan tanpa jaringan parut bekas insisi pada dinding abdomen (Kartono, 2010).Pemilihan prosedur bedah definitif yang harus dipilih bergantung pada masing masing spesilis bedah yang mengerjakan, prosedur mana yang biasa dikerjakan. Semua prosedur pada dasarnya memiliki keberhasilan yang kurang lebih sama, selama pembedahan dikerjakan sesuai dengan spesifikasi tahapan masing masing prosedur yang dipilih dikerjakan dengan baik. Keberhasilan prosedur bedah single stage melalui laparoskopik pada pasien neonatus masih perlu pengamatan (follow up) jangka panjang (Kartono, 2010).2.2.9. KomplikasiEnterokolitisEnterokolitis yang menyertai penyakit Hirschsprung atau HAEC (Hirschsprung associated enterocolitis) adalah keradangan pada usus dengan gejala klinis demam, distensi perut, diare dan sepsis. Pada pemeriksaan otopsi penderita HAEC juga didapatkan kelainan berupa abses pada kriptus, ulserasi mukosa, dan nekrosis transmural (Pratignyo, 2014).Walaupun terdapat kemajuan dalam mendiagnosis dan menanganani penyakit Hirschsprung, penyakit Hirschsprung yang diikuti enterokolitis tetap memberikan angka morbiditas dan mortalitas yang tinggi. Enterokolitis dapat terjadi sebelum ditegakkanya diagnosa penyakit Hirschsprung maupun setelah operasi definitif (Pratignyo, 2014).Beberapa teori telah diajukan sebagai patofisiologi dari keadaan ini, (1) obstruksi parsial yang menyebabkan iskemia mukosa dan invasi bakteri pada segmen yang terdilatasi, (2) hipersensitifitas terhadap antigen bakteri, (3) infeksi khusus kman Clostridium difficile, meskipun kuman ini tidak ditemukan pada semua kasus enterokolitis yang menyertai penyakit Hirschsprung, (4) hilangnya pertahanan imunitas mukosa, termasuk diantaranya gangguan transfer imunoglobulin sekretori A pada mukosa sel. Dalam suatu penelitian dilaporkan bahwa semua pasien yang menderita enterokolitis mengalami penurunan jumlah Ig A sekretori, bahkan sampai absen (Pratignyo, 2014).Beberapa faktor risiko enterokolitis pada penyakit Hirschsprung adalah keterlambatan diagnosis. Selain itu enterokolitis lebih sering terjadi pada penyakit Hirschsprung dengan segmen yang lebih panjang. Hal ini berhubungan dengan kemungkinan tersisanya segmen aganglion pasca bedah definitif dan kemudian akan menyebabkan stasis aliran isi lumen (Pratignyo, 2014).Bayi dengan trisomi 21 dikatakan memiliki risiko tinggi terkena HAEC, begitu juga pada pasien dengan riwayat HAEC sebelumnya. Redding et al melaporkan angka rekurensi sebanyak 37% sebelum operasi, sedangkan insidens setelah operasi sebanyak 63%. Risiko HAEC juga meningkat sebanyak 2,8 12% pada pasien yang memiliki keluarga menderita penyakit Hirschsprung (Pratignyo, 2014).Menurut Bill dan Chapman, HAEC adalah sindroma yang terdiri dari distensi abdomen, nyeri, diare eksplodif cair, demam, dan penurunan keadaan umum. Elhalaby juga mencirikan insiden gejala sebagai berikut : distensi abdomen (91%), diare ekspolsif cair (82%), muntah (61%), demam (40%), letargi (32%), perdarahan peranum (6%), dan syok hipovolemik (6%) (Pratignyo, 2014).Gejala enetrokolitis pada penyakit Hirschsprung bervariasi mulai dari yang sederhana hanya kembung sampai syok hipovolemik. Gejala yang tidak khas dapat menyebabkan keterlambatan diagnosa. Pada pemeriksaan darah dapat ditemukan leukositosis dengan pola shift to the left atau hasil kultur darah menunjukkan bakteremia (Pratignyo, 2014).Untuk imaging pada HAEC mencakup foto polos abdomen, dimana menurut analisa Delphi didapatkan : (1) gambaran cut off kolon rektosigmoid yang tidak terisi udara, (2) dilatasi loop usus, (3) air fluid level, (4) pneumatosis intestinalis, (5) gambaran sawtooth dengan dinding mukosa yang irregular, (6) dan udara bebas yang dapat dilihat pada kasus lanjut akibat perforasi kolon (Pratignyo, 2014).Pasien dengan kecurigaan HAEC memerlukan antibiotik berspektrum luas dan resusitasi cairan. Pasien diberikan antibiotik golongan ampisilin, gentamisin, dan metronidazol, lalu dimonitor ketat cairannya. Pasien dimasukkan ke ruang intensif bila gejalanya berat atau dalam keadaan sepsis untuk mendapatkan vasopresor atau ventilasi. Rectal wash out segera dilakukan, dengan rektal tube yang besar sesuai ukuran pasien, menggunakan NaCl 20 40 cc per kg, dilakukan 2 4 kali. Pada awalnya wash out sebaiknya dilakukan sesering mungkin sampai cairan yang keluar jernih, selanjutnya 2 kali sehari sampai cairan menghilang. Cairan yang keluar harus diperhatikan agar tidak sampai terjadi retensi cairan klisma yang dapat menyebabkan usus terdilatasi dan meningkatkan risiko perforasi (Pratignyo, 2014).Sebagian peneliti mencoba nebggunakan metode non invasif untuk merelaksasikan sfingter interna, yang dikenal sebagai chemical sfincterectomi, untuk mencegah HAEC. Dengan menggunakan isosorbit dinitrat topikal atau nitrogliserin yang dioleskan ke anal kanal (Pratignyo, 2014).
Kebocoran anastomosisKebocoran anastomosis dinilai merupakan komplikasi pascabedah yang serius dan dapat menyebabkan kenaikan angka morbiditas dan mortalitas pasca bedah (Kartono, 2010).1. Ketegangan pada garis anastomosis. Pada kedua ujung usus yang dianastomosiskan terjadi tarikan yang dapat berakibat dengan kebocoran atau bahkan terlepas sama sekali.2. Vaskularisasi pada tepi sayatan kedua ujung usus yang dianastomosiskan tidak adekuat yag disebabkan oleh kurang baiknya pembebasan koolon yang akan dianastomosiskan. Pembuluh darah yang terikat pada waktu anastomosis juga dapat merupakan penyebab kebocoran anastomosis.3. Infeksi dan abses disekitar anastomosis menyebabkan proses penyembuhan anastomosis terganggu.4. Trauma akibat colok dubur atau businasi pasca bedah yang dikerjakan terlalu dini dan kurang hati hati. Colok dubur sebaiknya dikerjakan dua minggu pasca bedah.5. Pemasangan rectal tube yang terlalu besar dapat menyebabkan nekrosis tekan pada anastomosis.6. Distensi usus pasca bedah menimbulkan tegangan pada garis anastomosis yang berakhir dengan disrupsi anastomosis.Angka kebocoran anastomosis bervariasi, sperti yang ditemukan dalam survei Seksi Bedah American Academy Pediatrics (1979). Frekuensi terjadinya kebocoran anastomosis pada prosedur Swenson yang dilaporkan oleh Swenson sendiri adalah 2,5 5%, namun angka ini meningkat pada prosedur Swenson yang dikerjakan oleh spesialis bedah lain. Angka kebocoran dipengaruhi oleh prosedur bedah dan ketrampilan spesialis bedah yang mengerjakan (Kartono, 2010).Pada kebocoran ringan terdapat tanda umum peradangan ringan, seperti sedikit peningkatan suhu badan, selain itu pada daerah perineum bisa ditemukan adanya abses atau infiltrat. Sedangkan pada kebocoran berat, didapatkan tanda umum peradangan lebih nyata, seperti kenaikan suhu tubuh yang tinggi dan menetap. Pada dasarnya, pada kebocoran anastomosis terjadi proses radang di rongga pelvis, pelvioperitonitis, atau peritonitis umum dengan tanda tanda ileus. Kenaikan suhu tubuh yang disertai tanda tanda ileus harus dicurigai sebagai proses infeksi yang berhubungan dengan pembedahan yang dilakukan (Kartono, 2010).Keadaan ini disebabkan karena infeksi di sekitar daerah anastomosis, baik dengan atau tanpa disrupsi anastomosis sebagian atau seluruhnya, akibat retraksi atau nekrosis kolon yang dianastomosiskan. Manifestasi seperti yang disebutkan diatas, erat hubungannya dengan proses radang dan gangguan fungsi usus bagian distal yang selanjutnya menyebabkan kecacatan dan kematian (Kartono, 2010).Berbagai komplikasi dan kematian yang dibahas oleh Swenson dari tinjauan 483 kasusnya, sebagian besar disebabkan oleh kebocoran anastomosis. Nixon juga sependapat bahwa penyulit prosedur Swenson terutama terutama berhubungan dengan infeksi yang disebabkan oleh enterokolitis dan kontaminasi abdominal yang bersumber dari kebocoran anastomosis. Sedangkan Darmawan Kartono berpendapat bahwa sebenarnya prosedur bedah apapun memiliki peluang untuk terjadi kebocoran selama dilakukan anastomosis langsung (Kartono, 2010).Pencegahan kebocoran anastomosis dilakukan dengan memperhatikan faktor predisposisi saat tindakan pembedahan. Deteksi dini kebocoran anastomosis perlu dilakukan, dan bila menemui kebocoran anastomosis harus segera dilakukan pengamanan dengan pembuatan kolostomi pada segmen proksimal. Tujuan utama pada prosedur Duhamel modifikasi Adang adalah anastomosis yang dikerjakan tidak langsung dengan memprolapskan kolon yang ditarik. Hal ini pada dasrnya adalah upaya untuk mencegah kebocoran anastomosis kolon (Kartono, 2010).StenosisStenosis adalah salah satu komplikasi pasca bedah selain kebocoran, yang dapat disebabkan oleh gangguan penyembuhan luka di daerah anastomosis. Infeksi primer atau akibat kebocoran anastomosis dapat mengakibatkan pembentukan jaringan fibrosis di garis anastomosis dan sekitarnya (Kartono, 2010).Prosedur bedah yang digunakan. Prosedur bedah tertentu memiiki kecenderungan untuk menjadi stenosis tertentu. Stenosis sirkular pada garis anastomosis dapat disebabkan oleh prosedur Swenson atau Rehbein. Stenosis berbentuk segitiga atau oval di bagian posteriordisertai sisa septum yang tidak terpotong tuntas terjadi pada prosedur Duhamel. Stenosis memanjang dapat terjadi pada prosedur Soave (Kartono, 2010).Stenosis di daerah anastomosis menyebabkan gangguan defekasi dengan segala akibatnya. Pada saat defekasi feses akan keluar sedikit demi sedikit karena dorongan feses pada daerah proksimal, sehingga menyerupai inkontinensi. Kemudian akan diikuti oleh enterokolitis yang ditandai dengan distensi abdomen, kenaikan suhu tubuh, dan feses cair yang berbau busuk. Komplikasi lain yang dapat terjadi yaitu fistulasi rektoperineal (Kartono, 2010).Pencegahan dapat dilakukan dengan melakukan pemeriksaan pasca bedah yang cermat pada daerah anastomosis. Bila terdapat stenosis, jika perlu dapat dilakukan businasi atau tindakan koreksi yang lain. Dengan memperhatikan penyebab stenosis pada masing masing prosedur maka dapat dilakukan upaya perbaikan prosedur bedah sehingga komplikasi stenosis dapat dhindari (Kartono, 2010).Khusus upaya pencegahan Stenosis pada prosedur Duhamel :1. Puntung rektum yang ditinggalkan jangan terlalu pendek, sebaiknya 3 cm di atas dasar peritoneal.2. Septum harus dipotong tuntas3. Ruang retrorektal harus dibebaskan sempurna sepanjang dinding posterior puntung rektum hingga sfingter analGangguan Fungsi Sfingter AnalPembedahan definitif dikatakan berhasil bila pasien dapat defekasi spontan, setiap hari, tanpa bantuan obat laksana maupun suppositoria. Pasien dapat menguasai fungsi sfingter anal dengan baik. Gangguan fungsi sfingter anal terdiri dari :InkontinensiaPasien tidak dapat menguasai sfingter anal sama sekali, dimana feses mengalir terus menerus. Hal ini disebabkan karena pemotongan rektum yang terlalu rendah atau terlalu dekat dengan garis mukokutan. Prosedur Rehbein dilaporkan memiliki insidens inkontinensia paling kecil, yaitu 0%. Hal ini dikarenakan pada prosedur Rehbein reseksi segmen rektum dilakukan intraabdominal, sehingga rektum aganglion masih tersisa cukup panjang. Sebaliknya, masalah pada prosedur Rehbein adalah obstipasi berulang.Pada prosedur Swenson reseksi rektum dilakukan perineal, sehingga pemotongan rektum dapat dilakukan sesuai kebutuhan. Swenson menganjurkan pemotongan rektum dilakukan pada 2 sampai 3 cm dari garis mukokutan (Kartono, 2010).Pemotongan sisa rektum yang terlalu panjang mengakibatkan obstipasi, dan sisa rektum yang terlalu pendek mengakibatkan inkontinensia. Akan tetapi pemotongan yang terlalu pendek atau terlalu panjang cukup sulit dihindari, karena usia pasien saat pembedahan berbeda - beda. Pemotongan 2 cm pada bayi berbeda maknanya dengan pemotongan 2 cm pada anak yang lebih besar. Hal ini menyebabkan obstipasi atau inkontinensia sulit dihindari (Kartono, 2010).Prosedur Duhamel merupakan prosedur dengan insidens obstipasi ulang dan inkontinensi yang paling kecil, hal ini dikarenakan pada prosedur Duhamel tidak seluruh lingkaran reseksi sfingter anal direseksi, reseksi hanya dilakukan pada setengah lingkaran bagian posterior. Spasme sfingter anal internal juga jarang ditemukan pada prosedur Duhamel, sehingga insidens enterokolitis juga lebih rendah (Kartono, 2010).SoilingPasien kadang tidak dapat menahan defekasi, sehingga feses keluar dan mengotori celana (soiling). Pada masa pasca bedah prosedur Duhamel, soiling disebabkan oleh sisa septum. Soiling akan berakhir setelah sisa septum dipotong tuntas. Swenson menemukan 10 dari 483 pasiennya mengalami soiling permanen atau inkontinensia (Kartono, 2010).Obstipasi berulangPada keadaan ini pasien tetap tidak dapat defekasi secara spontan dan harus ditolong dengan laksans atau supoitoria dengan atau tanpa manifestasi gangguan pasase usus. Keadaan ini disebabkan oleh sfingter anal yang masih panjang, atau segmen aganglionik yang ditinggalkan terlalu panjang. Keketatan anal (anal tightness) pasca bedah prosedur Swenson mencapai 8% (Kartono, 2010).2.2.10. PrognosisBanyak perbedaan pada laporan penelitian jangka panjang pasca bedah definitif untuk penyakit Hirschsprung. Beberapa peneliti melaporkan tingkat keberhasilan yang tinggi, sementara peneliti lain melaporkan kejadian yang signifikan dari obstipasi dan inkontinensia. Secara umum, lebih dari 90% laporan penelitian pasien pasca bedah definitif penyakit Hirschsprung memiliki hasil yang memuaskan. Namun, banyak pasien mengalami gangguan fungsi usus selama beberapa tahun sebelum penahanan defekasi yang normal berkembang. Sekitar 1% dari pasien dengan penyakit Hirschsprung memiliki inkontinensia yang menetap dan membutuhkan kolostomi permanen (Wagner, 2014).Total aganglionosis kolon dihubungkan dengan hasil yang lebih buruk, dengan 33% dari pasien yang mengalami inkontinensia persisten dan 14% membutuhkan ileostomy permanen. Pasien dengan kelainan kromosom dan sindrom tertentu juga memiliki hasil klinis yang lebih buruk (Wagner, 2014).
BAB IIIKESIMPULANPenyakit Hirschsprung atau kongenital megakolon merupakan penyakit kongenital yang disebabkan kegagalan migrasi krista neural, sehingga usus bagian distal menjadi aganglion dan tidak dapat berrelaksasi. Ras Asia memiliki angka kejadian tertinggi, yaitu sebesar 2,8 per 10.000 kelahiran.Penyakit Hirschsprung harus didiagnosis dengan cepat dan tepat, karena keterlambatan diagnosis yang akan memperlambat tindakan bedah definitif akan menyebabkan komplikasi dan memperburuk prognosis.
DAFTAR PUSTAKA
Kartono, Darmawan, 2010, Penyakit Hirschsprung, Jakarta, Sagung SetoMoore, Keith L., 2002, Anatomi Klinis Dasar, Jakarta, Hipokrates.Pratignyo, Moh. Adjie, 2014, Penyakit Hirschsprung, Tangerang, SAP Publish Indonesia.Wagner, Justin P., 2014, Hirschsprung Disease http://emedicine.medscape.com/article/178493-overviewKessmann, Jennifer, 2006, Hirschsprungs Disease : Diagnosis and Management. < http://www.aafp.org/afp/2006/1015/p1319.html>Anonim, 2015, Teliti Mutasi Gen Penyakit Hirschsprung, Titis Raih Doktor http://ugm.ac.id/id/berita/9769-teliti.mutasi.gen.penyakit.hirschsprung.titis.raih.doktor
34