52939849 LTM Pemicu II Modul GCT Sindrom Nefritis
-
Upload
erry-saputro -
Category
Documents
-
view
90 -
download
0
Transcript of 52939849 LTM Pemicu II Modul GCT Sindrom Nefritis

5/16/2018 52939849 LTM Pemicu II Modul GCT Sindrom Nefritis - slidepdf.com
http://slidepdf.com/reader/full/52939849-ltm-pemicu-ii-modul-gct-sindrom-nefritis 1/3
LTM Pemicu II Modul Ginjal dan Cairan Tubuh
SINDROM NEFRITIK DAN NEFRITIS LUPUS
Adrian Himawan Singgih, 0806323681
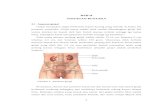
SINDROM NEFRITIK Sindrom nefritik merupakan suatu kompleks klinis,
biasanya mempunyai awitan akut, dan ditandai dengan:
1. hematuria dengan eritrosit dismorfik dan silinder
eritrosit dalam urin;
2. beberapa derajat oliguria dan azotemia;
3. hipertensi.Pada sindrom nefritik ini dapat ditemukan pula proteinuria
dan edema, tetapi tidak terlalu mencolok seperti pada sindrom
nefrotik. Lesi yang menyebabkan sindrom nefritik memperlihatkan
proliferasi sel di dalam glomerulus disertai sebukan leukosit. Reaksi
peradangan ini mencederai dinding kapiler darah sehingga eritrosit
dapat lolos ke dalam urin, dan menyebabkan perubahan
hemodinamik sehingga terjadi penurunan GFR (Glomerular Filtration
Rate) yang bermanifestasi sebagai oliguria, retensi cairan, dan
azotemia.
Glomerulonefritis Proliferatif Akut (Pascainfeksi)
Glomerulonefritis proliferatif (PGN) difus, salah satu
penyakit glomerulus yang sering ditemukan, biasanya disebabkan
oleh kompleks imun. Antigen pemicu berasal dari eksogen atauendogen. PGN difus pola eksogen biasanya berupa GN pascainfeksi,
sedangkan yang disebabkan oleh antigen endogen biasanya berupa
nefritis lupus. Infeksi oleh organisme lain, selain streptokokus, juga
bisa disebabkan infeksi pneumokokus dan stafilokokus tertentu
serta sejumlah infeksi virus umum, seperti campak, gondongan,
cacar air, hepatitis B dan C.
Patogenesis
Pembentukan kompleks imun berperan dalam patogenesis
GN pascastreptokokus akut. Ditemukan gambaran tipikal pada
penyakit kompleks imun, seperti hipokomplementemia dan endapan
granular IgG dan komplemen di GBM.
Sifat antigen patogenik masih misterius, dan belum jelas
apakah kompleks dalam darah atau yang terbentuk in situ yangmerupakan bentuk predominan. Penelitian menunjukkan bahwa C3
mengendap di GBM sebelum IgG mengendap. Oleh karena itu, cedera
primer mungkin disebabkan oleh pengaktifan komplemen. Akhirnya,
terbentuk kompleks imun. Antigen yang terlibat dalam patogenesis
GN pascastreptokokus akut adalah endostreptosin dan protein
pengikat plasmin nefritis.
Histopatologi
Bila dilihat dengan mikroskop cahaya, perubahan paling
khas adalah peningkatan selularitas rumpun glomerulus yang
merata dan mengenai hampir seluruh bagian glomerulus (difus).
Peningkatan selularitas ini disebabkan oleh proliferasi dan
pembengkakan sel endotel dan mesangial serta oleh sebukan
neutrofil dan monosit. Kadang terdapat trombus di dalam lumenkapiler dan nekrosis dinding kapiler. Pada beberapa kasus juga dapat
ditemukan crescent cells di kapsula Bowman. Jika perubahan
tersebut melibatkan sebagian besar glomerulus, polanya akan
menyatu dengan yang ditemukan pada GN progresif cepat.
Pemeriksaan dengan mikroskop elektron memperlihatkan kompleks
imun tersusun sebagai punuk yang melekat ke GBM di subendotel,
intramembranosa, atau subepitel. Kadar komplemen serum rendah
selama fase aktif penyakit, dan titer antistreptolisin O serum
meningkat pada kasus pascastreptokokus.
Gejala Klinis
Awitan penyakit ginjal cenderung akut, didahului oleh
malaise, demam ringan, mual, dan sindrom nefritik. Pada kasus yang
biasa, oliguria, azotemia, dan hipertensi biasanya hanya ringansampai sedang. Biasanya terdapat hematuria makroskopik, urin
tampak coklat berasap dan bukan merah terang. Proteinuria adalah
gambaran konstan pada penyakit ini. Proteinuria ini terkadang
cukup berat sehingga dapat timbul sindrom nefrotik. Terdapat pula
gejala-gejala lainnya seperti diare, nafsu makan menurun, anoreksia,
dan edema.
Tata Laksana
Pengobatan glomerulonefritis pascainfeksi streptokokus
ditujukan untuk mengeliminasi infeksi streptokokus dengan
antibiotik dan menyediakan terapi suportif hingga terjadi resolusi
spontan dari inflamasi glomerulus. Selama fase inflamatoris akut,
pasien dianjurkan untuk beristirahat dan berbaring. Diuretik dan
obat anti hipertensi digunakan untuk mengontrol volume cairanekstraselular dan tekanan darah. Jarang digunakan dialisis untuk
mengontrol hipervolemia atau sindrom uremik.
Prognosis
Pada kasus epidemik, sebagian besar anak mengalami
pemulihan. Sebagian anak mengalami GN progresif cepat atau
penyakit ginjal kronis. Prognosis pada kasus sporadik tidak terlalu
jelas. Pada orang dewasa, 15% sampai 50% pasien mengalami
penyakit ginjal tahap akhir dalam beberapa tahun atau 1 sampai 2
dekade kemudian, bergantung pada keparahan klinis dan histologis.
Pada anak, prevalensi penyakit kronis setelah kasus sporadik GN
akut jauh lebih rendah.
Glomerulonefritis Progresif Cepat (Rapidly ProgressiveGlomerulonephritis)
Glomerulonefritis progresif cepat (RPGN) merupakan suatu
sindrom klinis dan bukan bentuk spesifik glomerulonefritis. Secara
klinis, penyakit ini ditandai dengan penurunan fungsi ginjal yang
cepat dan progresif disertai oliguria berat serta kematian akibat
gagal ginjal dalam beberapa minggu atau bulan bila tak diterapi.
Apapun penyebabnya, gambaran histologik ditandai
dengan kenampakan bulan sabit (crescentic cells) di sebagian besar
glomerulus akibat proliferasi sel epitel parietal di kapsula Bowman
dan sebagian oleh sebukan monosit dan makrofag.
Glomerulonefritis Crescentic (CrGN)
CrGN Tipe I (Anti-GBM)
Idiopatik
Sindrom Goodpasture
CrGN Tipe II (Kompleks Imun)
Idiopatik
Lupus eritematosus sistemik
Pascainfeksi
Purpura Henoch-Schonlein
CrGN Tipe III (Pausi Imun) Terkait ANCA
Idiopatik
Granulomatosis Wegener
Poliarteritis mikroskopik
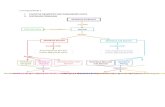
Patogenesis
Glomerulonefritis crescentic (CrGN) disebabkan oleh
sejumlah penyakit yang berbeda-beda, dimana sebagian terbatas di
ginjal dan sebagian lagi bersifat sistemik. Klasifikasi CrGN ini dibagi
menjadi 3 kelompok berdasarkan temuan imunologik karena
sebagian besar kasus cedera glomerulus disebabkan oleh proses
imunologis. 3 kelompok tersebut yaitu:
a. CrGN tipe I
CrGN tipe ini biasanya disebut sebagai penyakit anti-GBM
(anti- Glomerular Basement Membrane). Pada cedera jenis ini,
antibodi ditujukan pada antigen tetap di GBM. Nefritis anti-GBM spontan pada manusia terjadi akibat terbentuknya
autoantibodi terhadap GBM. Antibodi secara langsung
berikatan dengan molekul kolagen di sepanjang GBM, yang
pada pemeriksaan dengan mikroskop imunofluoresens
menghasilkan pola linier. Hal ini berbeda dengan kebanyakan
bentuk lain nefritis kompleks imun yang menunjukkan pola
granular.

5/16/2018 52939849 LTM Pemicu II Modul GCT Sindrom Nefritis - slidepdf.com
http://slidepdf.com/reader/full/52939849-ltm-pemicu-ii-modul-gct-sindrom-nefritis 2/3
Terkadang antibodi anti-GBM ini bereaksi silang dengan
membran basal alveolus paru, sehingga terjadi lesi di paru
dan ginjal secara bersamaan. Kelainan ini disebut juga
sindrom Goodpasture.
Nefritis anti-GBM ini merupakan penyebab cedera pada
sindrom Goodpasture. Antigen membran basal yang berperan
dalam nefritis anti-GBM klasik pada sindrom Goodpasture
adalah komponen dari domain nonkolagen dari rantai α3
kolagen tipe IV. CrGN tipe I ditandai dengan endapan linier
IgG dan C3 di GBM.
b. CrGN tipe II
CrGN tipe ini merupakan penyakit yang diperantarai oleh
kompleks imun. Penyakit ini dapat merupakan penyulit
semua nefritis kompleks imun, termasuk GN
pascastreptokokus, SLE (Systemic Lupus Erythematosus),
nefropati IgA, dan purpura Henoch-Schönlein. Pada beberapa
kasus, kompleks imun dapat dibuktikan, tetapi penyebab
yang mendasarinya tidak diketahui. Pemeriksaan
imunofluoresens menunjukkan pola granular khas (lumpy
bumpy ) pada semua kasus CrGN tipe II.
c. CrGN tipe III
CrGN tipe ini disebut juga CrGN tipe pausi-imun. Pada
pemeriksaan mikroskop imunofluoresens dan elektron, tidak
ditemukan antibodi anti-GBM atau kompleks imun. Sebagian
besar pasien memiliki antibodi antisitoplasma neutrofil
(ANCA) di dalam serumnya (ANCA berperan dalam sebagian
vaskulitis). Sebagian kasus CrGN tipe III merupakan
komponen suatu vaskulitis sistemik, seperti poliarteritis
nodosa mikroskopik atau granulomatosis Wegener. Sebagian
kasus CrGN tipe III juga ada yang terbatas di ginjal, sehingga
disebut idiopatik.
Sebagian besar penyakit CrGN ini bersifat idiopatik. Bila
penyebabnya dapat diidentifikasi, sekitar 12% pasien mengidap
CrGN tipe I dengan atau tanpa keterlibatan paru; 44% mengidap
CrGN tipe II; 44% sisanya mengidap CrGN tipe III pausi-imun.
Awitan RPGN mirip dengan yang ditemukan pada sindrom
nefritik, kecuali oliguria dan azotemia yang terlihat lebih mencolok
pada CrGN. Proteinuria terkadang mendekati rentang nefrotik.Sebagian pasien mengalami anuria dan memerlukan dialisis jangka-
panjang atau transplantasi.
Histopatologi
Ginjal tampak membesar dan pucat, sering dengan
perdarahan petekiae di permukaan korteksnya. Glomerulus mungkin
memperlihatkan nekrosis dan trombosis fokal, proliferasi endotel
fokal atau difus, dan proliferasi sel mesangial, bergantung pada
stadium penyakit yang mendasarinya. Gambaran histologik
didominasi oleh pembentukan struktur bulan sabit yang khas, yang
terbentuk dari proiliferasi sel epitel dan migrasi monosit ke ruang
Bowman, kadang disertai sel raksasa berinti banyak. Kadang-kadang
ditemukan sel T di bulan sabit dan ruang Bowman. Pada tipe pausi-
imun, sel ini diperkirakan berperan merekrut makrofag keglomerulus. Bulan sabit akhirnya menyebabkan obliterasi ruang
Bowman dan menekan glomerulus. Serat fibrin tampak mencolok di
antara lapisan sel di bulan sabit. Pada semua kasus ditemukan ruptur
GBM. Seiring dengan waktu, bulan sabit dapat menjadi jaringan
parut.
Tata Laksana
a. CrGN tipe I
Sebelum adanya terapi imunosupresif, 80% pasien dengan
nefritis anti-GBM mengalami penyakit ginjal tahap akhir dalam
waktu 1 tahun, dan banyak pasien yang meninggal karena
perdarahan paru atau komplikasi uremia. Dengan terapi
plasmaferesis dini dan rutin, ketahanan hidup pasien dan kondisi
ginjal meningkat secara dramatis. Plasmaferesis darurat dilakukan
tiap hari atau berselang-seling hingga antibodi anti-GBM tidak
terdeteksi lagi di sirkulasi darah (1 hingga 2 minggu). Untuk
menekan sintesis baru dari antibodi anti-GBM, digunakan
prednisone (1 mg/kg/ hari) yang dikombinasikan dengan
siklofosfamid (2-3 mg/kg/hari) atau azatioprin (1-2 mg/kg/hari).
Pasien yang membutuhkan dialisis jarang mengalami pemulihan
pada fungsi ginjalnya. Titer anti-GBM dimonitor secara periodik
untuk mengukur respons terhadap terapi. Pada pasien dengan
gangguan ginjal tahap akhir, transplantasi ginjal merupakan pilihan
yang tepat.
b. CrGN tipe III
Glukokortikoid dan siklofosfamid merupakan obat lini
pertama dalam pengobatan glomerulonefritis tipe pausi-imun dan
memperbaiki penyakit ini secara dramatis. Pada 3 hari pertama
secara berturutan diberikan steroid intravena yang kemudian diikuti
dengan steroid per oral sekitar 1 mg/kg BB. Siklofosfamid diberikan
per oral dengan dosis harian 1-2 mg/kgBB. Untuk mencegah
toksisitas siklofosfamid, pengobatan dapat dialihkan dari
siklofosfamid menjadi azatioprin atau mikofenolat setelah 6 bulan.
Pengobatan ini dilanjutkan hingga minimal 1 tahun.
Prognosis
Secara kasar, prognosis sebanding dengan jumlah bulan
sabit: pasien dengan bulan sabit kurang dari 80% glomerulus
memiliki prognosis sedikit lebih baik daripada mereka yang
persentase bulan sabitnya lebih besar.
NEFRITIS LUPUSLupus eritematosus sistemik (LES) adalah penyakit
multiorgan yang didasarkan kelainan imunologik. Organ yang sering
terkena yaitu sendi, kulit, ginjal, otak, hati dan lesi dasar pada organ
tersebut adalah suatu vaskulitis yang terjadi oleh karena
pembentukan dan pengendapan kompleks antigen-antibodi. Apabila
organ yang terkena ginjal disebut nefritis lupus. Nefritis lupus
biasanya mengikuti penyakit LES yang telah muncul sebelumnya,
tetapi sekitar 3-6% mendahului gejala-gejala lupus yang lain
sehingga ketika diagnosis LES ditegakkan, kelainan ginjalnya sudah
lanjut.
Nefritis lupus (NL) ditemukan pada 90% pasien lupus
eritematosus sistemik. Gambaran klinis NL sangat bervariasi, mulai
dari tanpa kelainan pada urinalisis atau hanya proteinuria/
hematuria ringan sampai gambaran klinis yang berat yaitu sindrom
nefrotik atau glomerulonefritis yang disertai penurunan fungsi ginjal
yang progresif.
Angka Kejadian
NL maupun LES pada umumnya terutama ditemukan pada
anak perempuan. Umumnya ditemukan setelah umur 10 tahun,
sangat jarang pada anak kurang dari 5 tahun. Perbandingan anak
perempuan dan lelaki adalah 5 : 1, sedangakan umur rata-rata pada
saat diagnosis ditegakkan adalah 11,7 (8-18) tahun.
Diagnosis
Diagnosis ditegakkan bila ditemukan ≥ 4 dari 11 kriteria
diagnostik LES menurut American College of Rheumatology yang
direvisi pada tahun 1982 :
1. Ruam kupu-kupu di muka (butterfly rash)
2. Ruam diskoid di kulit
3. Fotosensitif
4. Ulkus di mulut
5. Artritis6. Serositis (pleuritis atau perikarditis)
7. Kelainan ginjal (proteinuria >0,5 gram/hari atau atau
silinder selular: sel darah merah/Hb/granular/tubular
8. Kelainan neurologik: kejang atau psikosis
9. Kelainan hematologik: anemia hemolitik dengan
retikulositosis atau leukopenia (<4000/µl pada ≥ 2

5/16/2018 52939849 LTM Pemicu II Modul GCT Sindrom Nefritis - slidepdf.com
http://slidepdf.com/reader/full/52939849-ltm-pemicu-ii-modul-gct-sindrom-nefritis 3/3
pemeriksaan) atau limfopenia (<1500/µl) atau
trombositopenia (<100.000/µl)
10. Kelainan imunologik: sel LE positif atau titer abnormal anti
DNA terhadap DNA tubuh atau anti-Sm positif atau uji
serologi sifilis positif palsu (dalam 6 bulan terakhir)
11. Pemeriksaan antibodi antinuklir (ANA) positif
Etiologi
Penyebab berbagai kelainan imunologi yang ditemukan
pada LES yaitu disfungsi sel T, produksi autoantibodi, pembentukan
kompleks imun, hipokomplementemia yang akhirnya menyebabkan
kerusakan jaringan sampai saat ini belum dapat dipastikan. Diduga
kuat bahwa etiologi LES, dan juga NL, bersifat multifaktorial.
Beberapa hal yang disepakati berperan pada LES adalah:
1. Faktor genetik sebagai predisposisi
Hal ini didukung oleh beberapa fakta, yaitu:
LES ditemukan pada 63% kembar identik
Frekuensi penemuan genotipe HLA-DR3 dan DR2
meningkat
Frekuensi pasien LES pada anggota keluarga yang
lain juga meningkat
2. Faktor hormonal
Hal ini didukung oleh fakta bahwa:
Pasien perempuan jauh lebih banyak, terutama
pada masa pubertas dan pasca pubertas
Pada binatang percobaan yaitu tikus NZB/W yang
dibuat menderita LES. Bila pada yang betina
diberi hormon androgen gejala lupus akan
membaik. Sebaliknya pada tikus jantan bila diberi
estrogen akan menyebabkan gejala LES
bertambah buruk.
Patogenesis
LES adalah penyakit autoimun yang mengenai multiple
organ. Gambaran klinis yang ditemukan terjadi akibat terbentuknya
autoantibodi terhadap berbagai macam antigen jaringan.
Autoantibodi yang paling banyak ditemukan adalah terhadap inti sel
yaitu terhadap DNA tubuh sendiri berupa anti DNA double stranded
(dsDNA), juga anti DNA single stranded (ssDNA). Keduanya dapat
diekstraksi dari deposit atau endapan kompleks imun di glomerulus
pasien NL.
Kompleks imun juga ditemukan dalam sirkulasi pasien NL
yaitu komplek DNA-anti DNA yang kemudian terperangkap /
menyangkut di daerah membran basal glomerulus berupa
endapan/deposit. Namun, di samping itu kompleks imun juga dapat
terbentuk insitu di glomerulus yaitu karena adanya DNA dalam
sirkulasi yang mengendap di glomerulus kemudian disusul dengan
pembentukan antibodi anti-DNA. Belum jelas mana di antara kedua
mekanisme itu yang berperan pada NL. Setelah terjadi endapan
kompleks imun akan terjadi aktivasi sistem komplemen yang
kemudian menyebabkan kerusakan jaringan glomerulus yang
menimbulkan gejala-gejala nefritis. Deposit komponen komplemen
juga ditemukan di glomerulus.
Jenis antibodi lain yang banyak ditemukan terhadap inti sel
adalah anti-RNA (asam ribonukleat), anti Sm, anti Ro, anti La, anti
Histon, anti fosfolipid. Antibodi antifosfolipid sering dihubungkan
dengan risiko terjadinya trombosis dan pada wanita hamil dengan
kematian janin. Selain itu juga ditemukan berbagai macam antibodi
permukaan antigen spesifik terhadap jaringan tertentu yaitu:
Antibodi terhadap sel darah merah yang dapat
menyebabkan terjadinya anemia hemolitik autoimun
Antibodi terhadap glikoprotein trombosit yang
menyebabkan trombositopenia
Antibodi terhadap leukosit menyebabkan leukopenia
Antibodi terhadap lemak jaringan otak yang mungkin
sebagai penyebab kerusakan jaringan otak Antibodi terhadap kardiolipin yang menyebabkan reaksi
Wasserman (sifilis) positif palsu
Antibodi terhadap limfosit semula hanya dianggap
menyebabkan terjadinya leukopenia saja, tetapi ternyata terdiri atas
beberapa jenis antibodi dan yang sangat penting adalah antibodi
terhadap sel T supresor. Antibodi inilah yang diperkirakan
menyebabkan pembentukan antibodi oleh sel B tidak bisa
dikendalikan (overaktif) dan menyebabkan peningkatan IgG dan
berbagai macam autoantibodi yang kemudian mengendap sebagai
kompleks imun di berbagai organ tubuh.
Tata Laksana
Pada dekade terakhir angka mortalitas pada pasien NL
telah mengalami banyak perbaikan. Hal ini terutama disebabkan
karena penggunaan obat kortikosteroid dan sitostatik. Gejala
ekstrarenal akan cepat menghilang pada pemberian kortikosteroid.
Pada pasien dengan gejala ekstrarenal yang ringan tanpa adanya
gejala renal tidak perlu diberi kortikosteroid, cukup diberikan obat
salisilat, anti malaria atau obat NSAID.
Prognosis
Setelah pengobatan kortikosteroid dan sitostatik, prognosis
NL ataupun SLE pada umumnya mengalami perbaikan yang
dramatis. Angka hidup pada pengamatan 1 tahun adalah 90%, pada
10 tahun adalah 85%, dan pada 15 tahun 77%. Penyebab kematian
yang terbanyak adalah gagal ginjal, sepsis, dan kelainan susunan
saraf pusat.
Daftar Pustaka
1. Kasper DL. Harrison’s Principles of Internal Medicine. 16th
ed. USA: McGraw-Hill; 2005. P. 1681-8.
2. Price SA, Wilson LM. Patofisiologi. Vol. 2. Ed. 6. Jakarta: EGC;
2006. P. 924-9.
3. O’Callaghan, CA. The renal system at a glance. 2 nd ed.
Victoria: Blackwell Publishing; 2006. P. 75-78.