1. Dr. Noroyono Wibowo-Patogenesis Dan Deteksi Dini Preeklam
Transcript of 1. Dr. Noroyono Wibowo-Patogenesis Dan Deteksi Dini Preeklam

Patogenesis dan Deteksi Dini Preeklampsia [email protected]

0 4 14 28
Gland
Spongy layer
Implanta;on begins
Compact layer
Basal layer
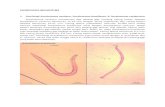
Menstrual phase Follicular or prolifera;ve phase
Progesta;onal or secretory phase
Gravid phase
Transformasi
Atherosis Kegagalan remodeling VSM
Synci:al knots Hyalin degenera:on Apoptosis -‐ Necrosis
STBM
Flow: jet Stream
Flow: Pulsa:on

< 8 mm > 12 mm
Mol Hum Reprod. 2000 Feb;6(2):178-‐84

MMP tPA Ν PAI-‐1 N
An:oxidant Ec SOD N HO-‐1 N
PP13
Eng
Angiogenic PLGF VEGF
Metabolic HOMA IR HOMA B
Inflamma;on CRP Pentraxin3 RBP 4
SEng
Sflt-‐1
NOO-‐ O2-‐
STBM
> 50% cotyledon rusak Keguguran IUGR Preterm PEE

Pathogenesis of Preeclampsia The “Angiogenic Imbalance” Theory
Ini;al mechanisms • Inflammatory challenges (disorders);
• Altera;ons in the regula;on and signalling of angiogenesis pathways contribute to inadequate cytotrophoblas;c invasion;
• Up-‐regula;on of an;-‐angiogenic factors (sFlt-‐1, s-‐Endog); • Down-‐regula;on of circula;ng angiogenic factors (VEGF, PlGF).
Young et al. Annu Rev Pathol Mech Dis 2010; 5: 173-‐192

Pathophysiology of Preeclampsia
Gene;c Suscep;bility
Environment / Maternal Characteris;cs
Immune / Inflammatory Factors
Abnormal Uterine Vascular Remodelling during early Pregnancy
Reduced Placental Perfusion
Hypoxia (OxidaMve Stress)
Placental DysfuncMon
Release of Placental Mediators in Maternal CirculaMon
Systemic Maternal Endothelial DysfuncMon
Placental Hypotrophia, Infarctus
Foetal Pain / Distress : Intrauterine Growth
Restric;on Intrauterine Foetal
Death
Hypertension Proteinuria Glomerular Endotheliosis
HELLP syndrome
Eclampsia
Adapted from Giguère et al (2011) submiTed

Pathophysiology of PE -‐ Biomarkers
• Abnormal Uterine Vascular Remodelling during early Pregnancy Abnormal profile of adhesion molecules (Δ VE-‐cadherin, VCAM-‐1, PECAM-‐1)
Decrease of plasminogen ac:va:on ( Δ urokinase, MMP-‐9, PAI-‐1)
Modifica:on of uterine angiogenesis (Δ sFlt-‐1, sEndog, PlGF, VEGF, hCG )
• Placental DysfuncMon AFP, hCG, PAPP-‐A, inhibin A, ac:vin A, PP-‐13
• Release of Placental Mediators in Maternal CirculaMon Growth Factors : EGF, IGF-‐II, TGF α/β, VEGF, PlGF, sFlt-‐1, sEndog;
Cytokines : TNFα; Interleukins 1, 6, 10; LIF; Interferon; Prostaglandins;
Enzymes : PAI 1, PAI 2, MMP-‐2, MMP-‐9;
Others : Peroxylated Lipids, Endothelins, Apopto:c/Necro:c debris,
Cell-‐free foetal nucleic acids
• Systemic Maternal Endothelial DysfuncMon
Adapted from Giguère et al (2011) submiTed

Altered Parameters before Occurrence of Clinical Symptoms of PE
• Clinical (maternal history and characteris;cs, BMI, MAP, …)
• Blood and Urine Parameters
• Doppler Uterine Artery Blood Flow Velocity Measurements
• 3-‐Dimensional Doppler Ultrasonography (placental volume)

Early Predic;on of PE
Objec;ves: To iden:fy women at high risk of developing preeclampsia later in pregnancy, and to offer specific preven:ve measures;
To apply prophylac:c interven:ons at op:mal :me;
To propose closer follow-‐up.

Interven;ons for the Preven;on of Preeclampsia
• Improved socio-‐economic condi;ons (perinatal policy)
• Structured prenatal counselling and follow-‐up • Poten;al prophylac;c therapies
An:platelet agents (aspirin) Inhibit thromboxane-‐mediated vasoconstric:on and
pathological blood coagula:on in the placenta
Low-‐molecular weight heparin

Clinical Interven;on and Treatment
Early recogni;on, key to preven;on and treatment.
• The objec:ve is to prolong pregnancy whenever possible to permit foetal lung maturity while preven:ng progression to severe disease;
• An:platelet prophylac:c therapy (aspirin);
• An:hypertensive therapy (>160/100 mmHg: methyldopa, labetalol, nifedipine);
• The defini:ve treatment is delivery;
• Eclampsia: emergency; High-‐risk morbidity/mortality.

PE can be Prevented by ASA
Bujold et al. (2010) Obstet Gynecol 116: 402-‐414
Study or subgroup
Treatment Control Risk ra;o Risk ra;o
Events Total Events Total Weight (%) M-‐H, random (95%
CI) M-‐H, random (95% CI)
1.1 16 or fewer weeks August 1994 Azar 1990 Beaufits 1985 Banigni 1989 Ebrashy 2005 Hormida 1997 Michael 1992 Tulppala 1997 Vainio 2002 Subtotal (95% CI) Total events
3 1 0 0 25 3 1 1 2
36
24 46 48 17 73 50 55 33 43 389
5 4 6 0 40 7 5 3 10
80
25 45 45 16 63 50 55 33 43 375
2.5 1.1 0.6
9.3 2.6 1.1 1.0 2.2 20.5
0.63 (0.17-‐2.33) 0.24 (0.03-‐2.10) 0.07 (0.00-‐1.25) Not es:mable 0.54 (0.37-‐0.78) 0.43 (0.12-‐1.56) 0.20 (0.02-‐1.66) 0.33 (0.04-‐3.04) 0.20 (0.05-‐0.86) 0.47 (0.34-‐0.65)
Heterogeneity: Tau3=0.00; Chi2=5.45; df=7 (P=.61), I2=O% Test for overall effect: Z=4.57 (P<.001)
1.2 More than 16 weeks Byaruhanga 1998 Cari:s 1996 CLASP 1994 Davies 1995 ECPPA 1996 Golding 1998 Ferrier 1996 Grab 2000 Hauth 1993 McParland 1990 Morris 1996 Rogers 1999 Roochell 1998 Schiff 1989 Schrocksnadel 1992 Wallenburg 1986 Yu 2003 Zimmerman 1997 Subtotal (95% CI) Total events
17 111 91 5 16 1 66 3 5 1 4 3 10 1 0 0 49 4
3
113 663 1,259 58 284 23
1,253 22 302 48 52 118 739 34 22 23 276 13
5,302
23 118 80 7 22 1 50 2 17 10 7 7 12 7 6 7 52 2
430
117 626 1,233 60 322 20
1,294 21 302 52 50 75 746 31 19 23 278 13
5,282
7.14 10.8 10.2 3.4 6.6 0.7 9.4 1.7 3.9 1.2 3.1 2.5 4.8 1.2 0.7 0.7 9.5 2
79.5
0.77 (0.43-‐1.35) 0.89 (0.70-‐1.12) 1.11 (0.83-‐1.49) 0.74 (0.25-‐2.20) 0.82 (0.44-‐1.54) 0.87 (0.06-‐13.02) 1.36 (0.95-‐1.95) 1.43 (0.27-‐7.73) 0.29 (0.11-‐0.79) 0.11 (0.01-‐0.81) 0.55 (0.17-‐1.76) 0.27 (0.07-‐1.02) 0.84 (0.37-‐1.94) 0.13 (0.02-‐1.00) 0.07 (0.00-‐1.11) 0.07 (0.00-‐1.10) 0.95 (0.67-‐1.35) 2.00 (0.44-‐9.08) 0.81 (0.63-‐1.03)
Heterogeneity: Tau2=0.09; Chi2=32.49; df=17 (P=.01), I2=48% Test for overall effect: Z=1.75 (P=.08)
Total (95% CI) Total events
423 5,691
510 5,657
100.0 0.68 (0.54-‐086)
Heterogeneity: Tau2=0.12; Chi2=51.55; df=25 (P=.001), I2=52% Test for overall effect: Z=3.19 (P=.001)
0.05 0.2 1 5 20 Favors experimental Favors control
Fig.2 . Forest plot of trials studying preeclampsia. Aspirin treatment to prevent preeclampsia according to gesta:onal age at the ini:a:on of interven:on. CI, confidence interval; M-‐H, Mantel-‐Haentszel. Bujold. Preeclampsia and IUGR Preven<on With Aspirin. Obstet Gynecol 2010.
Preven;on of Preeclampsia and Intrauterine Growth Restric;on With Aspirin Started in Early Pregnancy A Meta-‐Analysis
Emmanuel Bujold, MD, MSc, Stéphanie Roberge, MSc, Yves Lacasse, MD, MSc, Marc Burreau, MD, Franqois Audibert, MD, MSc, Sylvie Marcoux, MD, PhD, Jean-‐Claude Forest, MD, PhD, and Yves Giguète, MD, PhD
“ … current evidence indicates that low-‐dose aspirin started in early pregnancy may reduce the incidence of PE, IUGR and PTB in women iden;fied at moderate or high risk for PE.”
• 27 trials including 11,348 women

Clinical Maternal Risk Factors
Recommenda;ons for determina;on of HDP risk at 1st visit
• Intensity of monitoring
Ex.: Maternal age > 40 yrs; nulliparity, woman’s own birth weight, pre-‐exis:ng chronic hypertension, diabetes, previous PE, BMI > 30.
• Very few published data of performance
In one recent study by Poon et al. (J Hum Hypert (2010) 24 : 104-‐10), logis:c regression analysis of maternal characteris:cs shows: • At a false posi:ve rate of 5 %, detec:on rates:
for early PE 37% l t PE 29 % GH 20%
• Screening suggested by NICE (Natl. Inst. for Clinical Excellence): (essen:ally treats each factor as a separate screening test) false posi:ve rate of 64 %; detec:on rate of 89, 93 and 85 % , respec:vely.

Maternal Risk Factors for HDP as a priori Risk
• Elements from maternal history may serve to determine a priori risk using a mulMvariate approach. – Ethnicity, maternal age, woman’s own birth weight, prior PE, BMI…
• As for screening for Trisomy 21, pa;ent specific risk may be derived by mul;plying a priori risk by the likelihood ra;o associated with selected biochemical and biophysical parameters.
Cuckle (2011) Placenta 32: S42-‐S48

Poten;al Biomarkers for PE – Summary Marker Altered levels during Assessed in combina;on with Associated with
Before onset of PE
(1st /2nd trim.)
Ajer onset of PE
(3rd trim.)
Other biochem. markers
Ultrasound markers
Maternal characteris;cs
VEGF ↓ ↓ UtA PI GH, GDM, HELLP, T21
PIGF ↓ ↓ sFlt-‐1; PIGF; PAPP-‐A
UtA PI Ethnicity, MAP, weight, history CH, smoking, Concep:on
GH, GDM, HELLP, PTB, IUGR, T21, T18, T13, triploidy, Turner
sFlt-‐1 ↑ ↑ PIGF; sEng; UtA PI GH, GDM, HELLP, FD, IUGR, s:llbirth, T13
sEndog ↑ ↑ PIGF; sFlt-‐1; PAPP-‐A
UtA PI Weight GH, HELLP, FD, IUGR, SGA,
AFP ↑ ↑ hCG UtA PI GDM, GH, HELLP, PTB, FL, SGA, T21, Neural tube defects
hCG ↓ ↑ AFP, PAPP-‐A UtA PI GDM, GH, PTB, T21
Inhibin A
↑ ↑ PAPP-‐A, ac:vin A UtA PI Ethnicity, parity, BMI GDM, GH, HELLP, PTB, SGA, T21
PAPP-‐A ↓ ↑ sEng, PlGF PP-‐13, inhibinA
UtA PI
Weight, BMI, MAP, ethnicity, CH, parity, age concep:on, fetal CRL, smoking
GDM, GH, HELLP, PTB, FD, SGA, T21, T18, Turner

Poten;al Biomarkers for PE – Summary Marker Altered levels during Assessed in combina;on with Associated with
Before onset of PE
(1st /2nd trim.)
Ajer onset of PE
(3rd trim.)
Other biochem. markers
Ultrasound markers
Maternal characteris;cs
Cell free fetal DNA
↑ ↑ IUGR
Cell free fetal RNA
↑ ↑
P-‐Selec;n ↑ ↑ UtA PI
Ethnicity, MAP, weight, history CH, smoking, MAP, Concep:on
GH, PTB, SGA
VCAM ↑ ↑ GDM, GH, HELLP, SGA
PP-‐13 ↓ ↓ PAPP-‐A UtA PI Weight, smoking HELLP, PTB, T18, T13, Turner
ADAM-‐12 ↓ ↑ SGA
Visfa;n ↑ ↑ GDM, PTB, SGA
PTX3 ↑ ↑ GH, PPROM, PTB, IUGR
From Giguère et al. 2011 submiTed

Challenges with Measurement of Biochemical Markers to Predict PE Early in Pregnancy
• Concentra;on of marker changes during pregnancy; Necessity to express results in Mul;ple of Median – MoM
• Lack of standardized methods and reference materials, commercial availability and automa;on, CE label;
• Overlap of results between normal pregnancy and HDP.

Poten;al Biomarkers for PE
Which of the puta;ve biomarkers Are predic;ve of preeclampsia and other adverse pregnancy outcomes ?
Have demonstrated clinical u;lity ?

Summary of Criteria for Screening Jungner & Wilson WHO (1968); Holland et al. WHO
(2006) Condi;on : -‐ Important health problem;
-‐ Natural history understood; -‐ Recognizable latent or early symptoma:c stage;
Diagnosis : -‐ Suitable diagnos:c test available, safe and acceptable to the popula:on concerned;
-‐ Agreed policy, based on respectable test findings and na:onal standards, as to whom to regard as pa:ents;
-‐ Whole process, con:nuing;
Treatment : -‐ Accepted and established treatment / interven:on for individuals iden:fied as having the disease or predisease condi:on;
-‐ Facili:es for treatment should be available;
Cost : -‐ Cost of case-‐finding (including diagnosis and treatment) should be economically balanced in rela:on to possible expenditure on medical care.

Summary of Criteria for Evalua;on of Screening Tests (Holland et al. WHO (2006)) Simplicity The test should be simple to perform, easy to interpret and, where possible,
capable of use by paramedics and other personnel.
Acceptability Since par:cipa:on in screening is voluntary, the test must be acceptable to those undergoing it.
Accuracy The test must give a true measurement of the condi:on or symptom under inves:ga:on.
Cost The expense of the test must be considered in rela:on to the benefits of early detec:on of the disease.
Repeatability The test should give consistent results in repeated trials.
Sensi;vity The test should be capable of giving a posi:ve finding when the individual being screened has the condi:on being sought.
Specificity The test should be capable of giving a nega:ve finding when the individual being screened does not have the condi:on being sought.

Systema;c Reviews of Combina;ons of Biomarkers
• Un;l now, numerous systema;c reviews have been unable to demonstrate a single biochemical marker capable of detec;ng, early in pregnancy, those women suscep;ble to develop PE.
Conde-‐Argudelo et al. Obstet Gynecol. 2004; 104: 1367-‐1391. Cnossens et al. Health Techn. Assess. 2008; 12(6):1-‐128.
• Because of the heterogeneous nature of PE, a combina;on of independent biomarkers, each reflec;ng a different pathophysiological process, should increase the likelihood to derive suitable predic;ve algorithms.
• Indeed, combina;ons of biochemical and ultrasonographic markers into algorithms derived by mul;variate analysis improve the performance of early predic;on of PE.
• From the perspec;ve of integra;ve medicine, there is a clear need for prospec;ve large-‐scale studies with rigorous study design criteria to determine the clinical usefulness of combina;ons of biomarkers in different geographic and healthcare environments.
Giguère et al. Clin. Chem. 2010; 56(3): 361-‐374. CeMn et al. Placenta 2011; 32:S4-‐S16.

1 - Specificity 1.00 .75 .50 .25 0.00
Sen
siti
vity
1.00
.75
.50
.25
Predic;on of pre-‐eclampsia ROC curve of mul;variable model
AUC 0.884
Multivariable model (ENG, FLT-1, PlGF and parity)
Sekizawa A, et al. Br J Obstet Gynecol. 2010
95%CI: 0.844-0.922 p<0.001
1. Gene expression levels of angiogenesis-‐ and oxida;ve stress-‐related genes changed in the cellular component of maternal blood before the onset of preeclampsia
2. Predic;on of preeclampsia is feasible with high detec;on rate by analysis of cellular RNA in maternal blood.

Trisomy screening (Biochemistry)
Clinical Screening Strategies for PE Exis;ng Clinical Inves;ga;ons
Da;ng, Nuchal translucency Trisomy screening
Fetal Development (Ultrasound)
PREGNANCY
Screening for Gesta;onal Diabetes
Fetal Development (Ultrasound)
0 10-‐13 (1st trim.)
14-‐17 20 24-‐28 (2nd trim.)
30, 32, 36 (depending) (3rd trim.)
40
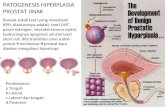
Development of Preeclampsia
Screening Strategies
1st trimester: Predic:on of HDP/ PE
(Preven:ve treatment for high-‐risk women)
2nd trimester: Late iden:fica:on of
imminent HDP / PE (Closer follow-‐up of high-‐risk
women)

Clinical screening strategies for PE
Benefits To develop an approach using biomarkers to detect, as early as possible, women at risk of developing preeclampsia with a greater performance than that of conven:onal methods in order to offer, in a targeted manner, prophylac:c interven:ons, specific surveillance and or closer management.
Risks • False posi:ve results crea:ng anxiety and possibly unnecessary interven:ons • False nega:ve results causing false reassurance or reduc:on of surveillance.

Challenges What should be the expected performance to reach clinical
u;lity?
Will the same factors for calcula;on of a priori risk and biomarkers (biochemical / biophysical) perform uniformly in different environments?
Commercial availability of best performing markers?
Cost-‐effec;veness studies? Op;mal ;me to screen?

In Summary • No individual biochemical or biophysical markers have met the criteria
for a screening test.
• Maternal history & risk factors, have as a whole poor predic;ve value; with some guidelines, 2/3 of the pa;ents would be falsely classified as high risk.
• A growing body of evidence suggests that the combina;on of maternal factors (BMI age parity BMI, age, parity, ethnicity, past history,...) with serum markers and UtA Doppler indices may iden;fy early in pregnancy women at risk of developing preeclampsia.

There is a need for large-‐scale prospec;ve studies to determine the usefulness of mul;variate risk-‐predic;on algorithms early in pregnancy, in different popula;ons.
This may lead to the implementa;on of an efficient screening procedure to iden;fy women at risk for PE who would benefit from early targeted interven;ons.
In Summary

References • Bujold et al. (2010) “Preven<on of Preeclampsia and Intrauterine Growth Restric<on With Aspirin Started in Early Pregnancy -‐ A Meta-‐Analysis” Obstet Gynecol 116:402–14)
• Ce:n et al. (2011) “Pregenesys pre-‐eclampsia markers consensus mee<ng: What do we require from markers, risk assessment and model systems to tailor preven<ve strategies?” Placenta 32: S4-‐S16.
• Cuckle, H. (2011) “Screening for Pre-‐eclampsia -‐ Lessons from Aneuploidy Screening” Placenta 32: S40-‐S48.
• Giguère et al. (2010) “Combining Biochemical and Ultrasonographic Markers in Predic<ng Preeclampsia: A Systema<c Review” Clin Chem. 56 : 361-‐374.
• Grill et al. (2009) “Poten<al markers of preeclampsia – a review” Reproduc<ve Biology and Endocrinology 7:70.
• Lindheimer et al. (2009) “ASH Posi<on Paper: Hypertension in Pregnancy” J Clin Hypertens (Greenwich) 11:214–225.
• Silasi et al. (2010) “Abnormal Placenta<on, Angiogenic Factors, and the Pathogenesis of Preeclampsia” Obstet Gynecol Clin Am : 239–253.
• Steegers et al (2010) “Preeclampsia” Lancet 2010; 376: 631–44.
• Wang et al. (2009) “Preeclampsia: The role of angiogenic factors in its pathogenesis”. Physiology 24:147-‐158.

Trends Cardiovasc Med. 2008 July ; 18(5-‐24): 186–194
Genetic Factors?
Renal Dysfunction • Microalbuminuria • Serum uric acid
• Urinary calcium excretion • Serapine 1
Fetoplacental Unit Endocrine Dysfunction • Human chronic gonadotropin • Alpha fetoprotein • Inhibin A • Activin A • Pregnancy-‐associated plasma protein A • Insulin resistance • Sex hormone-‐binding globulin • Adiponectin
Endothelial Dysfunction, growth factors and oxidative stress • Antiphospholipid antibodies • Antithrombin III • Plasminogen activator inhibitor • Serum lipids • Apoliprotein E • Endothelin • Prostacyclin • Thromboxane • Cytokines • Placenta growth factor • Isoprostanes • Soluble FMS-‐like tyrosine kinase • Soluble endoglin • ADMA
Placental Perfusion and Vascular Resistance Dysfunction
• Mean blood pressure in second trimester • 24-‐hour ambulatory blood pressure monitoring • Doppler ultrasound • Renin • Platelet • Platelet angiotensin II binding • Platelet calcium response to arginine vasopressin • PP13
Proteomics Metabolomics
Pre-‐eclampsia