BAB 2 TINJAUAN PUSTAKA 2.1 Infeksi Nifas 2.1.1 Definisi ...repository.ub.ac.id/3189/3/BAB 2.pdf ·...
Transcript of BAB 2 TINJAUAN PUSTAKA 2.1 Infeksi Nifas 2.1.1 Definisi ...repository.ub.ac.id/3189/3/BAB 2.pdf ·...

7
BAB 2
TINJAUAN PUSTAKA
2.1 Infeksi Nifas
2.1.1 Definisi Infeksi Nifas
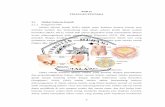
Infeksi nifas adalah sebuah istilah yang umum digunakan untuk
menjelaskan suatu keadaan dimana terdapat serangan berbagai bakteri pada
saluran reproduksi setelah persalinan. Infeksi nifas menyebabkan kematian 13%
pada masa kehamilan dan persalinan dan membentuk trias letal setelah pre-
eklamsia dan perdarahan (Cunningham et al., 2016).
Infeksi nifas ditandai dengan gejala demam dengan suhu mulai 38 sampai
390C selama 2 hari berturut-turut pada 10 hari pertama nifas, bila disertai
menggingil menunjukkan adanya bakteremia, lochea berubah warna dan berbau
dan nyeri pada tempat infeksi (Lowdermilk, 2010 ; Wong et al., 2015). Ibu biasanya
menguluh nyeri pada abdomen, nyeri parametrial muncul bila dilakukan
pemeriksaan bimanual dan abdominal. Leukositosis berkisar antara 15.000 hingga
30.000 sel/µL, namun pada kasus bedah caesar jumlah leukosit juga meningkat.
Pada wanita yang tidak menyusui atau sekitar 15% akan mengalami demam nifas
karena mengalami pembengkakan payudara, hal tersebut lebih rendah pada
wanita yang menyusui (Cunningham et al., 2016).
Perubahan yang terjadi pada masa nifas seperti konsentrasi hormon
steroid termasuk hormon estrogen, progesteron, glukokortikoid dan metabolisme
asam arakidonat saat mendekati persalinan berperan menekan fungsi leukosit
sehingga rentan terjadinya infeksi pada masa nifas (Weissenbacher et al., 2013).
Pada masa nifas terjadi penurunan jumlah dan fungsi limfosit seperti proliferasi
sel, produksi antibodi dan sitokin sehingga berkontribusi menyebabkan terjadinya
infeksi. Penurunan produksi sitokin pada masa nifas juga menyebabkan

8
perubahan respon imun sehingga meningkatkan kerentanan host terhadap infeksi
(Patra, 2013).
2.1.2 Faktor Predisposisi
2.1.2.1 Persalinan Per Vagina
Proses persalinan menjadi salah satu faktor utama penyebab terjadinya
infeksi uterus. Persalinan melalui bedah caesar meningkatkan infeksi yakni
hampir 25 kali lipat dibandingkan persalinan per vagina. Pada persalinan per
vagina, kasus metritis lebih jarang terjadi dibandingkan dengan bedah caesar.
Resiko terjadinya infeksi pada persalinan per vagina disebabkan oleh kasus
seperti pecah ketuban, persalinan lama, pemeriksaan pembukaan serviks yang
berulang, korioamnionitis dan manual plasenta juga mempunyai resiko
peningkatan kasus metritis (Cunningham et al., 2016).
2.1.2.2 Bedah Caesar
Pemberian profilaksis antimikrobial dosis tunggal perioperatif hampir rutin
diberikan pada pasien yang akan melakukan bedah sesar. American Collage of
Obstetricians and Gynecologists merekomendasikan pemberian profilaksis
antimikroba tersebut kepada ibu-ibu yang akan melakukan bedah sesar dengan
resiko tinggi mengalami infeksi pascapartum. Profilaksis antimikroba dosis tunggal
telah terbukti mampu mengurangi insiden dan keparahan infeksi pasca bedah
caesar dibanding tindakan lainnya yang telah terbukti selama 30 tahun terakhir
(Cunningham et al., 2016).
Faktor resiko infeksi pasca bedah caesar antara lain persalinan lama,
ketuban pecah, pemeriksaan pembukaan serviks yang sering, dan pemantaun
janin internal. Ibu-ibu dengan semua faktor resiko tersebut jika tidak diberikan
profilaksis antimikroba perioperatif maka mempunyai resiko 90% angka infeksi
pelvis yang serius (Manuaba, 2009).

9
2.1.2.3 Faktor Risiko Lainnya
Sebagaimana diketahui secara umum bahwa infeksi pelvis lebih sering
dialami oleh ibu dengan keadaan sosial ekonomi yang lemah dibandingkan
dengan ibu yang mampu, sedangkan anemia dan asupan nutrisi yang kurang bisa
dikatakan tidak banyak mempengaruhi presdisposisi terjadinya infeksi
(Cunningham et al., 2016).
Kolonisasi bakteri pada traktus genetalis bagian bawah dengan
mikroorganisme tertentu seperti streptokokus grup B, Chlamydia trachomatis,
mycoplasma hominis, ureaplasma urealyticum, dan gardnella vaginalis menjadi
penyebab meningkatnya resiko infeksi nifas. Pada 5 tahun terakhir, infeksi kulit
dan jaringan lunak karena community-acquired methicillin-resistant
Staphylococcus aureus (CA-MRSA) telah banyak terjadi, bahkan strain tersebut
bukan merupakan agen utama metritis puerperal tetapi merupaka penyebab
utama infeksi luka insisional (Cunningham et al., 2016). Seorang wanita dengan
selulitis episiotomi yang disebabkan oleh MRSA dan pneumonia nekrotikans yang
dapat menyebar dengan cara hematogen (Rotas, 2007).
Faktor lain yang menyebabkan meningkatnya resiko infeksi nifas yakni
mencakup bedah caesar untuk kehamilan kembar, usia ibu yang masih muda dan
nullipara, induksi persalinan yang lama, obesitas, dan cairan amnion yang
bercampur mekonium (Cunningham et al., 2016).
2.1.3 Bakteriologi
Penyebab tersering terjadinya infeksi pada masa nifas adalah masuknya
bakteri melalui perlukaan jalan lahir seperti episiotomi, diantara bakteri yang sering
teridentifikasi pada infeksi nifas antara lain : Chlamydia, Clostridium tetani,
Clostridium welchii, Escherichia coli, Gonococci, Staphylococci dan Streptococci
(Wong et al., 2015).

10
Penelitian pada sekitar 6077 pasien nifas yang melahirkan secara per
vagina dan bedah caesar di Rumah Sakit Khanevadah mulai tahun 2003 sampai
2008, ditemukan diantaranya 461 pasien yang mengalami infeksi nifas. Diantara
bakteri yang berhasil diisolasi antara lain : Peptostreptococcus spp sejumlah 57
pasien (12,4%), Enterococcus 54 (11,8%), Bakteroids spp sejumlah 50 pasien
(10,9), Peptococcus spp 49 (10,7%), E.coli dan enterobacteriaceae 43 (9,3%),
Staphylococcus aureus dan Staphylococcus epidermidis 36 (7,9%), Streptococcus
agalactie 34 (7,3%), Gardnerella vaginalis 31 (6,8%), Streptococcus pyogenes 31
pasien (6,7%), Staphylococcus saprophyticus 27 (5,8%), Mycoplasma hominis dan
Ureaplasma 15 (3,2%), Chlamydia trachomatis 11 (2,3%), Clostridium 10 (2,1%),
dan N.gonorheae 4 (0,8%) dan semua bakteri diatas adalah bakteri flora normal
vagina (Nahid et al., 2009).
Sedangkan pada penelitian lainnya ditemukan bahwa sekitar 42 ibu hamil
(8%) dari 524 ibu hamil dengan kehamilan aterm dan preterm positif terinfeksi
Staphylococcus aureus, selain itu bakteri lain yang juga teridentifikasi adalah
Candida albican 189 (36%), E.coli 42 (8%) dan Streptococcus agalactie 25 (4,8%)
(Dechen et al., 2010).
Namun pada beberapa tahun terakhir, infeksi pada kulit dan jaringan lunak
banyak disebabkan oleh bakteri staphylococcus. Dalam penelitian yang dilakukan
oleh Chen et al., (2006) dinyatakan bahwa 17% wanita hamil ditemukan koloni
Staphylococcus aureus di vagina mereka. Yang dikhawatirkan adalah galur bakteri
tersebut resisten terhadap beberapa antibiotik seperti penisilin, dan galur bakteri
yang resisten tersebut semakin banyak menyebar terutama galur bakteri
methicillin-resistant Staphylococcus aureus (MRSA). Sekitar 14.300 wanita hamil
atau postpartum mengalami infeksi MRSA pada tiap tahun secara invasif.
Akibatnya terjadi abses atau selulitis yang sebagian besar didapati pada wanita
yang terinfeksi HIV, pemakai narkoba suntik dan diabetes (Beigi et al., 2009).

11
2.1.4 Patogenesis
Infeksi nifas yang terjadi setelah persalinan per vagina melibatkan tempat
implantasi plasenta, desidua dan juga miometrium di sekitarnya, atau melalui
laserasi servikovaginal. Sedangkan patogenesis infeksi uterus pasca caesar
adalah pada tempat insisi bedah caesar. Bakteri yang bertempat pada serviks dan
vagina secara normal mendapatkan akses untuk masuk ke dalam cairan amnion
pada saat persalinan dan postpartum. Bakteri tersebut menginvasi jaringan mati
pada uterus, selanjutnya terjadi selulitis parametrial dengan infeksi jaringan ikat
fibroareolar retropritoneal pelvis. Pada proses terapi awal, infeksi hanya terjadi di
dalam jaringan paravaginal saja, tetapi selanjutnya dapat meluas hingga ke pelvis
(Cunningham et al., 2016). Skema patogenesis infeksi pada luka insisi dapat dilihat
pada gambar berikut :
Pemeriksaan serviks Pemantauan internal Persalinan lama Insisi uterus
Trauma Pembedahan Jahitan Jaringan mati Darah dan serum
Gambar 2.1 Skema Patogenesis Metritis Pasca Bedah CaesarInfeksi nifas pada bedah caesar dapat terjadi melalui cairan amnion padaservikovaginal saat proses persalinan, selanjutnya bakteri akan menginvasijaringan mati di uterus dan dapat menyebar ke organ yang lainnya melaluidarah (Cunningham et al., 2016).
Flora normal bakteriservikovaginal
Inokulasi Insisi Uterus
Kondisi Anaerob
Infeksi KlinisProliferasi Bakteri

12
2.1.5 Sindrom Syok Toksik
Sindrom syok toksik ditandai dengan keluhan demam akut dengan
komplikasi yang berat mempunyai resiko meningkatkan angka kematian 10 hingga
15%. Keluhan seperti demam, sakit kepala, stres, ruam eritematosa makular difus,
edema subkutan, mual, muntah, diare air, dan hemoknsentrasi yang jelas. Gagal
ginjal dan disertai gagal hati, koagulasi intravaskular diseminata dan kolaps
kardiovaskular dapat menyertai di dalam urutan dengan sangat cepat
(Cunningham et al., 2016).
Bakteri Staphylococcus aureus telah ditemukan pada hampir semua pasien
yang mengalami infeksi. Secara spesifik, eksotoksin stafilokokus atau yang
dinamakan dengan Toxic Shock Syndrome Toksin-1 (TSST-1) menyebabkan
manifestasi klinis yang memicu kerusakan endotel yang parah. Dalam jumlah yang
sangat sedikit, TSST-1 mampu mengaktifkan 5 hingga 30% sel T untuk membuat
“badai sitokin” (Cunningham et al., 2016).
Berdasarkan beberapa kasus, infeksi tidak terlihat tetapi kolonisasi
permukaan mukosa menjadi sumber infeksi. Pada wanita hamil terdapat 10-20%
terdapat kolonisasi Staphylococcus aureus pada vagina, sehingga tidak
mengherankan jika resiko infeksi karena kolonisasi bakteri tersebut akan
berkembang pada saat postpartum. Penemuan yang hampir serupa dengan syok
septik ditemukan pada wanita dengan kolonisasi bakteri Clostridium sordelli
(Cunningham et al., 2016).
Pemberian antimikroba selain mencakup terapi untuk bakteri
Staphylococcus dan Streptococcus juga harus mencakup agen terapi infeksi
polimikroba. Pada kasus dengan infeksi seperti disebut diatas membutuhkan
debridemen luka yang intensif karena mempunyai kemungkinan histerektomi.
Karena toksin tersebut sangat poten sehingga semakin meningkatkan resiko
mortalitas maternal dan fetal (Cunningham et al., 2016).

13
2.2 Staphylococcus aureus
2.2.1 Pengertian
Staphylococcus aureus merupakan bakteri gram positif yang tersusun
berkelompok seperti buah anggur (seperti yang terlihat pada gambar 2.2). Bakteri
ini umumnya terdapat pada kulit dan membran mukosa. Staphylococcus aureus
merupakan jenis bakteri yang banyak menyebabkan infeksi terutama pada
manusia (Brooks et al., 2007). Staphylococcus aureus menjadi penyebab infeksi
di masyarakat dan juga nosokimial, kolonisasi bakterial sendiri seringkali tidak
terlihat menimbulkan gejala dan banyak hidup di hidung manusia (Dzen et al.,
2003).
Staphylococcus aureus bersifat aerob atau anaerob fakultatif, tes katalase
positif serta mampu bertahan hidup di lingkungan halofilik (tinggi kandungan
garam) misalnya NaCL 10% (Jawetz et al., 1996).
(a) (b)
Gambar 2.2 Bakteri Staphylococcus aureus(a) Staphylococcus aureus dengan pewarnaan gram menunjukkan bahwaadalah jenis bakteri gram positif, akan terlihat bergerombol seperti anggur,berbentuk bulat dan berwarna ungu; (b) Staphylococcus aureus yangditanam di media Mannitol Salt Agar (MSA) akan memfermentasi manitoldan akan berwarna kuning keemasan (Jawetz, et al., 2014 & Acharya, T.2013).

14
Staphylococcus aureus merupakan bakteri gram positif yang berbentuk
kokus dengan ukuran diameter sekitar 0,5 – 1 µm. Pada pemeriksaan secara
mikroskopis Staphylococcus aureus tampak seperti berpasangan seperti buah
anggur. Staphylococcus aureus bersifat tidak motil dan tidak membentuk spora
bila dipengaruhi oleh obat seperti pensilin (Brooks et al., 2007).
2.2.2 Klasifikasi
Klasifikasi Staphylococcus aureus menurut Bergey dalam Capuccino
(1998) adalah sebagai berikut :
Domain : Bacteria
Phylum : Firmicutes
Kelas : Bacilli
Ordo : Bacillales
Family : Staphylococcaceae
Genus : Staphylococcus
Spesies : Staphylococcus aureus
2.2.3 Patogenesis Staphylococcus aureus
Patogenesis Staphylococcus aureus dibedakan menjadi 3 yaitu infeksi
invasif, toksikosis dan campuran. Cara invasif yaitu Staphylococcus aureus
penetrasi melalui kulit atau mukosa sehingga menyebabkan terjadinya infeksi
lokal, yang ditandai dengan keluarnya sekret purulen dan abses. Contoh infeksi
lokal Staphylococcus aureus adalah mastitis puerperalis. Yang kedua yakni
toksikosis dapat menyebabkan terjadinya keracunan makanan, yang ditandai
dengan gejala mual, muntah, diare berat yang terjadi setelah makan makanan
yang sudah terkontaminasi oleh enterotoksin. Dan yang terakhir adalah tipe
campuran, gejala klinis patogenesis campuran antara lain : dermatitis exfoliative,
pemphigus nenonatorom dan bullous impetigo yang disebabkan oleh toksin

15
eksfoliatif. Sedangkan gejala klinis dari TSST-1 adalah sindrom syok toksik yakni
berupa hipotensi, demam dan lesi pada kulit scarlatinifum (Kayser et al., 2005).
2.2.4 Patofisiologi Staphylococcus aureus
Staphylococcus aureus memiliki faktor virulensi yang dapat menimbulkan
infeksi pada saat memasuki tubuh dan menghadapi respon imun. Berikut adalah
beberapa cara bakteri Staphylococcus aureus menimbulkan infeksi pada tubuh
berdasarkan Naber (2009) antara lain :
a. Adhesi dan kolonisasi
Staphylococcus aureus menghasilkan taichoid acid pada permukaan kulit,
yang dapat menyebabkan bakteri tersebut memiliki kemampuan untuk menempel
dan berkolonisasi pada kulit selanjutnya akan merusak tempat yang ditempeli
tersebut sehingga menyebabkan infeksi yang serius pada aliran darah.
b. Invasi
Staphylococcus aureus mengganggu pertahanan imun pertama pada kulit
dengan cara mengeluarkan exfoliative toxin, hemolysin yang dapat membentuk
pori pada membran sel kulit, serta beberapa enzim lainnya yang dapat merusak
jaringan. Invasi terjadi pada saat adanya gangguan sistem imun (immune
compromised), terdapat kerusakan intergument secara fisik dan pada saat terjadi
inflamasi.
c. Evasi
Staphylococcus aureus juga dapat menghindari respon imun dengan cara
mengeluarkan protein anti-opsonisasi (protein yang menghambat kemotaksis)
dengan cara mencegah fagositosis dari neutrofil yang disebut dengan potein A
yang memiliki bahan anti-fagositosik pada permukaan sel S.aureus. Selain itu
Staphylococcus aureus juga mengeluarkan leukotoxin yang dapat melisiskan
leukosit dan mengekspresikan superantigen (yang menyebabkan Toxic Shock
Syndrome) sehingga mampu mengalahkan respon imun dengan induksi kuat,

16
stimulasi polyclonal dan ekspansi dari reseptor sel T Vβ-Spesifik sel T (diikuti oleh
supresi sel T).
d. Biofilm
Staphylococcus aureus mampu meregulasi ekspresi gen hingga
membentuk biofilm yang tipis pada kulit yang rusak, peralatan medis, katup
jantung yang sehat maupun yang rusak. Koloni Staphylococcus aureus pada fase
stasionery dengan adanya biofilm, menunjukkan hampir seluruhnya resisten
terhadap agen antimikroba. Matriks biofilm ini mampu memproteksi sel imun
terutama imunoglobulin serta membatasi penetrasi antibiotik.
e. Resistensi Antibiotik
Staphylococcus aureus mampu meningkatkan resistensinya terhadap
beberapa antibiotik diantaranya : penisilin, methicillin, vancomycin, linezolid dan
cephalosporin. Staphylococcus aureus akan menghasilkan β-lactamase sehingga
menyebabkan efek penicillin. Methicillin-Resistants Staphylococcus aureus
(MRSA) memiliki gen mec sebagai pengikat penicillin dan gen fem mampu
memberikan resistensi terhadap methicillin, penicilline-resisten dan
cephalosporins. Resistensi terhadap vancomycin bergantung pada gen vanA dan
resistensi terhadap linezoid disebabkan oleh mutasi pada RNA S.aureus.
2.2.5 Faktor Virulensi Staphylococcus aureus
Bakteri Staphylococcus aureus dapat menimbulkan berbagai penyakit
dengan cara pembentukan berbagai macam zat seperti protein, enzim dan toksin,
berikut adalah faktor yang berperan sebagai faktor virulensi menurut Jawetz et al.
(2014), Irianto (2014) dan Todar (2005) adalah sebagai berikut :
1. Katalase
Katalase adalah enzim yang menyebabkan bakteri mampu bertahan terhadap
proses fagositosis. Uji katalase mampu membedakan genus bakteri
Staphylococcus dan Streptococcus.

17
2. Koagulase
Enzim koagulase yang terdapat pada bakteri Staphylococcus aureus dapat
menyebabkan penggumpalan plasma oksalat dan plasma sitrat. Selain itu,
esterase yang dihasilkan juga dapat meningkatkan penggumpalan, sehingga
terbentuk deposit fibrin pada permukaan bakteri yang dapat menghambat
fagositosis.
3. Hemolisin
Hemolisin adalah protein eksotoksin yang dikode di kromosom dan mempunyai
kemampuan melisiskan eritrosit, membebaskan Hb dan menghancurkan
banyak sel-sel lain. Hemolisin adalah imunogenik yang aktifitasnya dapat
dinetralkan oleh antibodi. Hemolisin dapat merusak eritrosit, menyebabkan
nekrosis jaringan lokal dan membunuh hewan coba. Hemolisin dibedakan
menjadi hemolisin alfa, beta, delta toksin.
Alfa toksin (α-toksin) adalah toksin yang mempunyai karakteristi diproduksi oleh
S.aureus. Pada manusia, α-toksin paling sensitif terhadap trombosit dan
monosit sedangkan pada hewan adalah eritrosit. α-toksin dapat dinetralkan
oleh IgG, namun tidak mampu dinetralisir oleh IgA dan IgM.
Beta toksin (β-toksin) merupakan sphingomyelinase yang banyak selaput lipid.
Toksin dapat menyebabkan hot-cold lysis pada eritrosit domba, setalah
diinkubasi selama 1 jam pada suhu 370C. Bakteriofag yang lisogenik diketahui
menyandi toksin tersebut.
Delta toksin (δ-toksin) merupakan peptida yang sangat kecil yang diproduksi
oleh bakteri Staphylococcus aureus dan S.epidermis, namun perannya belum
jelas diketahui.
4. Leukosidin
Leukosidin adalah protein toksin multicomponent yang dihasilkan sebagai
komponen terpisah. Toksin ini mampu membunuh sel darah putih pada

18
beberapa hewan tetapi patogenesis pada manusia masih belum jelas. Karena
diketahui bahwa, Staphylococcus patogen tidak mampu membunuh sel darah
putih pada manusia karena dapat difagositisis.
5. Toksin eksofoliatif
Toksin eksofoliatif dikenal mempunyai aktifitas proteolitik yang dapat
melarutkan matriks mukopolisakarida epidermis, sehingga menyebakan
terjadinya pemisahan intraepithelial pada ikatan sel di stratum granulosum.
Toksin ini yang menybabkan Staphylococcal Scalded Skin Syndrome yang
ditandai dengan melepuh pada kulit.
6. Toxic Shock Syndrome Toxin (TSST)
Sebagian besar dari galur Staphylococcus aureus yang berhasil diisolasi dari
penderita sindrom syok toksik, didapatkan toksin eksotoksin pirogenik. Toksin
ini dikenal mampu menyebabkan demam, syok, ruam pada kulit dan gangguan
multisistem pada organ tubuh manusia jika bakteri berhasil menginvasi dalam
waktu 3-5 hari.
7. Enterotoksin
Enterotoksin merupakan enzim yang tahan panas, pH basa di dalam usus,
enzim ini adalah penyebab utama keracunan makanan dengan waktu inkubasi
1-8 jam.
2.3 Respon Imun
2.3.1 Sistem Imun Non Spesifik
Sebagaimana diketahui, tubuh manusia memiliki imunitas bawaan (innate
immunity) yang merupakan benteng pertahanan tubuh yang pertama setelah kulit
dan mukosa. Sistem imun bawaan akan mengaktivasi fagosit (neutrofil dan
makrofag) serta komplemen yang memegang peranan sangat penting. Aktivasi
fagosit tersebut menggunakan reseptor permukaan yaitu reseptor mannose,

19
reseptor Fc dan aktivasi Toll-like receptors (TLRs) yang berfungsi sebagai
pengenal bakteri ekstraseluler dan meningkatkan fagositosis terhadap mikroba.
Bakteri gram positif yang mengandung peptidoglycan pada dinding selnya dan
lipopolysacharida (LPS) yang meningkatkan aktivasi komplemen pada jalur
alternatif. Bakteri tersebut juga mengekspresikan ikatan mannose-binding lectin
yang dapat mengaktifkan jalur lectin komplemen. Dimana fungsi daripada aktivasi
komplemen adalah untuk meningkatkan opsonisasi yang meningkatkan
fagositosis (Abbas & Litchman, 2014).
Proses fagositosis yang dilakukan oleh fagosit (neutrofil dan makrofag)
terjadi dalam 5 fase antara lain : fase pergerakan, perlekatan, penelanan
(ingestion), degranulasi, dan pembunuhan (killing). Diawali dengan penelanan
bakteri, dimana proses ini karena fagosit membentuk tonjolan pseudopodia,
kemudian membentuk kantung yang mengelilingi bakteri dan akan mengurungnya
sehingga bakteri akan terkurung di dalam kantung (vakuola) atau yang disebut
fagosom. Kemudian fagosom dengan berbagai jenis enzim dan protein lain dari
granula intraseluler bergabung (fusi) sehingga menyebabkan terjadinya
degranulasi dan respiratory burst di dalam fagolisosom. Enzim dan protein yang
terdapat di dalam granula tersebut mampu membunuh kuman, dengan cara
oksidatif maupun dengan cara non-oksidatif (Mayer, 2016).
Proses oksidatif dapat berlangsung dengan cara mieloperoksidase
ataupun tidak. Sedangkan proses non-oksidatif berlangsung dengan cara bantuan
protein sitolitik misalnya flavoprotein, sitokrom-β, laktoferin, lisozim, katepsin G,
defensin, dan sebagainya. Proses pembunuhan mikroba, pH dalam fagosom akan
meningkat menjadi basa selanjutnya turun kembali menjadi asam. Mekanisme
pembunuhan bakteri dengan cara non-oksidatif terjadi karena protein neutrofil
bermuara positif, sedangkan makrofag dalam suasana pH basa bersifat mampu
membunuh mikroba (Abbas & Litctman, 2015).

20
2.3.2 Sistem Imun Spesifik
Sistem imun spesifik bereaksi melawan mikroba dengan cara merangsang
limfosit B untuk mensekresikan antibodi. Limfosit T meregulasi sintesis antibodi
serta sel T yang bertugas sebagai sel T helper (Th1 dan Th2) dan sel T sitolitik.
Respon sistem imum spesifik diawali dengan terdeteksinya mikroba patogen oleh
makrofag sebagai Antigen Presenting Cells (APC) yang selanjutnya akan
dipresentasikan melalui MHC-II kepada sel TCD4+. Kemudian sel TCD4+ akan
mengeluarkan sitokin pro-inflamasi yang akan menginduksi terjadinya inflamasi
lokal, meningkatkan proses fagositosis, aktivitas mikrobisida dari makrofag dan
neutrofil, dan juga akan merangsang sel B untuk mensekresikan antibodi (Subowo,
2014).
Aktivasi sel B dapat terjadi dengan 2 cara yaitu aktivasi melalui jalur sel T
dependen dan sel T independen. Aktivasi melalui sel T dependen yaitu dengan
cara teraktivasinya sitokin-sitokin yang diproduksi oleh sel Th2 yaitu sitokin IL-4,
IL-5, IL-10 dan IL-13 maka akan meningkatkan proliferasi sel B yang akan
berdiferensiasi menjadi sel plasma yang mengeluarkan antibodi. Sedangkan
aktivasi melalui sel T independen berarti proliferasi sel B menjadi sel plasma dan
mengeluarkan antibodi tidak dibantu oleh jalur sitokin Th2 (Baratawidjaja dan
Rangganis, 2014).
Mekanisme antibodi dalam membunuh mikroba penyebab infeksi yaitu
dengan cara neutralisasi, opsonisasi dan fagositosis dan juga aktivasi komplemen.
Proses neutralisasi akan meningkatkan antibodi Immunoglobulin A (IgA) dalam
lumen organ mukosa, proses opsonisasi dan fagositosis dimediasi oleh subkelas
IgA dan aktivasi komplemen dimediasi oleh IgM dan IgG. IgA sendiri merupakan
produk sel plasma yang paling banyak ditemukan pada sekresi saluran nafas,
saluran cerna dan saluran kemih, keringat, ludah, air mata dan air susu ibu (ASI),
di dalam ASI bentuk sekretori IgA (sIgA) (Abbas & Lichtman, 2015).

21
2.3.3 Konsep Keseimbangan Th1 dan Th2
Pertumbuhan sel TH1 dan TH2 bukan proses acak tapi diatur oleh stimulus
yang diterima oleh sel T CD4+ yang naïf ketika mereka bertemu antigen mikroba.
Makrofag dan sel dendritik merespon banyak bakteri dan virus dengan
menghasilkan sitokin yang disebut IL-12. Ketika sel T naïf mengenali antigen dari
mikroba tersebut maka akan ditunjukkan oleh APC yang sama, sel T juga terpapar
dengan sitokin IL-12. IL-12 membantu diferensiasi sel T menjadi Th1, yang
kemudian memproduksi IFN- untuk mengaktifkan makrofag untuk mempercepat
pembunuhan mikroba (Abbas & Lichtman, 2015).
Produksi IL-12 oleh APC mempengaruhi respon imun adaptif, yang
mengarahkannya menuju sel Th1. Jika bakteri penyebab infeksi tidak
menyebabkan produksi IL-12 oleh APC, seperti kasus dengan helminth, sel T
sendiri yang akan memproduksi IL-2 yang mendorong diferensiasi sel ini menuju
bagian Th2, selanjutnya Th2 akan memproduksi IL-4 untuk sebagai respon imun
terhadap bakteri patogen dengan cara memproduksi antibodi, seperti yang terlihat
pada gambar 2.3 di bawah ini (Abbas & Lichtman, 2015).
Gambar 2.3 Perkembangan sel Th2 efektorKeseimbangan Th1 dan Th2 dipengaruhi oleh respon imun terhadap jenismikroba yang masuk, diferensiasi Th1 distimulasi oleh sitokin IL-2sedangkan pada Th2 diinduksi oleh sitokin IL-4 (Abbas & Lichtman,2015).

22
Keseimbangan antara diferensiasi Th1 dan Th2 dapat dipengaruhi oleh tipe
sel dendritik yang pada awalnya merespon infeksi dari mikroba tertentu. Jenis sel
dendritik akan dikenali tergantung pada jenis respon dan sitokin yang dikeluarkan.
Diferensiasi sel Th CD4+ menjadi bagian Th1 dan Th2 pada imunitas adaptif, dapat
menjelaskan bagaimana respon imun tubuh terhadap tipe mikroba yang masuk.
Selanjutnya, sel Th1 atau Th2 akan berkembang dari sel Th naif yang dikenali
antigen sehingga menghasilkan sitokin yang memperkuat diferensiasi sel T
(Baratawidjaja dan Rangganis, 2014).
Sel T CD8+ yang diaktifkan oleh antigen dan costimulator dibedakan
menjadi CTL (Cytolitic) yang mampu untuk membunuh sel terinfeksi yang
mempresentasikan antigen, CTL efektor akan membunuh sel yang terinfeksi
dengan cara mengeluarkan protein yang menimbulkan pori-pori pada membran
sel yang terkena infeksi dan mendorong pembagian DNA dan kematian sel.
Diferensiasi sel T CD8+ menjadi CTL efektor disertai dengan sintesis molekul yang
membunuh sel yang terinfeksi oleh mikroba (Abbas & Lichtman, 2015).
2.3.4 Respon Imun Mukosa Vagina
Vagina adalah pintu masuk ke dalam traktus genetalia pada wanita, vagina
dilapisi oleh epitel skuamus kompleks non-keratinisasi. Permukaan epitel kulit
vagina dan ektoserviks mempunyai kesamaan struktur, namun berbeda dengan
endoserviks yang dilapisi oleh sel epitel kolumner simpleks, dimana lapisan ini
memproduksi mukus yang membasahi dan melindungi epitel. Apabila terjadi
infeksi, trauma fisik, dan kimiawi maka dapat menyebabkan kerusakan sel epitel
dan membuka pintu masuknya patogen. Karena kulit dan mukosa merupakan
pertahanan awal terhadap patogen yang dapat menginfeksi masuk (Baratawidjaja
dan Rengganis, 2014).

23
Pertahanan kedua yakni sistem imum bawaan pada mukosa. Sistem ini
aktif bila dipicu oleh invasi patogen. Pengenalan antigen tersebut dimediasi oleh
Pattern Recognition-Receptor (PRR) yang terdiri dari Toll-Like Receptor (TLR),
NOD-like Receptor (NOD) dan Ribonukleated Acid (RNA) helicases. Reseptor-
reseptor tersebut mendeteksi antigen dengan cara pengenalan protein pemicu
yang dimiliki antigen atau yang dikenal dengan Pathogen-Associated Molecular
Pattern (PAMP), sebagai contoh bakteri gram negatif akan mengeluarkan
lipopolisakarida dan teichoid acid pada bakteri gram positif sebagai antigen PAMP
(Subowo, 2014).
Apabila PRR teraktivasi oleh patogen makan sel epitel akan melepaskan
beberapa kemokin seperti IL-8, RANTES, MIP-1α dan β, dan SDF-1 yang akan
mengumpulkan sel imun lain untuk menuju ke tempat yang terinfeksi. Selain itu,
sitokin proinflamasi juga dikeluarkan seperti IL-12, IFN-Ɣ, TNF-α dan IL-1β yang
akan mengaktifkan leukosit, serta sitokin IL-6, IL-15, TGF-β dan G-CSF yang
mempengaruhi diferensiasi dan regulasi respon limfosit T dan B. Sel-sel fagosit
yang terdiri dari makrofag, neutrofil, eosinofil, sel mast, sel dendritik, sel epithelial
dan sel Natural Killer (NK) berada pada jaringan mukosa (Pudjiati, 2010).
Pertahanan selanjutnya adalah sistem imun adaptif pada mukosa yang
terdiri dari imunitas humoral dan seluler. Imunitas humoral dimediasi oleh antibodi
yang diproduksi oleh sel plasma. Setelah di stimulasi oleh antigen yang masuk,
maka sel B di jaringan limfoid berdiferensiasi menjadi sel plasma yang selanjutnya
mengeluarkan IgA yang disekresi di mukosa jaringan limfoid genitourinaria yang
disebut dengan IgA sekretori (sIgA), sedangkan IgG bergerak ke sumsum tulang
atau ke daerah inflamasi (Baratawidjaja dan Rengganis, 2014).
Sedangkan imunitas seluler pada mukosa merupakan kunci pertahanan
terhadap patogen intraseluler. Pada mukosa genetalia terdapat sel T dan sel B,
regional kecil sistem imun adaptif yang khusus pada mukosa genitourinaria,

24
dimana terdapat Mucosal-Associated Lymphoid Tissue (MALT) yang kurang
menonjol. Pada saat sel densritik atau Antigen Presenting Cell (APC) yang berada
di lamina propia teraktivasi oleh antigen yang masuk, maka sel dendritik bermigrasi
menuju jaringan limfoid geniuterinaria dan mempresentasikan antigen ke limfosit
T, dari sini mulai terjadinya respon imun pada mukosa (Baratawidjaja dan
Rengganis, 2014).
2.3.5 Respon Imun pada Staphylococcus aureus
Respon imun berfungsi untuk melawan pathogen. Respon imun pada awal
infeksi bakteri Staphylococcus aureus ditandai dengan adanya sel neutrofil dan
makrofag setelah bakteri tersebut melewati barier kulit atau mukosa. Neutrofil dan
makrofag merupakan garis pertahanan terdepan (innate immunity) yang mampu
bergerak aktif dan dalam waktu singkat berkumpul dalam jumlah sangat banyak di
area yang mengalami inflamasi (Sunarso, 2007).
Selain itu, makrofag juga berperan sebagai antigen presenting cells (APC).
Peran makrofag, bakteri akan difagositosis dan juga akan dikenali oleh MHC II
selanjutnya akan dipresentasikan sebagai bentuk antigen peptida. Kemudian MHC
II akan berikatan dengan dengan limfosit T helper (CD4+) pada T Cell reseptor
(TCR) (Abbas, 2015).
Sel T CD4+ yang teraktivasi akan kehilangan CD62L dan mengekspresikan
berbagai molekul seperti CD25, CD44 dan CD69 sebagai bentuk perlawanan dan
meregulasi aktivitas sel T efektor yang teraktivasi akibat adanya paparan dari
antigen bakteri (Rifa’i, 2011). Selanjutnya sel T CD4+ efektor akan mensekresikan
IFN-Ɣ yang berfungsi sebagai aktivasi makrofag, fagositosis dan killing bacteri.
Kemudian sel T CD4+ akan mengeluarkan sitokin IL-2 yang mengakibatkan
aktivasi sel T sitotoksik (CD8+) dan sel Treg (CD4+ CD25+) (Abbas, 2015).

25
2.3.6 Inflamasi
Inflamasi didefinisikan sebagai reaksi pertahanan tubuh terhadap infeksi
atau kerusakan jaringan yang disebabkan karena trauma fisik atau kimia. Inflamasi
atau disebut juga peradangan dapat ditandai dengan gejala seperti rubor, kalor,
tumor, dolor, function laesa (Subowo, 2014). Inflamasi merupakan respon yang
terjadi terhadap respon rangsangan seperti terjadinya infeksi dan cidera jaringan.
Inflamasi dapat terjadi pada lokal, sistematik, akut dan kronis hingga menimbulkan
kelainan patologis (Baratawidjaja dan Rengganis, 2014).
Salah satu respon terhadap infeksi dan kerusakan jaringan adalah
terjadinya peningkatan sekeresi sitokin-sitokin proinflamasi untuk menginduksi
terjadinya inflamasi akut. Diantara sitokin yang dikeluarkan adalah IL-12 yang
kemudian merangsang perkembangan sel T naif menjadi aktif, selanjutnya
merangsang pengeluaran IFN-Ɣ sebagai salah satu sitokin proinflamasi akut
(Baratawidjaja dan Rengganis, 2014).
2.3.6.1 Sitokin Interleukin-12
1. Pengertian Interleukin-12
Interleukin 12 (IL-12) adalah interleukin yang secara alami diproduksi
oleh sel dendritik, makrofag dan limfoblastoid B manusia (NC-37) dalam
menanggapi rangsangan antigen. IL-12 merupakan sitokin heterodimer yang
dihasilkan oleh dua gene yang terpisah yaitu gene IL-12A (p35) dan IL-12B (p40)
(Subowo, 2014). IL-12 dikenal sebagai sitokin heterodimer yang memiliki beberapa
famili diantaranya IL-23, IL-27 dan yang baru ditemukan adalah IL-35, dimana
molekul-molekulnya mempunyai peran dalam imunitas seluler dan proses
perkembangan Th1 (Hamza et al, 2010).
Toll like receptors (TLRs) diyakini mempunyai peran yang sangat penting
dalam menjaga keseimbangan produksi pada IL-12 dan beberapa familinya. TLRs
menjadi bagian dalam proses aktivasi sistem imun seluler dalam melawan

26
patogen yang masuk yang menyebabkan terjadinya respon imun. Bentuk TLRs
dapat berbeda-beda tergantung pada sitokin yang ingin diaktifkan dari IL-12 dan
familinya. Sebagai contoh ligan TLR8 yang berpasangan dengan TLR3 atau TLR4
mampu menginduksi pengeluaran IL-12 lebih tinggi daripada hanya diinduksi oleh
satu TLR saja. IFN-regulatory factors (IRFs) terlibat dalam produksi IL-12,
termasuk diantaranya IRF1, IRF3 dan IRF7. Oleh sebab itu, sinyal IFN- melalui
IRF1 dan IRF8 dapat memicu induksi TLR memproduksi IL-12 (Hamza et al.,
2010).
IL-12 sangat penting dan mempunyai fungsi biologi yang menghubungkan
imunitas non-spesifik/innate immunity dan imunitas spesifik/adaptive immunity.
Awalnya IL-12 dikenal sebagai faktor diferensiasi sel T atau T cell Diferentiation
Factor (TCDF) dan Natural Killer Cell Stimulatory Factor (NKSF). Patogen yang
mempunyai lipopolisakarida (LPS), teichoic acid, peptigoglycan dan bacteril Cpg
DNA dapat menginduksi pengeluaran IL-12. Sitokin IL-12 teregulasi oleh feedback
positif dan negatif pada sitokin Th1 seperti IFN-γ, Th2 seperti IL-10 dan IFN-γ tipe
1 (Hamza et al,. 2010).
2. Peran IL-12 Pada Infeksi
IL-12 adalah sitokin yang terlibat dalam diferensiasi limfosit sel T CD4+ naif
menjadi sel Th1. IL-12 dikenal sebagai T cell-stimulating factor yang dapat
merangsang pertumbuhan serta fungsi sel T. Seperti yang terlihat pada gambar
2.4 di bawah ini bahwa IL-12 dapat merangsang produksi interferon-gamma (IFN-
γ) dan tumor necrosis factor-alpha (TNF-α) oleh sel limfosit T dan sel natural killer
(NK), dan mengurangi supresi IL-4 yang dimediasi oleh IFN-γ. Sel limfosit T yang

27
memproduksi IL-12 memiliki koreseptor yakni CD30, yang berhubungan dengan
aktifitas IL-12 (Subowo, 2014).
Gambar 2.4 Peran IL-12 Dalam Fagositosis MikrobaIL-12 membantu peningkatan produksi IFN-γ sehingga memperkuat kinerjamakrofag dalam mempercepat proses fagositosis mikroba (Subowo, 2014).
IL-12 memainkan peran penting dalam kegiatan sel NK dan limfosit T, yaitu
dengan cara IL-12 meningkatkan aktivitas sitotoksik sel NK dan CD8+ (limfosit T
sitotoksik). Hal tersebut karena ada hubungan antara IL-2 dan sinyal transduksi
dari IL-12 dalam sel NK. IL-2 merangsang ekspresi dari dua reseptor yaitu IL-12
(IL-12R-β1 dan IL-12R-β2), selain itu juga mempertahankan ekspresi protein
penting yang terlibat dalam sinyal IL-12 dalam sel NK (Baratawidjaja, 2014).
IL-12 juga memiliki aktivitas anti- angiogenik , yang berarti dapat memblokir
pembentukan pembuluh darah baru. Hal ini dilakukan dengan meningkatkan
produksi interferon gamma, selanjutnya akan menginduksi peningkatan produksi
kemokin IP-10 yang akan memberikan efek anti-angiogenik (Subowo, 2014).
Dari gambar 2.5 berikut ini dapat dipahami bahwa IL-12 mempunyai
banyak peran dalam mencegah terjadinya infeksi yaitu dengan cara meningkatkan
proliferasi haematopoietic progenetor yang bekerja sinergis sebagai colony-
stimulating factors, juga proliferasi sel NK, sel NKT, dan sel T yang akan
meningkatkan sitotokisitas dan memproduksi sitokin seperti IFN- yang
merupakan produksi dari sel Th1 yang akan memberikan feedback kembali
kepada makrofag untuk membunuh bakteri, dan juga memproduksi sel B melalui

28
efek sitokin Th1 yaitu IFN- yang akan meningkatkan aktivasi dan memproduksi
immunoglobulin seperti IgG sehingga infeksi dapat dicegah (Hamza et al., 2010).
Gambar 2.5 Aktivitas IL-12 Dalam Mencegah InfeksiPeran IL-12 selain membantu diferensiasi sel T naif menjadi sel Th1, jugamembantu proliferasi sel NK, sel NKT serta memproduksi sel B melalui efeksitokin Th1 seperti IFN- sehingga meningkatkan produksi antibodi (Hamzaet al., 2010).
Sebuah hasil pemeriksaan menyebutkan bahwa kurangnya kadar IL-12
pada mencit yang diinduksi oleh bakteri Staphylococcus aureus menyebabkan
penyebaran koloni bakteri ke beberapa organ. Hal tersebut disebabkan karena
produksi IFN- juga kurang pada mencit tersebut. Sehingga bila kadar IL-12
menurun maka resiko terjadinya infeksi arthritis pada mencit tersebut meningkat
(Hultgren et al., 2000).
Penelitian lainnya menilai kadar IL-12 dan perbedaannya pada anak yang
mengalami kondisi septik, dimana hasilnya berupa kadar IL-12 tidak dapat
dibedakan pada pasien dengan keadaan septik, kadar IL-12 dapat terjadi
peningkatan pada suatu waktu-waktu (Martin et al., 2012).
IL-12 berpeluang menjadi agen immunoterapetik karena mempunyai peran
sentral dalam meregulasi respon imun innate dan adaptiv, serta mempu bekerja

29
secara sinergis bersama dengan sitokin lainnya dalam meningkatkan
immunoregulator. Beberapa penelitian pada manusia dan hewan coba
menunjukkan adanya hasil yang baik daripada mekanisme IL-12 dalam mencegah
ataupun mengobati infeksi yang disebabkan oleh salah satunya bakteri (Hamza et
al., 2010).
2.3.8 Interferon-gamma
1. Pengertian Interferon-Gamma
IFN-γ (interferon-gamma) merupakan sitokin yang diproduksi oleh sel NK
yang teraktivasi, sel Th1, dan sel TCD8+ sitotoksik. Produksinya juga banyak
diregulasi oleh sitokin seperti IL-12, IL-18 dan TNF-α (Schulte et al., 2013).
IFN-γ merupakan sitokin yang kritis terhadap imun alami dan imun adaptif
dalam melawan virus dan infeksi bakteri intraselluler dan untuk mengontrol tumor.
Ekspresi IFN-γ dihubungkan dengan sejumlah penyakit autoinflamatori dan
autoimun. Hal yang paling penting dari IFN-γ dalam sistem imun adalah
kemampuannya untuk menghambat replikasi virus secara langsung, Namun, yang
paling terpenting, adalah pengaruh immunostimulator dan immunomodulatornya
(Baratawidjaja dan Rengganis, 2014).
Fungsi IFN-γ termasuk mengaktivasi makrofag untuk meningkatkan proses
fagositosis dan kemampuan membunuh sel-sel tumor dan juga mengaktifkan dan
meningkatkan pertumbuhan sel-sel T sitolitik dan sel NK (Baratawidjaja dan
Rengganis, 2014).
2. Peran Interferon-gamma Dalam Infeksi
IFN-γ meregulasi ekspresi antigen MHC klas I, dan menginduksi MHC klas
II dan ekspresi reseptor Fcγ pada makrofag dan sel-sel lainnya termasuk sel-sel
limfoit, sel-sel endotel, sel-sel mast dan fibroblas sehingga mempengaruhi

30
kemampuan sel-sel tersebut untuk menyajikan antigen. Dengan diaktifkannya
MHC klas II pada sel-sel endotel, sel-sel ini kemudian menjadi peka terhadap aksi
sel-sel T sitolitik spesifik klas II (Subowo, 2014).
IFN-γ merupakan sitokin yang sangat penting untuk imunitas alami dan
adaptif pada infeksi virus dan infeksi bakteri intraseluler serta terhadap kontrol
tumor, IFN-γ berfungsi sebagai pengaktif utama sel makrofag. Ekspresi IFN-γ
berhubungan dengan penyakit autoimun dan peradangan (Abbas & Lichtman,
2015). Skema IFN-γ dalam mengaktifkan makrofag untuk membantu proses killing
bakteri dapat dilihat pada gambar di bawah ini :
Gambar 2.6 Aktivitas IL-12 dan IFN-γ Dalam Membunuh BakteriIFN-γ dapat mengaktifkan makrofag untuk meningkatkan fungsinya dalammelakukan fagositosis terhadap mikroba yang masuk (Abbas & Lichtman,2015).
Reseptor IFN-γ hampir dimiliki oleh semua jenis sel kecuali eritrosit dan
merespons rangsangan IFN-γ dengan cara meningkatkan ekspresi MHC kelas I,
dimana MHC kelas I berperan penting dalam penyajian epitop antigen endogen
kepada limfosit sitotoksik (limfosit T CD8+) dalam respons imun seluler. IFN-γ juga
berperan dalam meningkatkan ekspresi MHC kelas II yang penting dalam
penyajian epitop antigen kepada limfosit TCD4+. Selain itu, IFN-γ juga memiliki
aktifitas potensial bagi sel makrofag yang dirangsang sehingga mendorong sekresi

31
monokin IL-1, IL-6, IL-8 dan TNF; dan juga IFN-γ berperan pada aktivasi sel
netrofil, sel NK dan sel-sel endotel (Subowo, 2014).
Secara fisiologi pembentukan osteoklas diatur oleh sitokin-sitokin utama
osteoklastogenik M-CSF dan RANKL. Bagaimanapun, kondisi fisiologik yang
terjadi, seperti selama berlangsungnya inflamasi, infeksi, dan defisiensi estrogen,
resorpsi tulang secara signifikan distimulasi sehubungan dengan penambahan
produksi faktor-faktor disregulasi pro- dan anti- osteoklastogenik, termasuk IFN-γ,
yang menjadi pusat mediator imun adaptif (Abbas & Lichtman, 2015).
Penelitian menyebutkan bahwa mencit yang kekurangan kadar IFN-γ
menunjukkan lebih rentan dimasuki oleh bakteri patogen intraseluler seperti
Leishmania major, Listeria monocytogenes, Mycobacteria dan beberapa virus
lainnya. Kadar IFN-γ pada orang sehat tidak dapat terdeteksi, namun pada pasien
dengan sepsis level IFN-γ justru tinggi akan tetapi tidak berkorelasi secara
significan dengan parahnya sepsis ataupun kematian (Schulte et al., 2013).
Peran IFN-γ pada penyembuhan sepsis telah dilaporkan, dimana selama
immunoparalytic fungsi fagositosis pada makrofag terganggu dan berkurangnya
jumlah sitokin Th1 yang terjadi selama simulasi oleh produk-produk bakteri.
Namun, Flohe et al., mengatakan bahwa IFN-γ bekerja sebagaimana Granulocyte-
Macrophage Colony-Stimulating Factor (GM-CSF) yang mampu mengembalikan
fungsi makrofag untuk mencegah mencit sepsis selama terjadi rangsangan dari
bakteri (Schulte et al., 2013).
Terapi IL-12 menstimulasi sel Th untuk mensekresikan sitokin Th1 seperti
IFN-γ. Aktivasi makrofag memproduksi sitokin IL-12 yang semakin banyak, dan ini

32
memberikan positif feedback dimana IL-12 sendiri menstimulasi pengeluaran IFN-
γ dan sel NK sehingga memperkuat makrofag untuk membunuh bakteri sebagai
upaya mencegah terjadinya infeksi seperti dijelaskan gambar 2.7 berikut (Schulte
et al., 2013).
Gambar 2.7 Aktivasi Makrofag oleh IFN-γProduksi IFN-γ yang distimulasi oleh IL-12 melalui sel Th1 dapatmengaktivasi makrofag dalam membunuh bakteri patogen yangmasuk ke dalam tubuh (Schulte et al., 2013).
2.4 Turi Merah
2.4.1 Pengertian, Morfologi dan Klasifikasi Turi Merah
Tanaman turi atau Sesbania grandiflora atau agati merupakan
tanaman yang berbentuk pohon dan digolongkan ke dalam subfamili
Faboideae. Turi banyak ditemukan di beberapa daerah tropikal di Asia
seperti Indonesia, India, Malaysia, Myanmar, dan Filipina. Di India
tanaman turi banyak digunakan dalam teknik pengobatan Ayurveda.
Tanaman legum ini sudah banyak dikenal di seluruh Indonesia, terutama
di wilayah Indonesia bagian tengah dan timur. Hal tersebut
menyebabkan banyak nama yang diberikan pada tanaman ini (Nasution,
2010).

33
Daun dari tanaman ini berbentuk lonjong (oval), bersifat majemuk
menyirip ganda, dan letaknya tersebar. Panjang daun sekitar 20-30 cm
dengan daun penumpu dimana panjangnya sekitar 0.5-1 cm. Anak daun
bertangkai pendek dengan jumlah yaitu kurang lebih 20-50 pasang anak
daun dalam satu tangkai. Helaian anak daun berbentuk jorong
memanjang, tepi rata, panjang 3-4 cm, lebar 0,8-1,5 cm (Nasution,
2010). Gambaran bentuk daun dan bunga turi merah dapat dilihat pada
gambar dibawah ini.
Gambar 2.8 Daun Dan Bunga Turi MerahTanaman turi merah terdiri dari batang, daun, bunga, buah dan akar.Kelopak bunga membentuk bulan sabit berwarna merah. Daunnya menyiripberganda dengan bentuk bulat sampai bulat memanjang (Nasution, 2010)
Klasifikasi dari tanaman turi merah menurut Nasution, (2010)
antara lain :
Kingdom : Plantae (tumbuhan)
Devisi : Mangnoliphyta (tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping daun/dikotil)
Ordo : Fabales
Famili : Fabaceae (suku polong-polongan)
Bangsa : Robinieae
Genus : Sesbania

34
Spesies : Sesbania grandiflora (L) Pers
2.4.2 Kandungan Kimia Dalam Daun Turi Merah
Uji fitokimia dengan beberapa jenis pelarut dilakukan untuk menguji
kandungan fitokimia secara kualitatif dari tanaman turi (sesbania grandiflora), dari
uji fitokimia tersebut disimpulkan bahwa beberapa kandungan kimia yang terdapat
dalam daun turi antara lain seperti alkaloid, saponin, karbohidrat, terpenoid,
flavonoid, tanin, fenol, fitosterol, dan triterpenen (Dethe et al., 2014). Namun hanya
dengan menggunakan pelarut etanol maka kandungan seperti flavonoid, saponin
dan tanin dapat terdeteksi secara kualitatif, hal tersebut sebagaimana ditampilkan
dalam tabel berikut :
Tabel 2.1 Fitokimia Ekstrak Aqueous, Ethanol Dan Acetone Daun TuriKandungan daun turi merah yang mempunyai sifat sebagai antibakteri yaituflavonoid, tanin dan saponin yang ketiganya dapat dikeluarkan dengan caraekstraksi menggunakan pelarut etanol (Dethe et al., 2014).
Terdapat beberapa kandungan kimia yang diduga mempunyai efek
sebagai anti bakteri yaitu antara lain flavonoid, saponin dan tanin.
2.4.2.1 Flavonoid
Flavonoid atau dikenal sebagai bioflavonoid adalah jenis polifenol yang
terdapat hampir pada seluruh tanaman yang terkonsentrasi di bagian daun, kulit,

35
buah, biji dan bunganya. Senyawa-senyawa flavonoid umumnya bersifat
antioksidan dan banyak yang telah digunakan sebagai salah satu komponen
bahan baku obat-obatan. Flavonoid merupakan senyawa polar yang umumnya
mudah larut dalam pelarut polar seperti etanol, methanol, butanol, dan aseton
Dethe et al., 2014).
Penelitian di bidang farmasi menunjukkan bahwa flavonoid mampu menjadi
antioksidan yang baik. Jenis flavonoid seperti flavones dan katekin merupakan
yang paling kuat dalan menangkal reactive oxygen spesies (ROS) yang menjadi
penyebab kerusakan sel dan jaringan tubuh. Selain itu, terdapat beberapa derivat
flavonoid yang dapat digunakan sebagai antijamur, antibakteri dan antivirus
(Cushnie and Lamb, 2005).
1. Flavonoid sebagai antibakteri
Flavonoid merupakan golongan terbesar dari senyawa fenol. Senyawa
fenol mempunyai sifat efektif menghambat pertumbuhan virus, bakteri dan jamur,
karena menyebabkan terjadinya kerusakan permeabilitas dinding sel bakteri.
Selain itu, flavonoid juga mampu menghambat motilitas bakteri (Darsana et al.,
2012).
Fungsinya sebagai antibakteri, flavonoid bekerja dengan tiga mekanisme
yaitu mencegah sintesis asam nukleat maka akan menghambat sintesis DNA dan
RNA dari bakteri, menghambat sitoplasma bakteri dan menegatif nghambat
metabolisme energi bakteri. Selain itu, katekin yang juga masih kelompok
flavonoid yang memiliki aktifitas yang sangat besar sebagai antibakteri pada
bakteri gram positif dan negatif dengan cara merusak membran bakteri dan
menggnggu fungsi barier bakteri (Cushnie and Lamb, 2005).
Flavonoid merupakan senyawa fenol yang berfungsi sebagai koagulator
protein. Flavonoid berfungsi sebagai antibakteri dengan cara membentuk senyawa

36
kompleks pada protein ekstraseluler sehingga mengakibatkan terganggunya
integritas membran sel bakteri (Juliantina, 2008).
2. Farmakokinetik flavonoid
Sebagian besar flavonoid yang berada pada tumbuhan akan terkonjugasi
dengan glikosida yaitu β-glycosides. Glukosides merupakan salah satu glikosida
yang diserap oleh usus kecil. Penyerapan melalui usus kecil akan lebih efisien
daripada penyerapan melalui usus besar, dimana penyerapan melalui usus kecil
terjadinya peningkatan plasma (Holman, 2004).
Absorbsi flavonoid dari makanan tergantung pada sifat fitokimia seperti
ukuran mlekul, konfigurasi, lipofilisitas, kelarutan dan pKa. Flavonoid secara garis
besar berikatan dengan molekul gula, sehingga usus akan mengubahnya menjadi
aglycon bebas gula. Hal tersebut dikarenakan hanya aglycon saja yang mampu
diserap di dalam usus kecil, sedangkan glikosida dianggap terlalu hidrofilik
untukpenyerapan pasif difusi melalui usus kecil (Holman, 2004).
Setalah penyerapan di usus kecil, flavonoid selanjutnya akan terkonjugasi
dengan glucuronic acid atau sulfate atau O-methylation. Reaksi konjugasi tersebut
sangat efisien, dikarenakan tidak ditemukan aglycon flavonoid yang bebas di
dalam urine kecuali jenis flavonoid katekin. Flavonoid yang tidak dapat diserap
oleh usus kecil selanjutnya akan melewati proses fermentasi di usus besar dan
dimetabolisme kembali oleh mikroflora di usus, mikroorganisme ini akan
mengubah flavonoid menajdi stuktur cincin (Holman,2004).
Selanjutnya flavonoid diserap melalui membran gastrointestinal lalu dibawa
menuju ke hati, karena metabolisme flavonoid terjadi di hati dan terkonjugasi
dengan glucoronic acid, sulfate atau glycine lalu akhirnya akan disekresikan
melalui urine (Holman, 2004).

37
2.4.2.2 Saponin
Saponin merupakan senyawa glikosida kompleks dengan berat molekul
tinggi yang dihasilkan terutama oleh makanan. Saponin banyak dimanfaatkan oleh
masyarakat sebagai bahan pembuat sabun. Saponin diketahui larut dalam air dan
etanol, tetapi tidak larut dalam eter, sehingga ekstraksi saponin paling tepat
dilarutkan dengan etanol 70%-96% atau pelarut metanol (Suharto et al., 2001).
Saponin mengandung gugus gula terutama dalam bentuk glukosa,
galaktosa, xylosa rhamnosa atau methilpentosa yang berikatan dengan suatu
aglikon hidrofobik (sapogenin) berupa triterpenoid, steroid atau steroid alkalid.
Saponin banyak ditemukan pada berbagai jenis tanaman, baik itu tanaman liar
ataupun tanaman yang dibudidayakan (Suharto et al., 2001).
1. Saponin sebagai antibakteri
Mekanisme kerja saponin sebagai antibakteri adalah dengan menurunkan
tegangan permukaan sehingga mengakibatkan naiknya permeabilitas atau
kebocoran sel dan mengakibatkan senyawa intraseluler keluar (Nuria, 2009).
Selain itu, saponin bekerja sebagai antibakteri dengan cara mengganggu
stabilitas membran sel bakteri yang menyebabkan penurunan tegangan
permukaan dan peningkatan permeabilitas sel bakteri sehingga mengakibatkan
kerusakan membran sel karena disebabkan oleh komponen penting dari bakteri
sudah keluar seperti protein, asam nukleat, dan nukleatida yang akhirnya
membuat bakteri lisis (Darsana et al., 2012).
2. Famakokinetik saponin
Saponin memiliki sifat fisikokimia yang kurang menguntungkan dari segi
proses penyerapan ke dalam tubuh, hal tersebut disebabkan karena saponin
memiliki massa molekul sebesar >500 Da, kapasitas hydrogen-binding yang tinggi
yaitu >12 dan fleksibilitas molekul yang tinggi yaitu >10. Kesulitan penyerapan
terutama terjadi di dalam usus halus dan dapat menurunkan permeabilitas

38
membran, hal tersebut ditunjukkan dengan konsentrasi saponin pada sebagian
jaringan tikus lebih rendah dibandingkan di dalam plasmanya. Namun, konsentrasi
saponin banyak ditemukan di dalam hati, sedangkan pada ginjal saponin
melibatkan mekanisme transfer-mediated uptake yang cukup tinggi. Saponin
dapat dihidrolisis oleh mikroflora kolon. Beberapa saponin seperti ginsenosides
Ra3, Rb1, dan Rd serta Dioscin mampu diekskresikan secara perlahan ke dalam
empedu dengan waktu paruh yang panjang yaitu selama 7-25 jam pada tikus
(Keyu et al., 2012).
Saponin juga diketahui dapat menigkatkan permeabilitas sel mukosa
intestinal, menghambat transpor aktif zat-zat makanan dan memudahkan
masuknya substansi yang dalam kondisi tidak dapat diserap. Saponin juga
diketahui dapat mengganggu penyerapan mineral dan vitamin dalam tubuh,
saponin juga menekan konsentrasi Fe hati dengan cara penyerapan Fe yang tidak
sempurna dengan membentuk kompleks Saponin-Fe. Sponin lucerne diketahui
dapat meningkatkan ekskresi Fe dan Mg, serta menurunkan Ca dan Zn pada
plasma (Keyu et al., 2012).
Mekanisme kerja saponin di dalam usus halus belum dipahami mendalam.
Saponin yang dikonsumsi mempunyai ligand yang potensial di dalam usus halus
seperti garam empedu, kolesterol, sterol membran sel mukosa dan antinutrisi,
ligand-ligand tersebut mampu menurunkan atau menghambat efektifitas saponin
(Suparjo, 2011).
2.4.2.3 Tanin
Tanin adalah kelompok dari metabolit fenolik dengan berat molekul antara
500 dan 30000 Da yang terdapat pada banyak makanan nabati dan minuman.
Bagian tumbuhan yang banyak terdapat kandungan tanin adalah kulit, kayu daun,
akar dan buah (Serrano et al., 2009).

39
Tanin banyak dikandung pada beberapa jenis makanan seperti teh, biji
kokoa, anggur dan strawberry. Bahan astrigen dari tanin dapat mendorong dan
menyatu dengan enzim dari mikroba. Dengan demikian, akan menghambat banteri
membentuk diri dikarenakan enzim dari bakteri bercampur dengan enzim dari
tanin. Adanya ion logam yang berkumpul dan membentuk tannins toxocity yang
mempengaruhi pembentukan membran mikroorganisme (Akiyama et al., 2001).
1. Tanin sebagai antibakteri
Mekanisme tanin tanin sebagai antibakteri yaitu tanin diketahui mempunyai
kemampuan dalam menginaktivasi molekul yang menempel pada sel hospes yang
terdapat pada permukaan sel. Enzim yang terikat pada membran sel dan
polipeptida dinding sel akan menyebabkan kerusakan pada dinding sel, kerena
mempunyai senyawa fenol. Karena kerusakan pada dinding sel bakteri maka
dapat menyebabkan kerusakan membran sel bakteri tanpa dinding atau yang
dikenal dengan protoplast (Naim, 2004).
Kerusakan pada dinding sel bakteri menyebabkan kerusakan membran sel
bakteri yaitu hilangnya sifat permeabilitas membran sel, sehingga keluar dan
masuknya zat-zat seperti air, nutrisi, enzim-enzim yang tidak terseleksi. Apabila
banyak zat yang keluar dari dalam sel bakteri maka akan menghambat
metabolisme sel sehingga menyebabkan terhambatnya pembentukan ATP yang
diperlukan untuk pertumbuhan dan perkembangbiakan sel bakteri. Bila hal
tersebut terjadi maka kematian sel bakteri (Hayati et al., 2009).
Selain itu, tanin juga menghambat enzim reverse transcriptase dan DNA
topoisomerase sehingga jumlah asam amino yang menjadi pembentuk sel bakteri
tidak dapat terbentuk (Nuria et al., 2009).
2. Farmakokinetik tanin
Tanin yang bersumber dari ekstrak tumbuhan akan dapat diabsorpbsi
dengan cepat di dalam saluran cerna serta melewati proses distribusi dan eliminasi

40
yang cukupcepat pula. Bioavailabilitasnya sangat rendah pada pemberian peroral.
Konsentrasi dalam plasma sekitar 213 ng/ml setelah 1 jam pemberian peroral
sebanyak 0.8 g/kgBB ekstrak yang mengandung tanin. Tanin banyak mengalami
hidrolisis yang terjadi pada usus besar pada pH alkalin (Wang et al., 2010).
Substrat tanin yang dicerna pada usus besar akan difermentasi oleh bakteri
mikroflora bersama dengan substrat lainnya yang tidak dapat dicerna.
Metabolisme tanin di dalam usus besar dibantu oleh enzim mikrobiota yang
mengakibatkan terjadinya kerusakan struktur asli tanin menjadi sulit diserap dan
akan tetap berada di dalam lumen usus dimana akan menetralkan peroksidan dari
makanan yang berada di dalam usus besar yang dihasilkan selama metabolisme
mikroba usus. Sebagaimana dilaporkan bahwa hydrolysable yang tergradasi
menjadi gallic acid, pirogalol, phloroglucinol dan akhirnya menjadi asetat dan
butiran yang terjadi melalui aksi enzim bakteri yang berbeda-beda. Galotanin
sangat mudah tergradasi oleh bakteri, jamur dan ragi, sedangkan residu galloy
hanya mampu terhidrolisis pada ellagitannins oleh mikroba (Serrrano et al., 2016).
Senyawa tanin seperti ellagic acid dapat bereaksi bersama dengan radikal
bebas karena kemampuannya untuk berikatan dengan ion-ion metal, sehingga
mempunyai efek antioksidan yang poten terhadap lipid peroksidasi dalam
mitokondria dan mikrosom. Kemampuannya sebagai antioksidan dinilai dengan
cara tanin menyediakan elektron yang mampu mengeliminasi radikal bebas hasil
peroksidasi lipid (Wang et al., 2010).
2.4.3 Daun Turi Merah Sebagai Antibakteri
Tanaman turi dikenal memiliki aktifitas sebagai antibakteri berdasarkan
pada beberapa penelitian berikut ini :
1. Ekstraksi daun turi merah terbukti memiliki kemampuan sebagai antibakteri
terhadap bakteri Klebsiella pneumoniae secara in vitro dengan kadar hambat
minimal pada kosentrasi 17,5% dan kadar bunuh minimal (KHM) pada

41
konsentrasi 20%. Semakin tinggi konsentrasi ekstrak etanol daun turi merah,
maka semakin rendah jumlah koloni bakteri Klebsiella pneumoniae yang
tumbuh pada media NA (natrium agar) (Ikrimah, 2013).
2. Ekstrak etanol daun turi merah mempunyai efek sebagai antibakteri secara in
vivo terhadap bakteri Staphylococcus aureus dengan kadar hambat minimum
konsentrasi 14% dan kadar bunuh minimum (Yusniawati, 2015).
3. Ekstrak bunga turi merah mempunyai efek antibakteri secara in vivo terhadap
bakteri Staphylococcus aureus dengan KHM 5% dan KBM 6% (Mirza, 2008).
4. Senyawa kimia dari daun turi selain dapat dapat dijadikan sebagai terapi
antibakteri juga sangat potensial sebagai terapi antifungi dan juga anti-
inflamasi. Hal tersebut berdasarkan hasil penelitiannya dengan
membandingkan efektifitas daun turi sebagai antibakteri pada bakteri E.coli dan
Pseudomonas aeruginosa dan sebagai antifungi pada Candida albicans
(Kumar, 2015).
5. Daun turi mempunyai kemampuan sebagai antibakteri dan potensial
berpeluang sebagai produk antibiotik terbaru yang sangat efektif untuk
pencegahan, dan pengobatan infeksi dan kemoterapi (Vipin et al., 2011).
2.4.4 Manfaat lain dari Turi Merah
Selain mempunyai khasiat sebagai antibakteri, tanaman turi juga diketahui
memiliki kemampuan lainnya yakni sebagai imunomudulator. Hal ini dibuktikan
dengan hasil ekstrak metanol dari bunga turi tidak hanya dapat menstimulasi
respon imun nonspesifik seperti aktifitas fagositosis, tetapi juga mampu
meningkatkan respon imun humoral serta imunitas seluler dengan sangat efektif
(Arunabha, 2014).
Imunomudulator terbagi menjadi imunosupresan dan imunopotensiasi
yang terbagi menjadi imunorestorasi dan imunostimulan. Imunosupresan adalah
suatu proses supresi sistem imun untuk meminimalisir reaksi penolakan pada

42
kejadian transplantasi maupun akibat daripada kejadian inflamasi. Imunorestorasi
merupakan proses pengembalian fungsi sistem imun yang terganggu dengan
berbagai komponen sistem imun seperti transplantasi sumsum tulang, sedangkan
imunostimulan merupakan suatu proses perbaikan fungsi sistem imun dengan
menggunakan bahan-bahan yang dapat meningkatkan fungsi sistem imun baik
dari bahan biologis seperti hormon dan sitokin maupun sintetis seperti levamisol
(Baratawidjaja dan Rengganis, 2014).
Pemberian ekstrak rumput mutiara yang mempunyai kandungan flavonoid,
dapat meningkatkan aktivitas fagositosis makrofag. Mekanisme flavonoid dapat
meningkatkan fagositosis yakni dengan cara memacu produksi IFN-Ɣ dan
mempercepat diferensiasi monosit menjadi makrofag di dalam jaringan.
Kemampuan sebagai imunostimulator dari flavonoid tersebut tidak hanya dilihat
dari indeks fagositosis tetapi juga dapat dilihat dari fungsi makrofag seperti mampu
memfagositosis partikel asing contohnya mikroorganisme, makromolekul yang
mempresentasikan sel atau jaringan yang mengalami kerusakan atau mati, dan
juga sebagai APC kepada sel T dan mampu memproduksi sejumlah sitokin
(Azenda, 2006).
Selain itu, penelitian secara in vivo menyatakan bahwa pemberian ekstrak
tumbuhan yang mengandung saponin secara oral dapat meningkatkan proliferasi
sel dan menginduksi proliferasi sel T dan sel B independen yang distimulasi oleh
LPS (Chavali et al.,1987).
2.5 Mus musculus
2.5.1 Pengertian Mus musculus
Mencit (mus musculus) adalah anggota Muridae (tikus-tikusan) yang
berukuran kecil yang dapat hidup pada daerah dingin dan panas. Mencit
merupakan hewan yang banyak digunakan sebagai hewan model dalam penelitian

43
biomedis, pengujian dan pendidikan yaitu berkisar antara 40%-80%. Hal ini
dikarenakan memiliki keunggulan-keunggulan seperti mudah dibiakkan, siklus
hidup yang relatif pendek, jumlah perkelahiran banyak, variasi sifat-sifatnya tinggi,
mudah ditangani serta tergolong murah (Kusumawati, 2004).
Mencit termasuk hewan poliestrus dimana siklusnya berlangsung setiap 4-
5 hari, lama birahi 9-20 jam, dan estrus dapat terjadi pada 20-40 jam pasca partum.
Mencit betina dikenali dengan cara jarak lubang genital dan lubang anusnya yang
berdekatan sedangkan mencit jantan dikenali pada saat organ seksualnya sudah
matang maka testisnya akan terlihat sangat jelas, karena ukurannya yang relatif
besar dan biasanya tidak tertutupi oleh rambut (Kusumawati, 2004). Gambaran
bentuk mencit dapat dilihat pada gambar berikut :
Gambar 2.9 Mencit (Mus musculus)Mencit galur Balb/c berwarna putih termasuk sebagai hewanmamalia (Kusumawati, 2004).
2.5.2 Klasifikasi Mus musculus
Klasifikasi mencit (Mus musculus) menurut Kusumawati (2004) antara lain
sebagai berikut :
Kingdom : Animalia
Filum : Chordata
Sub Filum : Vertebrata

44
Kelas : Mamalia
Ordo : Rodentia
Sub Ordo : Myoimorphia
Famili : Muridae
Genus : Mus
Spesies : Mus musculus
2.5.3 Karakteristik Mus musculus
Karakteristik mencit (mus musculus) menurut Syamsuddin dan Darmono
(2011) antara lain sebaagi berikut :
Lama hidup : 1-2 tahun, bisa sampai 3 tahun
Lama produksi ekonomis : 9 bulan
Lama bunting : 19-21 hari
Kawin sesudah beranak : 1-24 jam
Umur dewasa : 35 hari
Umur sapih : 21 hari
Umur dewasa : 35 hari
Umur dikawinkan : 8 minggu (jantan dan betina)
Siklus estrus (menstruasi) : 4-5 hari
Lama estrus : 12-14 jam
Ovulasi : dekat akhir periode estrus, spontan
Fertilisasi : 2 jam sesudah kawin
Berat dewasa : 20-40 gram jantan, 18-35 gram betina
Berat lahir : 0,5 – 1 gram
Jumlah anak : rata-rata 6-15
Suhu rektal : 37,50C
Laju respirasi : 40

45
Denyut jantung : 165 x/mm
Pengambilan darah maksimum : 310-840 x/mm
Jumlah sel darah merah : 7,7 ml/kg
Jumlah sel darah putih : 8,4 x 103/µl
Kadar haemoglobin (Hb) : 8,7-10,5 x 106/µl
Konsumsi pakan perhari : 5 gram (umur 8 minggu)
Konsumsi air minum perhari : 6,7 ml (umur seminggu)
2.5.4 Mus musculus nifas
Pada mencit, fase nifas estrus akan dimulai antara sekitar 10 dan 24 jam
setelah melahirkan dan fase estrus ini cenderung terjadi pada malam pertama dan
berlangsung setelah 10 jam melahirkan (Gillbert et al., 1985). Jarak kelahiran dan
ovulasi berikutnya pada mencit yakni sekitar 14-28 jam (Long dan Mark, 1911).
Masa nifas (postpartum) mencit terjadi secara acak dalam jangka waktu 24
jam dan masa ovulasi dan pembuahan sangat dipengaruhi oleh cahaya. Namun
kecenderungan ovulasi berkurang selama 12-18 jam setelah kelahiran (Runner
dan Ladman, 1950).
2.5.5 Mus musculus Model Infeksi
Berdasarkan penelitian disebutkan bahwa pemberian bakteri
Staphylococcus aureus sebanyak 5 x 107 sebanyak 0.2 ml pervaginal pada Mus
musculus terbukti mampu memberikan efek antagonis dan berpengaruh terhadap
respon imun (Liudmilla et al., 2012). Inokulasi bakteri Staphylococcus aureus
dengan dosis 5 x 107 sampai 5 x 108 dapat menyebabkan mencit mengalami
infeksi dan memiliki potensi mengalami syok septik dan mematikan dalam waktu
12-48 jam. Sedangkan dalam waktu 2-3 jam mencit telah menunjukkan gejala
klinis antara lain mengacak-acak bulu, aktivitas dan nafsu makan mulai berkurang,

46
postur membungkuk, diare, dehidrasi hingga pernafasan yang tidak teratur (Kim,
2014).
Uji konfirmasi yang telah dilakukan oleh peneliti pada tanggal 3-29 Maret
2017 dengan menginokulasi bakteri Staphylococcus aureus pada 3 kelompok
mencit nifas yaitu pembedahan 1 jam (K1), pembedahan 2 jam (K2) dan
pembedahan 4 jam (K3) lalu diambil darah jantung untuk diukur jumlah leukosit
dan mengambil organ untuk menghitung koloni bakteri di beberapa organ seperti
uterus, limpa, ovarium, dan hati. Hasil yang didapatkan adalah terjadi peningkatan
jumlah leukosit diatas normal pada kelompok 2 dan 3 dengan jumlah leukosit
antara 13.000-19.000 sel/µl. Jumlah leukosit normal pada mencit berkisar antara
5.100-11.600 sel/µl (Saputri, 2006). Jumlah leukosit yang meningkat menunjukkan
adanya infeksi, inflamasi, nekrosis jaringan ataupun neoplasia leukemik, pada
sepsis biasanya jumlah leukosit sangat tinggi (Atmadja, 2016).