5 BAB II TINJAUAN PUSTAKA 2.1 Anatomi Fisiologi Pankreas
-
Upload
khangminh22 -
Category
Documents
-
view
2 -
download
0
Transcript of 5 BAB II TINJAUAN PUSTAKA 2.1 Anatomi Fisiologi Pankreas
5
BAB II
TINJAUAN PUSTAKA
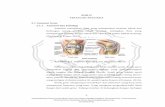
2.1 Anatomi Fisiologi Pankreas
Pankreas memiliki struktur seperti kelejar ludah. Pada manusia dewasa yang
normal dan sehat, pankreas memiliki berat sekitar 100 g, dengan panjang 14 sampai
25 cm, volume sekitar 72,4 ± 25,8 cm3 dan berbentuk lobular dan bentuknya
memanjang (Longnecker, dkk, 2018). Pankreas terdiri dari tiga bagian yaitu,
kepala, badan, dan ekor pankreas. Kepala pankreas terletak di sebelah kanan rongga
abdomen, di dalam lekukan duodenum yang melingkarinya. Badan pankreas
terletak di belakang lambung dan di depan vertebra lumbalis. Ekor pankreas
berbentuk runcing disebelah kiri menyentuh limpa. Pada pankreas juga terdapat
kepulauan langerhans yang membentuk organ endokrin untuk mengekresikan
insulin, yaitu sebuah hormon antidiabetik yang diberikan dalam pengobatan
diabetes. Pankreas endokrin terdiri dari gugus sel kecil yang disebut pulau
Langerhans, mengandung beberapa sel endokrin, yaitu sel α penghasil glukagon,
sel β penghasil insulin, sel δ penghasil somatostatin, dan sel PP penghasil
polipeptida pankreas (Pearce, 2019).
Gambar 2. 1 Anatomi Fisiologi Pankreas (Atkinson, 2020)
6
Sel β terletak di pulau kecil langerhans, yang tersebar di dalam eksokrin
pankreas. Setiap pulau mengandung 1000 sel β bersama dengan sel endokrin lain
seperti sel alfa, sel delta, sel polipeptida pankreas (PP) dan sel epsilon, dan total 1
juta pulau ada di pankreas. Massa sel β mengacu pada massa total sel β sekitar 1 g
pada manusia. Sel β pankreas berperan memproduksi hormon insulin (70% dari
pulau Pankreas). Apabila sel β rusak maka sel β tidak dapat memproduksi insulin.
Akibatnya, sel tubuh tidak dapat mengambil glukosa, dan kadar glukosa darah naik
terlalu tinggi. DM tipe 2 disebabkan oleh disfungsi sel β semakin memburuk dengan
durasi penyakit. Disfungsi sel β dikaitkan dengan memburuknya glikemik
kegagalan kontrol dan pengobatan, sehingga penting untuk mempertahankan atau
memulihkan massa fungsional sel β di pengelolaan DM tipe 2 (Saisho, 2015).
Insulin adalah sebuah protein yang dapat dicernakan oleh enzim pencerna
protein, maka tidak diberikan melalui mulut tetapi dengan suntikan subkutan.
Insulin dapat mengendalikan kadar glukosa didalam tubuh seperti pada diabetes
melitus akan memperbaiki kemampuan sel tubuh mengabsorpsi dan menggunakan
glukosa dan lemak (Pearce, 2019). Gula dalam darah atau glukosa merupakan
energi utama bagi sel tubuh bagian otot dan jaringan. Glukosa berasal dari makanan
dan diproduksi oleh hati. Gula dari makanan yang masuk dari mulut akan dicerna
dilambung dan diserap oleh usus, kemudian masuk ke dalam aliran darah. Gula
membutuhkan insulin dalam menjalankan fungsinya. Hormon insulin diproduksi
oleh sel β di pulau langerhans dalam pankreas. Setiap makanan yang masuk ke
dalam tubuh kita, pankreas memberi respon dengan mengeluarkan insulin ke dalam
aliran darah. Insulin bekerja membuka jalan agar gula dapat masuk ke dalam sel,
sehingga kadar glukosa menjadi turun (Tandra, 2017).
Selain tempat pusat memproduksi gula, hati merupakan tempat
penyimpanan gula. Ketika kadar insulin meningkat, maka hati akan menimbun
glukosa dari makanan yang masuk kedalam tubuh, dan akan dialirkan ke sel-sel
tubuh jika telah dibutuhkan. Timbunan gula di dalam hati atau disebut glikogen
akan diubah kembali menjadi glukosa dan dikeluarkan ke aliran darah menuju sel-
sel tubuh, jika insulin dalam darah rendah karena tidak makan atau kondisi lapar.
Sel alfa yang berada di dalam pankreas, berfungsi memproduksi hormon glukagon.
Apabila kadar gula darah rendah, maka glukagon akan merangsang hati untuk
7
memecah glikogen menjadi glukosa. Tubuh kita juga mempunyai hormon yang
fungsinya berlawanan dengan insulin, seperti glukagon, epinefrin atau adrenalin,
dan kortisol atau hormon steroid. Hormon tersebut berkerja memacu hati agar
mengeluarkan glukosa, sehingga gula darah naik (Tandra, 2017).
Pasien diabetes mengalami gangguan keseimbangan gula yang disimpan di
hati dan transportasi gula. Oleh karena itu, kadar gula darah meningkat kemudian
diekskresikan melalui urine, sehingga urine lebih banyak dan mengandung gula.
Hal ini terjadi, karena pankreas tidak mampu memproduksi insulin dan sel tidak
memeri respon pada kerja insulin sebagai pembuka jalan agar gula dapat masuk ke
dalam sel, sehingga kadar gula dalam darah menjadi turun (Tandra, 2017).
2.2 Definisi Diabetes Melitus
Diabetes melitus menjadi salah satu ancaman kesehatan global. Jumlah
kasus dan prevalensi diabetes melitus terus meningkat beberapa waktu terakhir.
Diabetes merupakan salah satu penyakit kronis serius karena pankreas tidak dapat
menghasilkan insulin yang mengatur gula darah atau glukosa, sehingga terjadi
peningkatan glukosa dalam darah. Semua jenis diabetes dapat menyebabkan
komplikasi di bagian tubuh manapun dan dapat meningkatkan risiko kematian dini
(WHO, 2016). Satu diantara 2 orang terkena diabetes belum terdiagnosis, hal ini
membuat mereka rentan mengalami komplikasi akibat diabetes, menyebabkan
kecacatan substansial, kematian dini atau premature (Kemenkes RI, 2016).
Diabetes melitus merupakan salah satu penyakit gangguan metabolik dalam
tubuh dengan gejala hiperglikemia akut maupun kronik yang ditandai dengan tidak
normalnya metabolisme karbohidrat, lemak, dan protein. Diabetes melitus
disebabkan adanya kelainan sekresi insulin, kelainan kerja insulin ataupun
keduanya, dan menyebabkan komplikasi kronis mikrovaskular, makrovaskular dan
neuropati (Dipiro et al, 2016). Terdapat beberapa faktor lainnya seperti faktor
genetik, faktor usia, faktor gaya hidup dan pola makan (Perkeni, 2015).
2.3 Epidemiologi Diabetes Melitus
Word Health Organitation menyebutkan, bahwa pada tahun 2016 sebanyak
1,6 juta kematian disebabkan oleh diabetes. Diabetes merupakan penyebab 70%
8
dari total kematian didunia (WHO, 2016). Menurut International Diabetes
Federation (IDF) sekitar 463 juta orang dewasa berumur 20-79 tahun menderita
diabetes, jumlah ini diperkirakan akan meningkat menjadi 700 juta pada tahun
2045. Pada tahun 2015 di tingkat global diperkirakan setengah dari pasien diabetes
dewasa sekitar 193 juta orang tidak mengetahui bahwa mereka pasien diabetes,
dimana hampir seluruhnya merupakan kasus diabetes tipe 2. Jumlah kematian
penyebab diabetes mencapai 4,2 juta. Tiogkok, India, Amerika Serikat, Pakistan,
Brazil, Meksiko, Indonesia, Jerman, Mesir, dan Bangladesh merupakan 10 negara
dengan jumlah pasien diabetes orang dewasa berumur 20-79 tahun tertinggi di
dunia. Prevalensi diabetes di Indonesia cenderung meningkat. Indonesia berada di
peringkat ketujuh dengan jumlah 10,7 juta orang (IDF, 2019).
Jumlah pasien diabetes melitus tipe 2 di Indonesia diperkirakan mengalami
kenaikan pada tahun 2000 berjumlah 8,4 juta menjadi 21,3 juta pada tahun 2030.
IDF memprediksikan terjadi kenaikan jumlah pasien diabetes melitus pada tahun
2013-2017 sebanyak 10,3 juta menjadi 16,7 juta pada tahun 2045 (IDF, 2019).
Kasus diabetes yang terkonfirmasi di Indonesia pada tahun 2019 mencapai
3.941.698 pasien. Provinsi Jawa Timur berada peringkat pertama sebanyak 844.018
pasien, diikuti dengan Provinsi Jawa Barat sebanyak 552.151 pasien, dan Provinsi
Riau sebanyak 501.921 pasien (Kemenkes RI, 2019).
Hasil riset kesehatan dasar menunjukkan peningkatan prevalensi dari 6,9%
pada tahun 2013 menjadi 8,5% pada tahun 2018. Prevalensi diabetes paling tinggi
berada di Kota Madiun dengan 4,22%, sedangkan Kota Malang dengan 2,4%
berada di urutan ke 13 dari 38 kabupaten/kota di Jawa Timur (Riskesdas, 2018).
Dilihat dari data dinas kesehatan Malang tahun 2015 tercatat pasien diabetes
melitus sebanyak 27.930 pasien di wilayah Malang, pasien baru sebanyak 5.905
pasien dan pasien lama sebanyak 22.025 pasien (Dinkes Malang, 2015).
2.4 Klasifikasi Diabetes Melitus
Penyakit diabetes melitus diklasifikasikan menjadi 4 yaitu diabetes tipe 1,
diabetes tipe 2, diabetes gestasional, dan diabetes tipe lainnya. Diabetes melitus
merupakan penyakit yang tidak ada tanda-tanda atau gejala yang terlihat, hal ini
9
mengakibatkan banyak pasien masuk RS dengan diagnosa penyakit kronis disertai
komplikasi (ADA, 2018).
2.4.1 Diabetes Melitus tipe 1
Diabetes melitus tipe 1 terjadi akibat tidak terkontrolnya gula darah di dalam
tubuh karena adanya kerusakan sel beta pankreas sehingga berkurangnya produksi
insulin. Pada DM tipe ini terdapat sedikit atau tidak sama sekali sekresi insulin,
sehingga gula menjadi menumpuk dalam peredaran darah karena tidak dapat
diangkut ke dalam sel. Manifestasi klinik pertama dari penyakit ini adalah
ketoasidosis (ADA, 2018). DM tipe 1 ini banyak terjadi pada pasien anak dengan
rentang usia 5-6 tahun dan sampai 12 tahun. Perlu diketahui lebih dari setengah
persen penderita baru tipe 1 berusia >19 tahun (World Diabetes Foundation, 2015)
Diabetes melitus tipe 1 biasanya merupakan penyakit autoimun, dimana
terdapat gangguan sistem imun yang mengakibatkan kerusakan sel β pankreas.
Rusaknya sel pankreas ini juga terjadi karena adanya pengaruh genetik atau
keturunan, infeksi virus, dan malnutrisi. Penyakit ini biasanya terjadi pada usia
muda seperti anak-anak atau remaja baik pria maupun wanita, namun saat ini juga
ditemukan pada usia tua. Diabetes melitus tipe 1 disebut juga insulin-dependent
diabetes. Diabetes melitus tipe ini sangat bergantung dengan insulin, dimana pasien
memerlukan suntikan insulin setiap hari untuk memenuhi kebutuhan insulin di
dalam tubuhnya (Tandra, 2017).
2.4.2 Diabetes Melitus tipe 2
Diabetes melitus tipe 2 ditandai dengan sekresi hormon insulin dan produksi
glukosa darah secara berlebihan. Hal ini disebabkan ketidakmampuan sel target
insulin dalam merespon hormon insulin secara normal sehingga gula darah tidak
dapat masuk ke dalam sel. Gejala DM tipe ini secara perlahan-lahan bahkan tidak
terlihat. Dengan pola hidup sehat, yaitu mengonsumsi makanan bergizi seimbang
dan olah raga secara teratur biasanya pasien brangsur pulih. Pasien juga harus
mampu mepertahannkan berat badan yang normal. Namun pada penerita stadium
akhir kemungkinan akan diberikan suntik insulin (ADA, 2018).
Pada diabetes melitus tipe 2, pankreas masih bisa membuat insulin, namun
insulinnya tidak dapat berfungsi dengan baik. Pasien tidak perlu tambahan suntikan
insulin dalam pengobatannya, tetapi memerlukan obat yang dapat memperbaiki
10
fungsi kerja insulin dalam menurunkan gula dan memperbaiki pengolahan gula di
dalam hati. Pada pasien diabetes melitus tipe 2 yang obesitas, terjadi ketidakpekaan
atau resisten terhadap insulin pada sel-sel jaringan tubuh dan otot, sehingga gula
tidak dapat masuk ke dalam sel dan tertimbun di peredaran darah (Tandra, 2017).
Diabetes melitus tipe 2 sering terjadi pada usia 40 tahun, namun prevalensinya tiap
tahun mengalami peningkatan. Saat ini ditemukan pasien diabetes melitus berusia
remaja dan dewasa yang dipicu oleh gaya hidup tidak sehat, kurang olahraga atau
aktivitas fisik, sering makan yang manis-manis, dan meningkatnya jumlah obesitas
(Nair & Peate, 2015).
2.4.3 Diabetes Melitus Gestasional
Diabetes melitus gestasional terjadi selama masa kehamilan, seorang ibu
hamil memutuhkan insulin lebih banyak untuk mempertahankan metabolisme
karohidrat secara normal. Hal ini terjadi, karena adanya pembentukan hormon pada
ibu hamil yang menyebabkan resistensi insulin. Diabetes melitus tipe ini ditandai
dengan intoleransi glukosa, pertama kali pada masa kehamilan yang terjadi
trimester kedua atau ketiga kehamilan, hal ini disebabkan ketidakmampuan tubuh
dalam memproduksi insulin lebih banyak. Diabetes melitus gestasional
berhubungan dengan meningkatnya komplikasi perinatal. Pasien diabetes melitus
gestasional memiliki risiko lebih besar menderita diabetes melitus tipe 2 setelah
melahirkan. Wanita yang didiagnosis diabetes melitus gestational harus menerima
skrining seumur hidup untuk pradiabetes dan diabetes tipe 2 (ADA, 2018).
2.4.4 Diabetes Melitus Tipe Lain
Diabetes melitus tipe lain terjadi akibat penyakit lain yang dapat
mengganggu produksi insuin atau mempengaruhi kerja insulin yaitu berupa
munculnya gangguan genetik fungsi sel beta, kerja insulin yang terganggu,
gangguan eksokrin pankreas, infeksi, endokrinopati, sebab imunologi yang jarang
dan sindroma genetik lainnya yang kadang dihubungkan dengan diabetes melitus.
Diabetes tipe ini dapat dipicu oleh obat atau bahan kimia seperti dalam pengobatan
HIV/AIDS atau setelah transplantasi organ (ADA, 2018). Penyebab diabetes ini
yaitu, radang pankreas, gangguan kelenjar adrenal atau hipofisis, penggunaan
hormon kortikosteroid, pemakaian beberapa obat antihipertensi atau antikolesterol,
malnutrisi, dan infeksi (Tandra, 2017).
11
2.5 Etiologi dan Faktor Risiko Diabetes Melitus
Diabetes melitus ditandai hiperglikemia kronis yang mempengaruhi
metabolisme karbohidrat, protein, dan lemak. Hiperglikemia pada diabetes melitus
dapat tidak terdeteksi karena bersifat asimptomatik atau tidak ada gejala yang pasti
dan menyebabkan kerusakan vaskular sebelum penyakit terdeteksi (Gabriellyn,
2016). Naiknya kadar gula darah pada diabetes melitus karena pankreas tidak
berfungsi dengan baik menyebabkan kurangnya sekresi insulin. Kurangnya hormon
insulin menyebabkan gangguan metabolisme karbohidrat, protein, dan lemak.
Diabetes melitus berhubungan dengan kerusakan jangka panjang, disfungsi
beberapa organ tubuh, seperti mata, ginjal, saraf, jantung dan pembuluh darah
(ADA, 2018). Beberapa hormon yang bekerja sebagai antagonis insulin dapat
menyebabkan terkena diabetes (Putra & Berawi, 2015).
Diabetes melitus tipe 1 biasanya terjadi pada masa anak-anak sebagai
bentuk hiperglikemia kronis yang disebabkan oleh kerusakan imunologis atau
autoimun sel beta pankreas karena faktor genetik. Sedangkan diabetes melitus tipe
2 merupakan bentuk hiperglikemia kronis yang disebabkan oleh meningkatnya
resistensi insulin dan berkurangnya kapasitas sekresi insulin. Diabetes melitus tipe
2 biasanya muncul pada usia dewasa, namun saat ini sering dikaitkan dengan
obesitas, gaya hidup, dan pola makan sehingga juga dapat terjadi pada anak-anak
dan remaja dan kejadian meningkat secara drastis (Katzung, 2018).
Diabetes melitus gestasional ini terjadi ketika nilai glukosa darah di atas
normal pada masa kehamilan. Wanita dengan diabetes melitus gestasional berisiko
terkena diabetes tipe 2 dan beberapa mengalami komplikasi selama kehamilan dan
persalinan (WHO, 2016). Diabetes tipe lain disebabkan karena penyebab dari
penyakit lain, misalnya cacat genetik pada fungsi sel β, cacat genetik pada kerja
insulin, penyakit eksokrin pankreas seperti fibrosis kistik serta dampak penyakit
dan obat-obatan kimia (ADA, 2018). Menurut Tandra 2017 terdapat faktor risiko
diabetes melitus yaitu:
2.5.1 Genetik
Pada faktor genetik / keturunan dapat dilihat bahwa pasien diabetes tipe 2
lebih banyak dibandingkan diabetes tipe 1. Sekitar 50% pasien diabetes tipe 2
merupakan turunan dari orang tuanya, dan lebih dari sepertiga dari saudaranya,
12
namun jika mempunyai saudara kembar maka kemungkinan terkena diabetes
sebesar 90%. Pada diabetes tipe 1 kemungkinan terkena diabetes sebesar 3-5%
apabila orang tua dan saudaranya terkena diabetes, namun jika mempunyai saudara
kembar kemungkinan terkena diabetes sebesar 35-40%. Menurut para ahli riabetes
merupakan penyakit yang berhubungan dengan kromosom seks, kemungkinan
besar penderitanya laki-laki. Sedangkan perempuan sebagai pembawa gen yang
dapat diturunkan kepada anaknya
2.5.2 Ras atau Etnis
Suku Indian di Amerika, Hispanik, dan orang Amerika di Afrika,
merupakan beberapa ras yang mempunyai resiko lebih besar terkena diabetes tipe
2. Orang-orang yang berkulit hitam terutama wanita lebih mudah terkena diabetes
daripada yang berkulit putih.
2.5.3 Obesitas
Obesitas sangat berkaitan dengan diabetes tipe 2, hal ini disebabkan karena
semakin banyak jaringan lemak, jaringan tubuh, dan otot yang resisten terhadap
insulin. Apabila kelebihan berat badan terkumpul di daerah perut, maka lemak akan
menutup kerja insulin agar gula tida dapat masuk ke dalam sel dan menumpuk di
peredaran darah. Menurunkan berat badan dengan merubah gaya hidup dan
berolahraga rutin akan membuat kadar gula darah kembali seimbang.
2.5.4 Pola Hidup / Kurangnya Aktivitas Tubuh
Pada kalangan masyarakat dikenal dengan males gerak. Semakin
berkurangnya aktivitas tubuh maka semakin mudah terkena diabetes. Apabila
kurang bergerak, maka masa otot berkurang sehingga gula darah tidak dipakai dan
menumpuk. Olahraga atau melakukan aktivitas fisik sangat diperlukan untuk
mengontrol berat badan, sehingga gula darah dibakar menjadi energi dan sel tubuh
lebih peka terhadap insulin.
2.5.5 Pola Makan
Pola makan yang berlebihan, jumlah kalori yang tidak terkontrol masuk ke
dalam tubuh, komsumsi makanan cepat saji, tinggi lemak, garam, gula dapat
membuat kadar glukosa dalam darah meningkat.
13
2.5.6 Metabolik Sindrom
Metabolik sindrom banyak ditemukan pada masyarakat saat ini. Gaya hidup
yang kurang banyak gerak dan makan yang berlebihan membuat semakin tinggi
risiko terkena diabetes. Hal ini disebabkan karena pada orang gemuk mempunyai
kandungan gula dan lemak yang tinggi di dalam darahnya.
2.5.7 Penyakit Lain dan Infeksi
Penyakit lain mudah terkena diabetes seperti pembuluh darah perifer,
hipertensi, radang sendi akibat asam urat dalam darah, jantung koroner, stroke,
infeksi kulit berulang cenderung diikuti dengan kadar gula yang tinggi. Pada anak-
anak diabetes tipe 1 disebabkan oleh infeksi virus, seperti campak, mumps,
coxsackie yang membuat sel pankreas rusak.
2.5.8 Usia
Seiring bertambahnya usia terutama pada usia 40 tahun keatas lebih berisiko
terkena diabetes melitus. Bertambahnya usia membuat penurunan fungsi kerja
tubuh terutama pada pankreas sebagai penghasil insulin, dan kurangnya
menggerakkan badan sehingga berat badan bertambah. Namun saat ini pada usia
muda seperti anak-anak dan remaja banyak terkena diabetes melitus tipe 2.
2.5.9 Stress
Cedera, infeksi berat, trauma hebat, operasi besar, penyakit berat lainnya,
dan adanya masalah dalam kehidupan dapat memicu terjadinya stress. Tubuh secara
alami akan merespon dengan banyak mengeluarkan hormon stress.
2.5.10 Riwayat Diabetes Pada Kehamilan
Pada ibu hamil harus diperiksa gula darahnya, biasanya diabetes hilang
setelah melahirkan. Namun juga terdapat ibu yang terkena diabetes tipe 2
dikemudian hari. Hal ini terjadi apabila ibu hamil melahirkan bayi berukuran besar
dengan berat badan lebih 4 kg, riwayat lahir mati atau melahirkan bayi dengan
kelainan bawaan, dan kelebihan glukosa dalam urin selama kehamilan.
2.5.11 Pemakaian Obat-obatan
Terdapat beberapa obaat yang dapat menyebabkan diabetes dengan
menaikkan kadar gula darah. Obat-obatan seperti hormon steroid, beberapa obat
antihipertensi, dan oat menurunkan kolesterol. Apabila berisiko terkena diabetes,
berhati-hati dalam menggunakan obat tersebut.
14
2.6 Manifestasi Klinis Diabetes Melitus
Gejala diabetes melitus dibedakan menjadi akut dan kronik. Gejala akut
diabetes melitus yaitu : poliphagia (banyak makan), polidipsia (banyak minum),
poliuria (banyak kencing/sering kencing di malam hari), nafsu makan bertambah
namun berat badan turun dengan cepat (5-10 kg dalam waktu 2-4 minggu), dan
mudah lelah. Gejala kronik diabetes melitus yaitu : Kesemutan, kulit terasa panas
atau seperti tertusuk tusuk jarum, rasa kebas di kulit, kram, kelelahan, mudah
mengantuk, pandangan mulai kabur, gigi mudah goyah dan mudah lepas,
kemampuan seksual menurun bahkan pada pria bisa terjadi impotensi, pada ibu
hamil sering terjadi keguguran atau kematian janin dalam kandungan atau dengan
bayi berat lahir lebih dari 4kg (Fatimah, 2015).
Tidak semua orang dapat merasakan adanya perbedaan pada bagian
tubuhnya. Banyak orang merasa cemas saat mengetahui mengidap penyakit
diabetes melitus. Hal ini disebabkan karena gejala yang bervariasi tergantung organ
mana yang terkena dan gejala berjalan secara lambat sampai tidak terasa. Tidak
sedikit orang yang mengetahui dirinya mengidap diabetes melitus, dan saat periksa
ke dokter telah mengalami komplikasi.Terdapat dua gejala utama yang harus
diketahui, yaitu sering kencing dan banyak, juga merasa sangat haus. Menurut
Tandra (2017) gejala diabetes yaitu :
2.6.1 Banyak Mengeluarkan Urin dan Rasa Haus
Banyak mengeluarkan urin dan rasa haus merupakan gejala umum bagi
pasien diabetes melitus. Kadar gula darah yang tinggi akan membuat ginjal tidak
dapat menyerap kembali kelebihan gula di dalam darah. Gula akan menarik air
keluar melalui urin, sehingga ginjal sering kali banyak mengeluarkan urin. Akibat
banyak mengeluarkan urin yang mengandung gula, sehingga terjadi dehidrasi yang
membuat rasa haus berlebihan. Untuk mengatasi dehidirasi tersebut, diharapkan
untuk minum yang banyak tetapi tidak minuman yang manis.
2.6.2 Berat Badan Turun
Penurunan berat badan terjadi karena adanya metabolisme yang terganggu.
Terganggunya metabolisme membuat gagalnya proses pembentukan energi. Otot
tidak mempunyai cukup gula untuk tumbuh dan mendapatkan energi, sehingga
jaringan otot dan lemak harus di pecah untuk memenuhi energi yang dibutuhkan.
15
2.6.3 Timbul Rasa Lapar dan Lemas
Kadar gula yang tinggi membuat penyimpanan gula di dalam tubuh sedikit,
karena pada pasien diabetes melitus gula menumpuk dalam peredaran darah. Hal
ini terjadi karena insulin tidak mampu menyalurkan gula ke dalam sel untuk
menjadi energi, sehingga tubuh menjadi merasa mudah letih, flu, capek, dan lemas.
Akibat gula tidak masuk ke dalam sel, maka akan timbul rasa lapar karena tidak ada
energi.
2.6.4 Mata Kabur
Mata akan mengalami kesulitan untuk fokus, sehingga pandangan kabur.
Hal ini disebabkan gula darah yang tinggi menarik cairan yang berada di dalam
lensa mata sehingga lensa menjadi tipis. Diharapkan pasien diabetes melitus dapat
mengontrol gula darah agar tetap normal, sehingga pengelihatan normal kembali.
2.6.5 Luka Sukar Sembuh
Luka yang sukar sembuh disebabkan oleh infeksi yang hebat akibat kuman,
jamur yang tumbuh saat gula darah tinggi, terjadi kerusakan dinding pada pembuluh
darah sehingga aliran darah tidak lancar, dan adanya kerusakan saraf atau luka yang
tidak terasa hingga membusuk.
2.6.6 Rasa Kesemutan
Kerusakan saraf akibat kadar gula yang tinggi dapat merusak dinding
pembuluh darah yang akan mengganggu nutrisi pada saraf, sehingga membuat rasa
kesemutan, nyeri, rasa terbakar pada anggota tubuh seperti tangan dan kaki.
2.6.7 Mudah Terkena Infeksi
Ketika gula darah tinggi rongga mulut tidak mampu melawan infeksi,
sehingga gusi menjadi bengkak dan merah, gigi terlihat tidak rata dan mudah
goyang. Leukosit tidak berfungsi dengan baik dalam melawan infeksi, sehingga
kulit mudah terkena infeksi terasa kering dan gatal. Infeksi jamur juga menyerang
kemaluan, seperti pada vagina yang mengeluarkan cairan kental putih kekuningan
disertai rasa gatal.
2.7 Patogenesis Diabetes Melitus
Menurut Schwatrz (2016) patogenesis hiperglikemia disebabkan oleh sebelas
hal yaitu :
16
Gambar 2. 2 Patogenesis DM (Schwatrz, 2016)
1. Kegagalan sel beta pankreas
Fungsi sel beta pada DM tipe 2 sangat berkurang. Obat anti diabetik yang diberikan
dan dikonsumsi adalah sulfonilurea, meglitinid, agonis glucagon-like peptide
(GLP-1) dan penghambat dipeptidil peptidase-4 (DPP- 4).
2. Disfungsi sel alfa pankreas
Sel alfa berfungsi untuk mempadukan glukagon, dalam kondisi puasa
kadarnya di dalam plasma akan meningkat. Peningkatan ini menyebabkan
pembentukan glukosa hati dalam kondisi basal meningkat secara bermakna
dibandingkan individu yang normal. Obat untuk membantu menghambat sekresi
glukagon atau menghambat reseptor glukagon yaitu agonis GLP-1, penghambat
DPP-4 dan amilin.
3. Sel lemak
Sel lemak yang kebal terhadap efek antilipolisis dari insulin, menyebabkan
terjadinya peningkatan proses lipolisis dan kadar asam lemak bebas dalam plasma.
Peningkatan FFA akan merangsang proses glukoneogenesis, dan mencetuskan
kekebalan insulin di hepar dan otot, sehingga mengganggu sekresi insulin.
Gangguan yang disebabkan oleh FFA ini disebut dengan lipotoksisitas. Obat yang
diberikan dan dikonsumsi adalah tiazolidinedion.
17
4. Otot
Pada DM tipe 2 terjadi gangguan kinerja insulin yang multipel di
intramioselular dikarenakan adanya gangguan fosforilasi tirosin, sehingga
terjadilah gangguan transport glukosa pada sel otot, penurunan sintesis glikogen,
dan penurunan oksidasi glukosa. Obat yang diberikan dan dikonsumsi adalah
metformin dan tiazolidinedion.
5. Hepar
Pada DM tipe 2 terjadi kekebalan insulin yang berat dan merangsang
pembentukan proses glukoneogenesis sehingga produksi glukosa dalam kondisi
basal oleh hepar mengalami peningkatan. Obat yang menekan proses
glukoneogenesis adalah metformin.
6. Otak
Insulin merupakan pemicu nafsu makan yang kuat. Pada individu yang
obesitas baik yang DM maupun tidak, didapatkan hiperinsulinemia yang
merupakan mekanisme kompensasi dari kekebalan insulin. Pada golongan ini
asupan makanan justru meningkat akibat adanya kekebalan insulin yang juga terjadi
di otak. Obat yang diberikan yaitu agonis GLP-1, amilin dan bromokriptin.
7. Kolon/Mikrobiota
Perubahan komposisi mikrobiota pada kolon berkontribusi dalam keadaan
hiperglikemia. Mikrobiota usus terbukti berhubungan dengan DM tipe 1, DM tipe
2, dan obesitas sehingga menjelaskan bahwa hanya sebagian dari individu yang
mempunyai berat badan berlebih yang akan berkembang DM. Probiotik dan
prebiotik diperkirakan sebagai mediator untuk menangani keadaan hiperglikemia.
8. Usus halus
Glukosa yang ditelan memicu respons insulin jauh lebih besar dibandingkan
dengan apabila diberikan secara intravena. Efek yang dikenal sebagai efek inkretin
ini diperankan oleh 2 hormon yaitu glucagon-like polypeptide-1 (GLP-1) dan
glucose-dependent insulinotrophic polypeptide atau disebut juga gastric inhibitory
polypeptide (GIP). Pada penyandang DM tipe 2 didapati bahwa ada defisiensi GLP-
1 dan kebal terhadap hormon GIP. Hormon inkretin juga segera dipecah oleh
keberadaan enzim DPP-4, sehingga otomatis hanya bekerja dalam beberapa menit.
18
Obat yang bekerja menghambat kinerja DPP-4 adalah DPP-4 inhibitor. Saluran
pencernaan juga mempunyai peran dalam penyerapan karbohidrat melalui kinerja
enzim alfa glukosidase yang akan memecah polisakarida menjadi monosakarida,
kemudian diserap oleh usus sehingga berakibat pada peningkatkan glukosa darah
setelah makan. Obat yang bekerja untuk menghambat kinerja enzim alfa
glukosidase adalah acarbosa.
9. Ginjal
Ginjal memfiltrasi sekitar 163 gram glukosa sehari. Sembilan puluh persen
dari glukosa terfiltrasi ini akan diserap kembali melalui peran enzim sodium glucose
co-transporter (SGLT-2) pada bagian convulated tubulus proksimal, dan 10%
sisanya akan diabsorbsi melalui peran SGLT-1 pada tubulus desenden dan asenden,
sehingga akhirnya tidak ada glukosa dalam urin. Pada kasus DM disini terjadilah
peningkatan ekspresi gen SGLT-2, sehingga terjadi peningkatan reabsorbsi glukosa
di dalam tubulus ginjal dan mengakibatkan peningkatan kadar glukosa darah. Obat
yang menghambat kinerja SGLT-2 ini akan menghambat reabsorbsi kembali
glukosa di tubulus ginjal sehingga glukosa akan dikeluarkan lewat urin. Obat yang
bekerja di kondisi ini adalah penghambat SGLT-2 seperti dapaglifozin,
empaglifozin dan canaglifozin.
10. Lambung
Pada lambung pasien diabetes terjadi penurunan produksi amilin yang
diakibatkan oleh dampak kerusakan sel beta pankreas. Kadar amilin yang menurun
menyebabkan percepatan pengosongan lambung dan peningkatan absorpsi glukosa
di usus halus, yang berhubungan dengan peningkatan kadar glukosa postprandial.
11. Sistem Imun
Sitokin menginduksi respons fase akut (inflamasi derajat rendah, bagian
dari aktivasi sistem imun bawaan/innate) yang berhubungan kuat dengan
patogenesis DM tipe 2 dan berkaitan dengan komplikasi seperti dislipidemia dan
aterosklerosis. Inflamasi sistemik derajat rendah berperan dalam induksi stres pada
endoplasma akibat peningkatan kebutuhan metabolisme untuk insulin. DM tipe 2
ditandai dengan resistensi insulin perifer dan penurunan produksi insulin, serta
disertai dengan inflamasi kronik derajat rendah pada jaringan perifer seperti
adiposa, hepar dan otot.
19
2.8 Patofisiologi Diabetes Melitus
2.8.1 Diabetes tipe 1
DM Tipe 1 diyakini dimulai dengan paparan pemicu lingkungan secara
genetik individu rentan. Ada hubungan antara genetik yang saat ini diketahui untuk
autoimunitas dan pengembangan DM tipe 1. Faktor risiko genetik dan lingkungan
berdampak pada peradangan, autoimunitas, dan stres metabolik. Keadaan ini
mempengaruhi jumlah dan fungsi sel β sehingga kadar insulin pada akhirnya tidak
dapat merespons secara baik terhadap permintaan insulin. Kerusakan dan disfungsi
sel β yang menyebabkan hiperglikemia dan masuk dalam kategori diabetes. Dalam
beberapa kasus, faktor risiko genetik dan lingkungan serta interaksi gen dan
lingkungan dapat secara langsung memengaruhi massa dan fungsi sel β. Kadar
glukosa darah yang tinggi kronis berhubungan dengan komplikasi mikrovaskuler
dan makrovaskular yang meningkatkan morbiditas dan mortalitas pada penderita
diabetes (Skyler, et al, 2017).
Gambar 2. 3 Patofisiologi DM Tipe 1 (Skyler et al, 2017)
Individu yang rentan secara genetik harus terkena pemicu yang memulai
proses autoimun dan penghancuran pankreas sel β. Proses autoimun dimediasi oleh
makrofag dan limfosit T dengan beredarnya autoantibodi ke berbagai antigen sel β
tunggal. Antibodi yang terdeteksi terkait dengan DM tipe 1 adalah autoantibodi sel
islet (ICAs). Antibodi lain dapat dibentuk untuk insulin, asam glutamat
decarboxylase 65 (GAD65), antigen-2 terkait insulinoma (IA-2), dan pengangkut
20
seng 8 (ZnT8). Antibodi ini umumnya dianggap sebagai penanda penyakit mediator
sel β. Penanda ini digunakan untuk mengidentifikasi risiko DM tipe 1 dan
merupakan tes penyaringan untuk memulai strategi pencegahan penyakit.
Gangguan autoimun lainnya seperti hashimoto tiroiditis, penyakit graves, penyakit
addison, vitiligo, dan celiac sprue lebih umum pada pasien dengan tipe 1 DM
(Dipiro et al, 2020).
2.8.2 Diabetes Tipe 2
Gambar 2. 4 Patofisiologi DM tipe 2 (Baynest, 2015)
Pada diabetes tipe 2 terdapat dua penyebab yaitu gangguan sekresi insulin
melalui disfungsi sel β pankreas dan gangguan kerja insulin melalui resistensi
insulin. Resistensi terhadap insulin mendominasi, sehingga massa sel β mengalami
transformasi yang mampu meningkatkan jumlah insulin dan mengkompensasi
permintaan yang berlebihan dan anomali. Secara absolut, konsentrasi insulin
plasma (baik puasa dan stimulasi makan) biasanya meningkat, meskipun “relatif”
terhadap beratnya resistensi insulin, konsentrasi insulin plasma tidak cukup untuk
mempertahankan homeostasis glukosa normal. Resistensi insulin dan
hiperinsulinemia menyebabkan gangguan toleransi glukosa terhadap kerja insulin
akan mengakibatkan gangguan pengambilan glukosa yang dimediasi insulin di
perifer (oleh otot dan lemak), pertahanan yang tidak lengkap dari output glukosa
hati, dan gangguan serapan trigliserida oleh lemak. Untuk mengatasi resistensi
21
insulin, sel pulau kecil akan meningkatkan jumlah insulin yang disekresikan.
Produksi glukosa endogen dipercepat pada pasien diabetes tipe 2 atau glukosa puasa
yang terganggu. Karena peningkatan ini terjadi dengan adanya hiperinsulinemia,
setidaknya pada tahap penyakit awal dan menengah, resistensi insulin hati adalah
pendorong hiperglikemia diabetes tipe 2 (Baynest, 2015).
Diabetes melitus tipe 2 terjadi akibat hasil dari disfungsi sel β ditambah
dengan beberapa tingkat insulin resistensi. Pankreas pada orang dengan fungsi
normal sel β mampu menyesuaikan sekresi insulin untuk mempertahankan kadar
glukosa plasma normal. Innondiabetik, individu obesitas, insulin meningkat secara
proporsional dengan tingkat keparahan resistensi insulin dan glukosa plasma tetap
normal. Sel β tidak dapat mempertahankan cukup sekresi insulin dan secara
paradoks, melepaskan lebih sedikit insulin sebagai kadar glukosa meningkatkan.
Pada pasien dengan diabetes melitus tipe 2, penurunan sekresi insulin postprandial
adalah hasil dari kedua gangguan pankreas sel β dan berkurangnya stimulus dari
hormon usus (Dipiro et al, 2020).
2.9 Diagnosis Diabetes Melitus
Diagnosis diabetes melitus ditegakkan berdasarkan pemeriksaan kadar
glukosa darah. Pemeriksaan glukosa darah yang dianjurkan adalah pemeriksaan
glukosa secara enzimatik dengan bahan plasma darah vena. Hasil pengobatan dapat
dilihat menggunakan glukometer. Diagnosis tidak dapat ditegakkan karena adanya
glukosuria. Kriteria diagnosis gula darah diabetes menurut ADA (2018) :
1. Glukosa darah puasa dengan kadar >126 mg/dl (7,0 mmol/l) puasa didefinisikan
sebagai tidak ada asupan kalori masuk kedalam tubuh dengan maksimal selama
durasi 8 jam.
2. Pada pasien dengan gejala klasik hiperglikemia gula darah acak > 200 mg/dl
(11,1 mmol/l).
3. Glukosa darah 2 jam > 200mg/dl (11.1 mmol/l) selama TTOG (tes toleransi oral
glukosa), asupan glukosa yang direkomendasikan WHO pada tes ini 75 gram
yang dilarutkan di air.
4. Pemeriksaan HbA1c (≥6,5%) dilakukan pada sarana laboratorium yang telah
terstandardisasi (ADA, 2018).
22
Tabel II. 1 Kadar Tes Laboratorium Darah untuk Diagnosis Diabetes dan Pre-
Diabetes (Perkeni, 2019)
HbA1c (%) Glukosa Darah
Puasa (mg/dL)
Glukosa Plasma 2 Jam
Setelah TTGO (mg/dL)
Diabetes ≥6,5 ≥126 ≥200
Pre-diabetes 5,7-6,4 100-125 140-199
Normal <5,7 70-99 70-139
Apabila hasil pemeriksaan tidak memenuhi kriteria normal diabetes melitus,
maka digolongkan ke dalam pre-diabetes kelompok toleransi glukosa terganggu
(TGT) atau glukosa darah puasa terganggu (GDPT). Diagnosis TGT ditegakkan
bila setelah pemeriksaan TTGO didapatkan glukosa plasma 2 jam setelah beban
antara 140–199 mg/dL dengan glukosa plasma puasa < 100 mg/dl. Diagnosis GDPT
ditegakkan bila setelah pemeriksaan glukosa plasma puasa didapatkan antara 100–
125 mg/dL dan pemeriksaan TTGO gula darah 2 jam < 140 mg/dL. Diagnosis pre-
diabetes berdasarkan HbA1c 5,7-6,4% (ADA, 2018).
2.10 Komplikasi Diabetes Melitus
Diabetes melitus apabila tidak tertangani secara benar, maka dapat
mengakibatkan berbagai macam komplikasi. Ada dua komplikasi pada DM yaitu
komplikasi akut dan komplikasi kronik. Komplikasi akut terjadi saat kadar glukosa
darah meningkat atau menurun secara tajam dalam waktu yang singkat. Sedangkan
komplikasi kronik ditandai dengan semakin tinggi kadar glukosa darah akan
menyebabkan gangguan organ di kemudian hari, terdiri dari komplikasi
makrovaskuler dan komplikasi mikrovaskuler (Subiyato, 2019).
2.10.1 Komplikasi Akut Diabetes Melitus
1. Hipoglikemia, adalah kadar glukosa darah seseorang di bawah nilai normal (<
60 mg/dl). Hipoglikemia lebih sering terjadi pada penderita DM tipe 1 yang
dapat dialami 1-2 kali per minggu, kadar gula darah yang terlalu rendah
menyebabkan sel-sel otak tidak mendapat pasokan energi sehingga tidak
berfungsi bahkan dapat mengalami kerusakan (Fatimah, 2015). Gejala yang
timbul yaitu rasa lapar, gemetar, mengeluarkan keringat, berdebar-debar,
pusing, gelisah, tidak sadar dan disertai kejang (Subiyato, 2019).
23
2. Hiperglikemia, adalah apabila kadar gula darah meningkat secara tiba-tiba,
menyebabkan keadaan metabolisme yang berbahaya. Gejala yang timbul rasa
sangat haus, pandangan kabur, muntah, berat badan menurun, sakit kepala,
kulit kering dan gatal, kesadaran menurun, rasa mengantuk, kekurangan cairan
akibat sering kencing (Subiyato, 2019).
3. Ketoasidosis diabetik (KAD) atau koma diabetik merupakan keadaan tubuh
yang sangat kekurangan insulin dan bersifat mendadak akibat infeksi, lupa
suntik insulin, pola makan yang terlalu berlebihan atau bebas dan stres.
Penderita dapat mengalami koma (tidak sadar) akibat otak tidak menerima
darah dalam jumlah yang cukup (Subiyato, 2019).
4. Koma hiperosmolar non ketotik (HONK) yang diakibatkan adanya dehidrasi
berat, tekanan darah yang menurun dan syok tanpa adanya badan keton (hasil
pemecahan asam lemak) dalam urin (Subiyato, 2019).
5. Koma lakto asidosis yang diartikan sebagai keadaan tubuh dengan asam laktat
yang tidak dapat diubah menjadi bikarbonat. Akibatnya, kadar asam laktat
dalam darah meningkat dan seseorang bisa mengalami koma (Subiyato, 2019).
2.10.2 Komplikasi Kronis Diabetes Melitus
1. Komplikasi makrovaskuler merupakan kerusakan pembuluh darah yang
mengirimkan darah ke jantung, otak, dan kaki. Pada umumnya yang
berkembang pada penderita diabetes yaitu trombosit otak (pembekuan darah
pada sebagian otak), mengalami penyakit jantung koroner (PJK), gagal jantung
kongetif, penurunan aliran darah ke kaki (PAD), dan stroke (Fatimah, 2015).
2. Komplikasi mikrovaskuler, terutama terjadi pada penderita diabetes melitus
tipe 1 seperti nefropati (gangguan pada ginjal), diabetik retinopati
(pengelihatan kabur sampai kebutaan), neuropati (mati rasa) pada kaki, dan
amputasi (Fatimah, 2015).
2.11 Penatalaksanaan Terapi Diabetes Melitus
Penatalaksanaan terapi diabetes melitus bertujuan untuk meningkatkan
kualitas hidup pasien dengan mengatur kadar gula darah tetap stabil, mengurangi
gejala yang timbul, mempertahankan rasa nyaman, dan mencegah munculnya
komplikasi. Tujuan akhir pengelolaan diabetes melitus adalah menurunkan
24
morbiditas dan mortalitas diabetes melitus (Decroli, 2019). Tindakan yang
dilakukan seperti mengajarkan mengenai diet diabetes mellitus yang tepat,
menganjurkan kegiatan fisik harian dan rutin, mengontrol berat badan agar tidak
obesitas, berhenti merokok, menganjurkan pasien dan keluarga untuk memantau
kadar glukosa darah secara rutin (Nair & Peate, 2015).
Disamping terapi farmakologis, perlu pelatihan khusus terkait pengetahuan
pasien dalam pemantauan perawatan mandiri terhadap perubahan pola hidup. Kunci
utama dalam penatalaksanaan terapi diabetes melitus adalah menerapkan hidup
sehat dan bersamaan dengan obat antidiabetes secara oral maupun suntikan. Obat
antidiabetes dapat diberikan tunggal maupun kombinasi (Perkeni, 2019)
2.11.1 Terapi Non Farmakologi Diabetes Melitus
1. Edukasi
Pengetahuan merupakan domain yang penting dalam pembentukan tindakan
seseorang. Sebagian besar pengetahuan seseorang diperoleh melalui indra
pendengaran yaitu telinga dan indra penglihatan yaitu mata. Edukasi akan diingat
oleh responden karena melibatkan beberapa panca indera (Lestari, 2015). Edukasi
ini berperan untuk meningkatkan pengetahuan mengenai diabetes melitus serta
meningkatkan keterampilan individu dan keluarga dalam pengelolaan diabetes
melitus secara mandiri (Nuari, 2017). Edukasi pada pasien diabetes sangat penting
sebagai upaya promosi hidup sehat untuk mencapai keberhasilan perubahan pola
hidup sehat. Pengetahuan tentang pemantauan glukosa darah dan tanda gejala
hipoglikemia serta cara mengatasinya penyakit diabetes harus diberikan kepada
pasien. Dalam upaya meningkatkan motivasi pasien diabetes sangat dibutuhkan
peran keluarga dan masyarakat. Materi edukasi terdiri dari dua tingkat, yaitu materi
edukasi tingkat awal diberikan oleh pelayanan kesehatan primer, sedangkan materi
edukasi tingkat lanjutan dierikan oleh pelayanan esehatan sekunder atau tersier
(Perkeni, 2019).
Prinsip proses edukasi yang perlu diperhatikan, yaitu : Memberikan
dukungan dan nasehat yang positif hindari terjadinya kecemasan; Memberikan
informasi secara bertahap dari hal yang sederhana dan dengan cara yang mudah
dimengerti; Melakukan pendekatan untuk mengatasi masalah dengan melakukan
simulasi; Dalam program pengobatan dan hasil laboratorium lakukan diskusi secara
25
terbuka dengan perhatikan keinginan pasien; Melakukan kompromi dan negosiasi
agar tujuan pengobatan dapat diterima; Memberikan motivasi dengan memberikan
penghargaan; Melibatkan keluarga/pendamping dalam proses edukasi; Perhatikan
kondisi jasmani dan psikologis serta tingkat pendidikan pasien dan keluarganya;
Gunakan alat bantu audio visual (Perkeni, 2019).
2. Terapi Nutrisi Medis
Terapi nutrisi medis dilaksanakan dalam beberapa tahap. Pengenalan
sumber dan jenis karbohidrat, pencegahan dan penatalaksanaan hipoglikemia harus
dilakukan terhadap pasien. Secara umum, terapi nutrisi medis meliputi upaya-upaya
untuk mendorong pola hidup sehat, membantu kontrol gula darah, dan membantu
pengaturan berat badan (Decroli, 2019). Pada pasian diabetes mellitus tipe 1, fokus
untuk mengatur pemberian insulin dengan diet seimbang agar dapat mencapai atau
mempertahankan berat badan yang sehat. Sedangkan pada pasien diabetes mellitus
tipe 2 sering membutuhkan keseimbangan kalori untuk meningkatkan berat badan
(Dipiro et al, 2016).
Tidak dapat mengendalikan pola makan merupakan problem pasien
diabetes, bukan sebagai penyebab saja tetapi juga sebagai dampak penyakit diabetes
(Hendro, 2018). Menurut perkeni 2019 komposisi makanan yang dianjurkan untuk
pasien diabetes melitus yaitu : karbohidrat sebesar 45-65% total asupan energi,
lemak sebesar 20-25% kebutuhan kalori tidak boleh melebihi 30% total asupan
energi, protein sebesar 10-20% kebutuhan energi, natrium sebesar < 1500 mg/hari,
serat 14 gram/1000 kalori atau 20-35 gram/hari, dan pemanis alternatif yang tidak
melebihi batas aman (Perkeni, 2019).
3. Latihan Jasmani
Latihan jasmani dapat dilakukan secara teratur 3-4 kali seminggu selama
30-45 menit, pasien sebisa nya dapat mencapai taget latihan dengan prosentase 70%
dari total BMI, namun tidak lupa disesuaikan dengan umur dan kesegaran jasmani
(Yanti, 2016). Selain untuk menjaga kebugaran latihan jasmani juga dapat
menurunkan berat badan dan memperbaiki sensitivitas insulin sehingga akan
memperbaiki kendali glukosa darah. Latihan jasmani aerobik seperti jalan kaki,
bersepeda santai, joging, dan berenang sangat dianjurkan (Perkeni.2019).
26
Prinsipnya tidak perlu latihan jasmani yang bersifat berat, cukup lakukan yang
ringan saja secara teratur (Dipiro et al, 2016).
2.11.2 Terapi Farmakologi Diabetes Melitus
Terapi farmakologi diberikan bersama dengan pengaturan makan dan
latihan jasmani (gaya hidup sehat). Terapi farmakologis terdiri dari obat oral (po)
dan bentuk suntikan (Perkeni, 2019).
Gambar 2. 5 Algoritma Tatalaksana DM (Perkeni, 2015)
A. Terapi OAD
Tabel II. 2 Profil Obat Antidiabetes Oral (Perkeni, 2019)
Golongan Obat Contoh Obat Cara Kerja
Biguanid Metformin Menurunkan produksi
glukosa hati dan
meningkatkan sensitifitas
insulin
Thiazolidinedione Pioglitazone dan
Rosiglitazone
Meningkatkan sensitifitas
insulin
27
Sulfonilurea Generasi pertama :
Klorpropamid, Tolazamid,
dan Tolbutamid
Generasi kedua :
Glibenklamide, Glipizide,
dan Glimepiride
Meningkatkan sekresi insulin
Meglitinide Repaglinid dan Nateglinid
Meningkatkan sekresi insulin
Penghambat Alfa
Glukosidase
Acarbose dan Miglitol Menghambat absorpsi
glukosa
Penghambat
DPP-4
Sitagliptin, Saxagliptin,
Alogliptin, dan Linagliptin
Meningkatkan sekresi insulin
dan menghambat sekresi
glukagon
Penghambat
SGLT-2
Canagliflozin,
Dapagliflozin,
Empagliflozin, dan
Ertugliflozin
Menghambat reabsorpsi
glukosa di tubulus distal
1. Pemacu Sekresi Insulin
a. Golongan Sulfonilurea
Sulfonilurea biasanya diberi dosis sekali atau dua kali sehari. Bekerja
dengan meningkatkan sekresi insulin dengan mengikat reseptor sulfonilurea
spesifik pada sel β pankreas. Sulfonilurea dibagi menjadi dua generasi yaitu
pertama dan kedua. Generasi pertama dengan resiko rendah yaitu klorpropamid,
tolazamid, dan tolbutamid sedangkan generasi kedua dengan resiko tinggi yaitu
glibenklamide, glipizide, dan glimepiride (Dipiro et al, 2020). Efek sampingnya
yang sering tejadi yaitu hipoglikemia serta peningkatan berat badan. Hati-hati
dalam pemakaian sulfonilurea terhadap pasien yang mempunyai risiko tinggi
hipoglikemia seperti orang tua, gangguan fungsi hati dan ginjal (Perkeni, 2019).
b. Golongan Meglitinide
Meglitinides mirip dengan sulfonilurea, kecuali yang memiliki onset lebih
cepat dan durasi tindakan yang lebih singkat. Terdapat dua obat yaitu repaglinid
(derivat asam benzoat) dan nateglinid (derivat fenilalanil). Dengan mengikat situs
28
yang berdekatan dengan. sulfonilurea reseptor, nateglinide dan repaglinide
merangsang sekresi insulin dari sel β pankreas. Nateglinide atau repaglinide harus
diberikan secara oral dengan makanan, dimulai pada dosis rendah, dan bertahap
dari waktu ke waktu sampai kontrol glikemik tercapai (Dipiro et al, 2020). Obat ini
diserap dengan cepat setelah diberikan dengan cara oral dan diekskresi dengan
cepat melalui hati. Obat ini mampu mengatasi hiperglikemia post prandial (Perkeni,
2019).
2. Peningkatan Sensitivitas terhadap Insulin
a. Golongan Biguanid
Biguanida yang tersedia di Amerika Serikat yaitu Metformin, untuk dosis
formulasi pelepasan segera diberi dosis dua kali sehari atau anformulasi extended-
release (XR) diberi dosis sekali atau dua kali sehari. Metformin telah menurunkan
produksi glukosa hati dan dapat meningkatkan sensitivitas insulin di jaringan
perifer (otot), sehingga meningkatkan pengambilan glukosa ke dalam sel otot.
Metformin tidak memiliki efek langsung pada sel β, tetapi konsentrasi insulin
berkurang karena peningkatan insulin sensitivitas (Dipiro et al, 2020). Efek
samping yang dirasakan yaitu gangguan saluran pencernaan seperti dispepsia, diare,
dan lain-lain (Perkeni, 2019).
b. Golongan Thiazolidinedione
Oral antidiabetes golongan thiazolidinedione (TZD) yang disetujui FDA
untuk pengobatan DM tipe 2 yaitu pioglitazone dan rosiglitazone. Pioglitazone
dapat diberikan, dosis awal yang biasa (1x15–30 mg/d) po dan dosis maksimum
(1x45 mg/d) po. Sedangkan Rosiglitazone cepat diserap dan sangat terikat protein
diberikan dosis sekali atau dua kali sehari sebanyak 2–8 mg (Katzung, 2018).
Tiazolidinedione merupakan agonis dari Peroxisome Proliferator Activated
Receptor Gamma (PPAR- gamma), suatu reseptor inti beberapa organ diantaranya
sel otot, lemak, dan hati. Aktivasi PPAR-γ mengubah transkripsi beberapa gen yang
terlibat dalam metabolisme glukosa dan lipid dan keseimbangan energi (Dipiro et
al, 2020).
Golongan ini dapat menurunkan resistensi insulin dengan meningkatkan
jumlah protein pengangkut glukosa, sehingga meningkatkan ambilan glukosa di
jaringan perifer. Tiazolidinedione meningkatkan retensi cairan tubuh sehingga
29
dikontraindikasikan terhadap pasien dengan gagal jantung (NYHA fungsional class
III-IV) dikarenakan mampu memperberat edema / retensi cairan. Hati-hati terhadap
gangguan faal hati, dan jika diberikan perlu pemantauan faal hati secara berkala.
efek termasuk edema perifer, gagal jantung, hemodilusi hemoglobin dan
hematokrit, dan penambahan berat badan (Perkeni, 2019).
3. Penghambat Alfa Glukosidase
Terdapat dua α-glukosidase yang disetujui oleh FDA yaitu acarbose dan
miglitol, antidiabetes oral ini diberikan sebelum makan. Pengobatan Acarbose
dimulai dengan dosis (2x50 mg) po dengan peningkatan bertahap menjadi (3x100
mg) po. Sedangkan terapi miglitol dimulai dengan dosis (3x25 mg) po.
Pemeliharaan yang biasa dosis adalah (3x50 mg) po, tetapi beberapa pasien perlu
(3x100 mg) po (Katzung, 2018). Obat ini tidak dimetabolisme dan dibersihkan oleh
ginjal. Antidiabetes oral tidak boleh digunakan dalam gagal ginjal. α-inhibitor
glukosidase secara kompetitif menghambat maltase, isomaltase, sucrase, dan
glukosamylase di usus kecil, menunda pemecahan sukrosa dan karbohidrat
kompleks (Dipiro et al, 2020).
Obat ini bekerja dengan menghambat kinerja enzim alfa glukosidase pada
saluran pencernaan sehingga dapat menghambat absorpsi glukosa di dalam usus
halus. Penghambat alfa glukosidase tidak dipakai pada keadaan LFG ≤ 30
ml/min/1,73 m2, kepada penderita gangguan faal hati yang berat, irritable bowel
syndrome. Efek samping yang timbul adalah bloating (penumpukan gas dalam
usus) sehingga sering memunculkan flatus (Perkeni, 2019).
4. Golongan Penghambat Enzim Dipeptidyl Peptidase-4 (DPP-4 inhibitor)
Empat inhibitor DPP-4 disetujui oleh FDA yaitu sitagliptin, saxagliptin,
linagliptin, dan alogliptin diberikan dengan dosis satu kali sehari. Antidiabetes oral
ini menghambat enzim DPP-4 yang bertanggung jawab untuk degradasi cepat GLP-
1 dan GIP, dengan demikian memperpanjang waktu paruh GLP-1 yang diproduksi
secara endogen (Dipiro et al, 2020). Enzim DPP-4 terekspresikan di berbagai organ
tubuh, termasuk di usus dan membran brush border ginjal, di hepatosit, endotelium
vaskuler dari kapiler vili, dan dalam bentuk larut dalam plasma. Penghambat DPP-
4 akan menghambat letak pengikatan pada DPP-4 sehingga mencegah inaktivasi
dari glucagon-like peptide (GLP)-1. Proses inhibisi ini akan mempertahankan kadar
30
GLP-1 dan glucose-dependent insulinotropic polypeptide (GIP) pada bentuk aktif
di sirkulasi darah, sehingga mampu memperbaiki toleransi glukosa, meningkatkan
respons insulin, dan mereduksi sekresi glukagon (Perkeni, 2019).
5. Golongan Penghambat Enzim Sodium Glucose co-Transporter 2 (SGLT-2
inhibitor)
Empat inhibitor SGLT-2 telah disetujui oleh FDA yaitu canagliflozin,
dapagliflozin, empagliflozin, dan ertugliflozin. Dosis diberikan satu kali sehari.
Inhibitor SGLT-2 mengurangi glukosa plasma dengan mencegah ginjal dari
reabsorbsi glukosa di tubulus proksimal kembali ke aliran darah, yang
menyebabkan peningkatan ekskresi glukosa dalam urin (Dipiro et al, 2020). Obat
golongan ini dapat menurunkan berat badan dan tekanan darah. Efek samping yang
dirasakan yaitu infeksi saluran kencing dan genital. Pada penyandang DM yang
mempunyai gangguan fungsi ginjal perlu dilakukan penyesuaian dosis, dan tidak
diperkenankan bila LFG kurang dari 45 ml/menit. Hati-hati karena dapat
mencetuskan ketoasidosis (Perkeni, 2019).
B. Antidiabetes Suntik/Insulin
1. Insulin
Insulin yang diproduksi secara endogen dibelah dari peptida proinsulin yang
lebih besar di sel β ke peptida aktif insulin dan C-peptida yang tidak aktif. Sebagian
besar insulin diberikan secara subkutan untuk pengelolaan diabetes kronis, kecuali
insulin manusia yang terhirup yang merupakan bubuk kering DNA rekombatan
insulin reguler yang terhirup dan diserap melalui jaringan paru-paru. Keuntungan
utama insulin daripada agen antihyperglycemic lainnya adalah dapat mencapai
berbagai target glukosa dan dosisnya dapat individual berdasarkan tingkat glikemik
(Dipiro et al, 2020).
Tujuan pemberian insulin yaitu untuk mengontrol kadar basal dan post
prandial, karena pada pasien DM tipe 2 terjadi gangguan sekresi insulin basal
(puasa) dan prandial (setelah makan). Formulasi insulin dengan tingkat awal kerja
(onset) dan lama kerjanya (duration) yang berbeda sering dikombinasi untuk
tercapainya tujuan ini. Berikut adalah klasifikasi insulin menurut Perkeni 2019 :
1. Insulin kerja cepat (rapid acting insulin)
2. Insulin kerja pendek (short acting insulin)
31
3. Insulin kerja menengah (intermediate acting insulin)
4. Insulin kerja panjang (long acting insulin)
5. Insulin campuran tetap, kerja pendek dan menengah (premixed insulin)
2. Golongan GLP1-RA
Terdapat tujuh golongan GLP1-RA tersedia di Amerika Serikat. Enam di
antaranya adalah diberikan secara subkutan dengan dosis mulai dari dua kali sehari
hingga sekali seminggu dan satu diberikan secara oral sekali sehari. Golongan ini
merangsang sekresi insulin dari sel beta pankreas dengan cara yang bergantung
pada glukosa. Selain itu, selama hiperglikemia, GLP1-RA mengurangi peningkatan
kadar glukagon secara tidak tepat, yang menyebabkan penurunan output glukosa
hati. Tindakan ini menghasilkan penurunan glukosa dan bobot. GLP1-RA juga
berpotensi mempertahankan fungsi sel beta pankreas dan melindungi dari apoptosis
yang diinduksi oleh sitokin. Semua GLP1-RA menghasilkan tingkat farmakologis
aktivitas GLP-1 dan tahan terhadap degradasi yang cepat oleh enzim dipeptidyl
peptidase 4 (DPP-4). GLP1-RAs meningkatkan sekresi insulin dengan cara
bergantung pada glukosa di respon terhadap asupan makanan; dengan demikian,
risiko hipoglikemia rendah bila digabungkan dengan metformin, inhibitor DPP-4,
inhibitor SGLT-2, atau TZD (Dipiro et al, 2020).
2.12 Tinjauan Obat Pioglitazone
2.12.1 Pengertian Pioglitazone
Pioglitazone merupakan antidiabetik golongan thiazolidinedione digunakan
untuk mengobati diabetes mellitus tipe 2. Pioglitazone dapat digunakan sendiri atau
kombinasi dengan obat lain seperti insulin, metformin, atau sulfonilurea.
Penggunaan pioglitazone didampingi dengan diet dan olahraga yang tepat untuk
membantu mengontrol kadar gula darah (Al-Majed, 2016).
Gambar 2. 6 Struktur Kimia Pioglitazone (Al-Majed, 2016)
2.12.2 Farmakologi Pioglitazone
32
Resistensi insulin dapat terjadi pada diabetes melitus tipe II kadar insulin
tidak mengaktifkan sinyal untuk menyerap glukosa. Thiazolidinedione seperti
pioglitazone adalah peroksisom sintetis yang kuat ligan proliferator-activated
receptor (PPARγ) yang telah terbukti efektif dalam pengobatan diabetes. Efek
penurunan glukosanya sedang dilakukan terutama melalui peningkatan sensitivitas
insulin dan oleh karena itu, memfasilitasi pengambilan dan pemanfaatan glukosa.
Thiazolidinedione dapat memasuki nukleus dimana mereka terikat ke PPARγ.
PPARγ diekspresikan paling banyak dalam adiposa jaringan tetapi juga ditemukan
dalam sel β pankreas, endotel vaskular, dan makrofag (Al-Majed, 2016).
Pioglitazone adalah agonis yang kuat dan sangat selektif untuk PPARγ.
Reseptor ini mengatur ekspresi lebih dari 100 gen, yang berkumpul bersama tetapi
tidak identik. Selain itu, respons sekresi insulin telah terjadi dilaporkan meningkat
pada subjek dengan gangguan toleransi dan tipe glukosa II diabetes, bahkan setelah
peningkatan sensitivitas insulin. Kemungkinan lain mekanisme tiazolidinedion
melibatkan penurunan adiposit sitokin dan hormon yang terlibat dalam patogenesis
insulin perlawanan. Pioglitazone bekerja menurunkan resistensi insulin,
mengaktifkan reseptor nukleus spesifik (peroxisome proliferator activated receptor
gamma), yang akan meningkatkan sensitivitas insulin di hati, jaringan lemak dan
sel-sel otot skeletal. Pada kasus resistensi insulin, pioglitazone menurunkan
produksi glukosa hati dan meningkatkan penggunaan glukosa perifer (Al-Majed,
2016).
2.12.3 Dosis dan Cara Penggunaan Pioglitazone
Pioglitazone dapat diminum sekali sehari secara per-oral. Dosis awal yang
biasa adalah (1x15mg/30 mg) po dan maksimum 45 mg/hari (po). Pioglitazone
disetujui sebagai terapi tunggal dan dalam kombinasi dengan metformin,
sulfonylureas, dan insulin untuk pengobatan diabetes tipe 2 (Katzung, 2018). Dosis
awal pioglitazone yang direkomendasikan adalah (1x15 mg) po. Dosis dapat
ditingkatkan setelah 3 sampai 4 bulan berdasarkan respon terhadap pengobatan dan
efek samping. Dosis maksimum dan dosis efektif maksimum dari pioglitazone
adalah (1x45 mg) po. Untuk meminimalkan penambahan berat badan dan edema,
dosis efektif terendah harus digunakan. Jika efek samping terjadi dengan dosis yang
lebih tinggi, dosis harus dikurangi. Dosis yang lebih rendah direkomendasikan bila
33
digunakan dalam kombinasi dengan insulin, dan edema serta penambahan berat
badan harus dipantau dengan hati-hati (Dipiro et al, 2020).
2.12.4 Farmakokinetik Pioglitazone
Pioglitazone diserap baik dengan atau tanpa makanan, dan keduanya diikat
oleh protein plasma sekitar lebih dari 99%. Pioglitazone akan melalui metabolisme
di hati oleh CYP2C8 enzim dan CY3A4 dan tereliminasi bersama dengan keluarnya
feses. Pioglitazone memiliki t ½ yakni 3 sampai 7 jam dengan durasi kerja
antihiperglikemik kurang dari 24 jam (Dipiro et al, 2016).
Proses ADME pada pioglitazone yaitu absorpsi pioglitazone pemberian
secara oral, konsentrasi puncak diperoleh setelah 2 jam pemberian. Jika obat
diberikan bersama makanan, tercapainya konsentrasi puncak lebih lambat, hingga
3-4 jam setelah pemberian, tetapi hal tersebut tidak menimbulkan perubahan
konsentrasi obat. Distribusi pioglitazone, rata–rata volume distribusi pioglitazone
pada pemberian tunggal adalah 0,63 ± 0,41 L/kgBB. Pioglitazone dapat berikatan
pada serum protein manusia terutama pada serum albumin (>99%). Metabolisme
pioglitazone melalui mekanisme hidroksilasi dan oksidasi. Hasil metabolitnya
sebagian diubah menjadi glukuronida atau konjugat sulfat. Metabolisme di hepar
diperantarai enzim sitokrom P45p, termasuk CYP2C8 dan CYP3A4, serta enzim
ekstrahepatik CYP1A1. Eliminasi pioglitazone, hasil metabolit pioglitazone
diekskresikan melalui saluran empedu dan dibuang bersama feses, sekitar 15-30%
hasil metabolit ditemukan pada urine. Obat ini diekskresikan sebagai metabolit dan
konjugasinya. Waktu paruh pioglitazone sekitar 3-7 jam (PUBCEM, 2020).
Konsentrasi serum total pioglitazone (pioglitazone plus aktifnya metabolit)
tetap meningkat 24 jam setelah pemberian dosis sekali sehari. Stabil konsentrasi
serum dari kedua pioglitazone dan total pioglitazone adalah dicapai dalam 7 hari.
Pada kondisi mapan, dua di antaranya aktif secara farmakologis metabolit
pioglitazone, metabolit III (M-III) dan IV (M-IV), mencapai konsentrasi serum
sama dengan atau lebih besar dari pioglitazone. Keduanya sehat relawan dan pasien
dengan diabetes tipe II, terdiri dari pioglitazone sekitar 30-50% dari total
konsentrasi puncak serum pioglitazone dan 20-25% dari total area di bawah kurva
konsentrasi waktu serum (AUC). Konsentrasi serum maksimum (C maks), AUC,
dan palung konsentrasi serum untuk pioglitazone dan total pioglitazone meningkat
34
secara proporsional dengan dosis (1x15 mg dan 30 mg) po. Ada yang sedikit kurang
dari peningkatan proporsional untuk pioglitazone dan total pioglitazone dengan
dosis (1x60 mg) po (Al-Majed, 2016).
2.12.5 Farmakodinamik Pioglitazone
Pioglitazone merupakan obat oral golongan thiazolinedione penambah
sensitivitas terhadap insulin untuk terapi diabetes melitus tipe 2. Prinsip kerja
pioglitazone yaitu meningkatkan sensitivitas insulin terhadap jaringan target,
seperti menurunkan glukogenesis pada hati. Pioglitazone merupakan suatu agonis
peroxisome proliferator activated receptor gamma (PPAR-γ) yang terdapat pada
jaringan penting insulin seperti adiposa, otot skelet, dan hati. Aktivasi reseptor inti
PPAR-γ mengatur transkripsi sejumlah gen responsif insulin yang terlibat dalam
kontrol metabolisme glukosa dan lemak (PUBCEM, 2020).
Gambar 2. 7 Mekanisme Aksi Thiazolidinedione (Singh, 2020)
TZD mengerahkan efek antidiabetesnya meningkatkan sensitivitas insulin.
TZD membantu mengurangi resistensi insulin di otot, hati, dan jaringan adiposa.
Karena PPAR-gamma sangat terkonsentrasi di jaringan adiposa, efek pada otot dan
hati tampaknya melalui pensinyalan endokrin dari adiposit. Agonis selektif reseptor
inti yaitu peroxisome proliferator activated receptor gamma (PPAR-γ) yang
banyak diekspresikan di sel adiposa. Obat ini berikatan dengan PPAR-γ kemudian
mengaktivasi gen responsif insulin yang mengatur metabolisme lipid dan
35
karbohidrat. TZD membutuhkan insulin dalam kegiatan mereka, meningkatkan
sensitivitas insulin, terutama di jaringan perifer. Dimediasi melalui efek pada sel
adiposa, karena sedikit reseptor PPAR-γ dalam jaringan otot. Pada adiposit,
diferensiasi ditingkatkan, lipolisis berkurang, dan tingkat sirkulasi adipositokin atau
adipokin yang berubah, yaitu penurunan tumor necrosis factor alpha dan leptin dan
peningkatan adiponektin (Singh, 2020).
2.12.6 Efektivitas Pioglitazone
Obat ini juga memiliki beberapa efek tambahan selain menurunkan glukosa.
Pioglitazone menurunkan trigliserida dan meningkatkan kolesterol high-density
lipoprotein (HDL) tanpa mempengaruhi kolesterol total dan kolesterol low-density
lipoprotein (LDL) (Katzung, 2018). TZD memiliki khasiat penurun glikemik yang
tinggi dan mengurangi nilai HA1C sekitar 1,0% hingga 1,5% (0,010 hingga 0,015;
11 hingga 22 mmol / mol), tingkat FPG hingga 60 hingga 70 mg / dL (3,3 hingga
3,9 mmol / L) secara maksimal dosis, dan mereka memiliki daya tahan tinggi dari
waktu ke waktu. Pioglitazone secara konsisten menurunkan kadar trigliserida
plasma sebesar 10% hingga 20% (Dipiro et al, 2020).
Studi klinis menunjukkan bahwa pioglitazone meningkatkan sensitivitas
insulin dalam resisten insulin. Pioglitazone meningkatkan respon seluler terhadap
insulin, meningkatkan pembuangan glukosa yang bergantung pada insulin, dan
memperbaiki disfungsional homeostasis glukosa. Pada penderita diabetes tipe 2,
insulin mengalami penurunan resistensi yang dihasilkan oleh pioglitazone telah
mengakibatkan penurunan glukosa plasma konsentrasi, kadar insulin plasma, dan
nilai HbA1c. Berdasarkan hasil dari klinis ekstensi label terbuka, efek penurunan
glukosa pioglitazone tampaknya bertahan setidaknya selama 1 tahun. Dalam uji
klinis terkontrol, pioglitazone dalam kombinasi dengan sulfonilurea, metformin,
atau insulin memiliki efek aditif pada kontrol glikemik (Al-Majed, 2016)
2.12.7 Interaksi Pioglitazone
Pioglitazone merupakan penginduksi lemah terhadap sitokrom P450
substrat 3A4 atau disingkat CYP3A4. Penghambat enzim P4502C8 atau disingkat
CYP2C8 (seperti gemfibrozil) dapat secara signifikan meningkatkan AUC
pioglitazone dan enzim penginduksi CYP2C8 (seperti rifampisin) dapat secara
signifikan menurunkan AUC pioglitazone. Oleh karena itu, jika inhibitor atau
36
penginduksi CYP2C8 mulai diberikan atau dihentikan selama pengobatan dengan
pioglitazone, akan terjadi perubahan dalam pengobatan diabetes dan dilihat
berdasarkan respon klinis (Desouza, 2010).
2.12.8 Kontraindikasi Pioglitazone
TZD merupakan kontraindikasi pada pasien dengan penyakit hati dan gagal
jantung kelas III dan IV dan harus sangat hati-hati digunakan pada pasien dengan
gagal jantung kelas I dan II. TZD tidak boleh digunakan pada pasien dengan kanker
kandung kemih aktif, sebelum penggunaan TZD harus benar-benar
dipertimbangkan manfaat dan risikonya (Dipiro et al, 2020). Pasien dengan
hipersensitivitas yang diketahui terhadap pioglitazone atau salah satu
komponennya. Ketoasidosis diabetik atau diabetes tipe 1, karena pioglitazone aktif
hanya dengan adanya insulin. Oleh karena itu hipoglikemia, perlu pemantauan gula
darah secara teratur (Singh, 2020).
2.12.9 Efek Samping Pioglitazone
Retensi cairan, edema, anemia, penambahan berat badan, edema makula,
patah tulang pada wanita (Katzung, 2018). TZD menyebabkan retensi cairan karena
vasodilatasi perifer dan peningkatan sensitisasi insulin di ginjal yang
mengakibatkan peningkatan natrium ginjal dan retensi air. Efek yang dihasilkan
termasuk edema perifer, gagal jantung, hemodilusi hemoglobin dan hematokrit, dan
penambahan berat badan. Penambahan berat badan juga terkait dengan dosis dan
merupakan hasil dari retensi cairan dan penumpukan lemak. TZD juga dikaitkan
dengan peningkatan angka patah tulang pada tungkai atas dan bawah wanita pasca
menopause (Dipiro et al, 2020).
2.12.10 Sediaan Pioglitazone
a. Pioglitazone (ISO, 2017)
Kandungan : Pioglitazone 15 mg, 30 mg.
Indikasi : Monoterapi atau kombinasi DM tipe 2.
Dosis : Dewasa monoterapi dosis tunggal (1x15 mg atau 30 mg) po, dosis
dapat ditingkatkan (1x45 mg) po. Kombinasi dosis awal (1x15-
30mg) po.
b. Pionix/Pionix-M (ISO, 2017)
37
Kandungan : Pioglitazone 15 mg, 30 mg, Pioglitazone 15 mg √ metformin 500
mg atau 850 mg.
Indikasi : Non Insulin Dependent Diabetes Melitus (NIDDM) Monoterapi
atau kombinasi DM tipe 2.
Kontraindikasi : Riwayat gagal jantung I-IV, gangguan hati ketoasidosis, pasien
terapi insulin.
Perhatian : Retensi cairan dan gagal jantung.
Efek samping : Peningkatan BB, gangguan pengelihatan, anemia, hipoestesia,
hipoglikemia, peningkatan nafsu makan, sakit kepala, flatulence.
Dosis : Monoterapi (1x15 mg atau 30 mg) po, kombinasi dengan
metformin atau sulfonilurea (1x15 mg atau 30 mg) po dan dosis
metformin atau sulfonilurea boleh diteruskan dengan
atau tanpa makanan.
c. Actos (ISO, 2017)
Kandungan : Pioglitazone 15 mg, 30 mg.
Indikasi : DM tipe 2 monoterapi atau kombinasi sulfonilurea atau
metformin saat makan, olahraga.
Kontraindikasi : Kerusakan jantung, kerusakan hati, pasien dialisa, dan kombinasi
terapi dengan insulin.
Efek samping : Edema ringan hingga sedang.
Dosis : Monoterapi (1x15 mg atau 30 mg) po, dapat ditingkatkan hingga
(1x45 mg) po. Kombinasi (1x15 mg atau 30 mg) po, sulfonilurea
atau metformin dilanjutkan hingga terapi inisiasi, sebelum atau
setelah makan.
d. Gliabetes (ISO, 2017)
Kandungan : Pioglitazone 30 mg.
Indikasi : Kombinasi sulfonilurea atau metformin pada DM tipe 2 (Non
Insulin Dependent Diabetes Melitus) ketika terapi tunggal tidak
menunjukkan hasil.
Kontraindikasi : Hipersensitivitas, gangguan fungsi hati, gagal jantung kelas
III/IV, diabetes melitus tipe 1 dan ketoasidosis, kombinasi dengan
insulin.