Referat Koriokarsinoma
-
Upload
ikke-rosella -
Category
Documents
-
view
22 -
download
9
description
Transcript of Referat Koriokarsinoma
BAB I
PENDAHULUAN
I.1. Latar Belakang
Istilah penyakit trofoblastik gestasional merujuk pada suatu spektrum tumor
plasenta terkait kehamilan, penyakit trofoblastik gestasional dibagi menjadi tumor mola
dan non-mola. Tumor non-mola dikelompokkan sebagai neoplasia trofoblastik
gestasional. American College of Obstetricians and Gynecologist (2004) menyebut
tumor-tumor ini sebagai penyakit trofoblastik gestasional maligna. Meskipun tumor-
tumor ini secara histologis berbeda dan memiliki kecenderungan yang bervariasi untuk
melakukan invasi dan metastasis, sepanjang tahun 1970an mulai terbukti bahwa
konfirmasi histologis tidak diperlukan untuk memberikan terapi yang efektif. Sebaliknya
diadopsi suatu sistem yang terutama didasarkan pada temuan klinis dan pengukuran
serial serum human chorionic gonadotropin (β-hCG). Dalam 30 tahun terakhir ini, telah
digunakan sejumlah skema untuk mengklasifikasikan tumor-tumor ini berdasarkan
potensi keganasannya, dan untuk menentukan stadium klinis dan terapi optimal. Skema
klasifikasi penyakit trofoblastik dari International Federation of Gynecology and
Obstetrics (FIGO) sering digunakan. Jika berbagai algoritme penatalaksanaan ini diikuti,
sebagian besar tumor gestasional baik jinak maupun ganas dapat disembuhkan
(Berkowitz dan Goldstein, 2009).1
Mola hidatidosa saat ini disebut dengan Penyakit Trofoblastik Gestasional (GTD).
Sekitar 9-20% pasien dengan mola hidatidasa komplet berkembang menjadi Penyakit
Trofoblas Ganas (PTG). Jika proses tersebut terbatas pada uterus disebut dengan
neoplasma tropoblastik nonmetastatik. Di samping neoplasma pascamola, tumor
trofoblastik dapat mengikuti aborsi (30%) dan kehamilan normal (20%).1
Angka kejadian mola hidatidosa berkisar antara 0,5 sampai 8,3 tiap 1000 kelahiran
hidup, 50% penderita mengalami anemia, 10% memerlukan kemoterapi karena
berkembang menjadi khoriokarsinoma.1
Insiden mola hidatidosa di Asia 7 sampai 10 kali lebih besar jika dibandingkan
dengan di Amerika Utara dan Eropa. Tingginya insiden pada populasi tertentu juga
dipengaruhi oleh faktor sosial ekonomi dan nutrisi. Dilaporkan bahwa rendahnya
konsumsi carotene (suatu prekursorvit A berpengaruh terhadap tingginya insiden mola
1
(Level of evidence C). Mola komplet terjadi pada 1 dari 1500 kehamilan di USA dan 1
dari 400 kehamilan di Korea serta Indonesia.1
I.2. Tujuan Umum :
Mampu untuk melakukan penilaian klinik dan penatalaksanaan dari penyakit
khoriokarsinoma.
I.3. Tujuan Khusus :
- Mengenali gejala dan tanda penyakit khoriokarsinoma
- Melakukan penatalaksanaan dari penyakit khoriokarsinoma
2
BAB II
TINJAUAN PUSTAKA
II.1. Penyakit Trofoblas Gestasional
Penyakit trophoblas merupakan suatu kelainan berupa proliferasi sel
trophoblas kehamilan yang abnormal.2
Penyakit trofoblas gestasional (PTG)/gestasional trophoblastic disease adalah
kelainan proliferasi trofoblas pada kehamilan, berupa suatu spektrum tumor saling
berhubungan tetapi dapat dibedakan secara histologis.1-3 Trofoblas adalah jaringan
yang pertama kali mengalami diferensiasi pada masa embrional dini kemudian
berkembang menjadi jaringan ekstraembrionik dan membentuk plasenta yang
merupakan interfase janin-maternal. Penyakit trofoblas dapat berupa tumor atau
keadaan yang merupakan predisposisi terjadinya tumor.
Petanda tumor yang khas pada penyakit ini adalah subunit β human Chorionic
Gonadotropin (β-hCG) dan memiliki kecenderungan invasi lokal dan penyebaran.
Neoplasia trofoblas gestasional (NTG-Neoplasia Trophoblastic Gestasional) adalah
bagian dari PTG yang berkembang menjadi jejas keganasan.3
Penyakit trofoblas gestasional meliputi suatu spektrum luas kelainan trofoblas.
Secara klinis, WHO membagi penyakit trofoblas gestasional menjadi dua kelompok,
yaitu :
Kelompok pra maligna, meliputi mola hidatidosa komplit dan parsial.
Kelompok maligna/Gestasional Trophoblastic Neoplasia (GTN), meliputi mola
invasif, khoriokarsinoma, dan metastating mole.
Pada semua kasus, diagnosis dan perjalanan penyakit dapat dimonitor secara
kuantitatif dengan pengukuran kadar hCG dan pemeriksaan radiologis.
Placental Site Trophoblastic Tumor (PSTT)
Suatu tumor yang berasal dari trofoblas atau pembuluh darah plasenta dan
terutama terdiri dari sel-sel sitotrofoblas. Tumor ini mencakup lesi keganasan
stadium rendah dan tinggi.3
PSTT merupakan variasi dari PTG tapi harus diklasifikasikan terpisah karena
memiliki sifat khas dan penatalaksanaan yang berbeda.4
3
Penyakit trofoblas non-gestasional
Penyakit trofoblas non-gestasional adalah khoriokarsinoma pada ovarium dan
testis.
II.2. Mola Hidatidosa
(Kehamilan anggur, hydatidiform pregnancy, benign form of gestational trophoblastic
disease/GTD)
a. Definisi
Molahidatidosa adalah plasenta dengan vili korialis yang berkembang tidak
sempurna dengan gambaran adanya pembesaran, edema, dan vili vesikuler sehingga
menunjukkan berbagai ukuran trofoblas proliferatif tidak normal. Molahidatidosa
terdiri dari molahidatidosa komplit dan molahidatidosa parsial; perbedaan antara
keduanya adalah berdasarkan morfologi, gambaran klinik patologi, dan sitogenetik.
Di Asia, insiden molahidatidosa komplit tertinggi adalah di Indonesia yaitu 1
dari 77 kehamilan dan 1 dari 57 persalinan. Faktor resiko molahidatidosa adalah
nutrisi, sosioekonomi (asupan karoten rendah, defisiensi vitamin A) dan usia
maternal.
Molahidatidosa parsial merupakan triploid yang mengandung dua set
kromosom paternal dan satu set kromosom maternal, tetapi pada triploid akibat dua
set kromosom maternal tidak menjadi molahidatidosa parsial. Pada molahidatidosa
parsial seringkali terdapat mudigah atau jika ditemukan sel darah merah berinti pada
pembuluh darah vili korialis.3
Kehamilan abnormal dengan ciri stroma villus khorialis langka vaskularisasi
dan edematosa. Dapat bersifat komplit dimana tidak dijumpai janin (90%) dan
parsial di mana masih dijumpai janin (10%).4
4
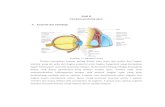
Gambar II.2.1 Gelembung Mola
Gambar II.2.2 Mola Hidatidosa Partialis
b. Faktor Resiko
Kejadian mola hidatidosa berkaitan faktor sosial ekonomi yang dapat memicu :
Resiko kejadian meningkat pada :
- Usia maternal yg ekstrim (>45 tahun atau <20 tahun)
- Wanita dengan riwayat mola hidatidosa
- Wanita dengan riwayat infertilitas dan abortus berulang
Kekurangan nutrisi :
- Protein dan kalori
- Defisiensi vitamin A
Studi menunjukkan bahwa wanita Asia dan Hispanik memiliki resiko yang lebih
besar. Dibanding negara maju kejadian di daerah miskin Asia termasuk Indonesia
lebih tinggi.
5
c. Penyebab
Terjadinya mola hidatidosa berkaitan dengan kromosom. Molahidatidosa
komplitus bersumber dari : fertilisasi ovum tanpa nukleus atau nukleusnya tidak
aktif sehingga tumbuh kembang didominasi inti spermatozoa. Oleh karena itu
gambaran kromosom pada mola hidatidosa komplitus : 46.XX. Pada mola hidatidosa
partialis, berlangsung pada ovum tanpa nukleus, mengalami fertilisasi ganda,
sehingga gambaran kromosomnya 46.XY.
Tidak berfungsinya atau hilangnya inti ovum, dikaitkan masalah sosial ekonomi :
Rendahnya nilai nutrisi, kekurangan protein.
Defisiensi vitamin A.
Mola hidatidosa mengalami degenerasi ganas menuju khoriokarsinoma, sekitar
10-15%. Molahidatidosa komplit hanya mengandung DNA paternal sehingga
bersifat androgenetik tanpa adanya jaringan janin. Hal ini terjadi karena satu sel
sperma membawa kromosom 23X – melakukan fertilisasi terhadap sel telur yang
tidak membawa gen maternal (tidak aktif), kemudian mengalami duplikasi
membentuk 46XX homozigot. Namun, fertilisasi juga dapat terjadi pada dua
spermatozoa yang akan membentuk 46XY atau 46XX heterozigot. Secara
makroskopis, pada kehamilan trimester dua molahodatidosa komplit berbentuk
seperti anggur karena vili korialis mengalami pembengkakan secara menyeluruh.
Pada kehamilan trimester pertama, vili korialis mengandung cairan dalam jumlah
lebih sedikit, bercabang dan mengandung sinsitiotrofoblas dan sitotrofoblas
hiperplastik dengan banyak pembuluh darah.3
Molahidatidosa komplet dan parsial mempunyai histology, morphology,
gambaran klinik atau penyebab yang berbeda. Molahidatidosa komplet, diploidi
dengan kariotipe 46-XX, kromosomnya seluruhnya paternal. Beberapa kasus
didapatkan kariotipe triploidi ataupun tetrapoidi. Secara klinis tidak dijumpai embrio
atau fetus, fetus hanya tampak bila kehamilan tersebut kehamilan ganda/kembar
dengan satu kehamilan fetus dan yang satu menjadi molahidatidosa. Mola hidatidosa
parsial umumnya dengan kariotipe triploidi (69 kromosome), faktor paternal dan
maternal. Molahidatidosa komplet mempunyai karakteristik degenerasi hidropik vili
khorialis dan proliferasi sel trophobast. Molahodatidosa parsialis mempunyai
komponen embrio atau fetus. Sedangkan karakteristiknya berupa degenerasi
hidropik fokal dengan hyperplasia trophoblast, kejadian koriokarsinoma sangat
6
rendah pada molahidatidosa parsialis. Kurang lebih 20% molahidatidosa akan
berkembang menjadi mola invasive ataupun khoriokarsinoma. Khoriokarsinoma
secara klinik disebut sebagai Penyakit Trophoblast Ganas.2
Kemungkinan lain yang menerangkan terjadinya molahidatidosa adalah faktor
kekurangan vitamin A. Risiko terjadinya molahidatidosa pada wanita yang
menderita defisiensi vitamin A meningkat menjadi 6,29 kali.2
d. Manifestasi Klinis
Gambaran histopatologi mola hidatidosa :
Villi khorialis membentuk massa yang mengandung air.
Tidak terdapat pembuluh darah pada villi khorialisnya.
Tidak terbentuk janin.
Proliferasi sel sito dan sinsitiotrophoblas, sehingga pengeluaran hCG tinggi,
pada urina dan serum.
Bersamaan dengan terjadinya mola hidatidosa, dijumpai :
Thirotoksikosis.
Preeklampsia – eklampsia pada umur kehamilan muda.
Gejala klinik hamil muda lebih dominan :
- Emisis gravidarum.
- Hiperemesis gravidarum.
Gambar II.2.3 Mikroskopis Mola Hidatidosa
7
Akibat hidropik degenerasi villi khorialis dan proliferasi sel trophoblas dapat
terjadi :
Hidropik degenerasi menyebabkan :
- Pembesaran uterus melebihi umur kehamilannya.
- Tidak teraba janin.
- Uterus lunak menyeluruh, karena tidak terdapat air ketubannya.
- Pembukaan serviks, bila kontraksi terjadi ekspulsi gelembung mola
hidatidosa.
Tanda klinik dan keluhan klasik mola hidatidosa kompleteus :
Uterus lebih besar dari umur kehamilan
hCG diatas 100.000 ml U/ml.
Lutein kista lebih besar dari 6cm.
Dapat dijumpai preeklampsia.
Dapat disertai hipertiroidsm.
Disertai hiperemesis gravidarum.
Terjadi trophoblastik emboli.
Kini dengan pemeriksaan ultra sonografi, diagnosa mola hidatidosa dengan jelas
dapat ditegakkan.
Proliferasi sel trophoblas :
Merusak pembuluh darah, menimbulkan perdarahan (97%).
Bentuk perdarahannya dapat :
- Tertimbun intra uterin.
- Keluarnya sedikit-sedikit melalui ostium uteri eksternum.
- Perdarahan banyak pada ekspulsi gelembung mola.
e. Dasar Diagnosa Mola Hidatidosa
Klinis pembesaran uterus yang lebih besar dari usia kehamilannya, sonde
uterus yang tidak menjumpai tahanan, serta keluarnya gelembung molahidatidosa.
Pada pemeriksaan ultrasonographi mempunyai gambaran yang cukup spesifik.2
8
Gambar klinik mola hidatidosa dapat :
50% perdarahan disertai ekspulsi gelembung mola hidatidosa sehingga
diagnosanya sangat jelas.
50% perdarahan pada hamil muda diduga abortus imminens.
Dikonfirmasikan dengan pemeriksaan ultra sonografi yang memberikan diagnosa
pastinya. Pada mola hidatidosa yang masih utuh, dasar diagnosanya :
Gejala hamil muda prominen :
- Emesis gravidarum – hiperemesis gravidarum
- Terdapat komplikasi :
Thirotoksikosis 2-5%
Hipertensi – preeklampsia 10-15%
Anemia akibat perdarahan.
Perubahan hemodinamik kardiovaskuler :
Gangguan fungsi jantung.
Gangguan fungsi paru akibat edema atau emboli paru.
Pemeriksaan palpasi :
- Uterusnya mengalami :
Lebih besar dari umur hamilnya 50-60%.
Besar uterus sama dengan umur hamil 20-25%.
Uterus lebih kecil dari umur hamilnya 5-10%.
Palpasi lunak seluruhnya.
Tidak terasa teraba bagian janin.
Terdapat bentuk asimetris, bagian menonjolagak padat – mola
destruen.
Pemeriksaan USG :
- Dipastikan mola hidatidosa seperti TV mati.
- Tidak terdapat janin.
- Tampak sebagian plasenta normal dan dapat tampak janinnya.
9
Gambar II.2.4 Gambaran USG Mola Hidatidosa
Pemeriksaan laboratorium :
- Beta hCG tinggi melebihi 100.000 ml/urine.
- Beta hCG serum diatas 40.000 IU/ml.
Pemeriksaan lain yang dapat dipergunakan adalah :
Memasukkan sonde intra uterine – tanpa tahanan – Hanifa positif. Artinya
mola hidatidosa.
Suntikan bahan kontras intra uterine – foto abdomen, tampak gambaran sarang
tawon.
Pemeriksaan MRI :
- Tidak tampak janin.
- Jaringan molahidatidosanya jelas.
Pemeriksaan terakhir jarang dipergunakan karena dengan USG diagnosanya
sudah jelas. Telah dikemukakan bahwa sekitar 10% dijumpai partial mola
hidatidosa dengan kariotipe : trisomi (triploidi) dengan perbandingan patologi
klinik sebagai berikut :
10
Tabel II.1.1. Perbedaan Antara Mola Hidatidosa Komplitus dan Inkomplitus
Penampakan Mola hidatidosa
komplitus
Mola hidatidosa
inkompleteus/partial
Kariotipe Umumnya 46 XX
(homolog)
46 XY (heterolog)
Tripoloidi 69 XXY
sebagian besar
(trisomi 16).
Jarang diploidi,
paternal/maternal.
Villi Khorealis Seluruhnya
mengalami
regenerasi hidropik,
hiperplasia.
Sebagian masih
normal.
Hiperplasia moderate.
Pembuluh
darah
Tidak dijumpai,
pembuluh darah
janin hilang.
Pada plasenta normal
dijumpai pembuluh
darah janinnya.
Terdapat fetal eritrosit.
Janinnya Tidak dijumpai Dapat dijumpai janin,
pada bagian plasenta
normal, sebagian
abnormal.
Trophoblas sel Proliferasi,
hiperplasia dengan
bervariasi.
Hiperplasia sedang
dan lokal.
Beta hCG Titernya tinggi. Titernya sedang
sampai rendah.
Degenerasi
ganas
15-20% Sekitar 5%
Umur
kehamilan
8-16 minggu 12-26 minggu
11
Mola HydatidosaPenilaian Awal
Riwayat Ob/gin cbc, pembekuan (jika ada indikasi)
Pemeriksaan fisik foto dadahCG BUN creatinin LFT
Evakuasi mola
Mola kompletEvakuasi uterus dengan suksen
laminaria (pilihan)
Mola parsialLaminaria (pilihan) dilatasi dan
evakuasi D&C
Tidak ada metastase
hCG tiap minggu (catat di kertas semi log)
Resolusi spontan hCG menetap meningkat selama 14 hari atau lebihplateau lebih dari 21 hari atau lebih
Diagnosa sebagai Gestasional Trofoblastik Neoplsama (GTN)
Investigasi dan stagingLanjut diagram III.3.1
Ikuti selama 6-12 bulan sebelum mengijinkan pulang
Diagram II.2.1 Panduan untuk Manajemen Penyakit Trofoblastik
Gestasional
Catatan : Penyakit Trofoblastik Gestasional (GTD) termasuk semua aspek dalam
entitas ini. Istilah penyakit Trofoblas Ganas (PTG) khusus digunakan untuk
kelompok yang memerlukan kemoterapi dan menggantikan istilah invasif unutk
mole malignant GTD dan istilah lain. Koriokarsinoma adalah istilah patologi.
PSTT dibedakan tersendiri.
12
f. Evaluasi Mola Hidatidosa Pasca Evakuasi
Pasca Kuretase, kadar β-hCG harus dimonitor untuk menilai adanya potensi
maligna :
o Tiap minggu sampai β-hCG tidak terdeteksi (umumnya 8 minggu pasca
evakuasi)
o Setelah β-hCG tidak terdeteksi, pemeriksaan dilakukan tiap bulan selama 6
bulan, lalu tiap 2 bulan selama 6 bulan berikutnya.
Indikasi radiologis untuk dilakukan kuretase kedua :
o Persistensi gambaran massa vesikuler di dalam uterus.
o Evaluasi serial tidak menunjukkan penurunan volume uterus.
o Didapatkan gambaran adanya invasi miometrium.
o Persistensi kista teka lutein setelah 4 bulan pasca evakuasi mola.4
Gambar II.2.5 Pemantauan Kadar β-hCG Urin 24jam
II.3. Penyakit Trofoblas Ganas
a. Definisi
Penyakit trofoblas ganas ditandai oleh proliferasi trofoblas yang persisten diluar
kehamilan. Secara histopatologis, dapat dibedakan menjadi dua kelompok, yaitu :
1. Penyakit trofoblas ganas jenis villosum (mola invasif).
Merupakan penyakit trofoblas ganas yaNg masih mengandung villus-villus
khorialis.
13
2. Penyakit trofoblas ganas non villosum
Merupakan spektrum penyakit trofoblas ganas di mana tidak dijumpai villi-villi
khorialis. Meliputi khoriokarsinoma dan Plasental Site Trophoblastic Tumor
(PSTT).
b. Manifestasi Klinis dan Diagnosis
Umumnya muncul setelah suatu mola hidatidosa, abortus, atau kehamilan normal.
Menimbulkan invasi lokal dan dapat bermetastasis ke organ jauh (terutama pada
khoriokarsinoma).
Gejala dan tanda yang dapat ditemukan :
o Amenorea, diikuti oleh perdarahan per vaginam disfungsional.
o Kadar β-hCG yang persisten atau justru meningkat setelah evakuasi suatu
kehamilan, baik kehamilan mola maupun kehamilan normal.
o Pembesaran uterus.
o Kista teka lutein ovarium akibat efek hiperstimulasi β-hCG.
Selain itu dapat ditemukan gejala-gejala akibat metastasis ke organ lain, yaitu :
o Hemoptisis, nyeri dada, dan distress pernafasan akibat metastasis paru.
o Nyeri dan perdarahan intraperitoneum akibat metastasis hati.
o Defisit neurologis akibat metastasis otak.
Kriteria diagnosis yang disetujui untuk penyakit trofoblas ganas, yaitu :
o Terjadi grafik peningkatan β-hCG paling sedikit 4x (hari 1, 7, 14, dan 21) atau
peningkatan secara bertahap selama 2 minggu atau lebih; dan
o Ditemukannya bukti metastasis paru pada pemeriksaan radiologis.
Pemeriksaan radiologis berperan dalam skrining pada pasien dengan peningkatan
β-hCG serta untuk deteksi metastasis jauh.
14
Gambar II.1.1. Khoriokarsinoma
Gambar II.1.2. Mikroskopik Mola Invasif dan Khoriokarsinoma
c. Stadium
Untuk kepentingan terapi dan prognosis, FIGO dan WHO telah mengembangkan
sistem staging klinis dari penyakit trofoblas ganas.
FIGO menyatakan semua diagnosis penyakit trofoblas ganas harus dilengkapi
dengan staging yang dinyatakan dengan angka Romawi diikuti dengan jumlah
angka resiko. Kedua angka ini dipisahkan oleh tanda baca titik dua. (misalnya :
stadium II:9 di mana angka II menandakan staging dan angka 9 menandakan
jumlah resiko).
15
Tabel II.3.1. Stadium Klinis Penyakit Trofoblas Ganas berdasarkan FIGO 2000
Stadium Deskripsi
I
II
III
IV
Penyakit terbatas pada uterus
NTG meluas keluar dari uterus tetapi terbatas pada
organ genitalia (adneksa, vagina, ligamentum
latum)
NTG meluas ke paru-paru dengan atau tanpa
melibatkan saluran genitalia
Metastase ke tempat lain
Untuk stratifikasi resiko (prognostic scoring), FIGO menggabungkan stratifikasi
resiko WHO dengan stratifikasi FIGO yang lama (1992), menjadi stratifikasi
resiko revisi FIGO 2000 (Revised 2000 FIGO Prognostic Scoring).
16
Tabel II.3.2 Sistem Skoring WHO untuk Penyakit Trofoblas Ganas
0 1 2 3
Usia (tahun)
Kehamilan sebelumnya
Jarak diagnosis dengan awal
kehamilan (bulan)
Kadar β-hCG (IU/L) sebelum
terapi
Ukuran tumor dan uterus (cm)
Lokasi metastasis
Jumlah metastasis
Kemoterapi sebelumnya
≤40
Mola hidatidosa
<4
<1000
<3
-
Paru
0
-
>40
Abortus
4-6
1000-
10.000
3-5
Limpa,
ginjal
1-4
1 obat
-
Aterm
7-12
10.000-
1000.000
>5
Saluran
cerna, hati
5-8
≥ 2 obat
-
-
>12
> 100.000
-
Otak
>8
-
Interpretasi : - PTG resiko rendah : skor < 7
- PTG resiko tinggi : skor ≥ 7
II.3.1. Mola Invasif
a. Definisi
Pertumbuhan trofoblas yang berlebihan disertai penetrasi komponen
trofoblas, termasuk villus khorialis ke dalam miometrium.
Secara patologi anatomis, penyakit ini ditandai oleh adanya :
o Invasi massa tumor ke jaringan di bawahnya.
o Proliferasi trofoblas yang berlebihan, dan
o Masih adanya gambaran villi khorialis.
b. Manifestasi Klinis dan Perjalanan Penyakit
Dijumpai pada wanita usia subur.
Umumnya berasal dari mola hidatidosa (50%); dapat pula muncul setelah
abortus (25%) dan kehamilan normal atau ektopik (25%).
Gejala dan tanda yang dapat ditemukan :
17
o Perdarahan uterus disfungsional; dapat menimbulkan perdarahan masif,
umumnya setelah evakuasi suatu mola hidatidosa.
o Kadar β-hCG yang persisten atau justru meningkat.
o Pembesaran uterus yang teraba lembek, dengan bahaya ruptur uteri.
o Kista teka lutein ovarium akibat efek hiperstimulasi β-hCG.
o Demam dan tanda-tanda sepsis dapat ditemukan bila terjadi rupture uteri.
Menimbulkan invasi lokal ke miometrium, peritoneum, parametrium, atau
vagina.
Jarang menimbulkan metastasis jauh.
Respon baik terhadap terapi (kemoterapi), dengan angka kesembuhan >
95%.
c. Pendekatan Diagnosis
Diagnosis didasarkan pada kadar β-hCG yang persisten atau justru
meningkat setelah evakuasi suatu kehamilan mola hidatidosa.
Pemeriksaan radiologis umumnya kurang mampu membedakan mola
invasif dari mola hidatidosa, kecuali bila telah terjadi invasi ke parametrium
dan organ pelvis.
Petunjuk diagnostik :
o Tumor yang hipervaskularisasi.
o Massa padat endometrium dengan area-area kistik punktata (4-5mm),
dan invasi ke miometrium, parametrium, atau organ pelvis disekitarnya.
o Area abnormal fokal pada miometrium.
o USG umumnya digunakan sebagai modalitas diagnostik awal.
o CT scan dan MRI digunakan terutama untuk mendeteksi adanya
metastasis jauh.
o MRI memiliki kelebihan dalam mengevaluasi invasi miometrium.5
18
II.3.2. Khoriokarsinoma
a. Definisi
Khoriokarsinoma merupakan neoplasma dari sel trofoblast plasenta
yang invasif. Koriokarsinoma terdiri dari sejumlah sel yang menginvasi
jaringan sekitar dan menyebar melalui rongga vascular. Secara
mikroskopis, neoplasma terdiri dari invasif proliferasi tanpa villi dari
syncytiotrophoblast dan cytotrophoblast yang dikelilingi oleh jaringan
nekrosis dan perdarahan. Terdapat intermediate trophoblastic
multinucleated giant cell, pembesaran inti dan mitosis yang abnormal.
Kebanyakan khoriokarsinoma memiliki cytogenetic aneuploidi.4
Khoriokarsinoma merupakan tumor ganas yang terdiri dari lapisan-
lapisan sel sitotrofoblas dan sinsitiotrofoblas dengan perdarahan, nekrosis,
dan invasi pembuluh darah yang jelas. Tumor ini digolongkan sebagai
karsinoma epitel korionik tetapi pola pertumbuhan dan metastasisnya
bersifat sarkoma.3
Khoriokarsinoma adalah keganasan sel epitel khorionik sebagai
akibat sekunder dari pertumbuhan invasif trofoblas dan erosi pembuluh
darah. Karakteristiknya tidak dijumpai gambaran villi khorialis dan
umumnya disertai metastasis jauh.4
Metastasisnya seringkali terjadi pada tahap dini dan hematogen
karena afinitas sel-sel trofoblas terhadap pembuluh darah. Tempat
metastasis paling sering adalah paru-paru (75%) dan vagina (sekitar 50%).
Kista teka lutein ovarium dapat ditemukan pada sepertiga kasus. Metastasis
pada paru-paru memberikan empat gambaran khas : pola alveolar atau
“badai salju”, densitas bulat, efusi pleura, serta emboli akibat oklusi arteri
pulmoner dan dapat menyebabkan hipertensi pulmoner.3
Transformasi malignant pada GTD terdiri dari banyak tahap dari
perubahan seri genetik termasuk aktivasi onkogen dan inaktivasi tumor
suppresor gen. Bagaimanapun, karena sel trophoblastic, secara alami,
membelah secara cepat dan menginvasi, peningkatan expresi gen ini secara
langsung mengontrol fungsi sel. Perubahan dari gen secara signifikan
secara pathogenesis dan transformasi malignan dari GTD masih belum
dapat dijelaskan secara pasti.5-6
19
b. Manifestasi Klinis
Gejala dan tanda yang sering dijumpai :
o Peningkatan kadar β-hCG di luar kehamilan.
o Perdarahan uterus disfungsional.
o Bila terjadi metastasis ke paru dapat timbul gejala sesak nafas dan
hemoptisis.4
Metastasis :
Metastasis terjadi dini dan umumnya hematogenik :
Paru : 60-95%
Vagina : 40-50%
Vulva serviks : 10-15%
Otak : 5-15%
Liver : 5-15%
Ginjal : 0-5%
Spleen : 0-5%
Usus : 0-5%
Metastase pada :
Liver dan otak tergolong resiko tinggi
Metastase vagina “phatognomonis” khoriokarsinoma, sekalipun masih
bentuk mola hidatidosa.5
Konsentrasi beta hCG tinggi di atas 100.000 mIU/ml, dalam urin 24 jam
Konsentrasi dalam serum lebih dari 40.000 mIU/ml
c. Pendekatan Diagnosis
Petunjuk diagnosis adalah adanya proses invasif ada endometrium disertai
peningkatan kadar β-hCG serta metastasis ekstrauterin. USG biasanya umum
digunakan sebagai modalitas diagnostik awal, namun mungkin tidak dapat
membedakan dari mola hidatidosa. Foto polos dada dapat digunakan untuk
mendeteksi kemungkinan metastasis paru, namun CT scan umumnya lebih
sering dipakai karena sensitivitasnya yang lebih tinggi. CT scan dan MRI
digunakan terutama untuk mendeteksi adanya metastasis jauh.
20
d. Pemeriksaan USG, CT scan dan MRI
Ultrasonografi (USG)
Terlihat massa kistik ireguler, berbagai ukuran (akibat adanya
perdarahan atau nekrosis), mengisi rongga rahim, menginvasi miometrium,
serviks atau vagina. Dapat menyerupai gambaran mola hidatidosa komplit.
USG Doppler : peningkatan kecepatan dengan penurunan hambatan (low
impedance, high diastolic flow).4
CT scan
Terlihat adanya pembesaran uterus, material kistik dalam cavum uteri
yang menginvasi miometrium, dan nodul paru ireguler disertai gambaran
ground glass dengan halo di sekitarnya yang menunjukkan adanya
perdarahan.
MRI
Seperti CT scan tapi memberikan gambaran batas massa yang lebih
jelas.
e. Terapi
Terapi bergantung pada stadiumnya, tapi umumnya meliputi evakuasi
massa, pembedahan, dan kemoterapi.
Terapi Khoriokarsinoma tergantung dari metastasis yang terjadi :
1. Pada khoriokarsinoma tanpa metastasis
Histerektomi
Bilateral oophorektomi
Tambahan kemoterapi
Indikasi histerektomi :
- Khemoterapi resisten
- Granda multipara/umur diatas 40 tahun
Untuk perdarahan lokal dilakukan :
- Angiografi disertai embolisasi arteria/vena sehingga pembuluh
darahnya tertutup dan perdarahan dapat dihentikan.
2. Metastasis pada sentral nervus sistem
21
Untuk memastikan lokalisasinya dilakukan :
- Computerized tomography scanning ( CT scan)
- Magnetic resonance imaging (MRI)
Terapi yang dianjurkan adalah :
- Radiasi yang dapat :
Menghentikan perdarahan
Menyebabkan dehidrasi sel tumor – membunuhnya.
3. Metastasis pada liver
Merupakan metastasis yang serius dan mempunyai resiko tinggi
Komplikasi metastasis pada liver adalah :
- Gangguan fungsi liver yang serius
- Perdarahan mendadak sampai fatal
Terapi radiasi liver secara menyeluruh dapat menghentikan perdarahan
4. Metastasis pada paru
Metastasis masif pada paru dengan gejala :
- 50% foto paru buram dan tak berfungsi
- Anemia
- Nyeri pada dada
Terapi : extrakorporal (di luar badan)
- Perfusi oksigen
- Obat antikoagulasia, mengurangi bahaya perdarahan.6
Terapi berdasarkan stadium :
a. Pengobatan PTG Risiko Rendah
Kriteria PTG risiko rendah adalah Skor WHO ≤6. Stadium FIGO I, II, dan
III. Diberikan kemoterapi tunggal (single agent).
o Metotrexate 0,4 mg/kgBB selama 5 hari, diulangi setiap dua minggu. Ini
merupakan protokol asli dalam GTD dan digunakan di Yale. Hal ini juga
merupakan protokol di The Brewer Trophoblast Center Chicago dengan
angka kegagalan 10%.
o Metotrexate dan Leucovorin. Metotrexate 1,0 mg/kgBB setiap hari dengan
empat dosis Leucovorin 0,1 mg/kg 24 jam setelah setiap dosis metotrexate.
22
Protokol ini digunakan di Inggris dan Amerika Serikat dengan angka
kegagalan 20-25%.
o Metotrexate 50 mg/m2 setiap dua minggu. Regimen ini memiliki angka
kegagalan 30%. Bila terjadi dapat diberikan Metotrexate 0,4 mg/kgBB
selama lima hari atau diganti dengan Actinomycin-D 12 mg/kg selama lima
hari.
o Actinomycin-D 12, 25 mg/m2 setiap dua minggu (pulse regimen). Protokol
ini memiliki angka kegagalan 20%. Ini merupakan langkah alternatif dari
pemberian Metotrexate secara mingguan.
o Actinomycin –D 12 mg/kgBB IV setiap hari selama lima hari, diulangi
setiap dua minggu. Protokol ini merupakan alternatif dari protokol
pemberian Metotrexate selama lima hari. Dapat digunakan pada pasien
dengan disfungsi hepar dengan angka kegagalan 8%.
o Metotrexate 250 mg infus selama dua belas jam. MTX ini merupakan
bagian dari protokol EMA-CO dengan angka kegagalan terapi 30%.
Catatan : Actinomycin-D menyebabkan kerusakan yang parah pada
kulit jika terinfiltrasi dan harus disuntikkan melalui infus intravena yang
baru. Jika terjadi ekstravasasi, area ini harus diinfiltrasi dengan 100 mg
hidrocortisone dan 2 cc xylocaine 1%.
Pemeriksaan serial darah lengkap, platelet, kreatinin, BUN dan SGOT
dilakukan terutama pada hari pertama pemberian pengobatan.
Pengukuran kadar β-hCG setiap minggu dilakukan setelah pemberian
kemoterapi, kurva regresi kadar β-hCG merupakan dasar utama pemberian seri
kemoterapi berikutnya. Setelah pemberian kemoterapi pertama.
Kemoterapi berikutnya diberikan setelah ada penurunan yang progresif dari
kadar β-hCG.
Tidak ada patokan pasti interval pemberian seri kemoterapi berikutnya.
Seri kedua pemberian kemoterapi diberikan pada keadaan β-hCG yang
meningkat.
Kadar β-hCG mendatar (plateau) selama tiga minggu, atau naik lagi.
23
Kadar β-hCG tidak menurun 1 log selama delapan belas hari setelah
pemberian kemoterapi pertama.
Bila respons setelah pemberian pertama adekuat dosis yang diberikan tetap
sama. Respons dikatakan adekuat bila ada penurunan kadar βhCG sebesar 1
log setelah pemberian kemoterapi, bila respons tidak adekuat dosis MTX
ditingkatkan 1,0 sampai 1,5 mg/kgBB. Bila setelah pemberian dua kali
respons tetap tidak adekuat maka bisa dikatakan resisten. MTX selanjutnya
diberikan Act-D, dan bila setelah satu pemberian Act-D tidak terjadi
penurunan kadar β-hCG sebesar 1 log maka dikatakan resisten terhadap Act-
D secara agen tunggal, dan penderita memerlukan kemoterapi kombinasi.5
b. PTG Risiko Tinggi
Kriteria PTG risiko tinggi adalah Stadium FIGO I, II, III dengan Skor
WHO ≥ 7 atau Stadium 4.
Pasien dengan risiko tinggi diterapi dengan kombinasi kemoterapi yaitu
EMA-CO sebagai terapi primer. EMA-CO adalah Etoposide, Metotrexate
dengan Leucovorin dan Actinomycin, pemberian pada hari kesatu dan kedua,
sedangkan Cyclophospamide dan Vincristine (Oncovin) diberikan pada hari ke
delapan. Sejauh ini, terapi kombinasi macam ini lebih dapat diterima dan efek
toksiknya lebih rendah dibanding kemoterapi Metotrexate, Actinomycin, dan
Cytoxan (MAC)-C sebenarnya adalah Chlorambucil. EMA-CO juga telah
mendesak keberadaan regimen Bagshawe II. Namun, beberapa senter kembali
menggunakan MAC karena risiko EMA-CO berupa leukemia yang terjadi
setelah lebih dari enam kali pemberian.
Pasien harus dimonitor ketat dan pemberian EMA-CO diulangi sampai
terjadi remisi. Neupogen biasanya diberikan untuk mempertahankan sel darah
putih.
Kemoterapi tetap diberikan dua sampai tiga seri setelah bila hCG tidak
terdeteksi pertama kali. Kadar hCG yang negatif menandakan bahwa jumlah
keberadaan sel-sel ganas dalam tubuh kurang dari 100 juta sel.
Fokus metastatik tertentu membutuhkan terapi spesifik. Contohnya pada
lesi di otak diterapi dengan meningatkan dosis Metotrexate sampai 1g/m2 di
protokol EMA-CO. Tergantung dari besar dan jumlah metastase pada otak,
pasien dapat diterapi dengan radiasi sebesar 25-30 grey atau dilakukan eksisi.
24
Pasien dengan metastase pada liver dapat dilakukan radiasi sebesar 20 grey
atau infus arteri hepar. Radiasi ini digunakan untuk mencegah perdarahan yang
hebat bukan sekedar untuk mengontrol penyakitnya.
Pasien yang resisten dengan EMA-CO atau multiagen kemoterapi yang
lain bisa diterapi dengan protokol EMA-EP. Protokol ini adalah EMA
ditambah dengan Etoposide dan Platinum, untuk kasus yang resisten pada
EMA-EP, Taxol dengan Cisplatin alternating dengan Taxol-Etoposide atau
Taxol-5-FU atau Iphosphospamide-Cisplatinum-Etoposide (ICE) atau
Vinblastine-Etoposide-Cisplastin telah digunakan.5
25
Stage IFaktor risiko ≤6
Stage IIFaktor risiko ≤6
Stage IIIFaktor risiko ≤6
Agen tunggal kemoterapi
Revolusi
Ikuti secara klinis dan dengan kadar hCG Selama 12 bulan sebelum mengijinkan hamil
Ubah jadwal atau agent kemoterapi dengan satu agent(Jika regular Act-D atau MTX ubah menjadi 5 hariJika tetap gagal ganti untuk mengganti Act-D atau MTX)
Tidak respon
Tidak respon
Kombinasi kemoterapi (putuskan TAH dengan uterine lesion)Tidak respon
Diagram III.3.2
Komplet atau parsial hydatidoform mole persisten hCGGestasional trofoblastik neoplasma didiagnosa dari metastase dan peningkatan hCGHistologi diagnosa choriocancer setelah hasil aterm
Diagnosa sebagai PTG
Investigasi staging dan skor faktor risiko
hCG, CBC, platelet, BUN, creatinin, LFT, pembekuan (jika ada indikasi), foto dada, USG pelvis.Jika foto dada positif CT/USG abdoment, particulary hari, CT/MRI otak jika ada indikasi
Stage IVFaktor risiko ≥7
Diagram II.3.1 Panduan untuk Managemen Trofoblastik Neoplasia
26
Post hydatidiform moleStage IV atau faktor resiko ≥7
Nonmolar GTN didiagnosis dari metastase
Investigasi, staging dan skor faktor risiko
hCG, CBC, platelet, BUN, creatinin, LFT, pembekuan (jika ada indikasi), foto dada, USG pelvis.Jika foto dada positif CT/USG abdoment, particulary hari, CT/MRI otak jika ada indikasi
Stage I, II, III dengan faktor risiko ≥7atau stage IV
Multipel agen kemoterapi EMA-CO)(untuk metastase serebral dosis MTX ditingkatkan sampai 1 g/m2)
Resolusi Neoplasma persisten
Ikuti dengan hCG dan surveilance klinis selama 1 tahunPutuskan pembedahan untuk isolated lesi yang resectable
(umumnya paru, otak dan hati)
Lini kedua multipel agen kemoterapi (EP-EMA)
Tidak respon
Putuskan Taxoll5-FU iphosphamide
Konsul pusat trofoblas
Diagram III.3.2 Panduan untuk Manajemen Trofoblastik Neoplasia
27
f. Prognosis
Prognosis umumnya baik (survival rate 90%); prognosis lebih buruk
pada splid tumor nest serta histopatologi jaringan dengan pleomorfisme dan
aktivitas mitotik yang tinggi.4
Kesembuhan khoriokarsinoma, dengan kemoterapi mendekati 90%.
Kesembuhannya kurang 50% mempunyai masalah dan digolongkan :
Khoriokarsinoma dengan metastasis tergolong resiko tinggi.
Memerlukan kombinasi beberapa khemoterapi.
Kategori khoriokarsinoma dengan resiko tinggi adalah :
- hCG urin/24 jam lebih dari 100.000 IU
- penyakit telah melebihi 4 bulan
- metastasis pada liver dan otak
- pengobatan terdahulu gagal
- terjadi pada kehamilan aterm
- serum β-hCG lebih dari 40.000 mIU/ml
g. Evaluasi Khoriokarsinoma pasca Kemoterapi
Pasca kemoterapi, monitoring dilakukan dengan :
- Pemantauan kadar β-hCG sampai tidak terdeteksi setelah 3 minggu
berturut-turut.
- Pemantauan secara radiologis, meliputi :
Pemantauan volume tumor secara serial
Evaluasi terhadap invasi parametrium dan tanda-tanda ancaman
perforasi
Evaluasi terhadap kista teka lutein yang persisten
Perubahan gambaran vaskularisasi pada USG Doppler
Perubahan lokasi metastasis
Manajemen Pasca Evakuasi
1. Monitor kadar β-hCG
Tiap minggu sekali sampai β-hCG tidak terdeteksi yang pada
umumnya delapan minggu pasca evakuasi. Jika terdapat anemia atau
infeksi yang harus diobati.
28
Saat β-hCG sudah tak terdeteksi, pemeriksaan dilakukan tiap bulan
selama enam bulan, lalu tiap dua bulan sekali selama enam bulan
berikutnya untuk memastikan hCG tetap tidak terdeteksi.
2. Pengukuran subunit β-hCG. Kadar β-hCG ≤ 5 mIu/ml penting untuk
monitor.
3. Pemakaian kontrasepsi, lebih baik dalam bentuk pil. Jika penurunan β-hCG
konstan, pasien boleh hamil setelah enam bulan. Jika penurunan kadar β-
hCG hanya sedikit-sedikit maka perlu waktu lebih lama lagi untuk hamil.
Perlu dilakukan USG pada kehamilan awal dan pemeriksaan kadar β-hCG.
Pemantauan kadar β-hCG dilakukan sampai kadarnya negatif setelah
melahirkan.
4. Pasien dengan usia kehamilan empat minggu yang besarnya lebih dari
normal dan adanya kista theca lutein berpeluang 50% memiliki trofoblastik.
5. Jika pasien diterapi dengan menggunakan kemoterapi untuk GTD persisten,
pasien dapat dianggap mengalami remisi setelah titer β-hCG negatif selama
tiga minggu berturut-turut. Setelah remisi, follow up masih harus dilakukan
untuk mengamati terjadinya rekurensi.1
29
BAB III
KESIMPULAN
Penyakit trophoblas merupakan suatu kelainan berupa proliferasi sel trophoblas
kehamilan yang abnormal. Petanda tumor yang khas pada penyakit ini adalah subunit β
human Chorionic Gonadotropin (β-hCG) dan memiliki kecenderungan invasi lokal dan
penyebaran. Neoplasia trofoblas gestasional (NTG - Neoplasia Trophoblastic Gestasional)
adalah bagian dari PTG yang berkembang menjadi jejas keganasan.
Khoriokarsinoma adalah keganasan sel epitel khorionik sebagai akibat sekunder dari
pertumbuhan invasif trofoblas dan erosi pembuluh darah. Karakteristiknya tidak dijumpai
gambaran villi khorialis dan umumnya disertai metastasis jauh. Kurang lebih 50% terjadi
setelah mola hidatidosa, 25% setelah abortus, 22,5% setelah kehamilan normal, dan 2,5%
setelah kehamilan ektopik. Gejala dan tanda yang sering dijumpai : peningkatan kadar β-hCG
di luar kehamilan, perdarahan uterus disfungsional, dan bila terjadi metastasis ke paru dapat
timbul gejala sesak nafas dan hemoptisis. Perlunya kemampuan menilai gejala klinis,
pendekatan diagnosis dan penatalaksanaan yang tepat diharapkan mampu mencegah invasi
dan metastasis lebih jauh.
30
DAFTAR PUSTAKA
1. Cunningham F. Gary, et al. Obstetri Williams Vol.2 Ed 23. Alih bahasa Brahim U Pendith.
Jakarta : EGC.2013.
2. Andrijono. Sinopsis kanker ginekologi. Jakarta. 2003.
3. Prawirohardjo Sarwono. Ilmu kebidanan. Edisi keempat. Jakarta : PT Bina Pustaka
Sarwono Prawirohardjo.2010.
4. Rasjidi Imam, Muljadi Rusli, Chayono Kristianus. Imaging ginekologi onkologi. Jakarta :
Sagung Seto. 2010.
5. Rasjidi Imam. Panduan penatalaksanaan kanker ginekologi berdasarkan evidence base.
Jakarta : EGC. 2007.
6. Manuaba Ida AC, Manuaba Ida Bagus GF, Manuaba Ida Bagus G. Buku ajar penuntun
kuliah ginekologi. Den Pasar : CV Trans Info Media. 2010.
7. Rasjidi Imam. Deteksi dini kanker pada wanita. Jakarta: Sagung Seto. 2009.
31