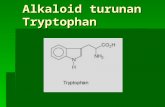
Damas Alkaloid
-
Upload
damas-anjar-purnama -
Category
Documents
-
view
174 -
download
4
description
Transcript of Damas Alkaloid

LAPORAN PRAKTIKUM
KIMIA FARMASI ANALITIK I
ALKALOID dan ANESTESI LOKAL
Disusun oleh
31111064 Damas Anjar Purnama
PROGRAM STUDI FARMASI
SEKOLAH TINGGI KESEHATAN
BAKTI TUNAS HUSADA
TASIKMALAYA
2013

A. Dasar Teori
a. Pengertian
Alkaloid adalah Kelompok senyawa yang mengandung nitrogen dalam
bentuk gugus fungsi amin. Pada umumnya, alkaloid mencakup senyawa
bersifat basah yang mengandung 1/ lebih atom nitrogen, biasanya dalam
gabungan sebagai bagian dari sistem siklik. Alkaloid biasanya beracun, jadi
banyak digunakan dalam bidang pengobatan. Alkaloid biasanya tanwarna,
sering kali bersifat optis aktif, kebanyakan berbentuk kristal tapi hanya sedikit
yang berupa cairan pada suhu kamarPada umumnya, alkaloid tidak sering
terdapat dalam gymospermae, paku-pakuan, lumut dan tumbuhan rendah.Suatu
Alkaloid secara umum mengandung paling sedikit satu buah atom nitrogen
yang bersifat basa dan merupakan bagian dari cincin heterosiklik. Kebanyakan
alkaloid berbentuk padatan kristal dengan titik lebur tertentu atau mempunyai
kisaran dekomposisi. Alkaloid dapat juga berbentuk amorf atau cairan. Dewasa
ini telah ribuan senyawa alkaloid yang ditemukan dan dengan berbagai variasi
struktur yang unik, mulai dari yang paling sederhana sampai yang paling sulit.
Dari segi biogenetik, alkaloid diketahui berasal dari sejumlah kecil asam
amino yaitu ornitin dan lisin yang menurunkan alkaloid alisiklik, fenilalanin
dan tirosin yang menurunkan alkaloid jenis isokuinolin, dan triftopan yang
menurunkan alkaloid indol. Reaksi utama yang mendasari biosintesis senyawa
alkaloid adalah reaksi mannich antara suatu aldehida dan suatu amina primer
dan sekunder, dan suatu senyawa enol atau fenol. Biosintesis alkaloid juga
melibatkan reaksi rangkap oksidatif fenol dan metilasi. Jalur poliketida dan
jalur mevalonat juga ditemukan dalam biosintesis alkaloid.
b. Sifat-Sifat Alkaloid
Beberapa sifat dari alkaloid yaitu :
1. Mengandung atom nitrogen yang umumnya berasal dari asam amino dan
golongan heterogen.
2. Umumnya berupa Kristal atau serbuk amorf.
3. Alkaloid yang berbentuk cair yaitu konini, nikotin dan spartein.

4. Dalam tumbuhan berada dalam bentuk bebas, dalam bentuk N-oksida atau
dalam bentuk garamnya.
5. Umumnya mempunyai rasa yang pahit.
6. sering beracun.
7. bersifat optis aktif dan berupa sistim siklik
8. Alkaloid dalam bentuk bebas tidak larut dalam air, tetapi larut dalam
kloroform, eter dan pelarut organik lainnya yang bersifat relative nonpolar.
9. Alkaloid dalam bentuk garamnya mudah larut dalam air.
10. Alkaloid bebas bersifat basa karena adanya pasangan elektron bebas pada
atom N-nya.
11. biasanya banyak digunakan dibidang farmasi.
12. sampel yang mengandung alkaloid setelah drx akan berwarna merah.
a. Sifat-Sifat Fisika
Umumnya mempunyai 1 atom N meskipun ada beberapa yang
memiliki lebih dari 1 atom N seperti pada Ergotamin yang memiliki 5
atom N. Atom N ini dapat berupa amin primer, sekunder maupun tertier
yang semuanya bersifat basa (tingkat kebasaannya tergantung dari struktur
molekul dan gugus fungsionalnya) Kebanyakan alkaloid yang telah
diisolasi berupa padatan kristal tidak larut dengan titik lebur yang tertentu
atau mempunyai kisaran dekomposisi. Sedikit alkaloid yang berbentuk
amorf dan beberapa seperti; nikotin dan koniin berupa cairan. Kebanyakan
alkaloid tidak berwarna, tetapi beberapa senyawa yang kompleks, species
aromatik berwarna (contoh berberin berwarna kuning dan betanin
berwarna merah). Pada umumnya, basa bebas alkaloid hanya larut dalam
pelarut organik, meskipun beberapa pseudoalkalod dan protoalkaloid larut
dalam air. Garam alkaloid dan alkaloid quartener sangat larut dalam air.
b. Sifat-Sifat Kimia
Kebanyakan alkaloid bersifat basa. Sifat tersebut tergantung pada
adanya pasangan elektron pada nitrogen.Jika gugus fungsional yang
berdekatan dengan nitrogen bersifat melepaskan elektron, sebagai contoh;
gugus alkil, maka ketersediaan elektron pada nitrogen naik dan senyawa
lebih bersifat basa. Hingga trietilamin lebih basa daripada dietilamin dan

senyawa dietilamin lebih basa daripada etilamin. Sebaliknya, bila gugus
fungsional yang berdekatan bersifat menarik elektron (contoh; gugus
karbonil), maka ketersediaan pasangan elektron berkurang dan pengaruh
yang ditimbulkan alkaloid dapat bersifat netral atau bahkan sedikit asam.
Contoh ; senyawa yang mengandung gugus amida.
Kebasaan alkaloid menyebabkan senyawa tersebut sangat mudah
mengalami dekomposisi, terutama oleh panas dan sinar dengan adanya
oksigen. Hasil dari reaksi ini sering berupa N-oksida. Dekomposisi
alkaloid selama atau setelah isolasi dapat menimbulkan berbagai persoalan
jika penyimpanan berlangsung dalam waktu yang lama. Pembentukan
garam dengan senyawa organik (tartarat, sitrat) atau anorganik (asam
hidroklorida atau sulfat) sering mencegah dekomposisi. Itulah sebabnya
dalam perdagangan alkaloid lazim berada dalam bentuk garamnya.
c. Penggolongan Alkaloid
Alkaloida tidak mempunyai tatanan sistematik, oleh karena itu, suatu
alkaloida dinyatakan dengan nama trivial, misalnya kuinin, morfin dan
strikhnin. Hampir semua nama trivial ini berakhiran –in yang mencirikan
alkaloida. Klasifikasi alkaloida dapat dilakukan berdasarkan beberapa cara,
yaitu :
1. Berdasarkan jenis cincin heterosiklik nitrogen yang merupakan bagian
dari struktur molekul. Berdasarkan hal tersebut, maka alkaloida dapat
dibedakan atas beberapa jenis sperti alkaloida pirolidin, alkaloida
piperidin, alkaloida isokuinolin, alkaloida kuinolin, dan alkaloida indol.
2. Berdasarkan jenis tumbuhan darimana alkaloida ditemukan. Cara ini
digunakan untuk menyatakan jenis alkaloida yang pertama-tama
ditemukan pada suatu jenis tumbuhan. Berdasarkan cara ini, alkaloida
dapat dibedakan atas beberapa jenis yaitu aklakoida tembakau, alkaloida
amaryllidaceae, alkaloida erythrine dan sebagainya. Cara ini mempunyai
kelemahan, yaitu : beberapa alkaloida yang berasal dari tumbuhan
tertentu dapat mempunyai struktur yang berbeda-beda.
3. Berdasarkan asal-usul biogenetik. Cara ini sangat berguna untuk
menjelaskan hubungan antara berbagai alkaloida yang diklasifikasikan

berdasarkan berbagai jenis cincin heterosiklik. Dari biosintesa alkaloida,
menunjukkan bahwa alkaloida berasal hanya dari beberapa asam amino
tertentu saja. Berdasarkan hal tersebut, maka alkaloida dapat dibedakan
atas tiga jenis utama, yaitu :
a. Alkaloida alisiklik yang berasal dari asam-asam amino ornitin dan
lisin.
b. Alkaloida aromatik jenis fenilalanin yang berasal dari fenilalanin,
tirosin dan 3,4-dihidrofenilalanin.
c. Alkaloida aromatik jenis indol yang berasal dari triptofan.
4. Sistem klasifikasi berdasarkan Hegnauer yang paling banyak diterima,
dimana alkaloida dikelompokkan atas :
a. Alkaloida sesungguhnya
Alkaloida ini merupakan racun, senyawa tersebut menunjukkan
aktivitas fisiologis yang luas, hamper tanpa terkecuali bersifat basa,
umumnya mengandung nitrogen dalam cincin heterosiklik, diturunkan
dari asam amino, biasanya terdapat dalam tanaman sebagai garam
asam organik. Beberapa pengecualian terhadap aturan tersebut adalah
kolkhisin dan asam aristolokhat yang bersifat bukan basa dan tidak
memiliki cincin heterosiklik dan alkaloida quartener yang bersifat agak
asam daripada bersifat basa.
b. Protoalkaloida
Protoalkaloida merupakan amin yang relative sederhana dimana
nitrogen asam amino tidak terdapat dalam cincin heterosiklik.
Protoalkaloida diperoleh berdasarkan biosintesa dari asam amino yang
bersifat basa. Pengertian amin biologis sering digunakan untuk
kelompok ini.
c. Pseudoalkaloida
Pseudoalkaloida tidak diturunkan dari prekusor asam amino. Senyawa
ini biasanya bersifat basa. Ada dua seri alkaloida yang penting dalam
kelompok ini yaitu steroidal dan purin.

d. Isolasi Alkaloid
Satu-satunya sifat kimia alkaloid yang paling penting adalah kebasaannya.
Metode pemurnian dan pencirian ialah umumnya mengandalkan sifat ini, dan
pendekatan khusus harus dikembangkan untuk beberapa alkaloid misalnya
rutaekarpina, kolkhisina, risinina) yang tidak bersifat basa.
Umumnya isolasi bahan bakal sediaan galenik yang mengandung alkaloid
dilakukan dengan beberapa cara, yaitu :
Dengan menarik menggunakan pelarut-pelarut organik berdasarkan azas
Keller. Yaitu alkaloida disekat pada pH tertentu dengan pelarut organik. Prinsip
pengerjaan dengan azas Keller yaitu alkaloida yang terdapat dalam suatu bakal
sebagai bentuk garam, dibebaskan dari ikatan garam tersebut menjadi alkaloida
yang bebas. Untuk itu ditambahkan basa lain yang lebih kuat daripada basa
alkaloida tadi. Alkaloida yang bebas tadi diekstraksi dengan menggunakan
pelarut – pelarut organic misalnya Kloroform. Tidak dilakukan ekstraksi
dengan air karena dengan air maka yang masuk kedalam air yakni garamgaram
alkaoida dan zat-zat pengotor yang larut dalam air, misalnya glikosida-
glikosida, zat warna, zat penyamak dan sebagainya. Yang masuk kedalam
kloroform disamping alkaloida juga lemaklemak, harsa dan minyak atsiri.
Maka setelai alkaloida diekstraksi dengan kloroform maka harus dimurnikan
lagi dengan pereaksi tertentu. Diekstraksi lagi dengan kloroform. Diuapkan,
lalu didapatkan sisa alkaloid baik dalam bentuk hablur maupun amorf. Ini tidak
berate bahwa alkaloida yang diperoleh dalam bentuk murni, alkaloida yang
telah diekstaksi ditentukan legi lebih lanjut. Penentuan untuk tiap alkaloida
berbeda untuk tiap jenisnya. Hal-hal yang harus diperhatikan pada ekstraksi
dengan azas Keller, adalah :
a. Basa yang ditambahkan harus lebih kuat daripada alkaloida yang akan
dibebaskan dari ikatan garamnya, berdasarkan reaksi pendesakan.
b. Basa yang dipakai tidak boleh terlalu kuat karena alkaloida pada umumnya
kurang stabil. Pada pH tinggi ada kemungkinan akan terurai, terutama
dalam keadaan bebas, terlebih bila alkaloida tersebut dalam bentuk ester,
misalnya : Alkaloid Secale, Hyoscyamin dan Atropin.

c. Setelah bebas, alkaloida ditarik dengan pelarut organik tertentu, tergantung
kelarutannya dalam pelarut organik tersebut.
Alkaloid biasanya diperoleh dengan cara mengekstraksi bahan tumbuhan
memakai air yang diasamkan yang melarutkan alkaloid sebagai garam, atau
bahan tumbuhan dapat dibasakan dengan natrium karbonat dan sebagainya dan
basa bebas diekstaksi dengan pelarut organik seperti kloroform, eter dan
sebagainya. Radas untuk ekstraksi sinabung dan pemekatan khusunya
digunakan untuk alkaloid yang tidak tahan panas. Beberapa alkaloid menguap
seperti,nikotina dapat dimurnikan dengan cara penyulingan uap dari
larutanmyang diabasakan. Larutan dalam air yang bersifat asam
danmmengandung alkaloid dapat dibasakan dan alkaloid diekstaksim dengan
pelarut organik , sehingga senyawa netral dan asam yang mudah larut dalam air
tertinggal dalam air. Cara lain yang berguna untuk memperoleh alkaloid dari
larutan asam adalah dengan penjerapan menggunakan pereaksi Lloyd.
Kemudian alkaloid dielusi dengan dammar XAD-2 lalu diendapkan dengan
pereaksi Mayer atau Garam Reinecke dan kemudian endapan dapat dipisahkan
dengan cara kromatografi pertukaran ion. Masalah yang timbul pada beberapa
kasus adalah bahwa alkaloid berada dalam bentuk terikat yang tidak dapat
dibebaskan pada kondisi ekstraksi biasa. Senyawa pengkompleksnya
barangkali polisakarida atau glikoprotein yang dapat melepaskan alkaloid jika
diperlakukan dengan asam.
Cara kedua dan ketiga merupakan cara yang paling umum dan cocok
untuk memisahkan campuran alkaloid. Tata kerja untuk mengisolasi dan
mengidentifikasi alkaloid yang terdapat dalam bahan tumbuhan yang
jumlahnya dalam skala milligram menggunakan gabungan kromatografi kolom
memakai alumina dan kromatografi kertas.
e. Kegunaan Alkaloida
Alkaloida telah dikenal selama bertahun-tahun dan telah menarik perhatian
terutama karena pengaruh fisiologisnya terhadap binatangmenyusui dan
pemakainnya di bidang farmasi, tetapi fungsinya dalam tumbuhan hampir sama
sekali kabur. Beberapa mendapat mengenai kemungkinan perannya ialah
sebagai berikut :

1. Salah satu pendapat yang dikemukakan pertama kali, sekarang tidak dianut
lagi, ialah bahwa alkaloid berfungsi sebagai hasil buangan nitrogen seperti
urea dan asam urat hewan.
2. Beberapa alkaloid mungkin bertindak sebagai tendon penyimpanan
nitrogen meskipun banyak alkaloid ditimbun dan tidak mengalami
metabolisme lebih lanjut meskipun sangat kekurangan nitrogen.
3. Pada beberapa kasus, alkaloid dapat melindungi tumbuhan dariserangan
parasit atau pemangsa tumbuhan. Meskipun dalam beberapa peristiwa bukti
yang mendukung fungsi ini tidak dikemukakan, ini barangkali merupakan
konsep yang direka-reka dan bersifat “manusia sentries”.
4. Alkaloid dapat berlaku sebagai pengatur tumbuh karena segi struktur,
beberapa alkaloid menyerupai pengatur tumbuh. Beberapa alkaloid
merangsang perkecambahan, yang lainnya menghambat.
5. Semula disarankan oleh Liebig bahwa alkaloid, karena sebagian bersifat
basa, dapat mengganti basa mineral dalam mempertahankan kesetimbangan
ion dalam tumbuhan. Sejalan dengan saran ini, pengamatan menunjukkan
bahwa pelolohan nikotina ke dalam biakan akar tembakau meningkatkan
ambilan nitrat. Alkaloid dapat pula berfungsi dengan cara pertukaran
dengan kation tanah.

B. Alat dan bahan
Alat
- Tabung reaksi
- Rak tabung
- Pipet tetes
- Beaker glass
- Gelas ukur
- Spatel
- Pembakar Spirtus
- Kaki tiga dan kasa
Bahan
- NaOH
- FeCl3
- CuSO4
- Reagen Mayer
- Reagen Dragendorf
- HNO3
- HCl encer
- AgNO3
- CH3COOH
- Diazo A
- Diazo B
- DAB-HCl
- KMnO4
- Phenol
- Kaporit
- NH4OH
- CHCl3
- K2Cr2O7
- HgCl2
- ZnCl2
- Reagen Bouchardat
- Roux
- Titan yellow
- Korek api

C. ProsedurUji Organoleptik
Uji Organoleptik
Bentuk
Bentuk Jarum Kofeina, Quinin, Strikinin, Kodein
HCl
Serbuk
Kofein, Teofilin, Antalgin, Paracetamol, Quinin, Kodein HCl,
Atropin Sulfat, Strikinin Sulfat, Efedrin HCl, Aminophilin, Papaverin
HCl, Reservin, Pirokain HCl, Lidokain HClButiran
Aminophilin
Warna
PutihKofeina, Teofilin, Paracetamol,
Quinin, Kodein HCl, Atropin Sulfat, Strikinin, Efedrin HCl, Papaverin HCl, Reservin, Prokain, Lidokain,
INHPutih Kekuningan
Antalgin, Aminofilin
Putih agak Coklat Muda
Reservin
Kelarutan
AirTeofilin, Paracetamol, Antalgin, Strikinin Sulfat, Kodein HCl, Efedrin
HCl, Aminophilin, INH, Lidokain HCl
EtanolQuinin, Atropin Sulfat, Prokain HCl,
Lidokain HCl
KloroformKofeina, Papaverin HCl, Reservin,
Lidokain HCl
Air PanasTeofilin, Strikinin Sulfat, Kodein
HCl, Rivanol

Uji GolonganUji Golongan Xantin(Reaksi Mureksid)
Zat + H2O2 3% / KOH padar + 1 tetes HCl 25 % aduk ↑ + NH4OHUngu Merah
Alkaloid Xantin
Pereaksi Parry + Uap Ammonia PekatUngu
Teofilin
Ungu CoklatAminophilin
Zat + Piramidon + CuSO4Ungu
Teofilin
Hijau Cofein
Cokalt TuaDiuretin
MarqiusMerah Rosa
Diuretin
FeCl3Ungu
Diuretin
Dengan Cu Asetat Ungu
Aminophilin
Tidak BerwarnaTeofilin
Uji Golongan Pirazolon Dengan FeCl3 + Air
Biru Kemudian Merah lalu hilangAntalgin
Merah Coklat Antipirin
Dengan AgNO3Ungu Abu-abu
Antalgin
Ungu Piramidon
Dengan CuSO4Ungu
Aminophilin / Teofilin, Piramidon

Uji Golongan Anilin Dengan FeCl3
Hijau BiruParacetamol
Dengan HNO3 pCoklat + GasParacetamol
Dengan Kalium Bikromat + H2SO4 / HCl? Amati Warna
Zat + HCl p + Air (panaskan) + Kalium Bikromat
Esterifikasi = Bau Etil Asetat
Zat + HCl p (panaskan) (dinginkan + NaOH)Ungu
Zat + HCl 25% (panaskan) → Amati Warna + Air Brom
Uji Golongan KininReaksi Telleonci
Hijau - Merah RosaKinin
Hijau Euchinin
Reaksi Eritrosin
Reaksi IodoformEuchinin
NaOH = Merah CoklatEuchinin
Golongan Opium Reagen Marquis
Ungu
Reaksi Seluras LefortUngu
Dengan FeCl3
Biru KehijauanMorfin
Asam-asam pekat HCl / HNO3 / H2SO4
Amati Warna
Reagen Gabrietti Ungu muda → Hijau Biru

D. Data Hasil Praktikum
UJI ORGANOLEPTIKSampel 78
Uji Orgnoleptik KemungkinanBentuk Tablet
Golongan Alkaloid
Warna CoklatBau -Rasa -Kelarutan Larut NH4OH dan
air
UJI GOLONGAN
Sampel 78
Perlakuan Kemungkinan1. Sampel + HCl e + Reagen Mayer
Endapan putih2. Sampel + HCl e + Reagen
Bouchardat Endapan3. Sampel + HCl e + Reagen
Dragendorf Endapan4. Sampel + FeCl3 Ungu
INHAminofillinTheofillin
UJI IDENTIFIKASISampel 78 Perlakuan Kemungkinan
1. Sampel + 1 ml Amonia pekat + 2 ml AgNO3 Endapan hitam
2. Sampel + Roux Hijau stabil
Theofillin
Uji Golongan LainReaksi Vitalli
Zat + HNO3 (panaskan) di wb + KOH - Etanol Ungu + Aseton = tetap
Atropin
Ungu + Aseton = Merah Strychinin
Reaksi WassiokyZat + pDAB + H2SO4 (panaskan)
Merah Darah Atropin
Reaksi IodoformBau Iodoform
Efedrin
Dengan Asam Sulfanilat + NaNO2

3. Sampel + Parry UnguUJI ORGANOLEPTIKSampel 34
Uji Orgnoleptik KemungkinanBentuk Larutan
Golongan Anestesi Lokal
Warna BeningBau -Rasa -Kelarutan Larut Air dan
Etanol
UJI IDENTIFIKASI
Sampel 34
Perlakuan Kemungkinan 1. Sampel + NaOH + KMnO4
Hijau2. Uji Korek api Merah
jingga3. Sampel + Carletti Coklat
merah
Lidocain HCl
E. Pembahasan
Sampel no. 78 berbentuk tablet berwarna coklat muda, kemudian
dipisahkan analit dari matriks pada tablet tersebut dengan cara di larutkan pada
air dan NH4OH. Hal ini dilakukan karena dilihat dari kelarutan analit nya,
setelah dilarutkan kemudian dipisahkan dengan cara filtrasi, kemudian didapat
fitrat dan residu yang akan digunakan untuk melakukan identifikasi. Hal
pertama yang dilakukan adalah meraksikan dengan pereaksi pada uji
penggolongan, seperti dengan reagen Mayer, Bouchardat, dan Dragendorf.
Didapat hasil positif dari tiap-tiap reaksi tersebut, hal ini menandakan bahwa
sampel ini termasuk golongan anestetik local. Kemudian dilakukan reaksi
selanjutnya yaitu direaksikan dengan pereaksi FeCl3 yang menghasilkan warna
ungu. Warna ungu tersebut terjadi karena pada golongan alkaloid xantin bila
direaksikan dengan pereaksi tersebut mendapat hasil yang sama. Setelah itu
dilakukan uji penegasan, pertama sampel direaksikan dengan pereaksi
ammonia pekat + AgNO3 yang menghasilkan endapan hitam, hal ini tidak
sesuai dengan dugaan, mungkin karena telah terkontaminasi nya tabung reaksi
yang digunakan saat dicuci. Kemudian direaksikan dengan reagen Roux yang
menghasilkan hasil positif. Hal ini memperbesar dugaan bahwa sampel tersebut
adalah Theofillin, kemudian direaksikan dengan pereaksi Parry yang

menghasilkan hasil yang positif. Hal ini menunjukan bahwa sampel no. 78
adalah Theofillin.
Pada sampel no. 34 memiliki bentuk larutan tidak berwarna, kemungkinan
sampel ini adalah berbentuk injeksi dan karena golongan anestetik lokal
sebagian dilihat bentuk sediaan nya adalah injeksi maka dugaan sampel ini
adalah kelompok anestetik lokal. Halpertama yang dilakukan adalah
dilarutkannya sampel pada air dan etanol yang menghasilkan sampel tersebut
larut sempurna. Kemudian direaksikannya sampel dean pereaksi NaOH +
KMnO4 yang menghasilkan warna hijau dan saat diteteskan pada kertas saring
tidak meninggalkan noda minyak, hal ini memperjelas bahwa sampel ini adalah
Lidocain HCl. Kemudian untuk memperjelas kembali dilakukan uji korek api
yang menghasilkan hasil positif, lalu dilakukan juga pereaksian dengan
pereaksi Carletti yang menghasilkan hasil positif. Hal ini menunjukan bahwa
sampel no. 34 adalah Lidocain HCl.
F. Kesimpulan
Berdasarkan praktikum ini dapat disimpulkan bahwa :
Menurut hasil reaksi dari sampel no. 78 dengan Pereaksi Roux menunjukan
hasil positif dan reaksi dengan pereaksi Parry menunjukan hal yang sama
menujukan bahwa sampel ini adalah Theofillin, meskipun pada pengujian
dengan ammonia pekat + AgNO3 menunjukan hasil negatif.
Menurut hasil reaksi antara sampel no. 34 dengan NaOH + KMnO4
menunjukan hasil yang positif dan dengan uji korek api menunjukan juga
hasil positif dapat disimpulkan bahwa sampel ini adalah Lidocain HCl, hal
ini dipertegas dengan pengujian dengan uji Carletti yang menunjukan hasil
positif.
G. Daftar Pustaka
- Raymond C Rowe, Paul J Sheskey and marian E Quinn. 2009. Handbook of
Phermaceutical Excipients. Sixth Edition.
- Underwood, A. L. 2002. Analisis Kimia Kualitatif. Jakarta Erlangga
- Fessenden & Fessenden. 1990. Kimia Organik. Jakarta : Erlangga

- Departemen Kesehatan Republik Indonesia. 1979. Farmakope Indonesia
edisi ketiga. Jakarta: Depkes RI.