Sejarah Atom
description
Transcript of Sejarah Atom
Zat Elementer
Zat ElementerAnggota Kelompok 1 :
1. Rizki Annisa(4201412054)2. Artika Sari(4201412059)3. Putri Nurmala Sari(4201412060)4. Rita Iva Fatmala(4201412063)5. Dian Ayu Antika (4201412116)
Pengantar Sejarah Perkembangan Zat Elementerapakah yang menyusun dan membentuk alam semesta ini ? ? ?
Siapa Democratus itu?DemocritusSeorang filsuf Mazhab AtomismeLahir di kota Abdera, Yunani Utara (460 SM - 370 SM)Murid dari Leukippos, pendiri mazhab Atomisme.Pengembang pemikiran tentang atom sehingga justru pemikiran Democritus yang lebih dikenal di dalam sejarah filsafat.
4ATOMSudah dikemukakan oleh filsuf India Kuno pada tahun 800 SM dijelaskan dalam naskah filsafat Jainisme.
Aliran mazhab Nyaya dan Vaisesika menjelaskan bagaimana atom-atom bergabung menjadi benda-benda yang lebih kompleks.
Teori Democritus mengenai atomFilosofi serupa juga terjadi di India, namun demikian ilmu pengetahuan modern memutuskan untuk menggunakan istilah "atom" yang dicetuskan oleh Democritus
7Bentuk Eksperimen
Pemikiran Democritus ditentang Aristoteles yang menganggap pemikiran itu tidak berguna bagi masa depan8JOHN DALTONSalah satu peneliti atom
Lahir : Tahun 1766 di Eaglesfield, Cumberland, InggrisMeninggal pada tahun 1844 di Manchester, InggrisMulai merumuskan hal tentang atom sekitar tahun1803
John Dalton Berhasil mengkaitkan konsep atom dengan prinsip-prinsip stoikiometri
Percobaan berdasarkan hukum kekekalan masa Lavoisier (Antoine Laurent de Lavoisier, 1743 1794, Perancis) dan hukum perbandingan tetap Proust Proust (Joseph Louis Proust, 1754 1826, Perancis). melaluiMenurut Dalton:Atom digambarkan sebagai bola pejal yang sangat kecil.Atom merupakan partikel terkecil yang tak dapat di pecah lagi.Atom dari unsur yang sama memiliki sifat yang sama, sedangkan atom dari unsure yang berbeda memiliki masa dan sifat yang berbeda.Senyawa terbentuk bila atom bergabung satu sama lain.Reaksi kimia hanya melibatkan penataan ulang atom-atom sehingga tidak ada atom yang berubah akibat reaksi kimia.
KelemahanKetidakterpisahan atom terbukti salah, karena, atom dapat dibagi lagi menjadi proton, neutron dan elektron. Namun atom adalah partikel terkecil, yang sangat berpengaruh dalam reaksi kimia.Menurut Dalton, atom-atom dari unsur yang sama adalah sama dalam segala hal. Pernyataan ini salah karena atom dari beberapa unsur berbeda dalam hal massa dan kepadatan. Atom seperti dari unsur yang sama memiliki massa yang berbeda disebut isotop. Misalnya, klorin memiliki dua isotop yang memiliki nomor massa 35 dan 37 satuan massa atom (sma)
Dalton juga mengatakan atom elemen yang berbeda berbeda dalam segala hal. Hal ini telah terbukti salah dalam kasus-kasus tertentu seperti atom argon dan atom kalsium, yang memiliki massa atom yang sama yaitu 40Menurut Dalton atom unsur yang berbeda bergabung dalam rasio nomor sederhana keseluruhan untuk membentuk senyawa. Hal ini tidak terlihat pada senyawa organik kompleks seperti gula C12H22O11.
Teori atom Dalton tidak dapat menerangkan suatu larutan dapat menghantarkan arus listrik.Bagaimana mungkin bola pejal dapat menghantarkan arus listrik? padahal listrik adalah elektron yang bergerak. Berarti ada partikel lain yang dapat menghantarkan arus listrik.16KelebihanMenggiatkan penelitian atom selanjutnyaMemungkinkan kita untuk menjelaskan hukum kombinasi kimia.Dalton adalah orang pertama yang mengakui perbedaan yang bisa diterapkan antara partikel dari suatu unsur (atom) dan dari senyawa (molekul)
Dengan begitu disebutlah John Dalton sebagai Bapak pencetusteori atommodern.
Ditemukan Elektron dan Gugurnya Teori DALTON
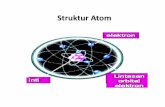
Teori Model Atom J.J ThomsonModel Atom ThomsonATOM NeutronProton
ElektronATOM bukanlah partikel terkecil dari suatu bendamaka Gugurlah Teori Atom DALTON...Mengapa Demikian???+-20Percobaan Sinar Katode
Netral+-Sinar katode merupakan partikel penyusun atom bermuatan negatif.Perbandingan antara muatan dengan massa elektron (e/m) sebesar 1,76 108C/g.Pada atom netral jumlah muatan listrik negatif sama dengan jumlah muatan listrik positif.
m elektron