Tatalaksana Nyeri Pada Lansia
description
Transcript of Tatalaksana Nyeri Pada Lansia

BAB I
PENDAHULUAN
Saat ini, pasien usia lanjut terdiri dari segmen dengan pertumbuhan tercepat dari populasi
dunia. Jumlah orang di seluruh dunia dengan umur 65 tahun keatas diperkirakan 506 juta pada
tahun 2008 dan pada 2040 akan meningkat menjadi 1,3 miliar. Biro Sensus Amerika Serikat
menegaskan bahwa ada 38.9 juta orang 65 tahun dan keatas pada tahun 2008, membuat 12.8%
dari total populasi. Segmen populasi ini, 5,7 juta adalah 85 tahun dan lebih tua, dan jumlah ini
berkembang.
Sakit kronis geriatrik dapat didefinisikan sebagai pengalaman sensoris dan emosi tidak
menyenangkan yang terkait dengan kerusakan jaringan aktual atau potensial, atau dijelaskan
dalam hal kerusakan tersebut, untuk orang yang baik berusia (65-79 tahun) atau sangat uzur (80
dan atas) dan yang telah sakit selama lebih dari 3 bulan. Konsekuensi dari rasa sakit ini termasuk
gangguan kegiatan kehidupan sehari-hari (ADLs) dan ambulation, depresi dan ketegangan pada
perekonomian perawatan kesehatan. Rasa sakit mungkin juga berhubungan dengan komplikasi
yang terkait dengan rhabdomiolisis, kelainan kiprah, kecelakaan, polifarmasi, dan penurunan
kognitif.
Prevalensi sakit terus-menerus meningkat dengan usia peningkatan nyeri sendi dan
neuralgia sangat umum. Mayoritas orang tua memiliki masalah nyeri yang signifikan dan yang
kurang tertangani. Antara 25% dan 40% pasien kanker lansia dipelajari memiliki sakit harian.
Diantara pasien-pasien ini, 21% yang antara 65 sampai 74 tahun dan 26 % yang berusia 75-84
tahun tidak menerima obat penghilang rasa sakit dan untuk orang-orang di atas usia 84, 30%
yang tersisa tidak diobati. Selain itu, deteksi dan penanganan sakit kronis tetap tidak mencukupi.
Dalam satu studi, 66% dari geriatrik panti jompo memiliki sakit kronis, tapi di hampir setengah
dari kasus (34%) itu tidak terdeteksi oleh dokter yang merawat.
1

BAB II
TINJAUAN PUSTAKA
2.1 NYERI
2.1.1 Fisiologi Nyeri
Nyeri menurut International Association for the Study of Pain adalah pengalaman
sensorik dan motorik yang tidak menyenangkan sehubungan dengan kerusakan jaringan baik
aktual maupun potensial.1 Nyeri tidaklah selalu berhubungan dengan derajat kerusakan jaringan
yang dijumpai. Namun nyeri bersifat individual yang dipengaruhi oleh genetik, latar belakang
cultural, umur dan jenis kelamin. Kegagalan dalam menilai faktor kompleks nyeri dan
bergantung pada pemeriksaan fisik sepenuhnya dan tes laboratorium mengarahkan kita pada
kesalahpahaman dan terapi yang tidak adekuat terhadap nyeri, terutama pada pasien-pasien
dengan resiko tinggi seperti orang tua, anak-anak dan pasien dengan gangguan komunikasi.1
Kata nosisepsi berasal dari kata “noci” dari bahasa Latin yang artinya harm atau injury
dalam bahasa Inggris atau luka atau trauma. Kata ini digunakan untuk menggambarkan respon
neural hanya pada traumatik atau stimulus noksius. Banyak pasien merasakan nyeri meskipun
tidak ada stimulus noksius.1,3 Nyeri nosiseptif disebabkan oleh aktivasi ataupun sensitisasi dari
nosiseptor perifer, reseptor khusus yang mentransduksi stimulus noksius.
Berdasarkan lamanya nyeri dapat dibedakan menjadi nyeri akut dan nyeri kronik.2 Nyeri
akut dapat didefinisikan sebagai nyeri karena stimulus noksius karena ada kerusakan jaringan,
proses penyakit ataupun fungsi abnormal dari otot atau organ dalam (viscera). Biasanya bersifat
nosiseptif. Merupakan bentuk nyeri yang paling sering yang dihasilkan dari pasca trauma, paska
operasi dan nyeri obstetrik seperti halnya nyeri yang diasosiasikan dengan kondisi medis kritis
yang akut seperti miokard infark, pancreatitis dan calculi renal. Kebanyakan nyeri akut bersifat
terbatas atau akan sembuh dalam beberapa hari atau minggu.2 Apabila nyeri gagal untuk sembuh
karena atau akibat abnormal penyembuhannya atau karena pengobatan yang tidak adekuat, nyeri
menjadi kronis. Nyeri kronis adalah nyeri yang menetap dialami lebih 3 bulan atau 6 bulan dari
sejak mulai dari dirasakan nyeri.2 Dapat bersifat nosiseptiv atau neuropatik ataupun gabungan
keduanya. Sedangkan tipe nyeri dapat dibagi menjadi nyeri somatik, nyeri visceral, dan nyeri
2

neuropatik. Nyeri somatik dideskripsikan sebagai sakit, menggerogoti, dan tajam dalam hal
kualitas. Secara umum dapat dilokalisasi dan diinisiasi oleh aktivasi nosiseptor di jaringan kulit
dan jaringan dalam. Contoh nyeri somatic termasuk nyeri akut pasca operasi dan patah tulang.
Nyeri visceral juga diasosiasikan dengan kerusakan jaringan, khususnya infiltrasi, kompresi dan
distensi dari organ dalam.3 Biasanya dideskripsikan sebagai nyeri yang tumpul dan sukar
dilokalisasi dan bisa menyebar ke tempat lain. Misalnya nyeri perut yang disebabkan oleh
konstipasi. Sedangkan nyeri neuropati dihasilkan dari kerusakan terhadap sistem saraf baik pusat
maupun periferl. Tertembak, sengatan listrik, ataupun luka bakar sering bersamaan dengan latar
belakang timbulnya sensasi nyeri dan terbakar. Contohnya, neuropati diabetik dan neuralgia post
herpetic.3
2.1.2 Mekanisme Nyeri
A. Respon Terhadap Stimulus Nyeri Akut1
Secara klinis nyeri dapat diberi label “nosiseptif” jika melibatkan nyeri yang berdasarkan
aktivasi dari sistem nosiseptif karena kerusakan jaringan. Meskipun perubahan neuroplastik
(seperti hal-hal yang mempengaruhi sensistisasi jaringan) dengan jelas terjadi, nyeri nosiseptif
terjadi sebagai hasil dari aktivasi normal sistem sensorik oleh stimulus noksius, sebuah proses
yang melibatkan transduksi, transmisi, modulasi, dan persepsi.1
Nyeri karena pembedahan mengalami sedikitnya dua perubahan, pertama karena
pembedahan itu sendiri, menyebabkan rangsang nosiseptif, kedua setelah pembedahan karena
terjadinya respon inflamasi pada daerah sekitar operasi dimana terjadi pelepasan zat-zat kimia
oleh jaringan yang rusak dan sel-sel inflamasi. Zat-zat kimia tersebut antara lain adalah
prostaglandin, histamine, serotonin, bradikinin, substansi P, leukotrien; dimana zat-zat tadi akan
ditransduksi oleh nosiseptor dan ditransmisikan oleh serabut saraf A delta dan C ke neuroaksis.1
Transmisi lebih lanjut ditentukan oleh modulasi kompleks yang mempengaruhi di medula
spinalis. Beberapa impuls diteruskan ke anterior dan anterolateral dorsal horn untuk memulai
respon refleks segmental. Impuls lain ditransmisikan ke sentral yang lebih tinggi melalui tract
spinotalamik dan spinoretikular, dimana akan dihasilkan respon suprasegmental dan kortikal.
Respon refeks segmental diasosiasikan dengan operasi termasuk peningkatan tonus otot lurik dan
spasme yang diasosiasikan dengan peningkatan konsumsi oksigen dan produksi asam laktat.
3

Stimulasi dari saraf simpatis menyebabkan takikardi, peningkatan curah jantung sekuncup, kerja
jantung, dan konsumsi oksigen miokard. Tonus otot menurun di saluran cerna dan kemih.
Respon refleks suprasegmental menghasilkan peningkatan tonus simpatis dan stimulasi
hipotalamus. Konsumsi dan metabolisme oksigen selanjutnya akan meningkat.
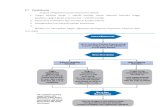
Gambar 1. Mekanisme Nyeri
B. Sensitisasi Perifer2
Sensitivitas daripada terminal nosiseptor perifer tidaklah tetap, dan aktivasinya dapat
dilakukan baik melalui stimulasi perifer berulang atau melalui perubahan komposisi kimia dari
terminal dapat mensensitisasi neuron sensor primer. Fenomena ini dikatakan sebagai sensitisasi
perifer.
C. Sensitisasi Sentral dan Modulasi2
Sebagai akibat perubahan pada sensitivitas terminal nosiseptor perifer, penambahan
sinaps transmisi nosiseptif di dorsal horn dari medulla spinalis terjadi. Dan ini berkontribusi
untuk meningkatkan sensitivitas terhadap nyeri, yang dikenal sebagai sensitisasi sentral. Input
yang intensif dari nosiseptor ke medula spinalis memicu sensasi segera dari nyeri yang berakhir
selama waktu stimulus noksius dan merefleksikan aktivasi langsung dari hasil potensial aksi dari
saraf yang diproyeksikan. Beberapa input, bagaimanapun juga menginduksi aktivitas yang
4

bergantung kepada modulasi proses sensori di dorsal horn yang menghasilkan hipersensitivitas
terhadap nyeri.
D. Nosiseptor
Nosiseptor adalah reseptor ujung saraf bebas yang ada di kulit, otot, persendian, viseral
dan vascular.3 Nosiseptor-nosiseptor ini bertanggung jawab pada kehadiran stimulus noxious
yang berasal dari kimia, suhu (panas, dingin), atau perubahan mekanikal. Pada jaringan normal,
nosiseptor tidakb aktif sampai adanya stimulus yang memiliki energi yang cukup untuk
melampaui ambang batas stimulus (resting). Nosiseptor mencegah perambatan sinyal acak
(skrining fungsi) ke CNS untuk interpretasi nyeri.
Saraf nosiseptor bersinap di dorsal horn dari spinal cord dengan lokal interneuron dan
saraf projeksi yang membawa informasi nosiseptif ke pusat yang lebih tinggi pada batang otak
dan thalamus.3 Berbeda dengan reseptor sensorik lainnya, reseptor nyeri tidak bisa beradaptasi.
Kegagalan reseptor nyeri beradaptasi adalah untuk proteksi karena hal tersebut bisa
menyebabkan individu untuk tetap awas pada kerusakan jaringan yang berkelanjutan. Setelah
kerusakan terjadi, nyeri biasanya menimal. Mula datang nyeri pada jaringan karena iskemi akut
berhubungan dengan kecepatan metabolisme. Sebagai contoh, nyeri terjadi pada saat beraktifitas
kerena iskemia otot skeletal pada 15 sampai 20 detik tapi pada iskemi kulit 20 sampai 30 menit.
Tipe nosiseptor spesifik bereaksi pada tipe stimulus yang berbeda. Nosiseptor C tertentu
dan nosiseptor A-delta bereaksi hanya pada stimulus panas atau dingin, dimana yang lainnya
bereaksi pada stimulus yang banyak (kimia, panas, dingin).3 Beberapa reseptor A-beta
mempunyai aktivitas nociceptor-like. Serat –serat sensorik mekanoreseptor bisa diikutkan untuk
transmisi sinyal yang akan menginterpretasi nyeri ketika daerah sekitar terjadi inflamasi dan
produk-produknya. Allodynia mekanikal (nyeri atau sensasi terbakar karena sentuhan ringan)
dihasilkan mekanoreseptor A-beta.
Nosiseptor viseral, tidak seperti nosiseptor kutaneus, tidak didisain hanya sebagai
reseptor nyeri karena organ interj,gnal jarang terpapar pada keadaan yang merusak. Banyak
stimulus yang merusak (memotong, membakar, kepitan) tidak menghasilkan nyeri bila dilakukan
pada struktur viseralis. Selain itu, inflamasi, iskemia, regangan mesenterik, dilatasi, atau spasme
5

viseralis bisa menyebabkan spasme berat. Stimulus ini biasanya dihubungkan dengan proses
patologis, dan nyeri yang dicetuskan untuk mempertahankan fungsi.
E. Perjalanan Nyeri3
Ada empat proses yang terjadi pada perjalanan nyeri yaitu transduksi, transmisi,
modulasi, dan persepsi.
1. Transduksi merupakan proses perubahan rangsang nyeri menjadi suatu aktifitas listrik
yang akan diterima ujung-ujung saraf. Rangsang ini dapat berupa stimulasi fisik, kimia,
ataupun panas. Dan dapat terjadi di seluruh jalur nyeri.
2. Transmisi adalah proses penyaluran impuls listrik yang dihasilkan oleh proses transduksi
sepanjang jalur nyeri, dimana molekul molekul di celah sinaptik mentransmisi informasi
dari satu neuron ke neuron berikutnya
3. Modulasi adalah proses modifikasi terhadap rangsang. Modifikasi ini dapat terjadi pada
sepanjang titik dari sejak transmisi pertama sampai ke korteks serebri. Modifikasi ini
dapat berupa augmentasi (peningkatan) ataupun inhibisi (penghambatan).
4. Persepsi adalah proses terakhir saat stimulasi tersebut sudah mencapai korteks sehingga
mencapai tingkat kesadaran, selanjutnya diterjemahkan dan ditindaklanjuti berupa
tanggapan terhadap nyeri tersebut.
6

Gambar 2. Perjalanan Nyeri
2.2 PERUBAHAN FISIOLOGI PADA LANSIA
Sesuai dengan usia yang bertambah, terjadinya perubahan fisiologi yang multiple pada tubuh
yang akan mempengaruhi farmakodinamik dan farmakokinetic obat-obatan. Hal ini akan
menyebabkan penanganan nyeri menjadi lebih sulit. Perubahan yang berlaku terpapar di Tabel 1.
Sementara terdapat beberapa obat analgetik yang seringkali dapat digunakan pada lansia,
terdapat sebahagian obatan analgetik yang berperan sebagai risiko yang tinggi kepada lansia
yang lemah dan bisa mempunyai gangguan kognitif oleh kerana risiko obatan yang berpotensi
bahaya. Obat anti-inflamasi non-steroid (selektif dan non-selektif) secara umum memberikan
risiko pendarahan saluran cerna yang mengancam nyawa dan memberikan kesan samping yang
signifikan pada fungsi renal pada pasien lansia yang lemah. Pethidine mempunyai metabolit aktif
yang berpotensi berakumulasi pada pasien lansia dengan masalah ginjal. Dextropropoxyphene
mempunyai half-life yang lama pada pasien lansia dan di asosiasikan dengan risiko kesan
samping yang signifikan pada lansia. Kodien dan tramadol mempunyai fungsi yang limited pada
lansia yang lemah, terutama pada yang memiliki gangguan kognitif, meskipun dianggap sebagai
7

agen opiate lemah, hal ini kerana risiko interaksi antara obat-obat dan interaksi penyakit-obat
yang signifikan dan juga dianggap mempunyai kesan samping yang berbagai.4
Paracetamol diserap secara komplit dan cepat di saluran cerna dan kadar kecepatan atau
ekstensi dari absorpsi tidak terpengaruh oleh umur. Distribusi paracetamol pada orang muda
yang sehat dilaporkan berkurang volume distribusinya yang di asosiasikan dengan peningkatan
umur dan jenis kelamin, dimana konsisten dengan sifat hidrophilicnya dan perubahan dalam
komposisi tubuh yang berkait dengan umur. Terdapat studi mengidentifikasi terdapat penurunan
clearance paracetamol pada lansia. Metabolisma paracetamol di hati termasuk konjugasi kepada
metabolit glucuronit dan sulphat. Sebuah studi menunjukkan clearance secara total berkurang
secara signifikan pada lansia yang sehat dan lemah jika dibandingkan dengan orang yang lebih
muda dan sehat. Berbagai factor yang meningkatkan risiko toksisitas hepar telah dikenalpasti
termasuklah konsumsi alcohol berlebihan, penggunaan dosis yang lebih dari 4g per hari,
penyakit hepar yang telah ada, penggunaan enzim microsomal dan kekurangan gizi, paracetamol
akan lebih berefek samping pada lansia yang lemah berbanding lansia yang lebih sehat.4
Morfin dimetabolisme secara ekstensif oleh hati dengan 10% dari dosis tidak berubah di
urin. Glucuronidasi merupakan jalur biotransformasi mayor untuk morfin dimana menghasilkan
2 metabolit aktif; morphine 3-glucuronide dan morphine 6-glucuronide. Morphine 6-glucuronide
mempunyai afiniti yang tinggi untuk reseptor µ dan mempenetrasi sawar darah-otak dan jika
diberikan secara intravena potensi analgetik menjadi 2 kali lipat. Morphine-3-glucuronide juga
menembusi sawar darah-otak tetapi mempunyai afiniti receptor µ yang rendah. Ianya dikatakan
bertanggungjawab pada efek neurotosik morfin. Fungsi renal amat penting kerana kedua
metabolit glucuronide dieksresi melalui ginjal dan bisa berakumulasi pada pasien dengan
gangguan ginjal yang akan menyebabkan risiki kesan samping yang tinggi.4
8

2.2 PENILAIAN NYERI
Pengobatan nyeri dimulai dengan penilaian apa yang menyebabkan rasa sakit, bagaimana
ia dapat dihentikan, dan modalitas manajemen paling efektif untuk pasien tertentu. Namun,
penilaian nyeri tidak terlalu mudah. Manifestasi klinis dari sakit terus-menerus seringkali
kompleks dan bisa disebabkan berbagai faktor dalam populasi yang lebih tua. Bahkan persepsi
nyeri mungkin berbeda dari yang dirasakan oleh lansia.5 Isu-isu aksesibilitas fisik ke perawatan,
biaya obat, terdapat penyakit penyerta, penggunaan obat-obatan, dan kemampuan untuk
memahami keluhan pasien yang memiliki kerusakan kognitif yang hanya beberapa faktor yang
berkontribusi terhadap kompleksitas dari situasi ini. Selain itu, kondisi pasien lansia seringkali
dirumitkan oleh depresi, masalah psikososial, penyangkalan, kesehatan yang buruk, dan ingatan
yang memburuk. Tanpa penilaian yang menyeluruh, sakit yang menyebabkan gangguan berat
tidak dapat diungkapkan untuk berbagai alasan pribadi, budaya atau psikologis.4
Rasa sakit sering tidak dipedulikan karena beberapa pasien lansia salah percaya bahwa
rasa sakit adalah proses normal penuaan. Dalam kasus lain, seperti dengan nyeri kanker, rasa
nyeri dibiarkan karena takut perkembangan penyakit. Selanjutnya, pengasuh dan kerabat
merupakan yang paling dapat diandalkan sebagai sumber informasi. Untuk mengatasi kebutuhan
untuk mengidentifikasi dan mendiagnosa sakit secara memadai, banyak artikel yang ditulis pada
penilaian nyeri pada pasien dengan demensia serta penelitian yang berfokus pada pengukuran
sakit.5
Kompleksitas penilaian nyeri pada pasien geriatri sering memerlukan pendekatan
multidisiplin untuk mendiagnosis dan manajemen. Dokter harus bekerja sama dengan seorang
psikolog atau psikiater kerana depresi seringkali hadir di pasien dengan rasa sakit kronis.
Fisioterapis harus menjadi bagian dari tim juga, untuk membantu dengan fungsionalitas.
Laboratorium dan studi pencitraan dapat digunakan untuk membantu menentukan diagnosis jika
riwayat rinci dan pemeriksaan fisik tidak cukup.5
Evaluasi terhadap tingkat fungsi pasien penting karena mempengaruhi derajat
kemandiriaan, tingkat kebutuhan untuk pengasuh, serta kualitas hidup. Kegiatan kehidupan
sehari-hari-makan, mandi, berpakaian dan instrumental ADLs (pekerjaan rumah tangga yang
ringan, belanja, mengelola uang, menyiapkan makanan) harus dinilai. Setelah diagnosis dibuat,
9

rencana pengobatan harus diterangkan yang mencakup modalitas untuk menurunkan persepsi
nyeri dan meningkatkan fungsi pasien.5
Untuk menilai intensitas nyeri, visual analog scale (VAS), verbal descriptor scale dan
numerical rating scale sering digunakan. Terdapat data yang mendukung penggunaan metode-
metode ini, tetapi pengunaan VAS harus lebih berhati-hati kerana tingginya frekuensi respon dari
lansia yang tidak bisa memberikan skor. Selain itu, pasien usia lanjut dilaporkan kesulitan dalam
menyelesaikan VAS.6
McGill Pain Questionnaire memiliki bukti untuk validitas, kehandalan, dan kemampuan
diskriminatif yang tidak berkaitan dengan usia. McGill Pain Questionnaire dapat digunakan
untuk menilai komponen sensorik, afektif, evaluatif, dan komponen nyeri yang lain.6
Setelah menilai intensitas nyeri, pemeriksaan yang mendalam harus dilakukan, ianya
meliputi:
1. Anamnesis dan pemeriksaan fisik yang lengkap dan lebih berfokus kepada nyeri yang
dialami pasien
2. Tinjauan terhadap lokasi nyeri, intensitas, faktor-faktor pemberat dan kesan terhadap
mood dan tidur pasien
3. Screening untuk masalah kognitif
4. Screening untuk adanya depresi
5. Tinjauan terhadap aktivitas kehidupan seharian
6. Penilaian keseimbangan dan cara berjalan
7. Screening untuk depresi sensori untuk menilai fungsi visual dan audiotori
Seorang dokter harus mencari bukti-bukti adanya nyeri kronis. Nyeri dianggap signifikan
jika ianya nyeri yang persisten, berulang dan mempengaruhi kapasitas fungsional dan/atau kualiti
hidup pasien. Karena sakit dapat diwujudkan dalam beberapa cara, berbagai istilah yang bisa
digunakan untuk mendeteksi gejala pada pasien lansia, seperti rasa terbakar, sakit, sesak,
ketidaknyamanan, tajam, dan berdenyut-denyut. Seseorang itu bisa menggunakan suara atau
perubahan pada fungsi untuk menyatakan sakitnya terutama pada pasien yang mempunyai
gangguan kognitif atau bahasa. Isyarat ini dapat ditunjukkan sebagai menangis, mengerang,
10

perubahan dalam kiprah atau postur atau perilaku ditarik/gelisah. Selain itu, jika terdapat
gangguan kognitif atau bahasa, dokter harus mencari laporan dari pengasuh atau keluarga
terdekat. Alasan mendasar gangguan ini harus ditangani secara optimal. Pendekatan multidisiplin
selalu dianjurkan.6
Pemeriksaan dilanjutkan dengan penilaian nyeri yang komprehensif meliputi
pemeriksaan fisikal dan anamnesis yang mendalam, tinjauan sistem dan hasil laboratorium yang
bersangkutan, pencitraan dan tes diagnostik.6 Perlu dicatat hubungan temporal di antara
peristiwa, intervensi medis, dan keluhan membantu menjelaskan diagnosis dan mungkin
prognosis. Intensitas, karakter, frekuensi, lokasi, dan durasi dari rasa sakit harus diselidiki.
Faktor memperbaik atau memperburuk membantu menunjukkan sifat rasa sakit tersebut.
Kemudian, riwayat pengobatan yang harus diteliti, serta penggunaan suplemen herbal over-the-
counter.
Daftar efek obat harus dicatat. Pemeriksaan fisik harus difokuskan pada sistem
neuromuskuler dengan memerhatikan adanya gangguan, kelemahan, hyperalgesia / hypoalgesia,
hyperpathia, " allodynia " mati rasa, dan kesemutan. Mungkin ada poin memicu, kelainan tulang,
atau peradangan lokal di situs tertentu yang mungkin menyarankan patologi tertentu. Fungsi fisik
dapat ditentukan dengan menilai kemampuan pasien untuk melakukan ADLs.7 Pemeriksaan
range of motion, kiprah, dan pengujian keseimbangan amat sesuai pada tahap ini. Fungsi
psikososial pasien bisa di ketahui dengan menilai mood, kelompok dukungan sosial, hubungan
keluarga dan pengasuh yang dipilih. Seterusnya penilaian nyeri pasien yang bersifat kuantitatif
dapat dipastikan dengan penggunaan VAS, numerical rating scale atau skala nyeri yang lain.
Akhirnya, buku catatan nyeri atau diari dapat membantu mengenalpasti bagaimana
modalitas penanganan yang berbeda akan berpengaruh pada fungsi dan intensitas nyeri pasien.7
Disfungsi dan tingkat keparahan akan menentukan waktu interval untuk follow-up. Ini mungkin
bisa dari 1 hingga 4 minggu tergantung dengan situasi pasien dan kepatuhan dalam berobat.
Kunjungan rutin akan membantu menilai semula pembaikan atau pemburukan kondisi,
komplikasi dengan pengobatan dan kepatuhan pasien. Pasien yang tidak bisa memandu untuk
bertemu dokter mungkin memerlukan panggilan kerumah atau bantuan keperawatan dirumah
11

untuk di follow-up. Efek positif dan negative obat analgetik dan modalitas terapi perlu dicatat
dan barulah rancangan perawatan dimodifikasi.7
Penilaian nyeri pada pasien dengan masalah kognitif amatlah rumit. Pertama, dokter
haruslah menilai terlebih dahulu fungsi kognitif pasien lansia. Untuk menilai fungsi kognitif,
banyak alat penilaian yang bisa digunakan. Mini Mental State Examination (MMSE),
Abbreviated Mental Test (AMT), Six-Item Screener (SIS), Six-Item Cognitive Impairment Test
(6CIT), Clock Drawing Test (CDT) dan Mini-Cog.8,9
Untuk menilai nyeri pada pasien dengan masalah kognitif, laporan sendiri oleh pasien
amatlah susah untuk diperoleh dan bisa tidak tepat. Oleh itu, penilaian berdasarkan pengamatan
perilaku adalah optimal pada pasien kelompok ini. Perilaku nyeri yang biasa ditunjukkan melalui
(1) ekspresi wajah seperti mengerutkan dahi, meringis, distorsi ekspresi dan berkedip mata yang
cepat, (2) verbal seperti mendesah, mengerang, meminta bantuan, (3) Pergerakan tubuh juga bisa
menunjukkan adanya nyeri seperti kaku, tegang, berjaga-jaga, gelisah, peningkatan mundar-
mandir, perubahan mobilitas seperti tidak aktif atau kegelisahan motorik, (4) perubahan
hubungan interpersonal seperti bertambah agresif, menolak perawatan, mengasingkan diri, (5)
perubahan pola aktivitas seperti perubahan nafsu makan, tidur dan penghentian rutinitas secara
tiba-tiba, (6) perubahan status mental seperti menangis, kebingungan, lekas marah dan tertekan.
Nyeri juga bisa bermanifestasi secara physiological seperti peningkatan denyut jantung, tekanan
darah, kadar pernapasan, berpeluh dan dilasi pupil. Pada pasien dengan masalah kognitif,
indikator nyeri bisa hadir sebagai perilaku yang merupakan karakteristik dari kebutuhuhan lain
yang tidak terpenuhi. Misalnya, suatu indikator bisa menunjukkan kelaparan, haus, stimulasi
yang berlebihan atau kurang, depressi atau cemas.10
Dokter haruslah memiliki berbagai alat penilaian nyeri yang bisa digunakan pasien lansia
dengan mudah. Setelah suatu alat dipilih, alat yang sama harus digunakan untuk menilai semula
nyeri pada pasien yang sama. Antara alat menilai nyeri secara laporan sendiri adalah:10
Verbally administered 0-10 scale: 0 is “no pain at all” and 10 is “the worst possible pain”
Visual analige scale
Verbal descriptor scale
Faces pain scale
Pain thermometer
12

McGill Pain Questionnaire
Penilaian nyeri perilaku untuk pasien lansia adalah:10
The Assessmnet of Discomfort in Dementia Protocol (ADD)
Checklist of Nonverbal Pain Indicators (CNPI)
Doloplus 2
Nursing Assistant-Administered Instrument to Assess Pain in Demented individual
(NOPPAIN)
The Pain Assesment Scale for Seniors with Severe Dementia (PACSLAC)
The Pain Assessment in Advanced Dementia Scale (PAINNAD)
2.4 PERUBAHAN FARMAKOKINETIC DAN FARMAKODINAMIK
2.4.1 Perubahan Farmakokinetic11
Distribusi obat akan dipengaruhi oleh perubahan fisiologi pada lansia dimana ia
menyebabkan bertambahnya lemak tubuh, berkurangnya otot dan air dalam tubuh. Penggunaan
obat diuretic juga menyebabkan pengurangan volume darah. Dengan pengurangan massa lemak
relatif, obat-obatan yang sangat lipophylic, seperti fentanil dan lidokain, dapat memiliki
peningkatan durasi efek kerana sedikit yang diserap oleh lemak. Sebaliknya, obat yang larut
dalam air seperti morphine kurang effisien dalam distribusinya dan tinggi konsentrasi dalam
darah pada dosis yang sama, menyebabkan terjadinya efek samping yang lebih sering.
Penurunan albumin serum khususnya di pasien lanjut usia dengan penyakit kronis dan
kekurangan gizi secara signifikan akan meningkatkan ketersediaan obat bebas. Perubahan
tersebut akan meningkatkan potensi terjadinya efek samping yang terkait dengan obat analgetik
yang sangat terikat dengan protein seperti NSAIDs dan agen anti kejang seperti valproate,
phenytoin dan carbamazepine. Ternyata pada pasien lansia, jumlah alpha 1-acid glycoprotein
pembawa dalam serum untuk obat dasar seperti meperidine) tidak berubah.
Fungsi hati dan ginjal akan berkurang seiring pertambahan usia dan akan kurang effisien
secara progresif untuk clearance obat. Half-life obat, kadar distribusi per clearance, adalah
meningkat untuk sebahagian antidepresi jenis benzodiazepine dan tricyclic.
13

Obat-obatan yang larut dalam lemak seperti lidokain dan analgesic narkortika adalah
contoh yang baik dari obat-obatan yang menjalani metabolisme first-pass secara signifikan
selama bagian dari saluran pencernaan ke hati. Puncak konsentrasi dalam plasma akan
meningkat dengan adanya potensi kesan samping yang berhubungan dengan dosis. Situasi ini
diperburuk dengan adanya kelainan pada curah jantung yang disebabkan penyakit. Obat yang
cenderung berikat dengan protein kurang dipengaruhi oleh metabolism first-pass. Reaksi hepatic
fase 1 iaitu oksidasi, hidrolisis dan reduksi lebih dipengaruhi oleh umur berbanding dengan
prosen konjugasi fase 2 (acetylation, glucuronidation, sulfation dan glycine conjugation).
Pengurangan clearance melalui ginjal merupakan efek farmakokinetic dari usia. Ini akan
diperberat dengan adanya penyakit yang akan menurunkan lagi fungsi ginjal. Hal ini akan
menyebabkan toksisitas obat pada dosis yang sesuai untuk pasien lebih muda dengan fungsi
renal yang normal. Obat yang secara dominant dieksresi melalui ginjal seperti gabapentin akan
terakumulasi sekiranya fungsi ginjal gagal.
2.4.2 Perubahan Farmakodinamik12
Perubahan farmakodinamik yang berkait dengan umur merupakan hasil dari perubahan fungsi
system efektor yang berkaitan dengan umur. Respon terhadap organ ini dipengaruhi oleh
perubahan fisiologis yang terjadi dengan bertambahnya usia dalam ketiadaan patologi.
Perubahan pada calcium channels dan reseptor beta-adrenergic yang berkait dengan umur
menarik minat ahli farmakologi dengan implikasi untuk kegunaan klinis mereka sebagai agonists
dan antagonists. Sebagai contoh, respon beta-adrenergic berkurang dengan pertambahan usia,
dan untuk mengontrol konsentrasi plasma, respon bradikardi terhadap labetolol berkurang pada
lansia. Kerana perubahan farmakokinetic dan farmakodinamik, lansia menunjukkan lebih sensitif
terhadap efek sedasi beberapa obat misalnya, mereka akan hilang kesadaran pada dosis dan
konsentrasi dalam plasma propofol yang rendah disitus efektor berbanding orang yang lebih
muda dan lebih sensitif terhadap sedasi dengan benzodiazepine seperti triazolam. Perubahan
terkait umur dalam sistem saraf otonom mempengaruhi orang tua untuk memiliki hipotensi
postural, yang mungkin lebih lanjut diperburuk oleh obat-obatan dengan efek antikolinergik dan
antihipertensi.
14

2.5 Terapi Nyeri9,10,11,12
Lansia sangat rentan untuk mengalami efek samping suatu pengobatan, oleh karena itu pada
pemberian obat untuk mengobati rasa nyeri perlu diperhatikan dosis yang akan diminum. Usia
berhubungan erat dengan efek metabolisme obat di dalam tubuh, jadi pemberian obat pada lansia
harus dilakukan dengan hati-hati. 9
2.5.1 Farmakologi
Nonopioids
a. Asetaminofen
Asetaminofen merupakan pilihan utama untuk dianggap sebagai farmakoterapi awal dan
berkelanjutan dalam pengobatan nyeri persisten, nyeri musculoskeletal dan pemberiannya
harus dibatasi. Maksimum dosis harian yang direkomendasikan dari 4 g per 24 jam tidak
boleh melebihi. Misalkan pemberian asetaminofen lebih dari 4000 mg sehari (dosis 4 kali
1000mg) dalam jangka lama dapat menimbulkan gangguan pada hepar. Pada dosis terapi,
salah satu metabolit Asetaminofen bersifat hepatotoksik, didetoksifikasi oleh glutation
membentuk asam merkapturi yang bersifat non toksik dan diekskresikan melalui urin, tetapi pada
dosis berlebih produksi metabolit hepatotoksik meningkat melebihi kemampuan glutation untuk
mendetoksifikasi, sehingga metabolit tersebut bereaksi dengan sel-sel hepar dan timbulah
nekrosis sentro-lobuler. Oleh karena itu pada penanggulangan keracunan asetaminofen terapi
ditujukan untuk menstimulasi sintesa glutation. Ini akan menyebabkan Serum Glutamik Piruvik
Transaminase ( SGPT) dan Serum Glutamik Oksaloasetik Transaminase (SGOT) yaitu enzim
yang dipakai didalam hati semakin banyak akan dapat masuk ke aliran darah jika fungsi hati
terganggu.9,10
15

b. Nonselektif NSAID
Penggunaan NSAID adalah untuk nyeri akut ringan-sedang dimana menghambatkan sintesa
prostaglandin, prostacyclin dan thromboxane. NSAID ini menggurangkan inflamasi dan anti
nyeri dimana nonselektif NSAIDs menghambat 2 jenis enzim COX yaitu COX-1 dan COX-2
dimana COX-1 melindungi mukosa gastro daripada asam lambong dan COX-2
bertanggungjawab untuk proses inflamasi dan nyeri. Penggunaan jangka panjang harus dihindari
karena seringkali terjadi efek samping misalnya perdarahan gastrointestinal dan gangguan fungsi
ginjal. Orang tua mengambil NSAID nonselektif seperti Ibuprofen dan Ketoprofen harus
menggunakan proton pump inhibitor atau misoprostol untuk perlindungan gastrointestinal.
Secara umum, COX-1 fungsi dalam pengendalian hemodinamik ginjal dan clearance creatinine
(CTT) dan COX-2 fungsi mempengaruhi garam dan air ekskresi. Sindrom ginjal disebabkan oleh
NSAID nonselektif dan coxib dapat dikelompokkan menurut efeknya terhadap prostaglandin
(PG) E dan PGI. Jadi sedangkan PGI atau prostasiklin, kebanyakan mempengaruhi mekanisme
homeostatis ginjal, PGE dan PGD melebarkan vaskular ginjal, dimana ginjal lebih rendah untuk
resistensi vaskuler, dan meningkatkan perfusi ginjal terutama pada lansia. Prostaglandin ini
menjadi kritis terlibat dalam mempertahankan GFR.9,10,12
Opioid
Pasien dengan nyeri sedang sampai berat, atau mempunyai gangguan fungsional yang berkaitan
nyeri berat atau berkurang aktivitas hidup karena sakit harus dipertimbangkan untuk terapi
opioid. Dosis aman maksimal dari acetaminophen atau NSAID tidak boleh melebihi saat
menggunakan dosis tetap agen kombinasi opioid sebagai bagian dari analgesic. Ketika persiapan
long-acting opioid, nyeri terobosan harus diantisipasi, dinilai, dan dicegah atau diobati dengan
menggunakan short-acting obat opioid untuk menghilangkan dengan segera. Tujuan opioid harus
untuk mengurangi rasa sakit cukup untuk memfasilitasi keterlibatan dengan rehabilitasi dan
pemulihan fungsi yang berguna dimana ia mengaktifkan reseptor µ, δ, к, σ dan menghambat
tranmisi input nosiseptif dari perifer ke spinal. Ini mempengaruhi aktivitas sistem limbic dan
aspek sensorik & afektif nyeri. Efek samping -mual muntah, pruritus, sedasi dan konstipasi.
Pengelolaan nyeri persisten tidak hanya berfokus pada pengurangan intensitas nyeri tapi juga
pada perbaikan dalam tidur, suasana hati, dan fisik, sosial dan emosional kesejahteraan.
16

Pengobatan Adjuvan
Pengobatan adjuvan (adjuvant medications) dapat diberikan untuk mengobati rasa nyeri kronik
pada lansia seperti golongan steroid, antikonvulsan, anestesi lokal topikal dan antidepresan..
Penatalaksaan rasa nyeri pada lansia yang mengalami rasa nyeri neuropatik seringkali
memerlukan antikonvulsan (karbamesepin, gabapentin), lidokain topikal 5% atau obat anti-
depresan. Golongan anti-depresan trisiklik seperti amitriptilin, nortriptilin dan desipramin
merupakan mendekatan tradisonal untuk mengobati rasa nyeri yang kronik ada lansia. Terutama
amitritilin dan nortriptilin merupakan obat analgesik yang efektif untuk mengobati rasa nyeri
neuropatik pada lansia. Pengobatan secara topikal dapat pula digunakan untuk mengurangi rasa
17

nyeri yang bersifat neuropatik atau sindrome rasa nyeri kompleks regional. Lidokain 5% secara
topikal sangat bermanfaat untuk mengatasi rasa nyeri yang terjadi pada postherpetic neuralgia.
Preparat topikal aspirin, kapsaisin, antidepresan trisiklik, lidokain dapat mengurangi rasa nyeri
terutama gangguan muskuloskeletal.9,10
Sekilas Rekomendasi WHO: Analgesik Ladder yang signifikan terjadi antara geriatri rasa sakit
dan nyeri kanker kronis. Untuk ini alasannya, mengikuti rekomendasi WHO untuk
nyeri manajemen yang tepat. Dalam rangka mempertahankan nyeri analgesic ladder harus
digunakan WHO merekomendasikan :
(1) administrasi obat mengikut jam (misalnya, setiap 3-6 jam)
(2) obat melalui mulut individual bagi pasien
(3) mengikuti'' tangga'' analgesik
Untuk nyeri ringan, yang paling tepat pilihan pertama untuk analgesia relatif aman adalah
acetaminophen. Untuk nyeri ringan sampai sedang atau nyeri yang tidak terkontrol dengan
acetaminophen, penggunaan NSAID adalah tepat. Untuk nyeri refrakter terhadap NSAID, atau
nyeri dinilai sebagai moderat awalnya, suatu opioid lemah (misalnya, kodein) adalah sesuai
pilihan pertama. Opioid lemah lainnya digunakan mencakupi hydrocodone, propoxyphene, dan
oxycodone dalam kombinasi dengan acetaminophen. Untuk nyeri refrakter dengan rencana
sebelumnya, atau sakit dinilai sebagai parah, suatu agonis opioid (misalnya, morfin)
dipilih. Opioid murni lain untuk dipertimbangkan termasuk hidromorfon, fentanil, levorphanol,
18

dan oxycodone. Obat ajuvan dapat digunakan untuk meredakan rasa takut dan kecemasan pada
pasien serta untuk sinergisme.9,10
2.5.2 Non Farmakologi
Walaupun pendekatan secara farmakologik lebih banyak digunakan dalam penatalaksaan
rasa nyeri, intervensi secara non-farmakologik merupakan strategi yang harus dimasukkan pada
penatalaksanaan rasa nyeri kronik pada lansia. Pendekatan non-farmakalogik merupakan
pengobatan yang efektif untuk rasa nyeri yang ringan dan sedikit terjadi efek samping. Teknik
mengurangi stres (stressreduction), konseling psikososial dan terapi fisik/pekerjaan
(physical/occupational), transcutaneous electric nerve stimulation (TENS), akupuntur dan
olahraga teratur bermanfaat untuk mengobati rasa nyeri kronik. Pengobatan alternatif
komplementer (complementary and alternative medication/ CAM) dapat pula diberikan,
terutama bagi penderita yang menyukainya. Pendidikan pada pasien dan pendampingnya dalam
penatalaksanaan rasa nyeri sangat diperlukan dan efektivitas dari program ini dalam
meningkatkan penanganan rasa nyeri telah dilaporkan. 9,10,11
Pendidikan dapat diberikan secara perorangan atau kelompok dengan menggunakan
media cetak untuk mendorong pasien dan pendampingnya memahami bahwa penanganan rasa
nyeri meliputi terapi secara farmakologik dan nonfarmakologik. Terapi kognitf perilaku juga
19

bermanfaat untuk meningkatkan ketrampilan dan pencegahan timbulnya serangan rasa nyeri.
Tujuan dari program pendidikan dalam penanganan rasa nyeri adalah untuk meningkatkan fungsi
dan menghindari ketidak pastian kondisi yang dirasakan lansia. Kegagalan untuk mengobati rasa
nyeri pada lansia seringkali terjadi bila edukasi pada penderita dan pendampingnya tidak cukup
memadai.Penderita dengan rasa nyeri kronik tidak hanya disarankan untuk meningkatkan
kekuatan otot dan mencegah terjadinya disfungsi, tetapi diperkenalkan pula penggunaan terapi
panas, dingin atau mengurut (massage).9,10
20

BAB III
KESIMPULAN
Sakit kronis geriatrik dapat didefinisikan sebagai pengalaman sensoris dan emosi tidak
menyenangkan yang terkait dengan kerusakan jaringan aktual atau potensial, atau dijelaskan
dalam hal kerusakan tersebut, untuk orang yang baik berusia (65-79 tahun) atau sangat uzur (80
dan atas) dan yang telah sakit selama lebih dari 3 bulan. Konsekuensi dari rasa sakit ini termasuk
gangguan kegiatan kehidupan sehari-hari (ADLs) dan ambulation, depresi dan ketegangan pada
perekonomian perawatan kesehatan. Rasa sakit mungkin juga berhubungan dengan komplikasi
yang terkait dengan rhabdomiolisis, kelainan kiprah, kecelakaan, polifarmasi, dan penurunan
kognitif.
Penatalaksanaan yang optimal bagi lansia yang menderita serangan rasa nyeri, baik nyeri
akut maupun kronik adalah dengan melakukan diagnosis dan penilaian yang tepat terhadap
sindroma nyeri yang dirasakan. Pemberian terapi farmakologik dan non-farmakologik yang
sesuai dengan diagnosis sangat efektif untuk mengobati rasa nyeri kronik ada lansia. Perlu
dipertimbangan efek farmakokinetik dan farmakodinamik penggunaan obat farmakologik pada
lansia. Edukasi bagi lansia dan pendampingnya harus diberikan supaya pengobatan rasa nyeri
pada lansia dapat lebih efektif.
21

DAFTAR PUSTAKA
1. Macintyre PE, Schug SA, Scott DA, Visser EJ, Walker SM; APM:SE Working Group of
the Australian and New Zealand College of Anaesthetists and Faculty of Pain Medicine
(2010), Acute Pain Management: Scientific Evidence (3rd edition), ANZCA & FPM,
Melbourne.
2. Charlotte ES. The Anatomy and Physiology of Pain. Basic Science, Surgery 27:12.
Elsevier. 2009:507-511.
3. Patel NB. "Physiology of Pain." In: Guide to Pain Management in Low Resource
Settings. Washington, USA: International Association for the Study of Pain (IASP);
2009.
4. McLachlan AJ, Bath S, Naganathan V, Hilmer SN, Le Couteur DG, Gibson SJ et al.
Clinical pharmacology of analgesic medicines in older people: impact of frailty and
cognitive impairment. Br J Clin Pharmacol; 71:3: 351–364.
5. Alan D. Kaye, Amir Baluch, Jared T. Scott. Pain Management in the Elderly Population:
A Review. Ochsner J. 2010 Fall; 10(3): 179–187.
6. Keela Herr. Pain Assessment Strategies in Older Patients. The Journal of Pain, Vol 12,
No 3 (March), Suppl. 1, 2011:pp S3-S13.
7. Rahul R and Brian DM. Management of chronic pain in elderly, frail patients: finding a
suitable, personalized method of control. Clinical Interventions in Aging 2013:8 37–46.
8. Woodford H.J and George J. Cognitive assessment in the elderly: a review of clinical
methods. QJ Med 2007; 100; 469-484.
9. Rosen SL and Reuben DB. Geriatric Assessment Tools. MOUNT SINAI JOURNAL OF
MEDICINE 2011 78:489-497.
10. Lee KL. Pain Assessment in Persons with Cognitive Impairment. Medscape Reference
2013;1-8.
11. Gary McCleane. Pharmacological pain management in the elderly patient. Clinical
Interventions in Aging 2007:2(4) 637–643.
12. Sarah N. Hilmer, Andrew J. McLachlan and David G. Le Couteur. Clinical
pharmacology in the geriatric patient. Fundamental & Clinical Pharmacology 21 (2007)
217–230.
22