Ppt penetapan ka atau kb secara p hmetri 11 3 smakbo
-
Upload
anindya-febriani -
Category
Technology
-
view
2.433 -
download
5
description
Transcript of Ppt penetapan ka atau kb secara p hmetri 11 3 smakbo

Penetapan Tetapan
Ion i sa s i Asam/Basa Lemah (Ka/Kb)
Secara pHmetr i

Asam asetat merupakan asam lemah dan natrium hidroksida merupakan basa kuat. Jika bereaksi maka akan menghasilkan garam natrium asetat, dimana garam yang dihasilkan merupakan larutan buffer. Dengan metode potensiometro, titik akhir penitaran dapat dideteksi dengan menggunakan pHmeter ataupun dengan kurva penitaran dengan cara menetapkan volume dimana terjadi lonjakan nilai pH.
Dasar

1. Menentukan nilai tetapan ionisasi asam/basa lemah
2. Menentukan titik akhir dari suatu penitaran
3. Membandingkan nilai pH larutan pada setiap titrasi
Tujuan

CH3COOH + NaOH → CH3COONa +H2O
Reaksi


Gambar Alat pHmeter
Elktroda pHmeter orion 210 A+


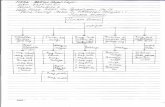
Bagan Kerja
±1,0 gr minuman serbuk
100 ml H2ODipipet 10 ml ± H2O hingga
100 ml±2-3 tetes PP
Larutan NaOHTA. Merah Muda Seulas

*menetukan tetapan ionisasi•Disiapkan alat dan bahan yang akan digunakan•Larutan CH3COOH 0,1 N dimasukkan ke dalam piala gelas 400ml•Buret 50ml diisi dengan larutan NaOH 0,1 N diseka dan dihimpitkan•Dipipet larutan CH3COOH 0,1 N sebanyak 100,0 ml•Dimasukkan ke dalam Erlenmeyer, dicek pH awal•Dilakukan penitaran dengan cara :
- ditambahkan 1,0ml titran (dari pHawal–pH ±5) a- ditambahkan 0,5ml titran (dari pH ±5–pH ±6) b- ditambahkan 0,1ml titran (dari pH ±6–TE)- ditambahkan 0,1ml titran (hingga angka bulat)- ditambahkan 0,5ml titran (sebanyak b kali)- ditambahkan 1,0ml titran (sebanyak a kali)

Bagan Kerja
100 ml CH3COOH 0,1 N
Larutan NaOH
ditambahkan 1,0ml titran (dari pHawal–pH ±5) a
ditambahkan 0,5ml titran (dari pH ±5–pH ±6) b
ditambahkan 0,1ml titran (dari pH ±6–TE)
ditambahkan 0,1ml titran (hingga angka bulat)
ditambahkan 0,5ml titran (sebanyak b kali)
ditambahkan 1,0ml titran (sebanyak a kali)

- Log Ka = pH ½ TE

Kesimpulan dari penetapan ini ialah tetapan ionisasi asam atau basa lemah merupakan Suatu tetapan yang menggambarkan tingkat ionisasi suatu asam atau basa lemah. Penetapan ini dilakukan berdasarkan pH asam atau basa lemah yang diukur dengan menggunakan alat atau instrumen berupa pH meter. Penitaran dilakukan hingga mencapai titik ekivalen, yang merupakan titik dimana jumlah titran dan titrat sudah setara.

T HAT HA NNK Y OUK Y OUF o r F o r
y o u r y o u r a t t e n t ioa t t e n t io
n n