Ltm Kitik Spektroskopi Ir
-
Upload
yenni-aulia -
Category
Documents
-
view
289 -
download
12
description
Transcript of Ltm Kitik Spektroskopi Ir

SPEKTROSKOPI INFRA MERAH
Oleh Yenni Auliawati, 0906640942, kelompok 2
Cahaya yang dapat dilihat oleh mata kita hanyalah bagian kecil dari spektrum
yang luas dari radiasi elektromagnetik. Di sisi energi langsung spektrum tertinggi ada
pada ultraviolet, dan di sisi energi rendah adalah inframerah (gambar1). Infra merah
memiliki rentang panjang gelombang dari 2.500 sampai 16.000 nm, dengan rentang
frekuensi yang sesuai dari 1,9 * 10 13-1,2 * 10 14 Hz.
Spektroskopi infra merah merupakan suatu metode yang
mengamati interaksi molekul dengan radiasi elektromagnetik yang
berada pada daerah panjang gelombang 2,5 – 50 µm atau pada
bilangan gelombang 4.000 – 200 cm-1
Berdasarkan pembagian daerah panjang gelombang (Tabel 1), sinar inframerah dibagi
atas tiga daerah yaitu:
a. Daerah infra merah dekat
b. Daerah infra merah pertengahan
c. Daerah infra merah jauh
Jenis Vibrasi Molekul
Ada dua jenis vibrasi yaitu:1. Vibrasi ulur (Stretching Vibration), yaitu vibrasi yang mengakibatkan
perubahan panjang ikatan suatu ikatan. Vibrasi stretching meliputi
stretching simetris dan stretching asimetris
2. Vibrasi tekuk (Bending Vibrations), yaitu vibrasi yang mengakibatkan
perubahan sudut ikatan antara dua ikatan
Vibrasi tekuk itu sendiri dibagi lagi menjadi empat:1. Scissoring atom-atom yang terikat pada atom pusatbergerak saling
mendekat dan menjauh hingga sudutnya berubah-ubah
1

2. Rocking atom-atom bergerak bolak balik dalam bidang
3. Wagging atom-atom bergerak bolak balik keluar bidang atau molekul
4. Twisting atom-atom terikat pada molekul yang diam berotasi di sekitar
ikatannya.
Spektra Vibrasi
Vibrasi molekul dapat terjadi dengan dua mekanisme yang berbeda:
Kuanta radiasi inframerah secara langsung mengeksitasi atom: absorpsi
radiasi inframerah oleh atom menghasilkan spektrum inframerah.
Kuanta radiasi tampak secara tidak langsung juga dapat menghasilkan
vibrasi molekul, disebut dengan efek Raman.
InstrumentasiDengan sumber cahaya apapun, spektrometer terdiri atas sumber sinar, prisma, sel sampel, detektor dan pencatat. Sumber sinar
Nearst Glower (rare-earth oxides)
Globar (Silicon carbide)
Nichrome wire
Monokromator:
Ada 3 jenis monokromator, yaitu:
Prisma: penguraian sinar didasarkan pada perbedaan indeksnya di udara dan di dalam
prisma, sehingga sinar diteruskan sesuai dengan panjang gelombang masing-masing.
Difraksi Grating: Penguraian sinar didasarkan pada grating (permukaan benda
seperti gergaji), grating dapat diputar dengan sudut tertentu, sehingga diperoleh sinar
dengan l seperti yang diinginkan.
Inteferometer: Memecah radiasi cahaya ke daerah gelombang yang
berbeda dalam satu proses.
Detektor:
2

Photon detector
Thermal detector
Cara Kerja Cahaya IR dilewatkan melalui sampel, dan jumlah energi yang diserap oleh
sampel per cm panjang gelombang akan disimpan.
Cahaya IR yang diinginkan akan dipilih oleh monokromator sebelum terkena
sampel 'Interferometer' digunakan untuk mengukur panjang gelombang semua
dalam satu waktu berjalan.
Data akan diterjemahkan ke dalam grafik yang diplot sebagai transmisi vs
panjang gelombang
Grafik dapat dibandingkan dengan diketahui referensi standar
Salah satu contoh spektrum adalah vanili, ditunjukkan di lampiran (gambar 4)
Kompleksitas spektrum ini adalah khas spektrum inframerah, yang menggambarkan
penggunaannya dalam mengidentifikasi zat.
Nilai dalam cm -1 adalah jumlah siklus gelombang dalam satu sentimeter, sedangkan,
frekuensi dalam siklus per detik atau Hz sama dengan jumlah siklus gelombang dalam
3 x 10 10 cm (jarak yang ditempuh oleh cahaya dalam satu detik). Panjang gelombang
satuannya dalam mikrometer, mikron (μ), bukan nanometer.
Daerah Identifikasi
Vibrasi yang digunakan untuk identifikasi adalah vibrasi tekuk, khususnya
vibrasi rocking (goyangan), yaitu yang berada di daerah bilangan gelombang 2000 –
400 cm-1. Karena di daerah antara 4000 – 2000 cm-1 merupakan daerah yang khusus
yang berguna untuk identifkasi gugus fungsional. Daerah ini menunjukkan absorbsi
yang disebabkan oleh vibrasi regangan. Sedangkan daerah antara 2000 – 400 cm -1
seringkali sangat rumit, karena vibrasi regangan maupun bengkokan mengakibatkan
absorbsi pada daerah tersebut. Dalam daerah 2000 – 400 cm-1 tiap senyawa organik
mempunyai absorbsi yang unik, sehingga daerah tersebut sering juga disebut sebagai
daerah sidik jari (fingerprint region). Pita-pita absorpsi pada daerah ini berhubungan
dengan vibrasi molekul secara keseluruhan. Setiap atom dalam molekul akan saling
mempengaruhi sehingga dihasilkan pita-pita absorpsi yang khas untuk setiap molekul.
3

Oleh karena itu, pita-pita pada daerah ini dapat dijadikan sarana identifikasi molekul
yang tak terbantahkan.
Penafsiran Spektrum Inframerah
Untuk penafsiran spektrum inframerah tidak ada aturan kaku,
namun syarat-syarat tertentu yang harus dipenuhi sebagai upaya
untuk menafsirkan suatu spektrum adalah:
1. Spektrum harus terselesaikan dan intensitas cukup memadai
2. Spektrum diperoleh dari senyawa murni
3. Spektrofotometer harus dikalibrasi sehingga pita yang teramati
sesuai dengan frekuensi atau panjang gelombangnya. Kalibrasi
dapat dilakukan dengan menggunakan standar yang dapat
diandalkan, seperti polistirena film.
4. Metode persiapan sampel harus ditentukan. Jika dalam bentuk
larutan, maka konsentrasi larutan dan ketebalan sel harus
ditunjukkan
Penggunaan dan Aplikasi
Aplikasi spektroskopi infra merah sangat luas baik untuk
analisis kualitatif maupun kuantitatif. Penggunaan yang paling
banyak adalah pada daerah pertengahan dengan kisaran bilangan
gelombang 4000 sampai 670 cm-1 at-au dengan panjang
gelombang 2.5 sampai 15 μm. Kegunaan yang paling penting
adalah untuk identifikasi senyawa berikatan kovalen karena
spektrumnya sangat kompleks terdiri dari banyak puncak-puncak.
Spektrum infra merah dari senyawa kovalen juga mempunyai sifat
fisik yang karakteristik artinya kemungkinan dua senyawa
mempunyai spektrum sama adalah kecil seka. Radiasi infra merah
dengan frekuensi kurang dari 100 cm-1 atau dengan panjang
gelombang lebih dari 100 μm diserap oleh molekul dan dikonversi
ke dalam energi rotasi molekul. Bila radiasi infra merah dengan
frekuensi dalam kisaran 10000 sampai 100 cm-1 atau dengan
4

panjang gelombang 1 sampai 100 um, maka radiasi akan diserap
oleh molekul dan dikonversi ke dalam energi vibrasi molekul.
Keuntungan
Memberikan sidik jari untuk sampel yang dianalisis Instalasi instrumen ke komputer memungkinkan
perbandingan spektrum sampel dan referensi standar dapat berjalan secara bersamaan
Kekurangan
Jarang digunakan untuk tujuan kuantitatif karena spektrum yang dihasilkan terlalu rumit untuk menentukan satu per satu
Preparasi sampel cukup sulit, perlu keterampilan untuk menanganinya.
Analisis Kualitatif dengan IR
Biasanya frekuensi (bilangan gelombang) dapat di hitung dari
massa atom dan konstanta gaya dengan menggunakan persamaan
σ= 12πc √ Kμ = 1
2πc √ K (m1+m 2)m1m 2
C = kecepatan cahaya; K = konstanta gaya; µ = massa tereduksi;
m1,m2 = massa atom
Akan tetapi secara umum lebih baik menggunakan bagan
korelasi untuk mengidentifikasi gugus fungsi (tabel 2). Ini umumnya
berguna untuk mengklarifikasikan seluruh daerah ke dalam tiga
sampai empat daerah yang lebar. Salah satu cara adalah dengan
mengklasifikasikannya ke dalam daerah IR dekat, tengah atau
fundamental, dan daerah jauh. Cara lainnya adalah dengan
mengklasifikasikannya sebagai daerah ulur hydrogen (2,7 – 3 µ),
daerah ikatan rangkap 3 (3,7 – 5,4 µ), daerah ikatan rangkap dua
(5,1 – 6,5µ) dan daerah sidik jari (6,7 – 14 µ). Dari kedua hasil ini
tampak bahwa dalam kategori kedua semua daerahnya adalah
daerah fundamental, dan ini paling banyak di gunakan. Dengan
menggunakan metode ini, kita dapat mengetahui informasi
mengenai keberadaan suatu senyawa.
5

Analisis Kuantitatif dengan Infra Merah
Dalam penentuan analisis kuantitatif dengan infra merah
digunakan hukum Beer. Hukum Beer menyatakan bahwa
absorbansi cahaya berbanding lurus dengan dengan konsentrasi
dan ketebalan bahan/medium. Yakni A = ε c l . Kita dapat
menghitung absorpsivitas molar (ε ¿ pada panjang gelombang
tertentu, dimana salah satu komponennya mengabsorpsi dengan
kuat sedangkan komponen yang lain absorpsinya lemah atau
bahkan tidak mengabsorpsi. Absorbansi zat yang tidak diketahui
jumlahnya di tentukan pada panjang gelombang ini dengan cara
spektrofotometri simultan. Adanya sinar hamburan pada suatu
waktu membuat hukum Beer tidak dapat digunakan, terutama pada
nilai absorbansi yang tinggi. Oleh karena itu, digunakan metode
empiris. Metode base line adalah metode untuk menyeleksi pita
absorpsi yang di analisis yang tidak jatuh kembali pada pita
komponen yang di analisis. Jika P0 menunjukkan intensitas sinar
yang di dapat dengan cara menarik garis lurus pada kurva spectrum
absorpsi pada posisi pita absorpsi yang di analisis. Transmitan untuk
Pt diukur dari titik absorbsi maksimum. Kurva kaliberasi didapakan
dengan mengalurkan nilai log (P0/Pt) terhadap konsentrasi.
Kebanyakan penggunaan spektroskopi infra merah dalam analisis
kuantitatif adalah untuk menganalisis kandungan udara. Contohnya
jika udara mengandung polutan seperti CO, metal etil keton,
methanol, dan etilen oksida, sampel udara yang mengandung
polutan atmosfer di analisis dengan alat IR.
Daftar Pustaka
6

Anonim. Infrared.
http://www2.chemistry.msu.edu/faculty/reusch/VirtTxtJml/Spectrpy/
InfraRed/infrared.htm (diakses pada 17 Oktober 2010)
Anonim. Spektroskopi Infra merah.
http://id.wikipedia.org/wiki/Spektroskopi_inframerah. (diakses pada
17 Oktober 2010)
S.M.Khopkar. 2008. Konsep Dasar Kimia Analitik. Depok: UI Press.
Lampiran
Gambar 1: spectrum cahaya dan gelombang elektromagnetikSumber:
http://www2.chemistry.msu.edu/faculty/reusch/VirtTxtJml/Spectrpy/InfraRed/infrared.htm
Ranges Far Infrared Middle Infrared
Near Infrared
Wavelength range
50-1000µm 2.5-50µm 0.8-2.5µm
Wavelength number
200-10cm-1 4000-200cm-1 12500-4000 cm-1
7

Energy range 0.025-0.0012eV 0.5-0.025eV 1.55-0.5eV
Tabel 1: Spektrum Infra MerahSumber: PPT Infrared Spectroscopy
Gambar 2: instrumen spektroskopi IR
Sumber:
http://www2.chemistry.msu.edu/faculty/reusch/VirtTxtJml/Spectrpy/InfraRed/infrared.htm
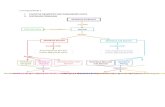
Gambar 3: Prosedur spektroskopi IR Sumber: PPT Infrared Spectroscopy
8

Gambar 4: contoh spektum dalam metode spektroskopi IR, spectrum vaniliSumber: http://www2.chemistry.msu.edu/faculty/reusch/VirtTxtJml/Spectrpy/InfraRed/infrared.htm
Tabel 2. Serapan Khas Beberapa Gugus fungsiGugus Jenis Senyawa Daerah Serapan (cm-1)C-H alkana 2850-2960, 1350-1470C-H alkena 3020-3080, 675-870C-H aromatik 3000-3100, 675-870C-H alkuna 3300C=C alkena 1640-1680C=C aromatik (cincin) 1500-1600C-O alkohol, eter, asam karboksilat, ester 1080-1300C=O aldehida, keton, asam karboksilat, ester 1690-1760O-H alkohol, fenol(monomer) 3610-3640O-H alkohol, fenol (ikatan H) 2000-3600 (lebar)O-H asam karboksilat 3000-3600 (lebar)N-H amina 3310-3500C-N amina 1180-1360-NO2 nitro 1515-1560, 1345-1385
9