LTM - Irsa Septiawan 130405100
-
Upload
damino-dam -
Category
Documents
-
view
222 -
download
0
description
Transcript of LTM - Irsa Septiawan 130405100
Nama : Irsa SeptiawanNIM: 130405100Kelompok: 1Laporan Tugas Mandiri
Reaksi pada Industri Kimia
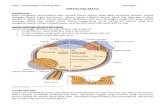
1.1 Reaksi KimiaKata kimia dapat diartikan sebagai suatu proses dimana sebelum dan sesudah proses terjadi perubahan identitas kimia yang ditandai dengan perubahan unsur-unsur penyusunnya dan atau perubahan massa molekulnya ataupun struktur molekulnya, dimana proses tersebut disebut dengan reaksi kimia. Bahan sebelum terjadinya proses reaksi kimia disebut dengan reaktan, hasil dari reaksi kimia tersebut disebut dengan produk, sedangkan proses reaksi kimia yang memisahkan sebelum dan sesudah proses menggunakan simbol panah, sebagaimana seperti contoh berikut :
Pada reaksi diatas, A dan B merupakan reaktan sedangkan P dan Q merupakan produk. Dalam hal ini reaktan dan produk terjadi perubahan identitas kimia yang dapat perubahan struktur, unsur ataupun molekul kimia.Reaksi kimia adalah suatu reaksi antar senyawa kimia atau unsur kimia yang melibatkan perubahan struktur dari molekul, yang umumnya berkaitan dengan pembentukan dan pemutusan ikatan kimia. Berlangsungnya proses tersebut mempunyai dua kemungkinan yaitu memerlukan energi atau melepaskan energi. Selain itu beberapa ciri fisik antara lain : Terbentuknya endapan Terbentuknya gas Terjadinya perubahan warna Terjadinya perubahan suhu atau temperaturSemua reaksi kimia menyangkut perubahan energi yang diwujudkan dalam bentuk panas. Kebanyakan reaksi kimia disertai dengan pelepasan panas, meskipun adapula beberapa reaksi kimia yang menyerap panas. Bahaya dari suatu reaksi kimia terutama adalah karena proses pelepasan energi yang demikian banyak dan dalam kecepatan yang sangat tinggi, sehingga tidak terkendalikan dan bersifat destruktif (merusak) terhadap lingkungan, termasuk operator/orang yang melakukannya.Banyak kejadian dan kecelakaan di dalam laboraturium sebagai akibat reaksi kimia yang hebat atau eksplosif (ledakan). Namun kecelakaan tersebut pada hakikatnya disebabkan oleh kurangnya pengertian atau apresiasi terhadap faktor faktor kimia-fisika yang mempengaruhi kecepatan reaksi kimia. 1.2 Faktor Faktor yang Mempengaruhi Laju Reaksi Sifat Dasar PereaksiZat zat berbeda secara nyata dalam lajunya mereka mengalami perubahan kimia. Natrium bereaksi sangat cepat dengan air pada temperatur kamar, tetapi bereaksi lebih lambat dengan metil alkohol dan etil alkohol. Masing masing reaksi tersebut bersifat serta merta, artinya perubahan energi bebasnya bernilai negatif. Selisih kereaktifannya dapat diterangkan dengan perbedaan struktur yang berlainan dari atom dan molekul bahan yang bereaksi. Jika suatu reaksi melibatkan dua spesi molekul dengan atom yang sudah terikat oleh ikatan kovalen yang kuat, tabrakan antara molekul molekul ini tidak memiliki energi yang cukup untuk memutuskan ikatan molekulnya, sehingga menjadi sulit bereaksi atau kurang reaktif. TemperaturLaju suatu reaksi kimia bertambah dengan naiknya temperatur. Kenaikan laju reaksi ini dapat diterangkan sebagian sebagai lebih cepatnya molekul molekul bergerak kian kemari pada temperatur yang lebih tinggi dan karenanya molekul tersebut lebih sering bertabrakan satu sama lain. Pada temperatur yang ditinggikan, persentase tabrakan yang mengakibatkan reaksi kimia akan lebih besar, karena semakin banyak molekul yang memiliki kecepatan lebih besar dan karenanya memiliki energi cukup untuk bereaksi.
KonsentrasiLaju suatu reaksi dapat dinyatakan sebagai laju berkurangnya konsentrasi suatu pereaksi, atau sebagai laju bertambahnya konsentrasi suatu produk. Oleh karena itu konsentrasi pereaksi tentu saja dapat mempengaruhi kecepatan dalam reaksi.
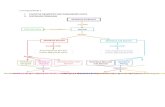
PengadukanPengadukan mempengaruhi laju reaksi dari suatu reaksi yang dapat dilihat pada grafik dibawah ini. Semakin cepat kecepatan stirrer, maka laju reaksi juga akan meningkat.
Gambar A Grafik Pengaruh Pengadukan dengan Laju Reaksi KatalisSalah satu cara lain untuk mempercepat laju reaksi adalah dengan menurunkan energi pengaktifan suatu reaksi. Hal ini dapat dengan menggunakan katalis.Katalis adalah zat yang dapat meningkatkan laju reaksi tanpa dirinya mengalami perubahan kimia secara permanen. Katalis yang berfungsi untuk mempercepat laju reaksi disebut katalisator. Katalisator dapat dibedakan sebagai berikut:1. (Katalisator Homogen), adalah katalisator yang mempunyai fasa sama dengan zat yang dikatalisis. Contohnya adalah besi (III) klorida pada reaksi penguraian hidrogen peroksida menjadi air dan gas oksigen. 2. (Katalisator Heterogen), adalah katalisator yang mempunyai fasa tidak sama dengan zat yang dikatalisis. Umumnya katalisator heterogen berupa zat padat. Banyak proses industri yang menggunakan katalisator heterogen, sehingga proses dapat berlangsung lebih cepat dan biaya produksi dapat dikurangi.Penambahan katalis memberikan perubahan yang berarti pada energi aktivasi. Katalis menyediakan satu rute alternatif bagi reaksi. Rute alternatif ini memliki energi aktivasi yang rendah. Diagram dibawah ini merupakan gambaran keadaan energi :
Katalis hanya mempengaruhi laju pencapaian kesetimbangan, bukan posisi keseimbangan (misal membalikkan reaksi). Katalis tidak menganggu gugat hasil suatu reaksi kesetimbangan dan konsentrasi reaksi atau massanya setalah reaksi selesai sama dengan konsentrasi atau massa reaksi sebelum reaksi dilangsungkan.
1.3 Macam Macam ReaksiNitrasiNitrasi merupakan reaksi substitusi atom H pada benzena oleh gugus nitro. Reaksi ini terjadi dengan mereaksikan benzena dengan asam nitrat (HNO3) pekat dengan bantuan H2SO4 sebagai katalis. Reaksi nitrasi aromatik berupa reaksi 2 tahap. Tahap pertama adalah pembentukan elektrofilik. Tahapan kedua serangan elektrofilik yang membentuk ion hidronium disertai pelepasan H+.
Gambar Reaksi Nitrasi pada Benzena
Sulfonasi Sulfonasi benzena dengan asam sulfat (H2SO4) menghasilkan asam benzena sulfonat. Sulfonasi bersifat mudah balik dan menunjukkan efek isotop kinetik yang sedang. Gugus asam sulfonat mudah digantikan oleh gugus lain. Oleh karena itu, asam arilsulfonat merupakan zat antara yang bermanfaat dalam sintesis
Gambar Reaksi Sulfonasi pada Benzena
Reaksi TransesterifikasiTransesterifikasi adalah proses transformasi kimia molekul trigliserida yang besar, bercabang dari minyak nabati dan lemak molekul yang lebih kecil, molekul rantai lurus, dan hampir sama dengan molekul dalam bahan bakar diesel. Minyak nabati atau lemak hewani bereaksi dengan alkohol dengan bantuan katalis yang menghasilkan alkil ester.
Reaksi Asam & BasaAsam. Secara sederhana (klasik) didefinisikan sebagai zat, yang bila dilarutkan dalam air, mengalami disosiasi dengan pembentukan ion positif hidrogen (H+) tingkat kekuatan asam dihubungkan dengan jumlah parsial H+, yang dihasilkan dari disosiasi. Makin besar jumlah parsial ion positif H yang dihasilkan, maka bisa dikatakan asam juga makin kuat.Secara umum beberapa disosiasi asam dapat digambarkan sebagai berikut :
Basa. Dalam pengertian yang disederhanakan, sifat basa dalam air dipengaruhi oleh pembentukan ion hidroksida. Di alam, unsurnsur golongan I A dan II A, akanmembentuk basa kuat dengan ion hidroksida. Artinya kebanyakan unsurunsur ini secara alamiah telah berikatan dengan hiroksida, sehingga jika melarut dalam air, akan langsung melepaskan ionion hidroksida (anionnya). Sedangkan basabasa lemah (biasanya molekul kovalen) harus bereaksi dengan air, menangkap H+ dari air, sehingga air menyisakan OH.Beberapa penguraian basa di air:
Garam. Suatu asam apa saja jika direaksikan dengan basa apa saja, pasti akan menghasilkan garam, hasil reaksi anion dari asam dengan kation dari basa. Asam kuat, HCl, jika direaksikan dengan basa kuat, NaOH, akan menghasilkan garam netral NaCl dan molekul air.
Masih terdapat banyak reaksi lagi pada industri kimia, seperti alkilasi, halidasi, halogenasi dan lain-lain.
1.4 Reaksi pada Industri KimiaPembuatan BiodieselBiodiesel dibuat melalui suatu proses kimia yang disebut transesterifikasi. Proses ini menghasilkan dua produk yaitu metil esters (biodisel) dan gliserin yang merupakan produk samping. Bahan baku utama untuk pembuatan biodiesel antara lain minyak nabati, lemak hewani, lemak bekas/lemak daur ulang. Sedangkan sebagia bahan baku penunjang yaitu alkohol, tetapi perlu diperhatikan juga kandungan air dalam alkohol tersebut. Bila kandungan air tinggi akan mempengaruhi hasil biodiesel sehingga kualitasnya rendah, karena kandungan sabun dan trigliserida yang tinggi. Disamping itu biodiesel juga dipengaruhi oleh tingginya suhu operasi proses produksi, lamanya waktu pencampuran atau kecepatan pencampuran alkohol.Katalisator dibutuhkan pula guna meningkatkan daya larut pada saat reaksi berlangsung, umumnya katalis yang digunakan bersifat basa kuat yaitu NaOH atau KOH. Katalis yang akan dipilih tergantung minyak nabati yang digunakan.
Reaksi Transesterifikasi