II. TINJAUAN PUSTAKA - repository.ipb.ac.idrepository.ipb.ac.id/bitstream/handle/123456789/51338/Bab...
Transcript of II. TINJAUAN PUSTAKA - repository.ipb.ac.idrepository.ipb.ac.id/bitstream/handle/123456789/51338/Bab...
5
II. TINJAUAN PUSTAKA
A. Metode Near Infrared (NIR) 1. Teori metode near infrared (NIR)
Metode infra merah dekat atau sering disebut dengan nama near
infrared (NIR) merupakan salah satu teknik yang menggunakan wilayah
panjang gelombang infra merah pada spektrum elektromagnetik antara 700
sampai 2500 nm (Dryden, 2003). Hal yang terpenting dari teori NIR reflektan
dan absorban elektromagnetik ini adalah menganalisis komponen, deteksi
kualitas, dan pemasakan (Mohsenin, 1984).
Kisaran panjang gelombang NIR telah lama dipelajari dan digunakan
sebagai metode analitik. Cahaya tampak diterima oleh mata sesuai dengan
besarnya pantulan, seperti halnya warna dihasilkan dari cahaya yang
dipantulkan dari suatu objek. Setiap bahan memiliki spektrum gabungan
pantulan NIR yang unik dan beragam yang dihasilkan dari efek penyebaran,
penyerapan dan pantulan cahaya oleh bahan.
Semua bahan organik terdiri dari atom, karbon, oksigen, hidrogen,
nitrogen, phospor, sulfur dengan sejumlah kecil elemen lain. Atom-atom ini
berkombinasi melalui ikatan kovalen atau elektrovalen membentuk molekul.
Karena sifat ikatannya, gaya elektrostatik ada dalam atom dan molekul
tersebut, sehingga molekul bergerak secara konstan, ini dikenal sebagai
keadaan stabil. Molekul bervibrasi pada frekuensi yang berkaitan dengan
panjang gelombang dalam daerah infra merah dari spektrum elektromagnetik.
Setelah dipancarkan maka radiasi ini akan diserap oleh semua bahan
organik dan informasi utama yang dapat diekstrak adalah stretching dan
bending ikatan kimia C-H (seperti bahan organik turunan minyak bumi), O-H
(seperti kadar air, karbohidrat, dan lemak), C-N, dan N-H (seperti protein dan
asam amino) yang merupakan ikatan dasar dari semua ikatan kimia bahan-
bahan organik.
Informasi tersebut dapat dilihat dari pantulan NIR yang dihasilkan
dalam bentuk spektrum pantulan. Radiasi infra merah tidak mempunyai energi
yang cukup untuk mengeksitasi elektron pada senyawa tetapi dapat
6
menyebabkan senyawa organik mengalami rotasi dan getaran (vibrasi) ikatan
inter-atomic (Osborne et al., 1993). Vibrasi stretching adalah pergerakan atom
yang teratur sepanjang ikatan antara dua atom sehingga jarak antara atom dapat
bertambah atau berkurang. Vibrasi bending adalah pergerakan atom yang
menyebabkan perubahan sudut ikatan antar dua atau pergerakan dari
sekelompok atom terhadap atom lainnya.
Cahaya infra merah dekat yang mengenai bahan memiliki energi yang
kecil dan hanya menembus sekitar satu milimeter permukaan bahan, tergantung
dari komposisi bahan tersebut. Jika cahaya mengalami penyebaran, spektrum
tersebut tetap mengandung informasi contoh penyerapan permukaan bahan
tetapi terjadi distorsi pada puncak gelombang (Dryden, 2003).
Variasi pada ukuran dan suhu partikel sampel mempengaruhi
penyebaran radiasi infra merah pada saat melewati sampel. Partikel berukuran
besar tidak dapat menyebarkan radiasi infra merah sebanyak partikel kecil.
Makin banyak radiasi yang diserap dapat memberikan nilai absorban yang
tinggi dan efeknya besar pada panjang gelombang yang diserap lebih kuat
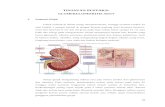
(Dryden, 2003). Pada Gambar 1 menunjukkan diagram penampakkan specular
radiasi near infrared dari sebuah sampel (Dryden, 2003).
Gambar 1 Diagram penampakkan specular (a) diffuse, (b) reflectances, dan (c) absorption radiasi near infrared dari sebuah sampel (Dryden, 2003).
Dalam penerapannya, metode NIR memiliki beberapa kelebihan, antara
lain: dapat menurunkan biaya tenaga kerja penganalisis komposisi, penggunaan
preparat contoh yang sederhana, waktu pendugaan komposisi yang singkat,
analisis contoh yang tidak merusak (non-destructive), tidak menggunakan
bahan-bahan kimia (analisis yang bebas limbah), dan dapat menganalisis
komposisi dengan kecepatan dan ketepatan tinggi (Williams, 1987).
(a) (b) (c)
7
Keunggulan dari gelombang infra merah dekat menurut Osborne et al.
(1993) dalam analisis bahan makanan adalah merupakan gabungan antara
tingkat ketepatan, kecepatan, dan kemudahan dalam melakukan percobaan
(prosedur tidak rumit).
2. Aplikasi metode near infrared (NIR)
Metode near infrared (NIR) telah banyak diperkenalkan dan digunakan
di beberapa negara maju pada benua seperti Eropa, Amerika Utara, Asia,
Australia, dan New Zealand baik dalam bidang industri maupun dalam bidang
pertanian. Sedangkan di Indonesia sendiri, metode ini belum banyak digunakan
terutama di dalam bidang pertanian.
Penerapan metode NIR telah lama berkembang terutama untuk
keperluan bahan pangan, pertanian, kedokteran, farmasi, dan industri kimia.
Untuk bahan pangan dan hasil pertanian seperti kedelai, jagung, beras, daging,
ikan, hortikultura, metode NIR dapat digunakan untuk penentuan komposisi
kimia seperti kadar air, lemak, asam, gula, protein dan berbagai senyawa
lainnya. Selain itu metode NIR digunakan dalam industri susu, yaitu untuk
menentukan kandungan protein, lemak, dan kadar air dalam susu murni dan
menentukan kandungan protein yang terdapat dalam tepung susu skim.
Berdasarkan sifat absorban dan reflektan dari energi radiasi yang
dipancarkan, maka metode NIR dapat digunakan untuk menduga komposisi
kimia suatu bahan. Aplikasi metode NIR dalam industri produk pangan dan
pertanian telah banyak dilakukan. Diawali oleh Norris dan Hart (1962) yang
menemukan bahwa kadar air yang terkandung pada biji-bijian dan bibit
tanaman dapat diukur pada panjang gelombang sebesar 1940 nm.
Pengaplikasian secara komersil metode NIR pertama diperkenalkan oleh
Williams (1973) yang menganalisis gandum dan biji-biji berkadar minyak.
Miller (1990) menggunakan turunan pertama pada pantulan spektrum
untuk mendeteksi adanya jamur hitam, jamur abu-abu dan kerusakan lain
seperti sunscald. Hasilnya menunjukkan bahwa indeks mutu tomat dapat
berdasarkan pada nilai turunan pantulan dengan jangkauan panjang gelombang
antara 590 – 710 nm, sehingga nilai ini dapat digunakan untuk memisahkan
antara tomat yang baik dari jamur hitam, jamur abu-abu dan sunscald.
8
Metode NIR juga dapat digunakan untuk memperkirakan konsentrasi
gula dan asam pada buah-buahan, seperti mangga yang dilakukan oleh
Budiastra et al. (1995). Mereka mengklasifikasikan mangga kedalam tiga jenis
rasa yaitu rasa manis, manis asam, dan asam yang diukur dengan teknologi
NIR pada 200 contoh mangga dengan kisaran panjang gelombang 1400 – 1975
nm. Metode stepwise dari regresi berganda (SMLR) digunakan untuk memilih
panjang gelombang optimal untuk menduga konsentrasi sukrosa dan asam
malat. Panjang gelombang terpilih untuk memprediksi sukrosa dengan NIR
adalah 1533 nm, 1605 nm, 1821 nm sedangkan untuk asam malat adalah 1621
nm, 1813 nm, 1821 nm, 1933, 1941 nm, 1965, dan 1968 nm.
Sugiana (1995) dengan menggunakan NIR Spectrophotometer untuk
mendeteksi kememaran buah apel varietas Rome Beauty dengan panjang
gelombang 900–1400 nm. Hasil yang diperoleh adalah panjang gelombang
NIR yang tepat untuk mendeteksi kememaran buah apel varietas Rome Beauty
adalah 930 nm, 940 nm, 950 nm, 960 nm, 1110 nm, dan 1390 nm. Disimpulkan
juga bahwa kekerasan buah apel tidak terlalu berpengaruh terhadap pantulan
spektrum yang dihasilkan, sehingga hasil pantulan spektrum yang diperoleh
dari setiap apel dikatakan mempunyai sifat sama.
Victor (1996) dengan menggunakan sistem NIR melakukan
pengelompokan buah varietas Manalagi berdasarkan kememaran dengan
panjang gelombang 900 – 2000 nm. Disimpulkan bahwa kedalaman dan
diameter memar buah apel tidak dipengaruhi oleh lama penyimpanan, tetapi
dipengaruhi oleh ketinggian perlakuan memar yang diberikan serta panjang
gelombang 1400 – 2000 nm tidak dapat digunakan untuk membedakan secara
nyata adanya kememaran pada buah apel Manalagi.
Chang et al. (1998) melakukan penelitian untuk menduga total padatan
terlarut jus jeruk, apel, papaya, pear dan pisang. Dari berbagai jus buah tersebut
dikembangkan algoritma umum untuk penentuan total padatan terlarut
beberapa jus buah.
Rosita (2001) menerapkan metode NIR untuk memprediksi mutu buah
duku. Dari penelitian tersebut disimpulkan bahwa NIR dapat memprediksi
kadar gula dan kekerasan buah duku dengan baik. Disimpulkan pula bahwa
9
data absorbansi NIR memberikan nilai korelasi yang lebih tinggi (0.91),
standar error lebih rendah (0.87) dan koefisien keragaman yang akurat (5.39).
Fontaine et al. (2002) menerapkan NIR dalam menduga kandungan
asam amino kedelai. Didapat bahwa 85 - 98 % variasi asam amino mampu
dijelaskan dengan baik menggunakan NIR. Mereka juga telah menggunakan
metode tersebut untuk memprediksi kandungan asam amino esensial beberapa
bahan pakan yakni kedelai, rapeseed meal, tepung biji bunga matahari, polong,
tepung ikan, tepung daging, dan tepung produk samping pemotongan ayam.
Munawar (2002) menerapkan metode NIR untuk menduga kadar gula
dan kekerasan buah belimbing. Dari hasil penelitian disimpulkan bahwa data
absorban NIR dapat menduga kadar gula dan kekerasan buah belimbing
dengan baik. Hal ini ditunjukkan dengan koefisien korelasi yang tinggi.
Mitamala (2003) menerapkan metode NIR untuk menduga kadar air,
karbohidrat, protein, dan lemak tepung jagung. Dari penelitian tersebut
disimpulkan bahwa NIR dapat memprediksi kadar air, karbohidrat, protein, dan
lemak tepung jagung dengan baik. Penggunaan data reflektan mampu
menentukan kadar protein lebih baik dari data absorban. Data absorban dapat
menduga kadar karbohidrat, lemak dan air lebih baik dari data reflektan.
Kusumaningtyas (2004) melakukan pendugaan kadar air, karbohidrat,
protein, lemak, dan amilosa pada beras (Oryza sativa L.) dengan metode NIR.
Panjang gelombang yang digunakan untuk menduga adalah 900 - 2000 nm.
Data reflektan NIR dapat menduga kadar air, karbohidrat, dan protein lebih
baik daripada data absorban. Sedangkan untuk menduga kadar lemak dan
amilosa, data absorban lebih baik dibandingkan data reflektan.
Marthaningtiyas (2005) melakukan pendugaan total padatan terlarut
dan kadar asam belimbing (Averrhoa carambola L.) dengan menggunakan
metode NIR dan JST. Penggunaan analisis komponen utama dalam mereduksi
hasil data absorbansi dari spektrum infra merah dekat sangat efektif.
Andrianyta (2006) menerapkan metode NIR dan jaringan saraf tiruan
(JST) dalam menentukan komposisi kimia jagung secara non-destruktif.
Komposisi kimia yang ditentukan, antara lain kandungan proksimat, lemak, air,
karbohidrat, methionin, tyrosin, threonin, arginin, dan leusin.
10
Quddus (2006) melakukan penentuan kandungan energi bruto tepung
ikan untuk bahan pakan ternak menggunakan metode NIR. Analisis pendugaan
kandungan energi pada tepung ikan tersebut menggunakan metode kalibrasi
SMLR dan PCR. Persamaan kalibrasi dengan metode SMLR menyatakan
bahwa hasil prediksi nilai EM menggunakan data reflektan dan absorban
mendekati hasil uji bioassay. Sedangkan persamaan kalibrasi dengan metode
PCR menghasilkan 10 komponen utama dalam tepung ikan tersebut.
Adrizal et al. (2007) yang melakukan pendugaan kandungan air,
protein, lisin, dan metionin tepung ikan dengan jaringan syaraf tiruan
berdasarkan absorban NIR. Dari hasil penelitian tersebut disimpulkan bahwa
metode JST mampu menduga kandungan air, protein, lisin, dan metionin
tepung ikan dengan akurasi yang lebih baik dibandingkan dengan
menggunakan persamaan regresi yang didapatkan melalui metode SMLR.
Susilowati (2007) pada panjang gelombang 900 - 1400 nm dapat
menduga total padatan terlarut buah pepaya selama penyimpanan dan
pemeraman dengan metode NIR, tetapi panjang gelombang tersebut tidak dapat
digunakan untuk mengukur kekerasan buah. Hubungan antara data absorban
NIR dengan total padatan terlarut dan kekerasan pada penelitian tersebut
dipelajari dengan kalibrasi menggunakan metode SMLR, PCR, dan PLS.
Kelebihan penggunaan metode NIR antara lain disebabkan banyak
komposisi kimia dari bahan pangan dan pertanian yang menyerap (absorption)
atau memantulkan (reflectance) cahaya pada rentang panjang gelombang 0.7 -
3.0 µm. Komposisi kimia lainnya memiliki pola serapan yang khas berbeda
satu dengan lainnya pada setiap panjang gelombang cahaya yang diberikan
(Mohsenin, 1984).
Kendala metode NIR adalah biaya investasi alat yang tinggi. Metode ini
masih tergolong metode sekunder karena memerlukan tahap kalibrasi terutama
bagi sampel uji yang belum pernah menggunakan metode ini misalnya tepung
ikan, bungkil inti sawit, dedak, tepung singkong dan sebagainya. Metode NIR
sangat membantu pekerjaan analisis yang bersifat rumit dan rutin, seperti kadar
air, kadar abu, pH, dan kadar amilosa. Metode ini sangat sesuai karena tidak
lagi banyak memerlukan tahap kalibrasi.
11
B. Kalibrasi dan Validasi
Osborne et al. (1993) menjelaskan bahwa instrumen NIR berguna dalam
menentukan komposisi kimia dengan menggunakan nilai pantulan (R) dan
absorban (log (1/R). Menentukan spektrum pantulan dan absorban NIR maka nilai
hasil analisis kimiawi laboratorium diperlukan. Untuk mengetahui hubungan
antara spektrum-spektrum tersebut dengan nilai referensi dari analisis kimiawi di
laboratorium (metode konvensional) maka perlu menggunakan metode
matematika dengan cara mengkalibrasinya. Untuk tahap kalibrasi sering
digunakan untuk sampel yang memiliki karateristik yang hampir mendekati sama.
Dalam kamus besar bahasa Indonesia (KBBI) kalibrasi adalah tanda-tanda
menyatakan pembagian skala. Kalibrasi dalam teknik spektroskopi diperoleh
dengan mengukur hubungan antara absorban dan reflektan dari panjang
gelombang yang dihasilkan dari spektrometer dengan konsentrasi larutan unsur
yang akan dianalisis (Nur dan Adijuwana, 1989 dalam Rumahorbo, 2004).
Kesulitan dalam mengkalibrasi menurut Osborne et al. (1993) adalah
masalah informasi alam yang kompleks dalam spektrum infra merah contohnya
setiap puncak spektrum hampir selalu tumpang tindih oleh satu atau lebih puncak-
puncak yang lain.
Berbagai macam metode kalibrasi spektrum NIR telah tersedia tetapi dapat
dibagi dalam dua kategori yaitu metode kalibrasi untuk panjang gelombang
terpilih atau sering disebut metode lokal dan metode yang melibatkan seluruh
spektrum atau sering disebut metode global atau juga disebut dengan metode
kalibrasi spektrum penuh (full spectrum calibration methods), seperti: principal
component regression (PCR) dan partial least squares (PLS).
Metode full spectrum banyak digunakan karena data dalam spektrum
direduksi untuk mencegah masalah overfitting tanpa mengurangi dan
menghilangkan satu atau beberapa informasi yang sangat berguna. Jumlah sampel
yang digunakan untuk tahap kalibrasi dan validasi harus cukup banyak. Jumlah
sampel untuk tahap kalibrasi harus lebih banyak dari pada untuk keperluan tahap
validasi. Validasi bertujuan menguji ketepatan pendugaan komposisi kimia
persamaan regresi kalibrasi yang telah dibangun.
12
Selain itu, dikenal pula beberapa perlakuan data sebelum spektrum
dianalisis seperti smoothing, normalisasi, derivatif pertama dan kedua, standard
normal variate (SNV) dan de-trending (DT) (Osborne et al., 1993). Setiap
perlakuan data mempunyai fungsi yang berbeda-beda terhadap data spektrum.
Pada penelitian ini perlakuan data yang diberikan adalah smoothing, derivatif
kedua Savitzky-Golay, dan kombinasi kedua perlakuan data tersebut.
Prosedur derivatif kedua yang paling umum digunakan yaitu prosedur
Savitzky-Golay yang dikelaskan oleh Norris dan William (1990). Data spektrum
sering diubah menjadi bentuk smoothing dan derivatif, secara umum untuk
memperbaiki bentuk dan model persamaan regresi kalibrasi.
Smoothing berfungsi untuk memilih penghalusan fungsi dengan teliti tanpa
menghilangkan informasi spektrum yang ada dan mengurangi guncangan (noise)
dan memperkecil galat (kekeliruan) yang terjadi selama pengukuran NIR dan
analisis kimiawi laboratorium. Derivatif kedua Savitzky-Golay berfungsi untuk
mereduksi efek basis dari adanya pertambahan dari proses absorban (shoulder
effect) serta menghilangkan masalah basis kemiringan persamaan regresi.
Kombinasi antara smoothing dan derivative kedua Savitzky-Golay dapat
diterapkan dan akan mendapatkan bentuk dan model persamaan regresi kalibrasi
yang optimum, layak, dan dapat dipercaya (Blanco dan Villarroya, 2002 dalam
Yogaswara, 2005).
C. Metode Kalibrasi Multivariatif
Analisis data NIR dapat dimanfaatkan dengan mempelajari hubungannya
dengan sifat bahan yang diukur. Kegiatan mempelajari hubungan tersebut pada
umumnya dilakukan dengan beberapa metode kalibrasi, antara lain Stepwise
multiple linear regression (SMLR), principal component regression (PCR),
backward dan partial least squares (PLS).
Lammertyn et al., (1998) menganalisis data NIR Spectroscopy
menggunakan metode kalibrasi multivariatif seperti principal component
regression dan partial least squares dalam memprediksi sifat-sifat kimiawi seperti
keasaman dan total padatan terlarut pada buah apel Jonagold.
13
Metode kalibrasi multivariatif yang digunakan pada penelitian yang
berjudul pendugaan komposisi kimia modified cassava flour adalah principal
component regression (PCR) dan partial least squares (PLS).
1. Metode principal component regression (PCR)
Metode principal component regression merupakan suatu metode
kombinasi antara analisis regresi dan analisis komponen utama (Principal
Component Analysis, PCA). Prinsip analisis komponen utama adalah mencari
komponen utama yang merupakan kombinasi linier dari variabel asli.
Metode regresi komponen utama (PCR) ditetapkan bila dalam
pembentukan model pendugaan variabel bebas yang digunakan banyak dan
terdapat hubungan yang erat antar variabel bebasnya. Metode tersebut dapat
digunakan untuk pendugaan kalibrasi peubah ganda dan mengatasi kolinier
ganda.
Menurut Miller & Miller (2000), komponen-komponen utama yang
dipilih sedemikian rupa sehingga komponen utama pertama memiliki variasi
yang terbesar dalam set data, sedangkan komponen utama kedua tegak lurus
terhadap komponen utama pertama dan memiliki variasi terbesar berikutnya.
Metode ini pertama kali diperkenalkan oleh Pearson (1901) dan secara
terpisah oleh Hotelling (1933). Pemikiran dasar metode analisis ini adalah
mendiskripsikan variasi sebuah set data multivariatif dengan sebuah set data
baru dimana variabel-variabel baru tidak berkorelasi satu sama lain. Variabel-
variabel baru adalah kombinasi linier dari variabel asal. Variabel baru
diturunkan dalam arah menurun sehingga beberapa komponen pertama
mengandung sebanyak mungkin variasi data asal (Pearson, 1901 dalam
Marthaningtiyas, 2005).
Siska dan Hurburgh (1996) dalam Andrianyta (2006), menggunakan
metode principal component regression (PCR) untuk mengidentifikasi variasi-
variasi utama pada spektrum absorban sampel jagung. Sedangkan Quddus
(2006) menentukan kandungan energi bruto tepung ikan untuk bahan pakan
ternak dengan data reflektan dan absorban menggunakan metode kalibrasi
multivariatif yaitu PCR.
14
2. Metode partial least squares (PLS)
Metode regresi kuadrat terkecil parsial atau sering disebut partial least
squares (PLS) pertama kali dikembangkan oleh Herman Wold (1982). Model
partial least square didefinisikan dari dua persamaan linier yang disebut model
struktural dan metode pengukuran (Wold, 1982 dalam Wulandari 2000).
Metode PLS digunakan untuk memperkirakan serangkaian variabel
tidak bebas (respons) dari variabel bebas (prediktor) yang jumlahnya sangat
banyak, memiliki struktur sistematik linear atau nonlinear, dengan atau tanpa
data yang hilang, dan memiliki kolinearitas yang tinggi. Metode ini
membentuk model dari variabel yang ada untuk merangkai respons dengan
menggunakan regresi kuadrat terkecil dalam bentuk matriks (Lindblom, 2004
dalam Saragih, 2007).
Metode tersebut juga mempunyai keuntungan yaitu dapat
mengoptimalkan hubungan prediktif antara 2 (dua) kelompok peubah bebas
dan tidak bebas dan permodelannya tidak mengasumsikan sebaran dari peubah
bebas saja tetapi peubah tidak bebas ikut diasumsikan (Wold, 1982 dalam
Wulandari 2000).
Jensen et al. (2001) mengevaluasi perubahan mutu butir walnut
(Junglens regia L.) dengan menerapkan metode NIR dan partial least square
sebagai metode kalibrasi. Model tersebut dapat melakukan kalibrasi NIR
dengan hasil yang tepat pada panjang gelombang 400 – 2490 nm. Selain itu,
NIR dapat menjelaskan kandungan heksanal kacang walnut sebesar 72%.
Pada dasarnya pendekatan PLS adalah penggabungan model pendugaan
sebagai pengembangan model-model kalibrasi yang melibatkan lebih dari dua
peubah laten (bebas dan tidak bebas). Proses pendugaan menggunakan metode
kuadrat terkecil yang diaplikasikan pada persamaan hubungan model struktural
dan model pengukuran (Ratnaningsih, 2004).
Metode kuadrat terkecil parsial (PLS) tidak memerlukan asumsi-asumsi
yang ketat terhadap sebaran dari peubah, sisaan dan parameter, sehingga
metode ini sering disebut metode lunak (Ratnaningsih, 2004). Metode tersebut
diperoleh secara iteratif dan tidak memiliki formula tertutup untuk mecari
ragam koefisien regresi.
15
D. Tepung Singkong
Ubi kayu atau singkong merupakan sumber karbohidrat yang penting
setelah padi, jagung, dan sagu. Ubi kayu ini berasal dari Negara Brasil. Singkong
memiliki nama botani Manihot esculenta Crantz tapi lebih dahulu dikenal dengan
nama Manihot utilissima Pohl, yang dalam nama daerahnya disebut pula kaspe,
budin, sampeu, atau ketela pohon (Mulyandari, 1992).
Tanaman ini merupakan tanaman dikotil yang termasuk ke dalam famili
Euphorbiaceae. Singkong dapat dimanfaatkan secara langsung sebagai bahan
pangan pokok ataupun diolah menjadi produk setengah jadi berupa pati singkong
(tepung tapioka), gaplek, dan tepung singkong (Febriyanti, 1990).
Menurut SNI 01-2997-1992, tepung singkong adalah tepung yang dibuat
dari bagian umbi singkong yang dapat dimakan, melalui penepungan singkong
iris, parut, ataupun bubur kering dengan mengindahkan ketentuan-ketentuan
kebersihan. Syarat mutu tepung singkong sesuai SNI dapat dilihat pada Tabel 1.
Tabel 1 Syarat mutu tepung singkong menurut SNI 01-2997-1992
No. Jenis Uji Satuan Persyaratan 1. Keadaan
Bau Rasa Warna
- - -
Khas singkong Khas singkong
Putih 2. Benda asing - Tidak boleh ada 3. Derajat putih % Min. 85 4. Kadar abu % b/b Maks. 1.5 5. Kadar air % b/b Maks. 12 6. Derajat asam Ml N NaOH/100g Maks. 3 7. Asam sianida Mg/kg Maks. 40 8. Kehalusan % lolos (80 mesh) Min. 909. Kadar pati % b/b Min. 75 10. Bahan Tambahan Pangan Sesuai SNI 01-02220-1995 - 11. Cemaran logam
Timbal Tembaga Seng Raksa Arsen
mg/kg mg/kg mg/kg mg/kg mg/kg
Maks. 1.0 Maks. 10.0 Maks. 40.0 Maks. 0.05 Maks. 0.5
12. Cemaran mikroba Angka lempeng total E. coli Kapang
Koloni/g APM/g
Koloni/g
Maks. 1.0 x 106
< 3 Maks. 1.0 x 104
Sumber: Dewan Standardisasi Nasional (SNI 01-2997-1992)
16
Tepung singkong telah banyak digunakan dalam pembuatan produk-
produk pangan, antara lain seperti roti, biskuit, mie instan, dan lain-lain. Tepung
singkong dapat dimodifikasi untuk memperoleh mutu produk yang lebih baik dan
sesuai dengan keinginan. Modifikasi tepung singkong telah dilakukan peneliti
terdahulu seperti Muharram (1992), yang memodifikasi tepung singkong dengan
pengukusan, penyangraian, dan penambahan GMS (Glyceril Mono Stearat).
Di beberapa Negara juga dikenal produk tepung-tepung dari bahan ubi
kayu (singkong) dengan nama yang berbeda-beda, misal saja menurut Meuser
(1978) dalam Febriyanti (1990) farinha de mandioca (Brazil) yang dibuat dengan
cara pengupasan kulit, pemerutan ubi, kemudian dikempa untuk mengurangi
kadar air awalnya dan pemanggangan dalam wadah tembaga.
Selain itu, dikenal juga gari (Nigeria) yaitu tepung singkong yang dibuat
dengan cara pencacahan ubi kayu, dan kemudian dilakukan fermentasi sebelum
pengeringan (Weber et al., 1978 dalam Rahman, 2007). Setiap produk tepung
singkong yang dihasilkan oleh beberapa Negara memiliki kadar air yang berbeda-
beda. Beberapa produk tepung singkong serta kandungan kadar airnya di beberapa
Negara dapat dilihat pada Tabel 2.
Tabel 2 Produk tepung singkong di beberapa Negara
Produk Kadar Air (%) Farinha grossa (Brazil) 9.1 Cassava starch (Berlin) 12.0 Cassava starch (Colombia) 12.4 Cassava flour “Hein” (Jerman) 8.6 Gari (Nigeria) 11.7
Sumber: Weber et al. (1978) dalam Rahman (2007)
Modifikasi tepung singkong juga telah dilakukan oleh Laboratorium
Kimia dan Biokimia Hasil Pertanian, Fakultas Teknologi Pertanian, Universitas
Jember (LAB. KBHP-UNEJ). Modifikasi tepung singkong tersebut dilakukan
proses fermentasi, sehingga dihasilkan produk baru yang merupakan turunan dari
tepung singkong yang diberi nama Modified Cassava Flour (MOCAF).
Komposisi kimia MOCAF tidak jauh berbeda dengan tepung singkong,
tetapi MOCAF mempunyai karakteristik fisik dan organoleptik yang spesifik.
Kandungan protein MOCAF lebih rendah dibandingkan tepung singkong, dimana
senyawa ini dapat menyebabkan warna cokelat ketika pengeringan dan
17
pemanasan. Perbedaan komposisi kimia MOCAF dengan tepung singkong dapat
dilihat pada Tabel 3.
Tabel 3 Perbedaan komposisi kimia MOCAF dengan tepung singkong
Parameter MOCAF Tepung Singkong Kadar Air (%) Max. 13 Max. 13 Kadar Protein (%) Max. 1.0 Max. 1.2 Kadar Abu (%) Max. 0.2 Max. 0.2 Kadar Pati (%) 85-87 82-85 Kadar Serat (%) 1.9-3.4 1.0-4.2 Kadar Lemak (%) 0.4-0.8 0.4-0.8 Kadar HCN (mg/kg) Tidak Terdeteksi Tidak Terdeteksi
Sumber: Subagio et al. (2008)
E. Modified Cassava Flour (MOCAF)
Modified cassava flour atau MOCAF merupakan produk turunan dari
tepung singkong yang menggunakan prinsip modifikasi sel singkong secara
fermentasi, dimana mikrobia BAL mendominasi selama fermentasi tepung
singkong ini (Subagio et al., 2008). MOCAF dalam bentuk kemasan plastik
dengan berat 100 gram dan 500 gram dapat dilihat pada Gambar 2.
Secara teknis, cara pengolahan MOCAF sangat sederhana, mirip dengan
cara pengolahan tepung singkong biasa, namun disertai dengan proses fermentasi.
Singkong dibuang kulitnya, dikerok lendirnya, dan dicuci sampai bersih.
Kemudian dilakukan pengecilan ukuran singkong dilanjutkan dengan tahap
fermentasi selama 12 – 72 jam. Setelah fermentasi, singkong tersebut dikeringkan
kemudian ditepungkan sehingga dihasilkan produk modified cassava flour.
Gambar 2 Modified cassava flour (MOCAF) dalam bentuk kemasan plastik dengan berat 100 gram dan 500 gram (Munthe, 2008).
18
Subagio et al. (2008) melaporkan bahwa mikroba yang tumbuh pada
singkong akan menghasilkan enzim pektinolitik dan selulolitik yang dapat
menghancurkan dinding sel singkong sedemikian rupa sehingga terjadi
pembebasan granula pati. Granula pati adalah butiran-butiran kecil yang memiliki
sifat mereflesikan cahaya terpolarisasi. Proses pembebasan granula pati ini akan
menyebabkan perubahan karakteristik dari tepung yang dihasilkan berupa naiknya
viskositas, kemampuan gelasi, daya rehidrasi, dan kemudahan melarut.
Selanjutnya granula pati tersebut akan mengalami hidrolisis menghasilkan
monosakarida sebagai bahan baku untuk menghasilkan asam-asam organik,
terutama asam laktat. Senyawa asam ini akan bercampur dalam tepung, sehingga
ketika tepung tersebut diolah akan menghasilkan aroma dan cita rasa yang khas
yang dapat menutupi aroma sampai 70% dari cita rasa singkong yang cenderung
tidak disukai konsumen (Subagio et al., 2008).
Proses hidrolisis pati menjadi monosakarida dapat menurunkan viskositas
MOCAF, akan tetapi proses hidrolisis pati ini terjadi setelah proses pembebasan
granula pati yang menaikkan viskositas. Selain itu, proses pembebasan granula
pati lebih dominan dibandingkan dengan proses hidrolisis pada fermentasi yang
terjadi. Hal ini nampak dari semakin meningkatnya viskositas pasta panas dan
pasta dingin MOCAF dengan semakin lama fermentasi.
Namun demikian, dengan fermentasi selama 72 jam akan didapatkan
produk MOCAF yang mempunyai viskositas mendekati tepung tapioka (data
tidak ditunjukkan). Hal ini dapat dipahami bahwa semakin lama waktu fermentasi
maka akan semakin banyak sel-sel singkong yang pecah, sehingga pembebasan
granula pati menjadi semakin meningkat (sangat ekstensif) (Subagio et al., 2008).
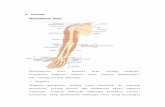
Pada Gambar 3 dan 4 menunjukkan tahapan proses pembuatan MOCAF
berdasarkan Prosedur Operasi Standar (POS) produksi MOCAF berbasis klaster,
dimana terdapat 2 (dua) kali proses perendaman. Perendaman I dilakukan pada air
yang telah ditambahkan dengan senyawa aktif A dengan ketentuan 1 m3 air sawah
dilakukan penambahan senyawa aktif A sebanyak 1 sendok teh, dan untuk 1 m3
air sumber pegunungan dilakukan penambahan senyawa aktif A sebanyak 1
sendok makan. Kemudian dilakukan penambahan senyawa aktif B, yang dibuat
dengan cara merendam chips singkong segar sebanyak 1 ons dalam air yang telah
19
dicampur enzim (1 sendok teh) dan kultur mikroba (1 sendok makan),
perendaman dilakukan selama 24 – 30 jam untuk menghasilkan senyawa aktif B
yang diinginkan. Senyawa aktif B yang dihasilkan dapat dipergunakan semua
untuk air sebanyak 1 m3 (Subagio et al., 2008).
Selanjutnya pada perendaman II, bahan direndam pada larutan senyawa
aktif C (1 sendok makan dalam 1 m3 air) selama 10 menit. Tujuan dari proses
perendaman ini adalah mencuci scum (protein) dari ubi yang dapat menyebabkan
warna cokelat ketika pengeringan dan juga akan menghentikan pertumbuhan lebih
lanjut dari mikroba (Subagio et al., 2008).
Gambar 3 Diagram alir proses pengolahan singkong menjadi chips kering (Subagio et al., 2008).
Singkong Segar
Penerimaan Singkong
Pengupasan
Pencucian
Pengecilan Ukuran (Tebal
chip = 1-1.5 mm)
Perendaman I T = 12-72 jam
Perendaman II (t ≥ 10 menit)
Pressing Pembuburan Pengeringan
Chips Kering
Pengakutan Chips
Perendaman (t = 24-30 jam)
Air
Air
Senyawa Aktif A
Senyawa Aktif C
Chips Singkong (± 1 Ons)
Senyawa Aktif B
Air Enzim
Kultur Mikroba
Kulit
Limbah cair
Limbah cair
Limbah cair
Penyimpanan
A
20
Gambar 4 Diagram alir proses pengolahan chips kering menjadi MOCAF di
pabrik induk (Subagio et al., 2008).
Selama proses fermentasi terjadi proses penghilangan komponen penimbul
warna, seperti pigmen (khususnya pada ketela kuning) dan protein yang dapat
menyebabkan warna coklat ketika pemanasan. Dampaknya adalah warna MOCAF
yang dihasilkan lebih putih jika dibandingkan dengan warna tepung ubi kayu
biasa. Selain itu, proses ini akan menghasilkan tepung yang secara karakteristik
dan kualitas hampir menyerupai tepung terigu dan tapioka (Anonimf, 2009).
MOCAF mempunyai karakteristik yang khas, sangat berbeda dengan
tepung terigu, tepung beras, tepung singkong, tepung tapioka ataupun tepung yang
lainnya. Sehingga dalam aplikasinya, diperlukan sedikit perubahan dalam formula
atau prosesnya sehingga akan dihasilkan produk dengan mutu optimal.
Pada penelitian ini bahan yang digunakan adalah MOCAF yang diperoleh
dari distributor PT. Tiga Pilar Sejahtera (TPS) Agro, Tebet, Jakarta selatan, tetapi
di produksi oleh koperasi Loh Jinawi, Trenggalek, Jawa Timur. Spesifikasi
MOCAF yang diproduksi oleh koperasi tersebut dapat dilihat pada Tabel 4.
Penerimaan Chip Kering
Pengeringan (Artificial drying)
Penepungan
Pengayakan
A
MOCAF
Pengayakan
Pengemasan
Pengangkutan
Produk MOCAF
Sortiran
Penyimpanan
21
Tabel 4 Spesifikasi modified cassava flour (MOCAF) yang diproduksi oleh Koperasi Loh Jinawi Trenggalek
No. Parameter Satuan Hasil 1. Keadaan:
Warna Aroma Rasa
- - -
Putih Netral Netral
2. Kadar Air % Max. 13 3. Kadar Protein % Max. 1.0 4. Kadar Abu % Max. 0.2 5. Kadar Pati % 82-87 6. Kadar Serat % 1.9-3.4 7. Kadar Lemak % 0.4-0.8 8. Kadar HCN mg/kg Tidak Terdeteksi 9. Derajat Keputihan % 88-91
Sumber: Subagio (2007)
MOCAF merupakan produk hasil olahan dari singkong yang dapat
dimakan (edible cassava). Oleh karena itu, syarat mutu MOCAF dapat mengacu
kepada CODEX STAN 176-1989 (Rev. 1-1995) tentang edible cassava flour.
Syarat-syarat mutu edible cassava flour dalam CODEX STAN 176-1989 (Rev. 1-
1995) dapat dilihat pada Tabel 5.
Tabel 5 Syarat mutu edible cassava flour dalam CODEX STAN 176-1989 (Rev. 1-1995)
No. Jenis Uji Satuan Persyaratan Mutu 1. Kadar air % Maks. 13 2. Kadar abu % Maks. 3 3. Kadar Serat Kasar % Maks. 2 4. Kadar HCN mg/kg Maks. 10 5. Residu pestisida - Sesuai dengan aturan yang berlaku 6. Logam berat - Tidak terdeteksi 7. Bahan Tambahan - Tidak terdeteksi
Sumber: CODEX STAN 176-1989 (Rev. 1-1995)
MOCAF ternyata tidak hanya bisa dipakai sebagai bahan pelengkap,
namun dapat langsung digunakan sebagai bahan baku dari berbagai jenis
makanan, mulai dari mie, bakery, cookies hingga makanan semi basah.
Namun demikian, Berdasarkan penelitian sebelumnya, produk-produk makanan
yang dibuat dengan berbahan baku 100% MOCAF mempunyai karakteristik yang
tidak jauh berbeda dengan produk yang dibuat menggunakan tepung terigu
berprotein rendah (pastry flour) (Anonimf, 2009).
22
Selain itu, hasil uji coba yang telah dilakukan menunjukkan bahwa
MOCAF dapat mensubstitusi tepung terigu hingga tingkat substitusi 15% pada
produk mie instan dengan mutu baik, dan hingga 25 % untuk mie bermutu rendah.
Bahkan alternatif aplikasi MOCAF untuk dipergunakan pada makanan bayi
sedang diteliti (Anonimf, 2009).
F. Pati, Amilosa, dan Amilopektin
Pati merupakan cadangan karbohidrat yang banyak terdapat pada tanaman,
yang memiliki homopolimer glukosa dengan ikatan α-glikosidik. Pati merupakan
sumber karbohidrat utama bagi manusia. Pati memiliki karakteristik tertentu
berdasarkan bentuk, ukuran, distribusi ukuran, komposisi, dan kekristalan
granulanya (Belitz dan Grosch, 1987 dalam Rahman, 2007).
Pada tanaman, pati terdapat dalam bentuk butiran-butiran kecil yang
disebut granula. Menurut Winarno (2002) menyatakan bahwa granula pati
mempunyai sifat mereflesikan cahaya terpolarisasi, sehingga dibawah mikroskop
terlihat kristal hitam putih. Sifat inilah yang disebut birefringent. Pada saat
granula pecah maka sifat birefringent ini akan menghilang.
Granula pati tersusun atas tiga komponen utama, yaitu amilosa,
amilopektin, dan bahan antara seperti lipid dan protein. Perbandingan jumlah
diantara ketiga komponen tersebut berbeda-beda untuk tiap jenis pati, tergantung
dari sifat-sifat botani sumber pati tersebut. Fraksi terlarut disebut amilosa dan
fraksi tidak terlarut disebut dengan amilopektin (Winarno, 2002).
Amilosa merupakan rantai lurus yang terdiri dari molekul-molekul glukosa
yang berikatan D-glukosa dengan ikatan α-(1,4) glikosidik. Struktur amilosa dapat
dilhat pada Gambar 5. Amilosa seringkali dikatakan sebagai struktur linier dari
pati, meskipun sebenarnya jika dihidrolisis dengan β-amilase pada beberapa jenis
pati tidak diperoleh hasil yang sempurna. β-amilase menghidrolisis amilosa
menjadi unit-unit residu glukosa dengan memutuskan ikatan α-(1,4) dari ujung
non-pereduksi rantai amilosa (Hoseney, 1998 dalam Panikulata, 2008).
Panjang polimer dipengaruhi oleh sumber pati dan akan mempengaruhi
berat molekul amilosa. Pada umumnya amilosa dari umbi-umbian mempunyai
berat molekul yang lebih besar dibandingkan dengan berat molekul amilosa
s
s
m
l
i
d
s
a
g
A
m
m
serealia, den
serealia (Mo
Juml
mirip denga
larut pada k
ikatan hydro
dalam Rahm
Amil
serta ikatan
amilopektin
glukosa dal
Amilopektin
mengendap
melarutkan p
ngan rantai
oorthy, 2004
lah atau kada
an pati tanam
kondisi yang
ogen dengan
man, 2007).
Gamb
lopektin ada
n α-(1,6)
sama sepe
lam jumlah
n dapat laru
kembali. A
pati dalam a
polimer leb
dalam Pani
ar amilosa p
man lain. Am
drastis sepe
n alkali atau
bar 5 Struk
alah polimer
pada titik
erti amilosa,
yang besa
ut dalam air
Amilopektin
air panas di b
bih panjang
ikulata, 2007
ati pada sing
milosa tidak
erti suhu yan
reagen yan
ktur amilosa
r dengan ik
percabanga
, yaitu terd
ar (Wurzbur
dan tidak
dan amilos
bawah suhu g
g daripada r
7).
gkong berad
dapat larut d
ng tinggi ata
g sesuai (Be
(Chaplin, 20
katan α-(1,4)
annya. Pad
iri dari ran
rg, 1968 da
mempunyai
sa dapat dip
gelatinisasi.
rantai polim
da pada kisar
dalam air, h
au dengan pe
elitz dan Gr
006).
) pada ranta
da dasarnya
ntai pendek
alam Rahm
kecenderun
pisahkan de
23
mer amilosa
ran 20-27%
hanya dapat
emotongan
osch, 1987
ai lurusnya
a, struktur
α-(1,4)-D-
man, 2007).
ngan untuk
engan cara