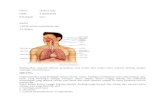
Hubungan DO Dan pH Dengan Respirasi Ikan
-
Upload
david-putra-pradana -
Category
Documents
-
view
607 -
download
6
description
Transcript of Hubungan DO Dan pH Dengan Respirasi Ikan

BAB I
PENDAHULUAN
A. Latar Belakang
Kualitas perairan ditentukan oleh faktor biologis, faktor kimia, dan faktor
fisika. Salah satu faktor kimia adalah kelarutan oksigen (DO) dan derajat
keasaman (pH). Menurut Yuliani dan Raharjo (2013), fluktuasi kualitas air
dipengaruhi antara lain oleh agitasi udara, fotosintesis tumbuhan air, dan aktivitas
mikroba dekomposter. Kadar oksigen rendah dan pH yang rendah akan
berpengaruh terhadap aktivitas respirasi ikan.
Kadar kelarutan oksigen menentukan kualitas suatu perairan, semakin
tinggi kualitas air semakin baik kehidupan ikan dan organisme air lain di
dalamnya. Proses metabolisme ikan membutuhkan oksigen untuk menghasilkan
energi untuk pertumbuhan dan perkembangbiakan. Sumber utama oksigen dalam
perairan berasal dari proses difusi dari udara bebas dan hasil fotosintesis
tumbuhan yang hidup dalam perairan tersebut (Salmin, 2000). Kecepatan difusi
oksigen dari udara, tergantung dari kekeruhan air, suhu, salinitas, pergerakan
massa air dan udara, kadar garam (salinitas), luas daerah permukaan perairan yang
terbuka, tekanan atmosfer, dan prosentase oksigen di sekelilingnya (Edward dan
FS. Pulumahuny, 2003). Ph sangat penting sebagai parameter kualitas air karena
dapat mengontrol tipe dan laju kecepatan reaksi beberapa bahan di dalam air,
selain itu ikan dan mahluk-mahluk akuatik lainnya hidup pada selang pH tertentu,
sehingga dengan diketahuinya nilai pH maka kita akan tahu apakah air tersebut
sesuai atau tidak untuk menunjang kehidupan organisme air termasuk di dalamnya
ikan dan tumbuhan air.
Ikan akan melakukan mekanisme homeostasi yaitu dengan berusaha untuk
membuat keadaan stabil sebagai akibat adanya perubahan variabel lingkungan.
Mekanisme homeostasis ini terjadi pada tingkat sel yaitu dengan pengaturan
metabolisme sel, pengontrolan permeabilitas membran sel dan pembuangan sisa
metabolisme. Reaksi enzimatis sangat bergantung pada suhu, karena aktifitas
metabolisme di berbagai jaringan atau kehidupan suatu organism bergantung pada
kemampuan untuk mempertahankan suhu yang sesuai dengan dalam tubuhnya.
1

Berdasarkan uraian di atas, maka dilakukan praktium dengan judul
“Pengaruh Kadar Oksigen Terlarut (DO) dan Derajat Keasaman (pH) terhadap
Aktivitas Ikan Nila (Oreochromis niloticus)” untuk mengetahui pengaruh DO dan
pH terhadap aktivitas ikan nila dan mempelajari hubungan antara oksigen terlarut
(DO) dan derajat keasaman (pH) di suatu ekosistem.
B. Rumusan Masalah
Berdasarkan latar belakang di atas, dapat dirumuskan masalah sebagai
berikut :
1. Bagaimana pengaruh kadar oksigen terlarut (DO) dan kadar pH terhadap
aktivitas ikan nila merah (Oreochromis niloticus) di kondisi terang maupun
gelap?
2. Bagaimana hubungan antara oksigen terlarut (DO) dan derajat keasaman (pH)
di suatu ekosistem?
C. Tujuan
Adapun tujuan dalam praktikum ini adalah sebagai berikut :
1. Untuk mengetahui pengaruh kadar oksigen terlarut (DO) dan kadar pH
terhadap aktivitas ikan nila merah (Oreochromis niloticus) di kondisi terang
maupun gelap.
2. Untuk mempelajari hubungan antara oksigen terlarut (DO) dan derajat
keasaman (pH) di suatu ekosistem.
2

BAB II
KAJIAN PUSTAKA
A. Ikan Nila Merah (Oreochromis niloticus)
Ikan nila (Oreochromis niloticus) termasuk dalam genus Oreochromis
yang merupakan spesies yang berasal dari kawasan sungai Nil dan danau-danau
sekitarnya di Afrika. Jenis ini merupakan ikan konsumsi air tawar yang banyak
dibudidayakan di lebih dari 85 negara. Saat ini telah tersebar ke negara beriklim
tropis dan subtropis, sedangkan di wilayah iklim dingin tidak dapat hidup dengan
baik (Sugiarto,1988 dalam Suyono, dkk 2011). Ikan nila merah mempunyai sifat
omnivora yang dapat memanfaatkan plankton dan perifiton, serta dapat mencerna
alga biru dan alga hijau sebagai makanan alaminya.
Ikan nila merah mempunyai ciri-ciri morfologi seperti bentuk tubuh
memanjang, pipih ke samping, dan warna putih kehitaman. Selain itu, mempunyai
garis vertikal sepanjang tubuh sebanyak 9 – 11 buah, garis-garis pada sirip ekor
bewarna merah, dan berjumlah 6 – 12 buah, pada sirip punggung terdapat garis-
garis miring, mata tampak menonjol dan besar, gurat sisi (linea lateralis) terputus
di bagian tengah badan kemudian berlanjut tetapi letaknya lebih ke bawah
daripada letak garis yang memanjang diatas sirip dada, sirip punggungnya
bewarana hitam, tetapi bagian pinggir bewarna abu-abu hitam (Khairul dan
Khoiruman, 2008 dalam Suyono dkk, 2011).
Gambar 2.1 Ikan nila merah (Oreochromis niloticus)Sumber: (http://bisnisukm.com/sukses-budidaya-ikan-nila.html)
Ikan nila merah merupakan ikan tropis yang menyukai perairan yang
dangkal. Ikan nila merah dikenal sebagai ikan yang tahan terhadap perubahan
lingkungan tempat hidupnya. Ikan nila merah hidup di lingkungan air tawar, air
3

payau, dan air asin. Kadar garam air yang disukai antara 0 – 35 ppt. Ikan nila air
tawar dapat dipindahkan ke air asin dengan proses adaptasi bertahap. Kadar garam
air dinaikkan sedikit demi sedikit. Pemindahan ikan nila secara mendadak ke
dalam air yang kadar garamnya sangat berbeda dapat mengakibatkan stress dan
kematian ikan (Suyanto, 2004 dalam Jaya, 2012).
Tempat hidup ikan nila merah biasanya berada pada perairan yang dangkal
dengan arus yang tidak begitu deras, ikan ini tidak suka hidup di perairan yang
bergerak (mengalir), akan tetapi jika dilakukan perlakuan terhadap ikan nila
seperti pengadaptasian terhadap lingkungan air yang mengalir maka ikan nila juga
bisa hidup baik pada perairan yang mengalir. (Djarijah, 2002 dalam Jaya, 2012).
Lingkungan tumbuh (habitat) yang paling ideal adalah perairan air tawar yang
memiliki suhu antara 14˚C – 38˚C, atau suhu optimal 25˚C – 30˚C. Keadaan suhu
yang rendah yaitu suhu kurang dari 14˚C ataupun suhu yang terlalu tinggi di atas
30˚C akan menghambat pertumbuhan nila. Ikan nila merah memiliki toleransi
tinggi terhadap perubahan lingkungan hidup. Batas bawah dan batas atas suhu
yang mematikan ikan nila berturut-turut adalah 11 – 12˚C dan 42˚C. Keadaan pH
air antara 5 – 11 dapat ditoleransi oleh ikan nila, tetapi pH yang optimal untuk
pertumbuhan dan perkembangbiakkan ikan ini adalah 7 – 8. Ikan nila merah
masih dapat tumbuh dalam keadaan air asin pada salinitas 0 – 35 ppm. Oleh
karena itu, ikan nila merah dapat dibudidayakan di perairan payau, tambak dan
perairan laut, terutama untuk tujuan usaha pembesaran (Rukmana, 1997 dalam
Jaya, 2012).
B. Fisiologi Respirasi Ikan
Sebagai biota perairan, Ikan merupakan mendapatkan Oksigen terlarut
dalam air. Pada hampir semua Ikan, insang merupakan komponen penting dalam
pertukaran gas, insang terbentuk dari lengkungan tulang rawan yang mengeras,
dengan beberapa filamen insang di dalamnya (Fujaya. 2004). Menurut Sukiya
(2005), Setiap kali mulut dibuka, maka air dari luar akan masuk menuju farink
kemudian keluar lagi melalui melewati celah insang, peristiwa ini melibatkan
kartilago sebagai penyokong filamen ikan. Selanjutnya Sukiya menambahkan
4

bahwa lamella insang berupa lempengan tipis yang diselubungi epitel pernafasan
menutup jaringan vaskuler dan busur aorta, sehingga karbondioksida darah dapat
bertukar dengan oksigen terlarut di dalam air.
Organ insang pada ikan ditutupi oleh bagian khusus yang berfungsi untuk
mengeluarkan air dari insang yang disebut operculum yang membentuk ruang
operkulum di sebelah sisi lateral insang. Laju gerakan operculum ikan mempunyai
korelasi positif terhadap laju respirasi ikan (Fujaya. 2004).
C. Pengaruh Kelaruan Oksigen Terhadap Fisiologi Ikan
Atmosfer bumi mengandung oksigen sekitar 210 ml/L. Oksigen
merupakan salah satu gas yang terlarut dalam perairan. Kadar oksigen yang larut
di perairan bervariasi, tergantung pada suhu, salinitas, turbulensi air, dan tekanan
atmosfer. Semakin besar suhu dan ketinggian serta semakin kecil tekanan
atmosfer, kadar oksigen terlarut semakin kecil (Effendi, 2003). Kandungan
oksigen terlarut (Dissolved Oxygen) minimal 4 ppm. Beberapa ikan hidup dengan
baik pada kandungan oksigen kurang dari 4 ppm, terutama ikan-ikan yang
mempunyai alat pernafasan tambahan, yang memungkinkannya mengambil
oksigen langsung dari udara bebas seperti lele (Clarias sp.), sepat (Trichogaster
sp.), gabus (Channa striata), gurami (Osphronemus gouramy) (Effendi, 2003).
Kelarutan oksigen yang rendah dalam air dapat menghambat aktivitas
ikan. Oksigen diperlukan untuk metabolisme dalam tubuh. Kebutuhan oksigen
pada masing-masing spesies berbeda antara satu dengan yang lain. Hal ini karena
perbedaan struktur molekul sel darah ikan yang mempunyai hubungan antara
tekanan partial oksigen dalam air dan dengan keseluruhan oksigen dalam sel darah
(Brown and Gratzek, 1980). Variasi oksigen terlarut dalam air biasanya sangat
kecil sehingga tidak menggangu kehidupan ikan (Brotowidjoyo et al, 1995).
Oksigen diperlukan dalam proses oksidasi berbagai senyawa kimia dan
respirasi berbagai organisme perairan. Kadar oksigen terlarut dan pengaruhnya
terhadap kelangsungan hidup ikan dalam Effendi (2003) sebagai berikut:
5

Tabel 2.1. Kadar Oksigen Terlarut dan Pengaruhnya pada Kelangsungan
Hidup Ikan
D. Hubungan pH dan DO dengan Aktivitas Ikan
Suatu komunitas yang berinteraksi dengan komunitas lainnya dan dengan
lingkungannya (air, udara, suhu,cahaya) disebut ekosistem. Ekosistem berjalan
dinamis, karena komunitas tumbuhan dan hewan yang terdapat dalam beberapa
ekosistem secara gradual selalu berubah karena adanya perubahan komponen
ligkungan fisiknya.
Organisme, populasi, komunitas, dan ekosistem mempunyai kemampuan
untuk melawan atau mengatasi perubahan atau tekanan dari luar. Dengan kata lain
ekosistem itu memiliki beberapa tingkatan stabilitas. Setiap organisme
mempunyai kisaran toleransi tertentu terhadap faktor lingkungan fisik dan kimia.
Adapun sifat-sifat kimianya antara lain pH dan DO.
6

E. Pengaruh pH terhadap Aktivitas Ikan
Kondisi asam atau basa pada perairan ditentukan berdasarkan nilai pH
(power of hydrogen). Nilai pH berkisar antara 0-14, yang mana pH 7
merupakan pH normal. Kondisi pH kurang dari 7 menunjukkan air bersifat
asam, sedangkan pH di atas 7 menunjukkan kondisi air bersifat basa.
Makhluk hidup atau biota perairan tawar masing-masing memiliki
kondisi pH yang berbeda-beda. Pengaruh pH pada biota terletak pada aktivitas
enzim, misalnya dalam pH asam, enzim akan mengalami protonasi. Keasaman
juga berpengaruh pada tingkat kelarutan suatu nutrien dalam perairan, yang
menentukan keberadaan suatu organisme. Polusi juga bisa diindikasi dari pH
yang terkait dengan konsentrasi oksigen (pH rendah pada konsentrasi oksigen
rendah).
Organisme akuatik dapat hidup dalam suatu perairan yang mempunyai
pH netral. pH yang ideal bagi kehidupan organisme akuatik pada umumnya
berkisar 7 sampai 8,5. Kondisi perairan yang bersifat asam maupun basa
membahayakan karena dapat menyebabkan terjadinya gangguan metabolisme
dan respirasi. Nilai pH rendah dapat menyebabkan mobilitas berbagai senyawa
logam berat semakin tinggi sedangkan pH yang tinggi akan menyebabkan
keseimbangan antara amonium dan amoniak akan terganggu sehingga dapat
menyebabkan meningkatkan konsentrasi amoniak yang bersifat toksik bagi
organisme (Barus, 2001).
Derajat keasaman perairan juga dipengaruhi oleh keadaan tanah. Nilai
pH asam tidak baik untuk budidaya ikan dimana produksi ikan dalam suatu
perairan akan rendah. Pada pH air netral sangat baik untuk kegiatan budidaya
ikan, biasanya berkisar antara 7 – 8, sedangkan pada pH basa dan asam tidak
baik untuk kegiatan budidaya. Pengaruh pH air pada perairan dapat berakibat
terhadap komunitas biologi perairan, untuk jelasnya dapat dilihat pada Tabel
2.2
7

Tabel 2.2. Pengaruh pH Air Terhadap Komunitas Biologi Perairan (Effendi, 2003)
Perubahan pH dapat mempunyai akibat buruk terhadap kehidupan biota
perairan baik secara langsung maupun tidak langsung. Tinggi atau rendahnya
pH air dipengaruhi oleh senyawa / kandungan dalam air tersebut. Faktor yang
mempengaruhi pH air yaitu sisa-sisa pakan dan kotoran yang mengendap di
dasar kolam. Selain itu juga berasal dari kandungan CO2 yang tinggi hasil
pernafasan (terjadi menjelang fajar sampai pagi hari). Dampak perubahan pH :
a. Terganggunya proses metabolisme ikan
b. Ikan mudah terserang penyakit
c. Pertumbuhan menurun, stress
d. pH tinggi dapat meningkatkan kandungan ammonia sehingga kualitas air
terganggu.
Cara mengatasi pH air, diantaranya yaitu :
a. Sebelum pengisian air, kolam dikeringkan kemudian diberi kapur secara
merata.
b. Dilakukan pengendapan sebelum air dimasukkan ke dalam kolam
8

c. Penggantian air untuk membuang sisa-sisa pakan dan kotoran dari dasar
kolam.
Keasaman ditentukan dengan memakai kertas pH universal dan pH
meter. Pengukuran dilakukan dengan variasi waktu siang dan malam. Langkah
tersebut didasarkan pada perbedaan aktivitas biota pada siang dan malam hari.
Pengambilan lokasi bisa dilakukan dengan berbagai cara, seperti transek pada
kedalaman yang berbeda dan tempat-tempat yang memiliki potensi
menimbulkan pencemaran (sumber pencemaran terpusat).
Kisaran optimal fluktuasi nilai pH air pagi dan sore adalah 0,2-0,5.
Fluktuasi nilai pH harian yang lebih dari 0,5 menunjukan bahwa karbonat
dalam air sebagai penyangga adalah kurang. Sebaliknya bila fluktuasi kurang
dari 0,2 atau bahkan sore hari sama dengan pagi hari, menunjukkan fotosintesis
tidak berjalan normal. Kondisi lingkungan lebih berbahaya bila nilai pH pagi
lebih tinggi dari sore hari.
Fluktuasi harian kandungan oksigen terlarut ditentukan kepadatan biota
yang ada dalam air terutama phytoplankton dan makroalga yang merupakan
produsen primer. Untuk menjaga oksigen terlarut tetap pada kondisi optimal
adalah dengan pemanfaatan proses fotosintesa, penggunaan aerasi dan
mengatur jumlah densitas plankton dan tanaman air. Kedalaman air optimal
tambak sederhana yang tidak menggunakan aerasi adalah 2 x nilai kecerahan.
Hubungan pH dengan suhu adalah derajat keasaman air pH = -log (H)+.
Ukuran konsentrasi ion Hidrogen (mol per Liter) menunjukkan suasana asam
atau basa suatu perairan.
F. Pengaruh DO (Oksigen Terlarut) terhadap Aktivitas Ikan
Oksigen terlarut (Dissolved Oxygen = DO) dibutuhkan oleh semua
jasad hidup untuk pernapasan, proses metabolisme atau pertukaran zat yang
kemudian menghasilkan energi untuk pertumbuhan dan pembiakan. Disamping
itu, oksigen juga dibutuhkan untuk oksidasi bahan-bahan organik dan
9

anorganik dalam proses aerobik. Sumber utama oksigen dalam suatu perairan
berasal dari suatu proses difusi dari udara bebas dan hasil fotosintesis
organisme yang hidup dalam perairan tersebut. Kecepatan difusi oksigen dari
udara, tergantung dari beberapa faktor, seperti kekeruhan air, suhu, salinitas,
pergerakan massa air dan udara seperti arus, gelombang, dan pasang surut.
Odum (1993) menyatakan bahwa kadar oksigen dalam air akan bertambah
dengan semakin rendahnya suhu dan berkurang dengan semakin tingginya
salinitas. Pada lapisan permukaan, kadar oksigen akan lebih tinggi, karena
adanya proses difusi antara air dengan udara bebas serta adanya proses
fotosintesis. Dengan bertambahnya kedalaman akan terjadi penurunan kadar
oksigen terlarut, karena proses fotosintesis semakin berkurang dan kadar
oksigen yang ada banyak digunakan untuk pernapasan dan oksidasi bahan-
bahan organik dan anorganik. Keperluan organisme terhadap oksigen relatif
bervariasi tergantung pada jenis, stadium dan aktivitasnya. Kebutuhan oksigen
untuk ikan dalam keadaan diam relatif lebih sedikit apabila dibandingkan
dengan ikan pada saat bergerak atau memijah. Jenis-jenis ikan tertentu yang
dapat menggunakan oksigen dari udara bebas memiliki daya tahan yang lebih
terhadap perairan yang kekurangan oksigen terlarut. Kandungan oksigen
terlarut (DO) minimum adalah 2 ppm di dalam keadaan normal dan tidak
tercemar oleh senyawa beracun (toksik). Kandungan oksigen terlarut minimum
ini sudah cukup mendukung kehidupan organisme. Idealnya, kandungan
oksigen terlarut tidak boleh kurang dari 1,7 ppm selama waktu 8 jam dengan
sedikitnya pada tingkat kejenuhan sebesar 70%.
Menurut Boyd (1990) dalam Fika (2009), jumlah oksigen yang
dibutuhkan oleh organisme akuatik tergantung spesies, ukuran, jumlah pakan
yang dimakan, aktivitas, suhu, dan lain-lain. Konsentrasi oksigen yang rendah
dapat menimbulkan anorexia, stress, dan kematian pada ikan. Bila dalam suatu
kolam kandungan oksigen terlarut sama dengan atau lebih besar dari 5 mg/l,
maka proses reproduksi dan pertumbuhan ikan akan berjalan dengan baik. Pada
perairan yang mengandung deterjen, suplai oksigen dari udara akan sangat
lambat sehingga oksigen dalam air sangat sedikit. Oksigen terlarut yang
terkandung di dalam air, berasal dari udara dan hasil proses fotosintesis
10

tumbuhan air. Oksigen diperlukan oleh semua mahluk yang hidup di air seperti
ikan, udang, kerang dan hewan lainnya termasuk mikroorganisme seperti
bakteri. Oksigen merupakan faktor pembatas dalam penentuan kehadiran
makhluk hidup di dalam air. Kepekatan oksigen terlarut bergantung kepada :
a. Suhu.
b. Kehadiran tanaman fotosintesis.
c. Tingkat penetrasi cahaya bergantung kepada kedalaman dan kekeruhan air.
d. Tingkat kederasan aliran air.
e. Jumlah bahan organik yang diuraikan dalam air seperti sampah, ganggang
mati atau limbah industri (Sastrawijaya, 2000).
Kehidupan di air dapat bertahan jika terdapat oksigen terlarut minimal
sebanyak 5 ppm (5 part per million atau 5 mg oksigen untuk setiap liter air).
Selebihnya bergantung kepada ketahanan organisme, derajat keaktifannya,
kehadiran bahan pencemar, suhu, pH, ketersediaan bahan organik, mineral, dan
sebagainya.
Rusaknya kadar kimia air akan berpengaruh terhadap fungsi dari air.
Besarnya beban pencemaran yang ditampung oleh suatu perairan, dapat
diperhitungkan berdasarkan jumlah polutan yang berasal dari berbagai sumber
aktivitas air buangan dari proses-proses industri dan buangan domestik yang
berasal dari penduduk. Telah banyak dilakukan penelitian tentang pengaruh air
buangan industri dan limbah penduduk terhadap organisme perairan, terutama
pengaruhnya terhadap ikan. Akibat yang ditimbulkan antara lain dapat
menyebabkan kelumpuhan ikan, karena otak tidak mendapat suplai oksigen
serta kematian karena kekurangan oksigen (anoxia) yang disebabkan jaringan
tubuh ikan tidak dapat mengikat oksigen yang terlarut dalam darah
(Sastrawijaya, 2000). Untuk mengetahui kualitas air dalam suatu perairan,
dapat dilakukan dengan mengamati beberapa parameter kimia, seperti oksigen
terlarut (Dissolved Oxygen = DO) dan kebutuhan oksigen biologis (Biological
Oxygen Demand = BOD).
Oksigen terlarut dapat dianalisis atau ditentukan dengan cara metode
titrasi dengan cara WINKLER. Metode titrasi dengan cara WINKLER secara
11

umum banyak digunakan untuk menentukan kadar oksigen terlarut. Prinsipnya
dengan menggunakan titrasi iodometri. Sampel yang akan dianalisis terlebih
dahulu ditambahkan larutan MnCl2 dan NaOH - KI, sehingga akan terjadi
endapan MnO2. Dengan menambahkan H2SO4 atau HCl maka endapan yang
terjadi akan larut kembali dan juga akan membebaskan molekul iodium (I2)
yang ekivalen dengan oksigen terlarut. Iodium yang dibebaskan ini selanjutnya
dititrasi dengan larutan standart natrium tiosulfat (Na2S2O3) dan menggunakan
indikator larutan amilum (kanji encer). Reaksi kimia yang terjadi dapat
dirumuskan sebagai berikut:
a. MnCl2 + NaOH → Mn(OH)2 + 2 NaCl
b. 2 Mn(OH)2 + O2 → 2 MnO2 + 2 H2O
c. MnO2 + 2 KI + 2 H2O → Mn(OH)2 + I2 + 2 KOH
d. I2 + 2 Na2S2C3 → Na2S4O6 + 2 NaI
Penentuan oksigen terlarut (DO) dengan cara titrasi berdasarkan metode
WINKLER lebih analitis apabila dibandingkan dengan cara alat DO meter.
12

BAB III
METODE PENELITIAN
A. Jenis Praktikum
Jenis praktikum ini bersifat eksperimen karena menggunakan variabel-
variabel praktikum, yaitu variabel manipulasi, variabel kontrol, dan varibel respon
serta adanya perlakuan.
B. Waktu dan Tempat Praktikum
Praktikum ini dilaksanakan pada tanggal 29 dan 30 April 2013 di
Laboratorium Fisiologi, Jurusan Biologi, Fakultas Matematika dan Ilmu
Pengetahuan Alam, Universitas Negeri Surabaya.
C. Variabel Praktikum
1. Variabel kontrol : Volume air dan ukuran toples.
2. Variabel manipulasi : Sumber cahaya, jumlah ikan, pakan ikan, dan
media air.
3. Variabel respon : Kadar DO dan kadar PH
D. Alat dan Bahan
1. Alat
a. Botol winkler 3 buah
b. Toples plastik transparan 3 buah
c. Erlenmeyer 3 buah
d. Pipet 5 buah
e. Gelas ukur 3 buah
f. Kertas lakmus
g. Gelas beker 3 buah
h. Alat pemanas air (hitter) 1 buah
2. Bahan
a. Air kolam bersih 1000 ml
b. Air isi ulang 2000 ml
c. Ikan nila 9 ekor
d. MnSO4 ± 20 ml
e. KOH-KI ± 20 ml
f. H2SO4 ± 20 ml
g. Na2S2O3 ± 40 ml
h. Larutan amilum 1%± 10 ml
i. Hydrilla sp
j. Pakan ikan
13

E. Prosedur Kerja
1. Menyiapkan alat dan bahan praktikum.
2. Membuat media air. Pembuatan media air ini dilakukan 24 jam sebelum
praktikum dengan terlebih dahulu menyiapkan toples yang telah diberi label
huruf A, B, dan C pada masing-masing toples, air, dan ikan mas. Pembuatan
media air pada tiap toples adalah sebagai berikut :
a. Toples A diberi air kolam sebanyak 750 ml. Membiarkan toples dalam
keadaan terbuka dan ditempatka di tempat yang terkena cahaya matahari
dengan harapan terkena angin dan terjadi fotosintesis pada alga hijau atau
biru.
b. Toples B diisi air isi ulang sebanyak ± 750 ml dan memasukkan 1 ekor ikan.
Kemudian toples ditutup dan ditempatkan di tempat yang teduh.
c. Toples C diisi air isi ulang ± 750 ml dan memasukkan 2 ekor ikan dan diberi
pakan ikan yang mudah hancur/ lembek dalam air. Kemudia toples ditutup
dan diletakkan di tempat yang teduh.
3. Setelah 1 x 24 jam, mengamati semua toples dan melihat perubahan yang
terjadi. Demikian pula mencatat jika terjadi perubahan pada ikan. Kemudian
melakukan pengukuran DO dan pH dari masing-masing media air (A, B, dan
C).
a. Pengukuran kadar DO
1) Mengambil sampel air dengan botol winkler gelap, usahakan tidak ada
O2 yang terperangkap
2) Menambahkan MnSO4 2 ml dan KOH-KI 2 ml (dengan membuka botol
winkler secara kati-hati) kemudian dikocok pelan (membolak-balik botol
secara hati-hati hingga perekasi tercampur dengan air sampel). Diamkan
selama 10 menit sampai terbentuk dua lapisan.
3) Menambahkan H2SO4 pekat 2 ml ke dalam botol secara hati-hati,
mengocok botol hingga larutan tercampur, kemudian melakukan titrasi.
4) Mengambil 100 ml sampel yang mendapat perlakuan tadi dan
memasukkan ke dalam erlenmeyer. Melakukan titrasi dengan Na2S2O3
sampai terjadi perubahan warna (dari coklat menjadi kuning muda).
14

Kemudian menambahakan amilum (1%) 10 tetes hingga tampak warna
biru dan melanjutkan titrasi dengan Na2S2O3 sampai warna biru hilang.
5) Menghitung DO dengan rumus sebagai berikut :
Keterangan :
a : volume titrasi yang dipakai
N : konstanta 0,025
6) Mencatat hasil ke dalam tabel.
b. Pengukuran pH
1) Mengambil sampel air.
2) Mengukur derajat keasaman dengan menggunakan kertas lakmus.
4. Setelah dilakukan pengukuran DO dan pH, kemudian pada masing-masing air
diberi perlakuan sebagai berikut:
a. Pada toples A, memasukkan 2 ekor ikan yang baru.
b. Pada toples B, mengambil ikan yang telah dipelihara selama 24 jam,
kemudian memasukkan lagi 2 ekor ikan yang baru.
c. Pada toples C, mengambil ikan yang telah dipelihara selama 24 jam,
kemudian memasukkan lagi 2 ekor ika yang baru.
5. Selanjutnya mengamati ventilasi respirasi ikan yang dipelihara pada ketiga
toples tersebut. Selain itu melakukan penghitungan membuka dan menutupnya
operkulum ikan per satuan waktu (menit I, II, III).
F. Rancangan Penelitian
15
Menyiapkan 3 percobaan masing-masing terdiri dari 1 toples.
Tandai toples dengan kode A, B, dan C.
Mengisi setiap toples dengan air kira-kira ± 750 ml

Pengukuran pH
16
Toples A diisi air
kolam sebanyak ±
750 ml
Menutup semua toples rapat-rapat, usahakan agar tutup tersebut
tidak bocor.
Toples B diisi air isi
ulang sebanyak ± 750
ml, memasukkan 1
ekor ikan.
Toples C diisi air isi
ulang ± 750 ml,
memasukkan 2 ekor
ikan dan diberi
pakan.
Menempatkan toples A di tempat yang terkena matahari.
Menempatkan toples B dan C di tempat yang teduh.
Setelah 1 x 24 jam, amati semua toples dan lihat perubahan yang
terjadi. Demikian pula catatlan bilamana terjadi perubahan pada ikan.
Setelah pengamatan selesai lakukan pengukuran terhadap kadar DO
dan pH.
Mengambil sampel air kemudian mengukur derajat keasaman dengan menggunakan kertas lakmus.

17
Botol winkler gelap diisi air sampel
Langsung dibawa ke laboratorium
Ditambah larutan MnSO4 2 ml
Ditambah larutan KOH-KI 2 ml
Dihomogenkan dan di biarkan mengendap
1/3 botol
Ditambah larutan asam sulfat pekat 2 ml
Endapan hilang
Kuning muda
100 ml sample dititrasi Na2S2O3
Ditambah 10-20 tetes amilum
Biru
Volume titran
Kuning mudaKuning tua
Dititrasi Na2S2O3
DO
Warna biru hilang
Pengukuran DO

BAB IV
HASIL DAN PEMBAHASAN
A. Hasil
Tabel 4.1 Pengaruh DO dan pH Terlarut terhadap Aktivitas Ikan Nila Merah (Oreochromis niloticus)
Media Air
DO (ppm)
pH
Ventilasi per menit
Ciri-ciri ikan setelah 24 jam
Ikan 1 Ikan 2
A 2,28 Basa
1’ = 982’ = 823’ = 72x = 84
1’ = 962’ = 883’ = 69x = 83
Ikan lama : –Ikan baru :Pergerakan ikan tenang, berenang di dasar dan jarang ke permukaan.
B 0,98Asam
(+)
1’ = 2342’ = 2193’ = 197x = 216
1’ = 2202’ = 2113’ = 182x = 204
Ikan lama :Ikan masih dapat hidup dengan normal dan keadaan air tetap jernih.Ikan baru :Ikan tidak selalu berada di dalam air tetapi terkadang muncul ke permukaan untuk bernafas. Keadaan air tetap jernih.
C 0Asam (++)
1’ = 2702’ = 2693’ = 256x = 265
1’ = 2612’ = 2573’ = 243x = 253
Ikan lama :1 ekor ikan mati dan 1 ekor lainnya selalu berenang ke permukaan untuk bernafas. Keadaan air berbusa dan berlendir.Ikan baru :Semua ikan selalu berenang ke permukaan untuk bernafas, pergerakan ikan cepat (agresif). Keadaan air berbusa dan keruh.
Keterangan: A : Toples berisi air kolam sebanyak ± 750B : Toples berisi air isi ulang sebanyak ± 750 ml dan 1 ekor ikan.C : Toples berisi air isi ulang ± 750 ml, 2 ekor ikan dan diberi pakan.
B. Analisis Data
Berdasarkan praktikum yang telah dilakukan yang dibagi menjadi 3
perlakuan yaitu dengan menggunakan media A dengan air kolam, media B dengan
air suling, dan media C dengan air suling yang diberi pakan, maka diperoleh data
18

mengenai pengaruh kadar DO dan pH terhadap aktivitas ikan nila merah serta
hubungan antara DO dan pH dalam suatu komunitas seperti yang terdapat pada
tabel 4.1 di atas.
Pada media A yang berisi air kolam yang diletakkan di tempat yang
terkena cahaya matahari dalam keadaan terbuka, setelah 24 jam diperoleh kadar
DO sebesar 2,28 ppm dan mempunyai pH basa. Kemudian setelah dimasukkan 2
ekor ikan nila merah yang baru dan dilakukan pengamatan, didapatkan rata-rata
respirasi ikan dari menit pertama sampai ketiga sebesar 84 kali/ menit pada ikan 1
dan 83 kali/ menit pada ikan 2. Aktivitas ikan setelah 24 jam adalah pergerakan
ikan tenang serta selalu berenang di dasar dan jarang ke permukaan.
Pada media B yang berisi air suling dan 1 ekor ikan nila merah yang
diletakkan di tempat yang teduh dalam keadaan tertutup, setelah 24 jam diperoleh
kadar DO sebesar 0,98 ppm dan mempunyai pH asam. Kemudian setelah
dimasukkan 2 ekor ikan nila merah yang baru dan dilakukan pengamatan,
didapatkan rata-rata respirasi ikan dari menit pertama sampai ketiga sebesar 216
kali/ menit pada ikan 1 dan 204 kali/ menit pada ikan 2. Aktivitas ikan setelah 24
jam adalah ikan tidak selalu berada di dalam air tetapi terkadang muncul ke permukaan
untuk bernafas.
Pada media C yang berisi air suling dan 2 ekor ikan nila merah yang diberi
pakan yang diletakkan di tempat yang teduh dalam keadaan tertutup, setelah 24
jam diperoleh kadar DO sebesar 0 ppm dan mempunyai pH yang lebih asam
daripada media B. Kemudian setelah dimasukkan 2 ekor ikan nila merah yang
baru dan dilakukan pengamatan, didapatkan rata-rata respirasi ikan dari menit
pertama sampai ketiga sebesar 265 kali/ menit pada ikan 1 dan 253 kali/ menit
pada ikan 2. Aktivitas ikan setelah 24 jam adalah semua ikan selalu berenang ke
permukaan untuk bernafas dan pergerakan ikan cepat (agresif).
Dari data diatas, dapat diketahui bahwa semakin tinggi kadar oksigen
terlarut maka makin tinggi pH pada media, dimana kedua faktor tersebut akan
mempengaruhi aktivitas (respirasi) pada ikan nila merah.
19

C. Pembahasan
Berdasarkan analisis diatas, maka dapat diketahui bahwa ada pengaruh
antara oksigen terlarut (DO) dan derajat keasaman (pH) dalam suatu ekosistem.
Pada media A yang berisi air kolam yang diletakkan di tempat yang terkena
cahaya matahari dalam keadaan terbuka, setelah 24 jam diperoleh kadar DO
sebesar 2,28 ppm dan mempunyai pH basa. Aktivitas ikan setelah 24 jam adalah
pergerakan ikan tenang serta selalu berenang di dasar dan jarang ke permukaan.
Hal ini berarti ikan bergerak dengan respirasi normal yang ditunjukkan dengan
rata-rata penghitungan frekuensi ikan sebanyak 84 kali/ menit pada ikan 1 dan 83
kali/ menit pada ikan 2. Hal ini menunjukkan bahwa pada media ini kaya akan
oksigen terlarut sehingga ikan tidak kesulitan dalam melakukan respirasi. Media
A hanya diisi dengan air kolam yang di dalamnya terdapat berbagai macam alga
yang akan berfotosintesis dengan meggunakan sinar matahari untuk mengubah
CO2 mejadi O2 untuk respirasi ikan, dimana oksigen berfungsi dalam proses
respirasi untuk mendapatkan energi berupa (ATP). Selain itu, kadar CO2 semakin
rendah akibat aktivitas dari alga tersebut berupa fotosintesis yang mengeluarkan
O2 sebagai hasil ekskresinya dan dapat diketahui juga bahwa kadar O2 yang tinggi
akan memenuhi kebutuhan hidup organisme di dalamnya. Alga juga dijadikan
sumber makanan bagi ikan sehingga ikan tetap sehat meskipun tidak diberi
makan.
Pada media B yang berisi air suling dan 1 ekor ikan nila merah yang
diletakkan di tempat yang teduh dalam keadaan tertutup, setelah 24 jam diperoleh
kadar DO sebesar 0,98 ppm dan mempunyai pH asam. Aktivitas ikan tidak selalu
berada di dalam air tetapi terkadang muncul ke permukaan untuk bernafas. Hal ini
menunjukkan aktivitas ikan yang lebih cepat dan aktif pada media B daripada
media A yaitu rata-rata respirasi ikan sebanyak 216 kali/ menit pada ikan 1 dan
204 kali/ menit pada ikan 2. Hal ini dikarenakan tidak terdapat alga untuk
mengubah CO2 mejadi O2 di dalamnya sehingga kadar oksigen terlarutnya lebih
rendah dibandingkan media A, begitu juga pH yang semakin menurun dari basa
menjadi asam. Hal ini disebabkan laju fotosintesis dan laju respirasi tidak sama
dimana semakin tinggi respirasi berlangsung maka kadar oksigen terlarut dalam
air semakin rendah sehingga mengakibatkan aktifitas operculum ikan lebih tinggi.
20

Pada media C yang berisi air suling dan 2 ekor ikan nila merah yang diberi
pakan yang diletakkan di tempat yang teduh dalam keadaan tertutup, setelah 24
jam diperoleh kadar DO sebesar 0 ppm dan mempunyai pH yang lebih asam
daripada media B. Aktivitas ikan setelah 24 jam adalah semua ikan selalu
berenang ke permukaan untuk bernafas dan pergerakan ikan cepat (agresif). Hal
ini berarti bahwa aktivitas ikan pada media ini lebih cepat dan agresif dibanding
dengan media B. Terlihat dari rata-rata respirasi sebesar 265 kali/ menit pada ikan
1 dan 253 kali/ menit pada ikan 2. Hal ini disebabkan tidak adanya proses
fotosintesis dari alga seperti perlakuan A yang menyebabkan kadar oksigen
terlarut rendah. Disamping itu, tingginya derajat keasaman disebabkan oleh
tingginya kandungan limbah organik dari pakan yang diberikan. Oksigen terlarut
pada media C lebih rendah dibanding perlakuan pada meidia A dan B dikarenakan
proses respirasi lebih tinggi dan proses fotosintesis tidak terjadi. Oksigen terlarut
yang ada digunakan respirasi dari ikan dan mikroba-mikroba aerob yang
mengeluarkan CO2 .
21

BAB V
PENUTUP
A. Simpulan
Berdasarkan hasil dan analisis di atas, maka dapat ditarik kesimpulan
sebagai berikut :
1. Semakin rendah kadar pH pada suatu perairan maka semakin rendah pula kadar
oksigen terlarut pada suatu perairan yang menyebabkan semakin cepat kegiatan
ventilasi pernapasan ikan per menit sehingga menyebabkan pergerakan ikan
menjadi sangat agresif dan selalu muncul di permukaan untuk bernafas.
Meningkatnya kadar CO2 di perairan akan menurunkan kadar pH di perairan
dan meningkatnya kadar oksigen terlarut di perairan akan meningkatkan kadar
pH air.
2. Hubungan DO dan pH dengan respirasi ikan adalah berbanding lurus, semakin
tinggi kadar DO di perairan maka semakin tinggi pula kadar pH di perairan,
sedangkan kegiatan ventilasi pernapasan ikan berbanding terbalik dengan nilai
DO dan pH, semakin rendah nilai DO dan nilai pH di perairan maka
menyebabkan kegiatan ventilasi ikan semakin cepat.
B. Saran
Pada praktikum ini perlu dipilih ikan-ikan yang mempunyai umur dan
ukuran yang sama agar presisi kebutuhan oksigennya seragam. Dalam pengukuran
pH sebaiknya menggunakan pH meter agar diketahui pasti nilai pH-nya sehingga
lebih mudah dalam menganalisis.
22

DAFTAR PUSTAKA
Barus, T. A. 2001. Metode Ekologis untuk Menilai Kualitas Suatu Perairan Lotik. Medan: Fakultas MIPA USU Medan.
Campbell. 2004. Biologi, Edisi Kelima-Jilid 3. Jakarta: Erlangga.
Fika. 2009. Oksigen Terlarut (DO) dan Kebutuhan Oksigen Biologi (BOD). Diakses melalui http://biarkanakumenulis.blogspot.com/2009/10/oksigen-terlarut-do-dan-kebutuhan.html pada tanggal 4 Mei 2013.
Fujaya, Yushinta. 2004. Fisisologi Ikan. Jakarta: Rineka Cipta.
Jaya, K. 2012. Ikan Nila (Oreochromis niloticus). Diakses melalui http://ikanmania25.blogspot.com/2012/03/ikan-nila-oreochromis-niloticus.html pada tanggal 4 Mei 2013.
Odum, E.P. 1993. Basic Ecologi (Dasar-dasar Ekologi). Yogyakarta: Universitas Gajah Mada Press.
Sastrawijaya, A. Tresna. 2000. Pencemaran Lingkungan. Jakarta: Rineka Cipta.
Sukiya. 2005. Biologi Vertebrata. Malang: Universitas Negeri Malang Press.
Suyono, dkk. 2011. Laporan Praktikum Biologi Dasar. Diakses melalui http://www.scribd.com/doc/91366750/45/Deskripsi-Ikan-Nila pada tanggal 4 Mei 2013.
Tunas, Arthama Wayan. 2005. Patologi Ikan Toloestei. Yogyakarta: Universitas Gadjah Mada Press.
Yuliani dan Raharjo. 2013. Panduan Praktikum Ekofisiologi. Surabaya: Laboratorium Fisiologi Tumbuhan Jurusan Biologi FMIPA Unesa.
23

LAMPIRAN
Penghitungan DO
Rumus DO = 8000 x N x a
V – 4
1. DO media A = 8000 x 0,025 x 2,8
250 – 4
=
= 2,28 ppm
2. DO media B = 8000 x 0,025 x 1,2
250-4
=
= 0,98 ppm
3. DO media C = 8000 x 0,025 x 0
250 – 4
=
= 0 ppm
24