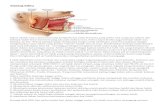
Korelasi Antara Kadar Iga Saliva Dengan Laju Aliran Saliva Pada Pasien Hiv Aids
Analisis Karakteristik Saliva
-
Upload
iness-fluida -
Category
Documents
-
view
35 -
download
1
description
Transcript of Analisis Karakteristik Saliva

ANALISIS KARAKTERISTIK SALIVA
Disusun Oleh :
NIKMATUL AMALIYAN N.C.
081610101026
KELOMPOK A
FAKULTAS KEDOKTERAN GIGIUNIVERSITAS JEMBER
2009

LAPORAN PRAKTIKUM BIOKIMIA
ANALISIS KARAKTERISTIK SALIVA
I. Tujuan
Mempelajari karakteristik kimiawi dan enzimatis saliva manusia melalui serangkaian
pengujian dan secara spektrofotometri.
II. Tinjauan Pustaka
Saliva terdiri dari sekitar 99,5% air. Bagian padatnya terdiri dari ptialin,
beberapa protein (mucin yang merupakan bahan yang paling penting) dan sedikit
substansi yang ditemukan di daerah darah dan urin seperti ammonia, asam amino,
urea, asam urik, kolesterol, kalsium, Na+, K+, Mg2+, P, Cl-, dan bikarbonat. Ph rata-
rata saliva sangat bervariasi, tetapi biasanya sekitar 6,8 (www.m-w.com)
Saliva merupakan cairan hipotonik. Kelenjar saliva mempertahankan
konsentrasi garam dalam saliva. Tiga kelenjar saliva utama yaitu kelenjar paratiroid,
kelenjar submandibularis, dan kelenjar sublingualis. Mucin merupakan kelas dari
glikoprotein yang ditemukan dalam saliva, cairan lambung, dan lain-lain yang
membentuk larutan kental dan bertindak sebagai lubrikan atau protein pada
permukaan eksternal dan internal tubuh, dan merupakan sekresi dari membran.
Menurut Robert R. Barefoot, pH normal darah, cairan spinal, dan saliva adalah 7,4
(www.alkalizeforhealth.com).
Dalam saliva terdapat lebih dari 20 jenis protein yang berbeda yang dapat
diidentifikasi. Yang paling dikenal adalah enzim amylase yang memecah pati menjadi
maltose, maltotriase, dan limit dextrin (www.arbl.cdostate.edu).
Dari semua elemen mineral, fosfat mempunyai pengaruh yang besar pada
system regulasi pH tubuh. Untuk mengetahui sensitivitas fosfat dapat menggunakan
test saliva yang cukup sederhana, yaitu dengan kertas lakmus (www.phosadd.com).
Konsentrasi kalsium dan fosfat dalam saliva bermacam-macam, tetapi rata-
ratanya adalah 1,5 mmole/liter dan tidak semua fosfat dalam bentuk unprotonasi.
Namun jumlah ini dapat dikalkulasi dan pada keadaan pH netral terdapat sejumlah 5
nm/liter. Menurut Robert R. Barefoot, kebutuhan kalsium dapat ditentukan melalui

pH saliva. Makin asam (<7) pH saliva tubuh makin kekurangan kalsium
(www.vreb.com/coral-calcium/dose.htm).
Phenolphthalein merupakan sensitif pH indikator dengan rumus C2OH14O4
sering digunakan dalam titrasi, yang mengubah warna larutan asam menjadi warna
pink. Jika konsentrasi indikator kuat, dapat berubah menjadi warna ungu.
Phenolphthalein tidak larut dalam air, tetapi biasanya larut dalam alcohol. Warna
molekul phenolphthalein tidak berwarna akan tetapi warna ion phenolphthalein
adalah pink (www.wikipedia.org)
Phenolphthalein pada larutan asam-basa: jika larutan asam ( >10 ) maka
larutan akan berwarna pink, jika larutan bersifat basa ( pH <8.2) maka larutan tidak
berwarna (www.chemcool.com).
Methyl merah merupakan indikator warna yang merubah larutan asam
menjadi berwarna merah. Rumusnya: C15H15N3O2.
Methyl orange merupakan indikator pH yang umumnya digunakan untuk titrasi.
Methyl orange ini beracun. Penggunaan indikator ini yaitu:
- semakin asam suatu larutan, jika ditambah methyl orange warna larutan akan
semakin kuning ( pH>4,4 )
- semakin basa suatu larutan ( pH<3,1 ), maka warnanya akan semakin merah dan
jika normal akan berwarna orange
Methyl biru merupakan komponen kimia untuk pewarnaan dalam histologi.
Pewarnaan methyl biru atau methyl blue merupakan kolagen biru dalam jaringan.
Rumus: C37H27N3O9S3Na2 (www.wikipedia.org).
Pada pH normal saliva, terjadi supersaturasi kalsium fosfat dengan fosfat lebih
banyak dalam bentuk mono- atau di-hidrogen fosfat. Dengan pH yang semakin asam,
tingkat supersaturasi menurun hingga suatu titik dimana saliva tersaturasi dengan
adanya mineral gigi. Keadaan ini disebut “kritikal pH” dengan pH 5,2-5,5. Jika pH
semakin basa, tingkat saturasi dengan mineral gigi meningkat dan kalsium fosfat
dalam larutan menjadi tidak stabil dan terpresipitasi, tidak sebagai hidroksiapatit
tetapi membentuk mineral yang disebut brushite dan ini akan menjadi kalkulus
(www.ncl.ac.uk/dental/oralbio/oralenu/calciumphosphate.com).

III. METODE PERCOBAAN
3.1 Alat dan Bahan
Alat-alat yang digunakan meliputi tabung reaksi/test tube + rak, pipet
tetes/Pasteur, pipet ukur/ Mohrl, pipet volume + ball pipet, beaker glass,
pengaduk gelas, pengatur waktu, erlenmeyer, spektrofotometer visible + kuvet,
water bath, dan botol semprot.
Bahan/reagent yang digunakan meliputi sample saliva, sodium hidroksida
NaOH 5% dan 10%, tembaga(II) sulfat CuSO4, asam asetat CH3COOH 5%, asam
nitrat HNO3 5%, perak nitrat AgNO3, asam klorida HCl 5% dan 0,05 N, mercuri
klorida HgCl2 2%, kalium iodide-kalium iodat Kl-KlO3, kalium iodide Kl,
amilum 1%, barium klorida BaCl, ammonium molibdat (NH4)6Mo7O24, asam
sulfat H2SO4 5%, ferri klorida FeCl3 2%, aquades, indikator-indikator
(phenolphthalein PP, methyl orange MO, methyl red MM, dan methyl blue MB),
kapas steril. Label kertas, dan tissue.
3.2 Skema Kerja
A. Preparasi Sampel Saliva
- diharuskan berkumur terlebih dahulu untuk membuang sisa
makanan
- kapas steril dikunyah untuk menstimulasi sekresi saliva
- dikumpulkan saliva dalam breaker glass hingga mencapai ± 20
ml
Diambil saliva non-patologis
Hasil

1. Pengukuran Sifat Keasaman atau pH Saliva
- ditambahkan 5 tetes PP, MO, MM, dan MB
- dicatat perubahan warna
2. Sifat Saliva Sebagai Protein- Uji Biuret
- ditambahkan 5 tetes NaOH 5% kemudian 3
tetes CuSO4
- dicatat perubahan warna yang terjadi
3. Pengujian Kandungan Mucin
- ditambah 1 tetes CH3COOH 5% pada tabung 1
- ditambah 5 tetes aquades pada tabung 2
- ditambah 2 tetes NaOH 10% pada tabung 1 dan 2
- dicatat perubahan yang terjadi
4. Pengujian Kandungan Klorida
- ditambahkan 3 tetes HNO3 5% kemudian 2 tetes AgNO3
- dicatat perubahan kekeruhan saliva
1 ml saliva dalam 4 tabung reaksi
Hasil
Diisi 1 ml aquades pada tabung 1 dan tabung 2 diisi 1 ml saliva
Hasil
Diisi 2 ml saliva pada tabung 1 dan 2
Hasil
1 ml saliva
Hasil

5. Pengujian Kandungan Sulfat
- ditambahkan 3 tetes HNO3 5% kemudian 2 tetes BaCl2
- dicatat perubahan kekeruhan saliva
6. Pengujian Kandungan Fosfat
- ditambahkan 3 tetes HNO3 5% kemudian 2 tetes BaCl2
- dicatat perubahan kekeruhan saliva
7. Pengujian Kandungan kalsium
- ditambahkan 1 tetes CH3COOH
- dicatat perubahan kekeruhan saliva
8. Pengujian kandungan nitrat
- ditambahkan 3 tetes H2SO4 5%
- ditambahkan 2 tetes KI dan 1 tetes amilum
- dicatat perubahan kekeruhan saliva
Hasil
1 ml saliva
Hasil
1 ml saliva
1 ml saliva
hasil
1 ml saliva
hasil

9. Pengujian kandungan thiosianat
- ditambahkan 1 tetes FeCl3 2% kemudian 3 tetes HCl 5%
- dicatat perubahan warna yang terjadi
- ditambahkan 1 ml HgCl2 2%
- dicatat warna yang timbul karena terbentuknya merkuri rhodamina
B. Pengujian karakteristik enzimatis – aktivitas amilase dalam air liur
- ditambah 1 ml substrat amilum 1%
- dikocok dengan shaker agar semua larutan tercampur
- disiapkan 2 tabung reaksi dan diberi tanda 0’ dan 20’
- tabung reaksi diisi 10 ml HCl 0,05 N
- dimasukkan ke dalam tabung reasksi bertanda 0’ sebanyak 1 ml saliva
dan dikocok
- dimasukkan 1 ml saliva ke dalam cairan sisa dan dicampur dengan
cepat dan dicatat waktunya
- diinkubasi dan sekali waktu digoyang agar tercampur
- dimasukkan 1 ml larutan dari erlenmeyer ke dalam tabung reaksi
bertanda 20’ tepat saat penunjuk waktu menunjukkan 20 menit
- dikocok sebentar
- ditambahkan 1 ml larutan KI-KIO3 ke dalam tiap tabung
- dicampur hingga merata dan ditunggu sampai 5-10 menit
- ditentukan intensitas warna yang timbul dengan spektrofoto meter
- ditentukan prosentase substrat yang dicerna oleh amilase saliva
IV. HASIL DAN PEMBAHASAN
1 ml saliva
hasil
5 ml aquades
hasil

4.1 HASIL
Pengujian Karkateristik Kimiawi
1. Pengukuran Sifat Keasaman atau pH Saliva
a. Tabung I : Saliva + PP =
b. Tabung II : Saliva + PP =
c. Tabung III : Saliva + PP =
d. Tabung IV : Saliva + PP =
2. Sifat Saliva Sebagai Protein-Uji Biuret
a. - Tabung I (berisi 1 ml aquades) + 5 tetes NaOH = warna tetap bening
- Tabung I (berisi 1 ml aquades) + 3 tetes CuSO4 = warna biru muda
b. - Tabung II (berisi 1 ml saliva) + 5 tetes NaOH = warna tetap bening
- Tabung II (berisi 1 ml saliva) + 3 tetes CuSO4 = warna bening, terdapat
gumpalan berwarna biru muda
3. Pengujian Kandungan Mucin
a. - Tabung I (berisi 2 ml saliva) + 1 tetes CH3COOH 5% = warna bening
- Tabung I (berisi 2 ml saliva) + 1 tetes CH3COOH 5% + 2 tetes NaOH
10% = keruh
b. - Tabung II (berisi 2 ml saliva) + 5 tetes aquades = bening
- Tabung II (berisi 2 ml saliva) + 5 tetes aquades + 2 tetes NaOH 10% =
keruh
4. Pengujian Kandungan Klorida
a. - Tabung I (berisi 1 ml saliva) + 3 tetes HNO3 5% = bening
- Tabung I (berisi 1 ml saliva) + 3 tetes HNO3 5% + 2 tetes AgNO3 =
keruh, terdapat endapan
5. Pengujian Kandungan Sulfat
a. - Tabung I (berisi 1 ml saliva) + 3 tetes HNO3 5% = keruh
- Tabung I (berisi 1 ml saliva) + 3 tetes HNO3 5% = putih keruh, terdapat
gumpalan
6. Pengujian Kandungan Fosfat

- 1 ml saliva + 1 tetes HNO3 5% = bening
- 1 ml saliva + 1 tetes HNO3 5% + 1 ml (NH4)6Mo7O24 = kuning keruh,
terdapat gumpalan dipanaskan = kuning bening, terdapat endapan
7. Pengujian Kandungan Kalsium
- 1 ml saliva + 1 tetes CH3COOH = bening
8. Pengujian Kandungan Nitrat
- 1 ml saliva + 3 tetes H2SO4 5% = bening
- 1 ml saliva + 3 tetes H2SO4 5% + 2 tetes KI = kuning
- ml saliva + 3 tetes H2SO4 5% + 2 tetes KI + 1 tetes amilum = hitam
keunguan, terdapat gumpalan kekuningan
9. Pengujian Kandungan Thiosanat
- 1 ml saliva + 1 tetes FeCl3 2% = putih, terdapat endapan dan terdapat
( seperti selaput) berwarna orange
- 1 ml saliva + 1 tetes FeCl3 2% + 3 tetes HCl 5% = tetap agak keruh
- 1 ml saliva + 1 tetes FeCl3 2% + 3 tetes HCl 5% + 1 ml HgCl2 2% =
bening, terdapat endapan dan ada (seperti selaput putih) diatas
Pengujian Karakteristik Enzimatis – Aktivitas Amilase Dalam Air Liur
- Tabung 20’ = kuning bening
- Tabung 0’ = hitam
Substrat yang dicerna (%) = 100% - ( absorbansi pd tabung 20’ / absorbansi pd
tabung 0’ x 100%)
= 100% - (0,010 / 1,059 x 100%)
= 100% - 16,95%
= 83,05%
4.2 PEMBAHASAN
Pada praktikum kali ini dilakukan pengujian saliva yang bertujuan untuk
mempelajari karakteristik saliva secara kimiawi dan enzimatis melalui
serangkaian pengujian dan secara spektrofometer. Dalam praktikum ini,
pengujian karakteristik kimiawi saliva meliputi pengukuran keasaman atau
PH saliva, sifat saliva sebagai protein dengan menggunakan uji biuret,
pengujian kandungan mucin, pengujian kandungan klorida, pengujian

kandungan sulfat, pengujian kandungan fosfat, pengujian kandungan
kalsium, pengujian kandungan nitrat, dan pengujian kandungan thiosianat.
Sedangkan pengujian karakteristik enzimatis digunakan untuk mengetahui
aktivitas amylase dalam air liur yang kemudian dari intensitas warnanya
dapat diketahui prosentase substrat yang dicerna oleh amylase saliva.
Uji karakteristik kimiawi yang pertama adalah pengukuran sifat
asam atau pH saliva. Pengujian sifat keasaman atau pH saliva ini diukur
dengan menggunakan indikator-indikator yaitu Phenolphthalein (PP),
Methyl Orange (MO), Methyl Red (MM), dan Methyl Blue (MB).
Berdasarkan dari hasil data yang tercantum di dalam lampiran hasil,
indikator-indikator menunjukkan sifat pH yang asam yang lebih dominant.
Warna biru yang dihasilkan dari indikator MB tidak begitu akurat,
sehingga dapat dipastikan bahwa saliva yang diukur mempunyai pH yang
bersifat asam. Hal ini sesuai dengan PH normal saliva yaitu 6. Namun
pada beberapa literature menyebutkan bahwa PH normal saliva adalah 7,4.
Pada uji karakteristik kimiawi yang kedua yaitu uji saliva sebagai
protein. Pada analisis sifat saliva sebagai protein dengan mengguanakan
uji biuret, membandingkan kandungan protein dalam aquades dan dalam
saliva. Setelah dilakukan dengan uji biuret, sampel menunjukkan warna
biru muda pada tabung I. Adanya endapan pada tabung II serta perubahan
warna menjadi biru agak tua menindikasikan adanya protein dalam saliva.
Kemudian juga dikarenakan adanya pembentukan kompleks Cu dengan
gugus CO dan NH dari rantai peptide dalam susuna basa.
Pengujian karakteristik kimiawi yang ketiga adalah pengujian
kandungan mucin. Pada tabung I yang diisi saliva ditambah 1 tetes
CH3COOH 5% menunjukkan tidak adanya perubahan apapun. Sementara
pada tabung II yang diisi saliva ditambah 5 tetes aquades menunjukkan
perubahan larutan menjadi keruh yang menunjukkan adanya sekresi

mucin. Mucin ini berfungsi sebagai pelican rongga mulut sehingga
makanan tetap basah dan mudah untuk ditelan.
Dari percobaan yang telah dilakukan pada pengujian kandungan
klorida ini didapatkan hasil yaitu saliva berubah menjadi putih keruh dan
terdapat gumpalan yang berwana putih juga. Adanya endapan tersebut
menandakan bahwa sampel saliva tersebut mengandung klorida.
Pada pengujian kandungan sulfat, digunakan larutan HNO3 5% dan
BaCl2 sebagai larutan untuk menguji kandungan sulfat pad sampel saliva
tersebut. Dari percobaan yang telah dilakukan didapatkan hasil yaitu saliva
berubah warnanya menjadi putih keruh dan terdapat endapan. Kekeruhan
yang dihasilkan ini menunjukkan bahwa dalam sampel saliva yang diuji,
terdapat kandungan sulfat didalamnya.
Kandungan fosfat dalam sampel saliva diuji dengan menambahkan
HNO3 5% dan (NH4)6Mo7O24. Setelah dilakukan pengujian, diperoleh
hasil bahwa saliva berubah warna menjadi kuning bening dan terdapat
endapan. Adanya endapan disini menunjukkan bahwa di dalam sampel
saliva yang diuji terdapat kandungan fosfat.
Untuk uji kandungan kalsium pada saliva menggunakan
CH3COOH dan dari hasil menunjukkan bahwa tidak terjadi perubahan.
Saliva tetap berwana bening. Mungkin dari sini terjadi kesalahan mekanis
pada waktu praktikan melakukan pengujian pada sampel saliva.
Seharusnya setelah saliva ditambahkan dengan CH3COOH berubah warna
menjadi putih keruh. Nah, kekeruhan inilah yang membuktikan bahwa
dalam saliva tersebut mengandung kasium.
Dalam menguji kandungan nitrat dalam saliva, saliva ditambah 3
tetes H2SO4 5% kemudian ditambahkan dengan 2 tetes KI dan 1 tetes

amilum. Dalam reaksi ini, saliva berubah warna menjadi keruh ungu
kehitaman. Hal ini menunjukkan terdapat kandungan nitrat di dalam
sampel saliva.
Pada pengujian kimiawi yang terakhir yaitu pengujian ada atau
tidaknya kandungan thiosianat dalam saliva. Dalam percobaan kali ini,
saliva ditambah dengan 1 tetes FeCl3 2% kemudian ditambahkan lagi
dengan HCl 5% dan yang terakhir ditambahkan dengan 1 ml HgCl2 2%.
Dala reaksi kali ini, saliva tidak menunjukkan tanda-tanda terbentuknya
warna merah pada larutan. Sehingga dapat disimpulkan bahwa saliva pada
sampel tidak mengandung thiosianat.
Pengujian karakteristik enzimatis – aktivitas amilase dalam saliva
ini dilakukan dengan menggunakan alat yaitu spektrofotometer. Alat ini
digunakan untuk mengukur intensitas warnanya sehingga dapat digunakan
untuk menentukan jumlah substrat yang tersisa. Aktivitas enzim amilase
dinyatakan sebagai jumlah substrat yang dicerna persatuan waktu. Dan
berdasarkan hasil praktikum, dalam substrat yang dicerna oleh amilase
saliva setelah melakukan perhitungan, didapatkan hasil 83,05% yang
menunjukkan bahwa prosentase amilase dala saliva cukup tinggi yang
menandakanbahwa aktivitas amilasenya juga cukup tinggi.
V. KESIMPULAN
- Sampel saliva yang digunakan dala praktiku kali ini mengandung protein, mucin,
klorida, sulfat, fosfat, nitrat, dan tidak mengandung kalsium dan thiosianat.
- Saliva manusia memiliki PH yang bersifat asam yaitu sekitar 6-7,4
- Aktivitas anzim amilase saliva dapat dinyatakan sebagai jumlah substrat yang
dicerna persatuan waktu.
DAFTAR PUSTAKA

www.m-w.com
www.alkalizeforhealth.com
www.arbl.cdostate.edu
Poedjiati. 1994. Dasar-dasar Biokimia. Jakarta: UI-Press