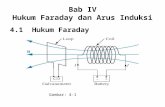
hukum faraday
-
Upload
yazid-al-johani -
Category
Documents
-
view
661 -
download
36
Transcript of hukum faraday
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
Satuan Pendidikan Mata Pelajaran Kelas/Semester Materi Pokok
: : : :
SMA 1 Suruh Kabupaten Semarang Kimia XII IPA Hukum Faraday dan Stoikiometri Elektrolisis
Alokasi Waktu Standar Kompetensi 2. :
:
3 X 45 menit (2 X pertemuan)
Menerapkan konsep reaksi oksidasi-reduksi dan elektrokimia dalam teknologi dan kehidupan sehari-hari
Kompetensi Dasar : 2.3 Menerapkan hukum Faraday untuk elektrolisis larutan elektrolit Indikator : 1. 2. 3. Menjelaskan hukum Faraday I. Menghitung massa zat hasil elektrolisis menggunakan hukum Faraday I. Menjelaskan hukum Faraday II.
4. Menghitung massa zat hasil elektrolisis menggunakan hukum Faraday II. 5. Menjelaskan prinsip-prinsip stoikiometri dalam elektrolisis.
6. Menghitung volume gas hasil elektrolisis menggunakan stoikiometri. A. Tujuan Pembelajaran : Setelah proses pembelajaran siswa dapat : Pertemuan pertama : 1. 2. 3. menjelaskan hukum Faraday I. menghitung massa zat hasil elektrolisis menggunakan hukum Faraday I. menjelaskan hukum Faraday II. 1
4. menghitung massa zat hasil elektrolisis menggunakan hukum Faraday II.
Pertemuan kedua : 1. 2. menjelaskan prinsip-prinsip stoikiometri pada elektrolisis. menghitung volume gas hasil elektrolisis menggunakan stoikiometri.
B. Materi Pembelajaran : 1. 2. 3. Hukum Faraday I Hukum Faraday II Stoikiometri Elektrolisis
C. Metode Pembelajaran : Pendekatan : Ketrampilan Proses Metode : Presentasi, latihan, dan tanya Jawab.
D. Kegiatan Pembelajaran : Pertemuan pertama : Unsur Kegiatan Langkah-langkah Kegiatan Pembelajaran Apersepsi : Tanya jawab reaksi elektrolisis. Pendahuluan Motivasi : Memberi informasi pada siswa bahwa hasil elektrolisis tidak hanya diketahui jenis zat-zatnya saja, tetapi kita juga bisa menghitung secara kuantitaif zat-zat hasil elektrolisis tersebut. Eksplorasi : Tanya jawab reaksi reduksi dan oksidasi serta tempat reaksi tersebut dalam sel elektrolisis. Elaborasi : Presentasi sel elektrolisis, susunannya, dan reaksi yang terjadi di anoda dan katoda. Latihan menuliskan reaksi elektrolisis suatu zat. Konfirmasi : Tanya jawab prinsip-prinsip dan ketentuan terjadinya reaksi pada sel elektrolisis. Penutup Menyimpulkan tentang sel elektrolisis. 5 2 Waktu (menit) 5
5
Inti
75
Pertemuan kedua : Unsur Kegiatan Langkah-langkah Kegiatan Pembelajaran Motivasi : Menyampaikan informasi kepada siswa agar melakukan percobaan dengan cermat sehingga memperoleh hasil percobaan yang akurat. Eksplorasi : Tanya jawab alat, bahan, dan cara kerja percobaan elektrolisis terhadap berbagai larutan. Elaborasi : Melakukan Percobaan elektrolisis berbagai larutan. Diskusi kelompok terhadap hasil pengamatan dan hasil percobaan. Konfirmasi : Diskusi kelas berkaitan dengan hasil pengamatan dan hasil percobaan. Penutup Menarik kesimpulan dari hasil percobaan dan memberi tugas individu membuat laporan resmi. 5 Waktu (menit)
Pendahuluan
5
Inti
80
E. Sumber Belajar : Sumber : 1. 2. Kimia untuk SMA Kelas XII 3A (Michael Purba) Halaman 72 75. Kimia untuk SMA Kelas XII 3(Ari Harnanto & Ruminten) Halaman 51 53.
Alat dan Bahan : F. Penilaian :
Teknik Penilaian : 1. 2. Tes Penugasan
Bentuk Instrumen : 1. Lembar soal tes 3
2.
Laporan praktikum
Instrumen Penilaian : 1. Tuliskan reaksi elektrolisis zat-zat berikut ini dengan elektroda grafit : a. larutan NaCl c. larutan Na2SO4 d. larutan KI e. lelehan MgCl2 f. lelehan Al2O3
b. larutan H2SO4 2.
Tuliskan elektrolisis terhadap zat-zat berikut ini : a. larutan CuSO4 dengan katoda Fe dan anoda Cu
b. larutan AgNO3 dengan katoda Fe dan anoda Ag 3. Jelaskan penggunaan elektrolisis dalam kehidupan sehari-hari !
Mengetahui : Kepala Sekolah
Guru Mata Pelajaran
Drs. HENDRO SAPTANTO NIP. 19581106 198703 1 001
Drs. YAZID AL JOHANI NIP. 19680324 199702 1 003
4