hemoglobin
description
Transcript of hemoglobin

BAB I
PENDAHULUAN
1.1. Latar Belakang
Penetapan Hb metode Sahli didasarkan atas pembentukan hematin asam setelah
darah ditambah dengan larutan HCl 0.1N kemudian diencerkan dengan aquadest.
Pengukuran secara visual dengan mencocokkan warna larutan sampel dengan
warna batang gelas standar. Metode ini memiliki kesalahan sebesar 10-15%,
sehingga tidak dapat untuk menghitung indeks eritrosi. Anemia adalah suatu
keadaan dengan kadar hemoglobin yang lebih rendah dari normal. Anemia bisa
juga berarti suatu kondisi ketika terdapat defisiensi ukuran atau jumlah eritrosit atau
kandungan hemoglobin. Anemia yang paling umum ditemukan di masyarakat
adalah anemia gizi besi. Terjadinya anemia gizi besi ini dapat disebabkan oleh
beberapa faktor, diantaranya kandungan zat besi dalam makanan sehari-hari,
penyerapan zat besi dari makanan yang sangat rendah, adanya parasit dalam tubuh
seperti cacing tambang atau cacing pita, diare, kehilangan banyak darah akibat
kecelakaan atau operasi karena penyakit (Wirakusumah, 1999). Anemia gizi besi
adalah anemia yang terjadi akibat kekurangan zat besi dalam darah. Artinya,
konsentrasi hemoglobin dalam darah berkurang karena terganggunya pembentukan
sel-sel darah merah akibat kurangnya kadar zat besi dalam darah. Semakin berat
kurangnya kadar zat besi yang terjadi, akan semakin berat anemia yang diderita.
Anemia gizi besi berakibat buruk bagi penderita terutama bagi golongan rawan gizi
yaitu anak balita, anak sekolah, remaja, ibu hamil dan ibu menyusui serta pekerja
1

terutama yang berpenghasilan rendah. Pada anak dan remaja yang terkena anemia
gizi akan terganggu 2 pertumbuhan fisik dan perkembangan. Selain itu, aktivitas
fisiknya juga akan menurun (Wirakusumah, 1999). Prevalensi anemia (< 12g/ dl)
adalah sebesar 27% ( remaja desa) dan 22% (remaja kota) pada saat tidak sedang
menstruasi. Sebanyak 24% (remaja desa) dan 27,8% (remaja kota) pada saat
menstruasi. Data tersebut menunjukkan bahwa kadar hemoglobin lebih tinggi pada
remaja desa pada saat menstruasi, sedangkan kadar hemoglobin lebih rendah pada
remaja desa pada saat tidak sedang menstruasi (Vasanthi et.al, 1991).
1.2. Tujuan
Untuk mengetahui kadar hemoglobin (Hb) darah dan mengetahui berapa jumlah
eritrosit seseorang dalam 1 mm3 darah
1.3 Metode dan Teknik
Dalam penyusunan makalah ini saya mengembangkan suatu metode yang
sering digunakan dalam pembahasan-pembahasan makalah sederhana, dimana saya
menggunakan metode dan teknik secara deskriptif dimana mencari sumber data dan
sumber informasi yang akurat lainnya. Setelah itu dianalisis sehingga diperoleh
informasi tentang masalah yang akan dibahas. Setelah itu, berbagai referensi yang
didapatkan dari berbagai sumber tersebut disimpulkan sesuai dengan pembahasan
yang akan dilakukan dan sesuai dengan judul makalah dan dengan tujuan
pembuatan makalah ini.Seperti itulah gambaran sekilas tentang metode dan teknik
yang digunakan dalam penyusunan makalah ini.
2

BAB II
TINJAUAN TEORI
2.1 Penetapan Kadar Hemoglobin
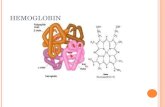
Hemoglobin (kependekan: Hb) merupakan molekul protin di dalam sel
darah merah yang bergabung dengan oksigen dan karbon dioksida untuk diangkut
melalui sistem peredaran darah ke tisu-tisu dalam badan. ion besi dalam bentuk
Fe+2 dalam hemoglobin memberikan warna merah pada darah. Dalam keadaan
normal 100 ml darah mengandungi 15 gram hemoglobin yang mampu mengangkut
0.03 gram oksigen.
Hemoglobin adalah molekul yang terdiri dari 4 kandungan haem (berisi zat
besi) dan 4 rantai globin, berada didalam eritrosit dan berfungsi untuk mengangkut
02. Kualitas darah dan warna darah ditentukan oleh kadar hemoglobin.
Kadar Hemoglobin Normal
Kadar hemoglobin biasanya ditentukan sebagai jumlah hemoglobin dalam gram
(gm) bagi setiap dekaliter (100 mililiter). Aras hemoglobin normal bergantung
kepada usia, awal remaja, dan jenis kelamin seseorang. Kadar normal adalah
sebagai berikut :
1) Bayi Baru lahir : 17-22 gm/dl.
2) Bayi Usia seminggu : 15-20 gm/dl.
3) Bayi Usia sebulan : 11-15gm/dl.
4) Kanak-kanak: 11-13 gm/dl.
3

5) Lelaki dewasa: 14-18 gm/dl.
6) Wanita dewasa: 12-16 gm/dl.
7) Lelaki separuh usia: 12.4-14.9 gm/dl.
8) Wanita separuh usia: 11.7-13.8 gm/dl.
Pemeriksaan Hemoglobin
Penetapan kadar hemoglobin dapat ditentukan dengan bermacam-macam
cara yang banyak dipakai di laboratorium klinik ialah cara fotoelektrik dan
kalorimetrik visual. Kadar hemoglobin dinyatakan dalam gr/dl darah. Pada pria
memiliki rata-rata sedikit lebih tinggi dari pada wanita. Kadar hemoglobin dapat
diukur dengan menggunakan dua cara terbaik ialah dengan teknik kalorimetri atau
fotometri
Macam-macam cara penetapan kadar hemoglobin:
1. Cara Tallquist
Prinsip : Membandingkan darah asli dengan suatu skala warna yang bertingkat-
tingkat mulai dad warna merah muda sampai warna merah tua. Cara ini hanya
mendapat kesan dari kadar hemoglobin saja, sebagai dasar diambil adalah
100%=15,8 gram hemoglobin per 100 ml darah. Tallquist mempergunakan skala
warna dalam satu buku mulai dari merah muda 10%. Ditengah-tengah ada lowong
di mana darah yang akan dibandingkan secara langsung sehingga kesalahan dalam
melakukan pemeriksaan antara 25-50%.
2. Cara Sahli
4

Prinsip : Hemoglobin diubah menjadi hematin asam, kemudian warna yang
terjadi dibandingkan secara visual dengan standar dalam alat. Cara sahli ini banyak
dipakai di Indonesia, walaupun cara ini tidak tepat 100%, akan tetapi masih
dianggap cukup baik untuk mengetahui apakah seseorang kekurangan darah.
Kesalahan dalam melakukan pemeriksaan ini kira-kira 10%. Kelemahan cara sahli
ini adalah hematrin asam itu bukan merupakan larutan sejati dan juga alat
hemoglobinometer sukar distandarisasi. Selain itu, tidak semua macam hemoglobin
dapat di ubah menjadi hematin, misalnya karboxy hemoglobin, methemoglobin dan
suffhemoglobin.
3. Cara cupri sulfat
Prinsip : Cara ini hanya dipakai untuk menetapkan kadar hemoglobin dari donor
yang diperlukan untuk transfuse darah. Hasil metode ini adalah persen hemoglobin.
Kadar hemoglobin dari seorang donor cukup kira-kira 80% hemoglobin. Kadar
minimum ini ditentukan dengan setetes darah yang tenggelam dalam larutan cupri
sulfat dengan berat jenis 1,053.
4. Cara Photo Elektrik kalorimetri
Prinsip : Hemoglobin diubah menjadi sianmethemoglobin dalam larutan
drabkin yang berisi kalium sianida dan kalium ferisianida. Absorbansi larutan
diukur pada panjang gelombang 540 nm. Larutan drabkin dipakai untuk mengubah
hemoglobin. Cara ini sangat bagus untuk laboratorium rutin dan sangat dianjurkan
untuk penetapan kadar hemoglobin dengan teliti karena standar sianmethemoglobin
5

kadamya stabil dan dapat dibeli. Larutan drabkin terdiri dari natrium biokarbonat 1
gram, kalium sianida 50 mg, kalium ferisianida 200 mg, aquadest 1000 ml.
Penetapan Hb cara Sahli
Pemeriksaan Hb menurut Sahli digolongkan kepada metoda colorimetri.
Prinsipnya, Hb darah diubah menjadi Hematin chlorida, yang warnanya menjadi
coklat tua (tengguli). warna yang terjadi diencerkan dengan aquadest sampai
dengan warna standart Hematin chlorida.
Alat dan bahan yang dipergunakan
a. Hemoglobinometer (hemometer), Sahli terdiri dari :
1) Gelas berwarna sebagai warna standard
2) Tabung hemometer dengan pembagian skala putih 2 sampai dengan 22.
Skla merah untuk hematokrit.
3) Pengaduk dari gelas
4) Pipet Sahli yang merupakan kapiler dan mempunyai volume 20/ul
5) Pipet pasteur.
6) Kertas saring/tissue/kain kassa kering
b. Reagen
1) Larutan HCL 0,1 N
2) Aquades
6

Tehnik Pemeriksaan :
1. Siapkan tabung dan isilah dengan HCl 0,1 N hingga garis yang terendah
(pada angka 2).
2. Kemudian buatlah luka kapiler pada jari sedemikian rupa hingga darah
keluar dengan baik tanpa memijat-mijat jari.
3. Hisaplah dengan pipet kapiler Hemoglobin (slang penghisap dibibir
pemeriksa) darah peripher tsbt. hingga garis batas 20 mm3.
4. Bersihkan, disapu dengan kertas saring, darah yang terdapt dibagian luar
ujung pipet. Hati-hati jangan sampai darah dalam kapiler turut keluar.
5. Masukkan pipet kapiler tsbt. kedalam tabung pengukur hingga tercelup
didalam HCl 0,1 N dan hembuskan perlahan-lahan. Isap dan hembuskan
lagi supaya isi tabung tercampur dengan baik. Letakkan tabung pengukur
tsbt. diantara dua telapak tangan dan kocoklah beberapa saat, Tunggulah 1-2
menit. Terjadi warna coklat tua.
6. Ambilah Aquadest dengan pasteur pipet dan teteskan tetes demi tetes
kedalam larutan Hematin chlorida yang berwrna coklat tua itu dan aduk
dengan batang gelas pengaduk. Dengan melatakkan kedalam celah diantara
cylinder warna standart kita samakan isi tabung perngukur itu. Bila masih
terlalu tua warnanya tetesi lagi aquadest. Bila terlampau banyak aquadest
dan warna menjadi lebih muda maka pemeriksaanharus diulang dari awal.
7. Setelah tercapai warna yang sama, kita perhatikan garis batas mana yang
dicapai oleh permukaan larutan, menumjukan skala atau kadar Hb. dalam gr
%.
7

Nilai normal dewasa : Laki-laki : 13-16g% Perempuan : 12-14g%
Catatan:
Tidak semua jenis Hb dapat dirubah menjadi asam hematin pada percobaan
Hb cara Sahli.
Kadar Hb cara Sahli ini masih banyak di pakai di Indonesia.
Sebenarnya kadar Hb ini berhubungan dengan jumlah eritrosit dan nilai Ht
dalam hal nulai MC (Mean Corpuscular). Secara kasar juga digunakan
hubungan nilai kadar Hb = 3 kali jumlah eritrosit permililiter kubik.
Kesalahan yang sering terjadi
1. Alat/reagen kurang sempurna, yaitu :
a. Volume pipet Hb tidak selalu tepat 20 ul
b. Warna standard sering sudah pucat.
c. Kadar larutan HCL sering tidak dikontrol.
2. Orang yang melakukan pemeriksaan :
a. Pengambilan darah kurang baik.
b. Penglihatan pemeriksa tidak normal atau sudah lelah.
c. Intensitas sinar/penerangan kurang.
d. Pada waktu waktu membaca hsil dipermukaan terdapat gelembung udara.
e. Pipet tidak dibilas dengan HCL
8

2.5 Menghitung Jumlah Eritrosit
Eritrosit merupakan bagian utama dari sel-sel darah. Setiap mm kubiknya
darah pada seorang laki-laki dewasa mengandung kira-kira 5 juta sel darah merah
dan pada seorang perempuan dewasa kira-kira 4 juta sel darah merah.
Eritrosit mempunyai bentuk bikonkaf, seperti cakram dengan garis tengah
7,5 uM dan tidak berinti. Warna eritrosit kekuning-kuningan dan dapat berwarna
merah karena dalam sitoplasmanya terdapat pigmen warna merah berupa
hemoglobin.
Hitung eritrosit adalah jumlah eritrosit per milimeterkubik atau mikroliter
dalah. Seperti hitung leukosit, untuk menghitung jumlah sel-sel eritrosit ada dua
metode, yaitu manual dan elektronik (automatik). Metode manual hampir sama
dengan hitung leukosit, yaitu menggunakan bilik hitung. Namun, hitung eritrosit
lebih sukar daripada hitung leukosit.
Prinsip hitung eritrosit manual adalah darah diencerkan dalam larutan
isotonis untuk memudahkan menghitung eritrosit dan mencegah hemolisis. Larutan
Pengencer yang digunakan adalah:
Larutan Hayem : Natrium sulfat 2.5 g, Natrium klorid 0.5 g, Merkuri klorid
0.25 g, aquadest 100 ml. Pada keadaan hiperglobulinemia, larutan ini tidak dapat
dipergunakan karena dapat menyebabkan precipitasi protein, rouleaux, aglutinasi.
9

Larutan Gower : Natrium sulfat 12.5 g, Asam asetat glasial 33.3 ml, aquadest 200
ml. Larutan ini mencegah aglutinasi dan rouleaux.
Nilai Normal
Dewasa laki-laki : 4.50 – 6.50 (x106/μL)
Dewasa perempuan : 3.80 – 4.80 (x106/μL)
Bayi baru lahir : 4.30 – 6.30 (x106/μL)
Anak usia 1-3 tahun : 3.60 – 5.20 (x106/μL)
Anak usia 4-5 tahun : 3.70 – 5.70 (x106/μL)
Anak usia 6-10 tahun : 3.80 – 5.80 (x106/μL)
Masa hidup eritrosit hanya sekitar 120 hari atau 4 bulan, kemudian dirombak di
dalam hati dan limpa. Sebagian hemoglobin diubah menjadi bilirubin dan
biliverdin, yaitu pigmen biru yang memberi warna empedu. Zat besi hasil
penguraian hemoglobin dikirim ke hati dan limpa, selanjutnya digunakan untuk
membentuk eritrosit baru. Kira-kira setiap hari ada 200.000 eritrosit yang dibentuk
dan dirombak. Jumlah ini kurang dari 1% dari jumlah eritrosit secara keseluruhan.
Hitung Eritrosit
Azas : Darah diencerkan dalam pipet eritosit dan tekanan dalam kamar hitung
Improved Neubauer. Jumlah eritrosit dihitung dalam volume tertentu, dengan
menggunakan factor konversi dalam jumlah eritrosit per mm3 darah dapat
diperhitungkan.
Alat dan bahan:
10

Pengencer dipakai larutan Hayem atau Gower,
Pipet isap
Kamar hitung Improved Neubuer
Mikroskop dengan objektif 40x.
Cara kerja:
1. Isap darah kapiler/perifer atau darah oksalat/EDTA sampai garis tanda 0,5
dan bersihkan ujung pipet.
2. Isap larutan Hayem dengan pipet tadi sampai garis tanda 101. Hati-hati
jangan sampai terjadi gelembung hawa pada pipet tersebut.
3. Kocok dengan menutup kedua ujung pipet dengan jari selama 3 menit.
4. Buang 3-4 tetes dan tetesan selanjutnya diteteskan pada kamar hitung
dengan menyinggung tepi kaca penutup. Dengan daya kapiler cairan
tersebut masuk ke dalam kamar hitung.
5. Tunggu beberapa saat agar eritrosit mengendap dan lihat dibawah
mikroskop dengan perbesaran 40 x.
6. Bahagian kamar hitung yang dihitung adalah bidang tengah sebanyak 5
bidang kecil dengan ukuran 1/25 mm2 (dengan kode E1, E2 , E3, E4 dan
E5).
Cara perhitungan:
Faktor pengenceran : 200x
Tinggi kamar hitung : 1.10mm
Luas 5 bidang kecil : 1/5mm2
11

Untuk mendapatkan jumlah eritrosit dalam 1mm3 maka luas bidang kecil harus
dikali 5
Maka dapat dirumuskan:
Jumlah eritrosit = (E1+E2+E3+E4+E5) x 5 x 10 x 200 = ∑ E x 10.000/mm3
12

BAB III
PENUTUP
3.1 KESIMPULAN
Cara Sahli ini bukanlah cara yang teliti. Kelemahan metode ini berdasarkan
kenyataan bahwa kolorimetri visual tidak teliti; bahwa hematin asam bukanlah
merupakan larutan sejati dan bahwa alat itu tidak dapat distandarkan.
Untuk menghitung eritrosit diperlukan pengalaman serta kemahiran dan
ketelitian agar kesalahn kecil sekali. Larutan yang dipakai adalah larutan Hayem
yang berfungsi untuk menghancurkan leukosit sehingga yang terlihat hanya eritrosit
saja.
3.2 SARAN
1. Pada saat melakukan percobaan sebaiknya mahasiswa berhati-hati agar tidak
terjadi kesalahan.
2. Pada saat pengambilan darah sebaiknya darah yang diambil melalui pipet jangan
sampai terputus, dan harus sesuai dengan ukuran yang ada.
Dan pada saat pengambilan sampel hendaknya berhati-hati dalam melihat warna,
karen harus sama dengan tabung yang ada di dalam alat Sahli.
13

DAFTAR PUSTAKA
Petunjuk Pemeriksaan Laboratorium Puskesmas, Jakarta, Departemen Kesehatan
RI, 1991
Harper, V. W Rodwell, P. A Mayes. 1979. Biokimia. Jakarta: EGC
Sadikin, M., 2001, Biokimia Darah, Widya Medika, Jakarta
14