Defeks Pankreas Pada Pre Diabetes
-
Upload
mukhyarjon-balmans -
Category
Documents
-
view
830 -
download
15
description
Transcript of Defeks Pankreas Pada Pre Diabetes

BAB I
PENDAHULUAN
Diabetes melitus (DM) merupakan suatu penyakit yang menjadi ancaman utama bagi
kesehatan umat manusia pada abad 21. Berdasarkan perkiraan yang dibuat oleh Organisasi
Kesehatan Dunia (WHO) bahwa pada tahun 2000 jumlah pengidap diabetes melitus di atas umur
20 tahun berjumlah 150 juta orang dan dalam kurun waktu 25 tahun kemudian, yaitu pada tahun
2025, jumlah ini akan membengkak menjadi 300 juta orang. Data terakhir dari WHO
menunjukkan bahwa terdapat kecendrungan peningkatan prevalensi DM yang lebih tinggi di
negara-negara Asia Tenggara termasuk di Indonesia. (1) Di Indonesia, jumlah penderita Diabetes
pada tahun 2000 adalah 8,4 juta orang dan diperkirakan jumlah ini akan meningkat pesat menjadi
21,3 juta orang pada tahun 2030. (2)
Besarnya dampak yang ditimbulkan oleh diabetes selain disebabkan oleh semakin
tingginya prevalensi diabetes juga diakibatkan oleh berbagai komplikasi yang ditimbulkannya.
Komplikasi diabetes berupa penyakit kardiovaskuler, penyakit pembuluh darah perifer, stroke,
kebutaan dan gagal ginjal sangat mengurangi kualitas hidup sehingga akan melambungkan biaya
kesehatan pada masyarakat terkait. Diabetes dapat mengenai segala lapisan masyarakat, segala
strata ekonomi, semua golongan umur baik pria maupun wanita. (3) Bahkan dilaporkan bahwa
diabetes merupakan penyebab kematian nomor 6 di Amerika Serikat pada tahun 2002 dan
peringkat ke 5 di seluruh dunia. (4)
Perkembangan prevalensi kasus diabetes di dunia, dan besarnya dampak yang
diakibatkan oleh komplikasi akut maupun kronis diabetes melitus menempatkan diabetes
menjadi salah satu penyakit yang menjadi perhatian badan-badan kesehatan dunia. Berbagai
upaya dilakukan dalam rangka pencegahan diabetes.
Salah satu tujuan pengobatan diabetes melitus adalah mencegahnya tumbulnya
komplikasi kronis. Tetapi pada kenyataannya pada waktu diagnosis ditegakkan sebagian besar
penderita sudah mempunyai komplikasi kronis sehingga pencegahan komplikasi tampaknya
1

sudah terlambat pada banyak kasus seperti itu. Melihat kondisi permasalahan tersebut maka akan
lebih baik bila diabetes dapat dicegah sebelum terjadinya diabetes. (3)
Peluang pencegahan diabetes dimungkinkan karena adanya suatu keadaan di dalam
spectrum perjalanan penyakit diabetes yaitu keadaan prediabetes. Keadaan prediabetes ini
merupakan suatu keadaan yang menjadi aba-aba untuk terjadinya diabetes di kemudian hari. (3)
Berbeda dengan keadaan diabetes yang bersifat irreversible, keadaan prediabetes merupakan
suatu titik yang dapat bergerak ke dua arah, yaitu ke arah normal atau ke arah diabetes. (4)
Berdasarkan pengamatan, individu dengan prediabetes dalam perkembangannya mempunyai 3
kemungkinan: sekitar 1/3 akan berkembang menjadi diabetes tipe 2, 1/3 berikutnya akan tetap
menjadi prediabetes sedangkan 1/3 sisanya akan menjadi normoglikemi. (5)
Dalam patogenenesis diabetes tipe 2 terdapat dua hal yang memegang peranan penting
yaitu insulin resisten dan defek sel beta pancreas. (4) (6) Banyak penelitian menyatakan bahwa
defek sel beta pancreas sudah terjadi pada keadaan prediabetes (7; 8; 9; 10) bahkan ada yang
menyebutkan hal ini sudah terjadi pada keadaan sebelum prediabetes . Hal ini tentu saja dapat
mempercepat \transformasi dari keadaaan prediabetes menjadi diabetes. Oleh karena itu dalam
refrat ini kami ingin menulis defek pancreas pada prediabetes yang meliputi mekanisme
(patofisiologi) dan pengobatannya. Dengan mencegah defek sel beta pancreas ini diharapkan
dapat mencegah atau memperlambat perubahan prediabetes menjadi diabetes.
2

BAB II
ANATOMI DAN FISIOLOGI PANKREAS
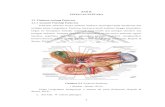
2.1 Anatomi
Kelenjar pancreas terdiri dari 0.7-1 juta kelenjar endokrin, yaitu pulau-pulau Langerhans,
tersebar di dalam struktur kelenjar pada kelenjar pancreas. Massa pulau Langerhans menyusun
1-1,5 % massa pancreas total dan dengan berat pada orang dewasa adalah 1-2 g. Di dalam
pancreas setidaknya terdapat 4 jenis sel yaitu A, B, D dan PP (juga dinamakan α, β, δ dan F)
yang berhasil dikenali pada kelenjar pancreas. Sel-sel ini tidak tersebar secara merata di
sepanjang pancreas. Sel PP yang mensekresikan polipeptida pancreas (PP), ditemukan paling
banyak di daerah posterior kaput pancreas (kaput posterior). Kaput posterior ini mendapatkan
perdarahan arteri mesenterika superior, bagian lain dari pancreas mendapatkan suplai darah dari
arteri coeliaca. (11)
Pulau-pulau pada lobus posterior terdiri dari 80-85% sel F, 15-20 % sel B dan kurang dari
0,5% merupakan sel A penghasil glukagon. Massa sel PP bervariasi menurut umur dan jenis
kelamin, cenderung lebih tinggi pada laki-laki dan orang yang lebih tua. Berbeda dengan lobus
posterior, pulau-pulau Langerhans yang minim PP terdapat pada ekor, badan dan bagian anterior
kaput pancreas, tumbuh dari tonjolan dorsal embrionik, utamanya mengandung sel-sel beta (70-
80%), dengan kandungan sel A penghasil glukagon 20% dan kira-kira 3-5% sel D yang
menghasilkan somatostatin. Gambaran sel-sel khusus penghasil berbagai hormone dapat dilihat
pada gambar 1. (11)
3

Gambar 1.Gambaran Histologis Pankreas. Sel-sel A merupakan sel yang lebih besar dengan
sitoplasma gelap. Sel D juga terdapat di bagian perifer, sedangkan sel B terdapat di tengah pulau
langerhans. (dikutip dari Basic Histology, 7 ed, 1992)
2.1 Sintesis dan Metabolisme Insulin
Insulin merupakan suatu protein yang terdiri dari 2 rantai peptida (rantai A dan B) yang
dihubungkan oleh 2 rantai sulfida. Prekursor insulin, preproinsulin (BM 11.500) disintesis di
dalam ribosom dan memasuki retikulum endoplasma sel Beta, yang mana dipotong oleh enzim
mikrosomal untuk membentuk proinsulin (BM 9000). Prosinsulin yang terdiri atas rantai A dan
B dihubungkan oleh peptide C yang terdiri atas 31 asam amino, diangkut ke apparatus Golgi,
dimana ia dikemas menjadi vesikel sekretorik. Sementara itu di dalam vesikel proinsulin
dipotong pada 2 tempat membentuk insulin (51 asam amino, BM 5808) dan suatu peptide C yang
tidak memiliki aktivitas biologis. Dengan demikian, sekresi insulin akan diikuti oleh sekresi
peptide C dengan jumlah molar yang sepadan, dan sejumlah kecil proinsulin yang urung
dipotong. (12)
Ketika hormon insulin disekresikan ke dalam darah, ia segera beredar di sirkulasi dalam
bentuk yang tidak terikat. Hormon ini hanya memiliki waktu paruh rata-rata 6 menit, sehingga
sebagian besar akan hilang dari dari sirkulasi dalam 10-15 menit. Pengecualian pada sebagian
4

hormon insulin yang berikatan dengan reseptor pada sel target, hormon ini akan didegradasi
oleh enzim insulinase yang terdapat di hati, dan sebagian kecil di ginjal dan otot. (13)
2.3 Sekresi Insulin
Glukosa merupakan senyawa kunci yang mengatur sekresi insulin. Selain itu terdapat
juga senyawa-senyawa lain yang turut mempengaruhi sekresi insulin diantaranya adalah asam
amino, benda-benda keton, peptida gastrointestinal, nutrisi lain dan neurotransmitter. Sintesis
insulin akan terstimulasi bila kadar glukosa >70 mg/dL, hal ini berlangsung dengan cara
meningkatkan translasi protein. (4)
Stimulasi sekresi insulin oleh glukosa dimulai dengan diangkutnya glukosa ke dalam sel
beta pancreas oleh protein pembawa GLUT2 (gambar 2). Langkah selanjutnya adalah fosforilasi
glukosa oleh enzim glukokinase yang merupakan tahapan yang rate limiting yang dapat
mengatur sekresi insulin. Langkah selanjutnya adalah metabolisme glukosa-6-fosfat yang
menghambat aktivitas kanal K+ sensitive ATP. Kanal ini terdiri dari dua protein terpisah: satu
berikatan dengan obat hipoglikemik oral tertentu (seperti sulfonylurea, meglitinid); yang lain
adalah protein kanal K+. penghambatan kanal K+ ini menginduksi depolarisasi membrane sel
beta, yang menyebabkan pembukaan kanal Ca2+ tergantung-voltase (menyebabkan influx Ca2+)
yang kemudian merangsang pelepasan insulin. (4) increatin yang dilepaskan oleh sel
neuroendokrin di saluran cerna meningkatkan sekresi insulin dan menghambat sekresi glucagon.
Pada individu sehat, respons sel-sel beta pancreas terhadap rangsangan oleh sekretagok
insulin (seperti glukosa) berlangsung secara bifasik, dimana terjadi sekresi insulin fase awal
selama 10 menit setelah rangsangan, diikuti oleh sekresi insulin fase lanjut yang berakhir dalam
beberapa jam. Sekresi insulin fase awal merupakan pelepasan insulin yang telah disintesis di
dalam granul-granul sekresi sel-sel beta pancreas, sementara sekresi inulin fase lanjut merupakan
pelepasan insulin yang baru disintesis sebagai respon terhadap rangsangan sel-sel beta pancreas
selanjutnya. (14)
5

Gambar 2. Stimulasi sekresi insulin oleh glukosa. (4)
Kelainan awal dalam pathogenesis DM tipe 2 adalah hilangnya sekresi insulin fase awal
setelah pemberian beban glukosa. Hal ini menyebabkan hambatan pencapaian puncak profil
insulin, yang akan diikuti dengan penurunan toleransi glukosa. Semakin berat progresifitas
gangguan toleransi glukosa, akan terjadi gangguan fungsi sel-sel beta pancreas yang akan
menyebabkan gangguan sekresi insulin baik fase awal maupun fase lanjut. Selama transisi dari
toleransi glukosa normal ke toleransi glukosa terganggu dan pada akhirnya DM tipe 2 klinis.,
akan diikuti dengan beberapa episode hiperglikemia post prandial. Sejalan dengan progresifitas
penyakit makan akan terjadi hiperglikemia baik dalam keadaan puasa maupun post prandial. (14)
6

BAB III
PREDIABETES DAN DEFEK SEL BETA PANKREAS
3.1 Prediabetes
IGT (Impaired glucose tolerance) dan IFG (impaired fasting glucose) disebut juga
prediabetes karena pada para penderita diabetes yang memiliki data lengkap, ternyata pada
umumnya menunjukkan keadaan tersebut lama sebelum diagnosis diabetes ditegakkan. (3)
Kelompok antara ini telah dikenali oleh komite ahli dalam diagnosis dan pengklasifikasian DM
sejak tahun 1997 dan 2003. (15) IFG atau GPT (glukosa puasa terganggu) ditegakkan bila kadar
gula darah puasa 100-125 mg/dL dan IGT atau TGT (toleransi glukosa terganggu) ditegakkan
bila didapatkan kadar gula darah 2 jam setelah pembebanan glukosa adalah 140-199 mg/dL. (16)
Selama ini HbA1C yang menunjukkan nilai rata-rata gula darah dalam 2-3 bulan
biasanya dikaitkan dengan risiko komplikasi menahun dan tidak dijadikan sebagai alat
diagnostik baik pada DM maupun prediabetes. Namun pada tahun 2010 ini, di dalam Standard of
Medical Care in Diabetes Mellitus-2010 yang diterbitkan oleh American Diabetes Association
(ADA), A1C telah digunakan sebagai diagnostic untuk prediabetes. Dalam standar yang` disusun
oleh ADA menetapkan nilai A1C 5,7 -6,4 % sebagai prediabetes. (16)
Keadaan prediabetes bukanlah suatu diagnosis penyakit namun merupakan suatu faktor
risiko untuk terjadinya penyakit, yaitu risiko untuk terjadi diabetes maupun risiko untuk terjadi
komplikasi lain seperti kardiovaskuler. (16) Di Amerika serikat prevalensi GPT diperkirakan
sebesar 26% dan TGT 15%, 57 juta Individu dinyatakan menjadi penyandang prediabetes,
beberapa diantaranya sudah menunjukkan kelainan mikrovaskular yang khas untuk komplikasi
diabetes. Di Indonesia prevalensi prediabetes cukup tinggi, mencapai 10,2 % yang merupakan
prevalensi glukosa darah puasa, sehingga diperkirakan terdapat sekitar 24 juta penduduk
Indonesia telah menderita kelainan ini. (5)
Seperti halnya pada DM tipe 2, maka dalam pathogenesis terjadinya prediabetes juga
melibatkan resistensi insulin dan kerusakan sel beta pankreas. Keadaan prediabetes ini erat
kaitannya dengan suatu sindroma yang disebut sindroma metabolik atau disebut juga sindroma
resistensi insulin dimana komponen utamanya adalah obesitas sentral. (16) overweight dan
7

obesitas berperan dalam persistensi prediabetes. (17) Selain resistensi insulin maka aspek lain
yang berperan adalah defeks sel beta pancreas. GPT dan TGT terjadi dengan mekanisme yang
berbeda hal ini dibuktikan dengan bervariasinya tingkat resistensi insulin dan defek fungsi sel
beta pada kedua kelompok ini. (8) (10)
3.2 Patofisiologi Defek Sel Beta Pankreas
Kerusakan sel beta merupakan bagian penting dalam patofisiologi terjadinya prediabetes
maupun pada diabetes. Ada beberapa teori yang menerangkan bagaimana terjadinya kerusakan
sel beta ini, diantaranya adalah teori glukotoksisitas, lipotoksisitas dan penumpukan amiloid.
(18) Efek hiperglikemi sendiri terhadap sel beta pancreas dapat manifes dalam beberapa bentuk:
pertama glukotoksisitas sel beta, yang merupakan kerusakan ireversibel; kedua adalah ausnya sel
beta (beta cell exhaustion), adalah kelainan yang masih reversible dan terjadi lebih dini
dibandingkan toksisitas dan yang ketiga adalah desensitasi sel beta, yaitu gangguan sementara
sel beta yang dirangsang oleh hiperglikemia yang berulang keadaan ini akan kembali normal bila
gula darah dinormalkan. (3) Ada beberapa teori yang menerangkan patofisiologi kerusakan sel
beta yaitu: glukotoksisitas, lipotoksisitas dan agregasi amiloid.
3.2.1 Glukotoksisitas
Terdapat fakta bahwa dengan perjalanan waktu telah terjadi penurunan fungsi sel beta
pada hampir semua pasien diabetes, sehingga muncul pendapat bahwa glukosa sendiri toksik
terhadap sel beta pancreas. (18) Hal ini juga telah terbukti melalui percobaan pada invitro atau
pada binatang percobaan. Pada suatu penelitian didapatkan bahwa glukotoksisitas dapat
menginduksi suatu gen yang disebut TRIB 3 yaitu suatu protein yang terlibat dalam jalur sinyal
yang menyebabkan apoptosis sel beta pancreas. (19) Secara invitro, perlakuan hiperglikemia
dapat menyebabkan menurunnya mRNA insulin dan menurunkan pula laju translasi protein
proinsulin. (20)
Selain menyebabkan kematian/apoptosis sel beta pancreas, glukotoksisitas juga
menyebabkan gangguan pada tahap akhir dari eksositosis insulin. (21) Metabolisme glukosa
yang bersifat oksidatif di sel beta pancreas juga akan menyebabkan pembentukan reactive
oxygen species (ROS) yang akan menyebabkan kerusakan sel beta (gambar 3). Sel beta pancreas
hanya mempunyai sedikit enzim katalase dan superoksida dismutase, yang berfungsi untuk
8

merubah ROS. ROS akan mengaktifkan NF-κB, yang merupakan jalur proapoptotik. Selain itu
efek hiperglikemia pada pancreas adalah menurunkan ekspresi gen duodenum homeobox-1,
yaitu suatu regulator transkripsi gen insulin. Mekanisme lain adalah melalui keterlibatan
upregulasi protein uncoupling 2 (UCP-2) oleh glukosa yang tinggi dapat menyebabkan
metabolism glukosa oksidatif berlangsung tanpa pembentukan ATP sehingga pembentukan ATP
menjadi rendah. (18)
3.2.2 Lipotoksisitas
Meskipun asam lemak bebas (FFA) merupakan suatu senyawa yang dapat merangsang
sekresi insulin, (4) namun demikian kelebihan beban asam lemak bebas yang kronik juga dapat
menyebabkan kerusakan sel beta pancreas. Salah satu bukti bahwa lipotoksisitas berperan dalam
patofisiolgi kerusakan sel beta adalah ditemukannya penumpukan lemak dari pemeriksaan post
mortem pada sel beta pancreas pasien DM dan subyek dengan faktor risiko. (22) Penderita DM
tipe 2 sering mengalami peningkatan kadar asam lemak bebas karena adanya resistensi insulin.
Gambar 3. Mekanisme defeks sel beta pancreas akibat glukotoksisitas dan lipotoksisitas (18)
Tingginya kadar glukosa sudah terbukti menghambat oksidasi beta asam lemak bebas, hal ini
akan menyebabkan penumpukan kompleks asam lemak rantai panjang-koenzim A (LC-KoA).
Hal ini akan mengganggu aktivitas pompa K+ normal, (18) atau UCP-2, yang ujung-ujungnya
9

adalah menghambat pembentukan ATP. (18; 23) Pengendalian pembentukan UCP 2 ini terjadi
melalui jalur PPARα, (23) PPARγ (24) dan leptin. (25)
Mekanisme lain defeks sel beta oleh lipotoksisitas adalah melalui sintesis seramida yang
dirangsang oleh asam lemak bebas atau melalui pembentukan oksida nitrit (NO). Pada jaringan
lain misalnya otot, penghancuran seramida dapat mencegah total resistensi insulin akibat asam
lemak bebas. Sehingga terdapat dugaan bahwa asam lemak bebas bekerja melalui pembentukan
seramida pada sel beta pancreas. Seramida telah dibuktikan dapat menhambat ekspresi gen
insulin dan mengakibatkan apoptosis melalui berbagai jalur. Pentingnya transduksi sinyal insulin
terhadap ekspresi gen insulin tidak dapat dianggap remeh, dan hal ini merupakan suatu hal
penting lain dari lipotoksisitas: melalui asam lemak-KoA dapat menghambat pensinyalan
reseptor insulin pada sel beta melalui pengaruh terhadap protein IRS, PI-3 kinase atau lebih ke
hulu dari kaskade pensinyalan insulin. (18)
3.2.3 Penumpukan Amiloid pada Sel Beta Pankreas
Berdasarkan pemeriksaan postmortem pada pasien dengan diabetes tipe 2 ditemukan
bahwa hampir semua jaringan pancreas pasien DM tipe 2 terdapat kandungan amioloid dalam
jumlah yang bermakna. Amiloid terdiri atas amiloid polipeptida (IAPP), atau amilin. IAPP
merupakan senyawa yang secara normal terdapat di dalam granul insulin sehingga ikut
disekresikan bersama insulin. Agregat kecil dari IAPP bersifat sitotoksik secara invitro, dan
diduga bahwa hal ini berhubungan dengan pembentukan saluran oleh molekul IAPP yang
beragregasi. Pembentukan saluran ini menyebabkan masukkan kalsium ke dalam sel beta;
kemungkinan lain adalah terbentuknya agregasi intraselular setelah terjadi interaksi dengan
membrane liposomal. Bila hiperglikemi dapat memicu agregasi IAPP, maka asam lemak bebas
dapat menambah sitotoksisitas agregat. (26) Meskipun ada kecendrungan bahwa peningkatan
sekresi insulin akan menyebabkan lebih banyak sekresi IAPP pada subyek dengan resistensi-
insulin yang kemudian menyebabkan agregasi IAPP, namun adanya temuan bahwa kurangnya
IAPP pada turunan pertama penderita DM dibandingkan kontrol membantah dugaan ini. (27)
Karena agregasi amiloid tidak dijumpai pada subyek non-DM dengan resistensi insulin telah
melahirkan anggapan bahwa agregasi amiloid merupakan kejadian lanjut pada patofisiologi DM.
10

3.3 Defek Sel Beta Pankreas pada Prediabetes
Sebagaimana pada DMT2, bahwa kerusakan sel beta pankreas juga merupakan salah satu
aspek penting pada prediabetes disamping resistensi insulin. Berbeda dengan pada diabetes
melitus bahwa kerusakan sel beta sudah berlansung lanjut (glucotoxycity), pada prediabetes
kerusakan sel beta mungkin masih bersifat glucoexhaustion, yang mana pada stadium ini
kerusakan masih bersifat reversible. (3)
Dari segi luasnya kerusakan pancreas, juga ditemukan perbedaan antara prediabetes dan
diabetes. Pada keadaan prediabetes (GPT dan TGT) kerusakan pancreas diperkirakan sekitar 50
% sedangkan pada diabetes sudah terjadi kerusakan yang lebih parah yakni sekitar 65%. Hal ini
lah yang menyebabkan terjadinya hiperglikemia yang nyata pada diabetes. (28)
3.3.1 Perubahan histopatologis pada prediabetes
Perubahan pada sel beta pankreas dari segi patologi anatomi merupakan suatu informasi
penting mengenai patofisiologi terjadinya diabetes. Namun demikian data-data tentang
perkembangan defek sel beta ini pada manusia sangatlah terbatas jumlahnya. Diabetes tahap
lanjut biasanya ditandai dengan menurunnya jumlah sel beta, penumpukan amiloid di dalam
pulau-pulau Langerhans, dan penumpukan lemak. Pemeriksaan histopatologi post mortem
biasanya dilakukan hanya pada pasien yang mengidap diabetes lama, karena teknik-teknik non-
invasif untuk melihat pulau-pulau pankreas tidak tersedia sehingga sangat sedikit yang diketahui
tentang perubahan histopatologi pada awal-awal diabetes. (29)
Suatu penelitian sudah lama yang dilakukan oleh Ogilvie pada tahun 1933 menemukan
bahwa terjadi hipertrofi pulau-pulau Langerhans pada pasien-pasien obesitas, dan ditemukannya
tumpukan amiloid pada sebagian kecil pasien lansia yang tidak menderita diabetes sebelumnya.
Berhubung kedua pasien ini mewakili orang-orang yang berisiko tinggi untuk menderita diabetes
maka perubahan-perubahan tersebut mungkin dapat mencerminkan keadaan-keadaan yang dapat
ditemukan pada prediabetes. (29)
Penelitian telah dilakukan pada tikus ZS (Zucker Fatty) yang memiliki mutasi pada gen
yang mengkode reseptor leptin (fa/fa) yang menyebabkan terjadinya obesitas dan hipertensi.
Pada tikus ini didapatkan peningkatan aktivitas sel beta dan keadaan fisiologis yang ditemukan
pada prediabetes yaitu beberapa sel tampak normal, banyak yang mengalami hipertrofi, dan
11

sedikit infiltrasi sel mononuclear, degenerasi sel beta dan fibrosis. Selain itu juga didapatkan
hiperinsulinemia sebagai kompensasi. (29)
Hal yang sama juga ditemukan pada penelitian pada pada tikus ZDF (Zucker diabetic
rat) yang membawa mutasi sehingga terjadinya hiperglikemia pada umur 7-10 minggu. Pada
awalnya beberapa pulau Langerhans tampak normal, sementara yang lain mengalami hipertrofi
dan sedikit irregular. Sejumlah kecil mengalami perubahan degenerative yang ditandai dengan
vakuolisasi dan hemoragis ke dalam jaringan pulau langerhans. Pada tahap ini terjadi
hipersekresi insulin, meskipun mRNA insulin masih normal. Setelah memasuki onset diabetes
struktur pulau Langerhans menjadi irregular dengan penonjolan ke arah eksokrin karena terjadi
hyperplasia/hipertrofi dan infiltrasi oleh sel-sel inflamasi. Pada keadaan tikus memperlihatkan
hiperglikemia gula darah puasa maka jumlah sel beta berkurang 50 % dibandingkan dengan pada
keadaan prediabetes replikasi sel beta menurun dan apopotosis meningkat. (30) Pada umur 14
minggu (keadaan diabetes lanjut) perubahan degeratif pada sel beta menjadi lebih berat, pulau
langerhans sebagian besar terdiri atas fibroblast, kolagen dan sel-sel mononuklear (29) (gambar
4)
3.3.2 Proses inflamasi pada prediabetes
Proses inflamasi yang melibatkan sitokin-sitokin inflamasi telah dibuktikan oleh
penelititian-penelitian baik pada manusia maupun pada hewan coba. Suatu penelitian kohor
yang melibatkan 27.628 subyek membuktikan bahwa pada orang yang berisiko terjadinya
diabetes terjadi peningkatan IL-6 dan CRP (C reactive protein) dibandingkan dengan kelompok
kontrol. 31 Hal yang sama juga ditemukan pada pasien-pasien dengan obesitas morbid dan
intoleransi glukosa (prediabetes) dimana didapatkan rendahnya kadar adiponektin dan tingginya
kadar CRP.32 penelitian lain mendapatkan bahwa tingginya kadar hCRP (human C reactive
protein) pada kelompok sinddroma metabolik berhubungan dengan meningkatnya kejadian
kardiovaskuler. 33
Dalam patofisiologi terjadinya prediabetes, terjadinya disfungsi sel beta merupakan suatu
hal yang tidak diragukan lagi, karena hal ini sudah dibuktikan oleh banyak penelitian-penelitian.
(8; 17; 9; 10) Hal yang menjadi perdebatan adalah patofisiologi GPT dan TGT dalam hal
kerusakan sel beta pancreas. Suatu penelitian menemukan bahwa disfungsi sel beta, maupun sel
12

alfa pada IFG dan TGT tidak ada perbedaan, namun terdapat perbedaan pada sekresi increatin
hormone dan fungsi insulin, (31) penelitian lain menyatakan bahwa pada GPT dan TGT terdapat
perbedaan baik sekresi insulin maupun pada fungsi insulin. (32; 33; 9; 34)
Mekanisme utama pada hiperglikemi pada GPT adalah terganggunya sekresi insulin basal
dan insulin fase I, sedangkan pada mekanisme utama pada TGT adalah resistensi insulin post
prandial yang menyebabkan hiperglikemi setelah pembebanan glukosa. (33) Dalam hal resistensi
insulin juga ditemukan perbedaan yang mana pada GPT, lebih didominasi oleh resistensi insulin
hati, sedangkan pada TGT, resistensi pada sel otot lebih menonjol. (32) Hal yang sama juga
ditemukan oleh penelitian yang melakukan studi terhadap perjalanan penyakit dari keadaan
normoglikemik menjadi TGT, GPT dan gabungan TGT/GPT. (34) Dengan adanya perbedaan
dalam hal derajat resistensi insulin pada TGT dan GPT maka dalam rangka prevensi DM untuk
TGT, yang didominasi oleh penurunan sensitivitas insulin hati, akan lebih logis bila diberikan
obat untuk meningkatkan sensitivitas insulin hati yaitu metformin. Sedangkan pada TGT yang
mana lebih menonjol resistensi insulin otot, lebih dianjurkan untuk memberikan obat yang
meningkatkan resistensi insulin otot yaitu peroxisom proliferator-activated receptor gamma
(PPAR-γ). (32)
13

14

Gambar 4. Karakteristik pulau pankreas pada Zucker fatty diabetic rat. (a) 6 minggu memperlihatkan 2
tampilan yang berbeda pada bagian kiri tampak sel mengalami hipertrofi dengan kompresi pada jaringan eksokrin,
kongesti vascular lebih dominan dan beta sel pada pinggir bersatu dalam kelompok linear. Pada bagian kiri sel
mengalami vakuolisasi dan tampak kongesti/perdarahan. (b) 6 minggu, dengan perbesaran lebih besar
memperlihatkan vakuolisasi sel, kematian sel. (c) 14 minggu tampak vakuolisasi sel beta dan degenerasi dan
sejumlah fibroblast. (d) degenerasi pulau pankreas yang ditandai dengan penurunan jumlah sel beta dengan berbagi
pewarnaan insulin. (e) 14 minggu, degenerasi merata pulau-pulau langerhans dengan sekresi insulin yang heterogen.
(f) 6 minggu, distribusi monosit/makrofag di pinggir pulau merupakan gambaran infiltrasi yang penting pada saat
ini. (g) 14 minggu, distribusi monosit/makrofag di pinggir pulau hampir tidak ada pada tahap ini dan telihat sedikit
sel beta, jaringan pulau pankreas digantikan oleh jaringan ikat. (h) 14 minggu distribusi kolagen yang banyak pada
pulau pankreas yang berdegenerasi.
15

BAB IV
PENGOBATAN PREDIABETES DAN IMPLIKASINYA
PADA FUNGSI SEL BETA PANKREAS
Berdasarkan buku panduan pengelolaan dan pencegahan prediabetes yang dikeluarkan
oleh PERKENI telah diusulkan beberapa langkah dalam pencegahan diabetes yang meliputi:
Intervensi gaya hidup dan terapi farmakologis. (5)
4.1 Intervensi gaya hidup
Modifikasi gaya hidup seharusnya merupakan bagian utama terapi dan diberikan pada
pasien pasien bahkan selalu ditingkatkan pada setiap kunjungan pasien. Gaya hidup merupakan
pendekatan pengelolaan fundamental yang dapat mencegah atau menunda berkembangnya
prediabetes menjadi diabetes serta menurunakan risiko penyakit mikrovaskular dan
makrovaskular. Lebih penting, intervensi gaya hidup memperbaiki semua faktor risiko diabetes
dan komponen sindroma metabolic, obesitas, hipertensi, dislipidemia, dan hiperglikemia. (5)
Berdasarkan studi yang dilakukan peneliti yang tergabung dalam Diabetes Prevention
Program mendapatkan bahwa modifikasi gaya hidup dapat menurunkan insidensi diabetes
melitus lebih baik dibandingkan metformin. Target penurunan berat badan dalam studi ini 5-10
% dan sedangkan aktivitas jasmani yang dianjurkan adalah intensitas sedang yang teratur 30-60
menit perhari, paling sedikit 4 hari dalam seminggu atau minimal 150 menit/minggu. Dengan
perubahan gaya hidup tersebut didapatkan penurunan insiden sebesar 58%, sedangkan dengan
metformin 31%. (35) Dalam suatu penelitian lain bahkan didapatkan efek aktivitas fisik singkat
tidak hanya memperbaiki resistensi insulin namun juga meningkatkan fungsi sel beta pada pasien
dengan TGT. (36) Pada studi yang dilakukan pada binatang percobaan didapatkan bahwa
mekanisme perbaikan jumlah dan fungsi sel beta oleh aktivitas jasmani adalah melalui aktivasi
insulin reseptor substrat-2 (IRS-2) dan perbaikan resistensi insulin adalah melalui peningkatan
ekspresi GLUT-2. (37)
3.2 Intevensi Farmakologi
16

Perubahan gaya hidup dalam kehidupan nyata sangat sulit dilakukan tanpa bantuan dan
pengawasan dari praktisi kesehatan professional. Tolak ukur potensial untuk menentukan
kberhasilan intervensi gaya hidup adalah penurunan berat badan 2 kg dalam sebulan atau 5%
penurunan BB pada 6 bulan. Hal ini serupa dengan penuruanan kadar glukosa plasma sebagai
respon yang diinginkan dar intervensi gaya hidup. Namun semua tidak semua individu dengan
risiko tinggi dapat menerima perubahan gaya hidup dan untuk mencapai ini diperlukan intervensi
lain yaitu dengan minum obat. Pengobatan dengan terapi farmakologis direkomendasikan
sebagai intervensi sekunder yang diberikan setelah atau bersama-sama dengan intervensi
modifikasi gaya hidup. Jika dengan intervensi gaya hidup belum didapatkan sasaran yang
inginkan maka dipertimbangkan untuk memulai penggunaan obat. (5)
3.2.1 Metformin
Metformin adalah obat yang telah digunakan secara luas dalam pengobatan diabetes
melitus tipe 2. Alasan penggunaan metformin ini adalah selain aman, hal ini disokong oleh masa
edarnya yang sudah 40 tahun, dan murah. Efektifitasnya dalam mencegah diabetes melitus tipe 2
sudah dibuktikan dalam penelitian diabetes prevention program. Penggunaan metformin 850 mg
2 kali sehari bersama makan mengurangi timbulnya DM sebesar 31 % dan sindroma metabolic
sebesar 17 %. Selain itu metformin juga dapat menurunkan berat badan pada kelompok dengan
BMI >30 kg/m2 sebesar 16-35%. (35)
Berdasarkan studi invitro pada kultur sel beta pancreas tikus didapatkan bahwa
metformin memiliki efek langsung terhadap sel beta pancreas baik basal maupun setelah induksi
glukosa. (38) Studi lain mendapatkan bahwa kombinasi vildagliptin dengan metformin selama
52 minggu meningkat fungsi sel beta pancreas dan sensitivitas insulin sesudah makan. (39)
Kekurangan metformin adalah dapat menyebabkan asidosis laktat (gangguan iskemia
pada ginjal dan hepar) sehingga tidak direkomendasikan pada semua TGT. (5) Selain itu
berdasarkan DPP metformin kurang berperan dalam mencegah diabetes pada orang dengan usia
>60 tahun. (35) Selain itu metformin juga memiliki efek yang tidak diinginkan pada saluran
cerna, namun hal ini dapat diatas dengan peningkatan dosis yang dilakukan secara bertahap.
3.2.2 Acarbose
Acarbose adalah obat yang bekerja dengan cara menghalangi pencernaa glukosa di usus
(inhibitor glukosidase alfa), sehingga mengurangi penyerapannya. (3) Pada studi STOP-NIDDM,
17

dalam follow up 3,3 tahun acarbose menurunkan risiko DM sebesar 25% dan risiko penyakit
kardiovaskular sebesar 49%. Adanya efek samping pada saluran cerna menimbulkan terjadinya
drop out sebesar 31% (dibandingkan 19% pada placebo) sehingga membatasi pengggunaanya
dalam mencegah DM. Studi ini merekomendasikan penggunaannya pada orang yang toleran
dengan efek samping saluran cerna untuk pencegahan DM dan risiko kardiovaskular. (5)
Glitazone
Pada studi DPP, pemberian glitazone dihentikan setelah pengobatan 1 tahun karena efek
samping hepatoksik. Hasil studi the Troglitazone in Preventing of Diabetes (TRIPOD)
menunjukkan, pemberian troglitazone lebih dari 3 tahun secara kumulatif menurunakan angka
kejadian timbulnya DM sampai nol. (5) Pada studi lain yang melibatkan 982 orang dengan IFG
dan IGT mendapatkan bahwa pemberian rosiglitazon, bukan ramipril, mengakibatkan
memperbaiki fungsi sel beta pancreas pada prediabetes. Efek ini juga berkonsekuensi terhadap
pencegahan diabetes. (40)
DPP4 inhibitor
Pada suatu studi yang memberikan vildagliptin 100 mg selama 6 minggu didapatkan hasil
bahwa obat ini dapat mencegah terjadinya prediabetes pada kelompok yang berisiko. Lebih jauh
dikatakan bahwa vildagliptin dapat memperbaiki resistensi insulin dan fungsi sel beta pancreas
pada pasien dengan GPT. (41) Studi lain yang memberikan vildagliptin pada pasien DM yang
telah mendapatkan metformin juga memberikan hasil perbaikan baik terhadap resistensi insulin
maupun fungsi sel beta pancreas. (39)
Orlistat
Orlistat adalah sebuah obat yang bekerja menghalangi enzim yang memecah trigliserda di
dalam saluran cerna. Hasil suatu penelitian mendapatkan bahwa orlistat dapat menurunkan berat
badan sebesar 3,5 kg dalam 6 bulan, yang dapat dipertahankan dalam 4 tahun. Pengobatan pada
subyek TGT yang obesitas dengan orlistat sebagai tambahan terhadap diit dan modifikasi gaya
hidup dapat menurunkan risiko terjadinya DMT2. (5)
18

BAB V
KESIMPULAN DAN SARAN
4.1 Kesimpulan
1. Defek sel beta pancreas merupakan salah satu aspek penting dalam patofisiologi
prediabetes
2. Defek sel beta pancreas dapat terjadi karena glukotoksitas dan lipotoksitas kronik
serta agregasi amiloid di dalam sel beta pancreas
3. Defek sel beta pada prediabetes terjadi dalam derajat lebih rendah (glucose
exhaustion) dan masih reversible.
4. Pada prediabetes terjadi perubahan pankreas pada tingkat genetika berupa
penurunan ekspresi gen PGC1 dan NRF1 dan mutasi DNA mitochondria; pada
tingkat molekuler terjadi defek enzim-enzim kunci seperti glukokinase, piruvat
dehidrogenase dan karboksilase; sedangkan pada tingkat selular dan
histopatologis terjadi hipertrofi dan hyperplasia sel beta pankreas
5. Perbedaan antara GPT dan TGT adalah: pada GPT, yang terganggu adalah sekresi
insulin basal dan fase I dengan mekanisme utama adalah gangguan sensitivitas
insulin hati; sedangkan pada TGT yang terganggu adalah sekresi insulin fase I dan
mekanisme utamanya adalah resistensi insulin otot.
6. Strategi pencegahan transformasi prediabetes menjadi DM meliputi modifikasi
gaya hidup dan terapi farmakologis yang terbukti dapat memperbaiki defek sel
beta pankreas
4.2 Saran
1. Perlu pemahaman tentang patofisiologi terjadinya kerusakan sel beta pada
prediabetes
2. Perlu penelitian lebih lanjut mengenai patofisiologi kerusakan sel beta pada
prediabetes
19

Daftar Pustaka
1. Suyono S. Diabetes melitus di Indonesia. Dalam: Sudoyo AW, editor. Buku Ajar Ilmu Penyakit Dalam Jilid III ed IV. Pusat Penerbitan Departemen Ilmu Penyakit Dalam FKUI; 2007. h. 1852-56
2. Wild S, Sicree R, Green A, et al. Global Prevalence of DM. Diabetes Care 2004; 27: 1047-53
3. Kariadi SHKS. Pengelolaan pra-diabetes dan pencegahan diabetes. Dalam: Manaf A, editor. Naskakh lengkap pertemuan ilmiah berkala X Ilmu Penyakit Dalam. Bagian Penyakit Dalam FK Unand/RS Dr M Djamil Padang; 2010. h. 235-242
4. Fauci AS, Kasper DL, Longo DL, et al. Harrison's Principle of Internal Medicine 17 ed. USA: MGraw-Hill Companies; 2008.
5. PB Perkeni. Buku panduan pengelolaan dan pencegahan prediabetes. Jakarta: Perkeni; 2009.
6. Codario RA. type 2 DM, pre-diabetes and metabolic syndrome: Humana Press; 2005
7. Rhee RY, Kwoon MK, Park JB,et al. Differences in insulin sensitivity and secretory capacity based on OGTT in impaired glucose regulation. The Kor J of Int Med 2007;22: 270-4
8. Bacha F, Lee SJ, Gungor N, et al. From Prediabetes to Type 2 diabetes in Obese Youth. 2010; 31: 12
9. Gani MAA, Tripathy D, DeFronzo RA, et al. Contributions of beta Cell Dysfunction and Insulin Resistance to the Pathogenesis of IFG and IGT. Diabetes Care 2006;29: 1130-39.
10. Pereult L, Breigman BC, Playdon, MC. Impaired fasting glucose with or without impaired glucose tolerance: progressive or parallel states of prediabetes? Am J Physiol Endocrinol Metab 2008; 295: 428-35
11. Masharani U, Karam JH. Pancreatic hormone and diabetes mellitus. Dalam: Greenspan FS, Gardner DG. Basic and clinical endocrinology 7th ed.McGraw Hill: 2004.
12. Funk JL. Dissorder of endocrine pancreas. Dalam: McPee SJ, Lingappa VR and Ganong WF. Pathophysiology of disease: an introduction to clinical medicine, 5th ed: McGraw Hill; 2006.
13. Guyton AC and Hall JE. Textbook of medical physiology, 11th ed. Philadelphia: Lange; 2006.
14. Shahab A. Fisiologi homeostasis glukosa dan sekresi insulin. Palembang: PAPDI palembang; 2006.
15. The Expert Commitee on Diagnosis and Clasification DM 2003. Report of the Expert Committee on the diagnosis and clasification of diabetes mellitus. diabetes care , 2003.
16. American Association of Diabetes. Standard of Medical Care in Diabetes Mellitus-2010. Diabetes Care 2010.
20

17. Goran MI. Persistence of Pre-diabetes in overweight and obese in Hispanic children. Diabetes 2008; 57. 231-5
18. Stumvold M, Goldstein BJ and van Haeten TW. Pathogenesis of type 2 DM . Dalam:Goldstein BJ and Wieland DM. Type 2 diabetes: principles and practice. Humana Press:2008; 13-27
19. Qian B, Wang H Men X. TRIB3 is implicated in glucotoxicity and oestrogen receptor-stress-induced b-cell apoptosis. J endocrinology 2008; 199:407-16
20. Zhang L, Lai E, Teodor T, et all. GRP78, but Not Protein-disulfide Isomerase, Partially Reverses Hyperglycemia-induced Inhibition of Insulin Synthesis and Secretion in Pancreatic Beta Cells. Journal Of Biological Chemistry 2009; 284: 5289-98
21. Dubois M. Glucotoxicity inhibit late step of insulin exocitosis. Endocrinology 2007; 148: 1606-1614
22. Tushuizen M, Bunck M, Pouwel. Pancreatic Fat Content and beta Cell Function in Men With and Without Type 2 Diabetes. Diabetes Care 2007;30:2916–2921
23. Amstrong MB, Towle HC. Polyunsaturated fatty acid stimulate hepatic UCP-2 expression via PPAR-alfa mediated pathway. Am J Physiol Endocrinol Metab 2001;1197-1204
24. Kelly LJ,Vicario PP,Thompson GM, et al. Peroxisome Proliferator-Activated Receptors gamma and alfa Mediate in Vivo Regulation of Uncoupling Protein (UCP-1, UCP-2, UCP-3) Gene Expression. Endocrinology 1998;139: 4920-27
25. Zhow YT, Shimabukuro M, Koyama, K . Induction by leptin of uncoupling protein-2 and enzymes of fatty acid oxidation. Proc. Natl. Acad. Sci, 1997; 94
26. Hull RL, Westermark GT, Kahn SE. 8 Islet Amyloid: A Critical Entity in the Pathogenesis of type 2 DM. The Journal of Clinical Endocrinology & Metabolism 2002; 89: 3629-35
27. Knowles NG, Lanchild MA, Fujimoto WY, Khan SE. Insulin and Amylin Release Are Both Diminished in First-Degree Relatives of Subjects With Type 2 Diabetes.Diabetes Care 2002;25:292-97
28. Matveyenk AV, Velduis JD, Buttler PC, et, al. Mechanisms of IGT and IFG Induce by 50% pancreatectomy. Diabetes 2006; 5:2347-56.
29. A review of islet of Langerhans degeneration in rodent model of type 2 DM . Nugent, DA and Smith, DM, Jones, HB. s.l. : Toxicology pathology, 2008, Vols. 36 (529-51).
30. Finegood DT, Mc Arhur MD , Kojwang D, et al. Rosiglitazone prevent the rise of net cell death. diabetes 2001; 50:1021-9
31. Pradhan AD, Manson JE, Rifai. C-Reactive Protein, Interleukin 6, and Risk of Developing Type 2 Diabetes Mellitus. JAMA 2001; 286:327-44
21

32. Hofso D, Ueland T, Hager H. Inflammatory mediators in morbidly obese subjects. European Journal of Endocrinology 2009;161:451-58
33. Devaraj S, Singh D, Jialal H, et al. Human C-reactive protein and the metabolic syndrome. Curr Opin Lipidol 2009; 20:182-89
34. Patti ME, Butte AJ, Crunkhorn S. Coordinated reduction of genes of oxidative metabolism in humans with insulin resistance and diabetes: Potential role of PGC1 and NRF1. PNAS 2003; 100:8466-71
35. Bensch KG, Mott JL, Chang SW, et al. Selective mtDNA mutation accumulation results in β-cell apoptosis and diabetes development.. Am J Physiol Endocrinol Metab 2009; 296: 672-680.
36. Færch K. Impaired fasting glycaemia vs impaired glucose tolerance, similar impairment of pancreatic alpha and beta cell function. Diabetologia 2008; 51:583-61).
37. Gani, MAA, Jeckinson CP, Richarson DK, Tripathy D, De Fronzo RA. Insulin Secretion and Action in Subjects With Impaired fasting glucose and impaired glucose tolerance. Diabetes, 2006; 55: 1430-35
38. Laakso M, Zilinskaite J, Hansen T. Insulin sensitivity, insulin release and glucagon-like peptide-1, levels in persons with impaired fasting glucose and/or impaired glucose tolerance in the EUGENE2 study.Diabetologia 2008; 51: 502–511
39. Faerch K, Vaag A, Holst JJ. Natural History of Insulin Sensitivity and Insulin Secretion in the Progression From Normal Glucose Tolerance to Impaired Fasting Glycemia and Impaired Glucose Tolerance: The Inter99 Study. Diabetes Care 2009; 32: 439-444
40. Diabetes Prevention Program Research Group. Reduction In The Incidence Of Type 2 Diabetes With Lifestyle. NEJM 2002; 346:394-403.
41. Bloom CJ and Chang AM. Short-Term Exercise Improves B Cell Function and Insulin Resistance in Older People with Impaired Glucose Tolerance.J. Clin. Endocrinol. Metab. 2008; 93:387-92.
42. Park, s, et al. Exercise improves glucose homeostasis that has been impaired by a high-fat diet by potentiating pancreatic B cell function and mass through IRS2 in diabetic rats. J Appl Physiol 2007; 103: 1764-71.
43. Patanè G. Metformin Restores Insulin Secretion Altered by Chronic Exposure to Free Fatty Acids or high glucose. Diabetes, 2000; 49.
44. Ahren . Improved Meal-Related beta Cell Function and Insulin Sensitivity by the Dipeptidyl Peptidase-IV Inhibitor Vildagliptin in Metformin-Treated Patients With Type 2. Diabetes Care 200; 28:1936-40
45. Hanley AJ, Zinman B, Sheridan P. Efect of Rosiglitazone and Ramipril on beta cell function in people with IGT and IFG . Diabetes Care 2010; 33:608–613
22

46. Utzschneider UKM, Tong J, Montgomery W. The Dipeptidyl Peptidase-4 Inhibitor Vildagliptin Improves beta cell Function and Insulin Sensitivity in Subjects With Impaired Fasting Glucose. Diabetes Care 2008; 31:108-13.
23

Daftar Pustaka
1. Suyono, S. Diabetes Melitus di Indonesia . [book auth.] AW Sudoyo, et al. Buku Ajar Ilmu Penyakit Dalam Jilid III ed IV . Jakarta : Pusat Penerbitan Departemen Ilmu Penyakit Dalam FKUI , 2007.
2. Global Prevalence of DM . Wild, S and Sicree, R. 2004 : Diabetes Care , Vol. 27.
3. Pengelolaan pra-diabetes dan pencegahan diabetes. Kariadi, SHKS. Padang : Bagian Penyakit Dalam FK Unand/RS Dr M Djamil Padang , 2010.
4. Fauci, AS, Kasper, DL and Longo, DL. Harrison's Principle of Internal Medicine. USA : MGraw-Hill Companies , 2008.
5. Perkeni, PB. Buku panduan pengelolaan dan pencegahan prediabetes. Jakarta : s.n., 2009.
6. Codario, RA. DM tipe 2, prediabetes .
7. Differences in Insulin Sensitivity and Secretory. Rhee, RY, Kwoon, MK and Park, JB. Korea : s.n., 2007, Vol. 22.
8. From Prediabetes to Type 2 diabetes in Obese Youth: Pathophysiological. Bacha, F, Lee, SJ and Gungor, N. 2010.
9. Contributions of beta Cell Dysfunction and Insulin Resistance to the Pathogenesis of IFG and IGT . Gani, MAA, Tripathy, D and DeFronzo, RA. 2006, Vol. 29.
10. Impaired fasting glucose with or without impaired glucose tolerance: progressive or parallel states of prediabetes? Pereult, L, Breigman, BC and Playdon, MC. 2, s.l. : Am J Physiol Endocrinol Metab, 2008, Vol. 295.
11. Masharani, U and Karam, JH. Pancreatic hormone and diabetes mellitus. [book auth.] FS Greenspan and DG Gardner. Basic and clinical endocrinology, 7th ed . San Francisco : McGraw Hill , 2004.
12. Funk, JL. Dissorder of endocrine pancreas. [book auth.] SJ McPee, VR Lingappa and Ganong WF. Pathophysiology of disease: an introduction to clinical medicine, 5th ed . s.l. : McGraw Hill , 2006.
13. AC, Guyton and JE, Hall. Textbook of medical physiology, 11th ed. philadelphia : s.n., 2006.
14. Fisiologi homeostasis glukosa dan sekresi insulin . Shahab, A. Palembang : PAPDI palembang , 2006.
24

15. The expert commitee on diagnosis and clasification DM, 2003. Report of the Expert Committee on the diagnosis and clasification of diabetes mellitus. s.l. : diabetes care , 2003.
16. Association, American Diabetes. Standard of Medical Care in Diabetes Mellitus-2010. 2010.
17. Persistence of Pre-diabetes in overweight and obese in Hispanic children. Goran, MI, et al. s.l. : Diabetes , 2008, Vol. 57.
18. Stumvold, M, Goldstein, BJ and van Haeten, TW. Pathogenesis of type 2 DM . [book auth.] BJ Goldstein and DM Wieland. Type 2 diabetes: principles and practice. New York : s.n., 2008.
19. TRIB3 is implicated in glucotoxicity- and oestrogen receptor-stress-induced b-cell apoptosis. Qian, B, Wang, H and Men, X. s.l. : Journal of endocrinology, 2008, Vol. 199.
20. GRP78, but Not Protein-disulfide Isomerase, Partially. Zhang, L, Lai, E and Teodoro, t: Volch Ak.
21. Glocotoxicity inhibit late step of insulin exocitois. Dubois, M, et al. Jakarta : Endocrinology, 2007, Vol. 148.
22. Pancreatic Fat Content and beta Cell Function in Men With and Without Type 2 Diabetes. Tushuizen, M, Bunck, M and Pouwel, PJ. s.l. : Diabetes Care, 2007, Vols. 30 (2916–2921).
23. Polyunsaturated fatty acid stimulate hepatic UCP-2 expression via PPAR-alfa mediated pathway. Amstrong, MB and HC, Towle. s.l. : Am J Physiol Endocrinol Metab, 2001, Vol. 281.
24. Peroxisome Proliferator-Activated Receptors gamma and alfa Mediate in Vivo Regulation of Uncoupling Protein (UCP-1, UCP-2, UCP-3) Gene Expression. s.l. : Endocrinology, 1998, Vol. 139.
25. Induction by leptin of uncoupling protein-2 and enzymes of fatty acid oxidation. Zhow, YT, Shimabukuro, M and Koyama, K. s.l. : Proc. Natl. Acad. Sci, 1997, Vol. 94.
26. Islet Amyloid: A Critical Entity in the Pathogenesis of. REBECCA L. HULL, GUNILLA T. WESTERMARK, PER WESTERMARK, AND STEVEN E. KAHN. 8, s.l. : The Journal of Clinical Endocrinology & Metabolism , 2002, Vol. 89.
27. Insulin and Amylin Release Are Both Diminished in First-Degree Relatives of Subjects With Type 2 Diabetes . Negar G. Knowles. s.l. : Diabetes Care , 2002, Vol. 25.
28. Mechanisms of IGT and IFG Induce by 50% pancreatectomy . Matveyenko, AV, Velduis, JD and Butler, PC. s.l. : Diabetes, 2006, Vols. 55 (2347-56).
29. A review of islet of Langerhans degeneration in rodent model of type 2 DM . Nugent, DA and Smith, DM, Jones, HB. s.l. : Toxicology pathology, 2008, Vols. 36 (529-51).
30. rosiglitazone prevent the rise of net cell death . Finegood, DT, Mc Arhur, MD and D, Kojwang. s.l. : diabetes, 2001, Vols. 50 (1021-9).
25

31. Impaired fasting glycaemia vs impaired glucose tolerance, similar impairment of pancreatic alpha and beta cell function. Færch, K, et al. s.l. : Diabetologia 51:853–861, 2008, Vols. 51 (583-861).
32. Insulin Secretion and Action in Subjects With Impaired fasting glucose and impaired glucose tolerance. Gani, MAA and Christopher, Jenkinson, CP. s.l. : Diabetes , 2006, Vol. 55.
33. Insulin sensitivity, insulin release and glucagon-like peptide-1, levels in persons with impaired fasting glucose and/or impaired glucose tolerance in the EUGENE2 study. Laakso, M, Zilinskaite, J and T, Hansen. s.l. : diabetologia , 2008, Vol. 51.
34. Natural History of Insulin Sensitivity and Insulin Secretion in the Progression From Normal Glucose Tolerance to Impaired Fasting Glycemia and Impaired Glucose Tolerance: The Inter99 Study. Faerch, K, Vaag, A and Holst, JJ. s.l. : Diabetes Care, 2009, Vol. 32.
35. REDUCTION IN THE INCIDENCE OF TYPE 2 DIABETES WITH LIFESTYLE. Group, Diabetes Prevention Program Research. s.l. : NEJM , 2002, Vols. 346 (394-403).
36. Short-Term Exercise Improves B Cell Function and Insulin Resistance in Older People with Impaired Glucose Tolerance. Bloom, CJ and Chang, AM. s.l. : J. Clin. Endocrinol. Metab. 2008 93:387-392, 2008, Vols. 93:387-392.
37. Park, s, et al. s.l. : J Appl Physiol , 2007, Vols. 103 (1764-1771).
38. Metformin Restores Insulin Secretion Altered by Chronic Exposure to Free Fatty Acids or high glucose. Patanè, G, et al. s.l. : DIABETES, 2000, Vol. 49.
39. Improved Meal-Related beta Cell Function and Insulin Sensitivity by the Dipeptidyl Peptidase-IV Inhibitor Vildagliptin in Metformin-Treated Patients With Type 2. Ahren, B, et al. s.l. : Diabetes Care , 2005, Vols. 28 (1936-40).
40. Efect of Rosiglitazone and Ramipril on beta cell function in people with IGT and IFG . Hanley, AJ, Zinman, B and Sheridan, P. s.l. : Diabetes Care 33:608–613, 2010, 2010, Vols. 33 (608-13).
41. The Dipeptidyl Peptidase-4 Inhibitor Vildagliptin Improves beta cell Function and Insulin Sensitivity in Subjects With Impaired Fasting Glucose. Utzschneider, UKM, Tong, J and Montgomery, W. s.l. : Diabetes Care , 2008, Vols. 31 (108-13).
26