BAB II TINJAUAN PUSTAKA A. Preparat Awetan Preparat...
Transcript of BAB II TINJAUAN PUSTAKA A. Preparat Awetan Preparat...

5
BAB II
TINJAUAN PUSTAKA
A. Preparat Awetan
1. Pengertian Preparat Awetan
Preparat adalah tindakan atau proses pembuatan maupun
penyiapan sesuatu menjadi tersedia, specimen patologi maupun
anatomi yang siap dan diawetkan untuk penelitian dan pemeriksaan
(W.A. New Dorland, 2002).
Karena pada umumnya dalam pengamatan preparat awetan
parasitologi dilakukan dengan menggunakan pengamatan langsung
secara mikroskopik, oleh sebab itu pengamatan ini tidak terlepas
dengan penggunaan mikroskop. Sedangkan pada penggunaan
mikroskop harus memperhatikan dua hal penting, yaitu :
a. Kemampuan memisahkan artinya jarak terkecil antara dua titik
objek, jika keduanya masih terlihat sebagai titik yang terpisah.
b. Pembesaran artinya sebagai rasio ukuran bayangan terhadap
ukuran objek dalam istilah jarak linear (Finn Geneser, 1994).
2. Macam Preparat
Dalam penyajian preparat awetan parasitology didasarkan atas
sampel yang digunakan dalam pembuatan preparat permanen :

6
a. Preparat cacing, preparat yang sampelnya berupa telur cacing
maupun cacing dewasa yang didapat lewat muntahan atau feaces.
b. Preparat protozoa, preparat yang menggunakan sampel berupa
protozoa yang ditemukan dalam feaces.
c. Preparat entomology, preparat yang menggunakan sampel berupa
kutu, insekta, dll.
d. Preparat tropozoit, preparat yang menggunakan sampel darah yang
dibuat apusan (darah tebal maupun darah tipis) untuk menemukan
tropozoit, sizon dan gametosit pada penyakit malaria.
(Is. Suhairiah Ismid, 2000)
3. Macam Pewarnaan
Macam-macam pewarnaan berdasarkan kegunaannya, antara
lain :
a. Teknik pewarnaan dan pengawetan MIF (Merthiolate [Thiomersal]
Iodine Formaldehyde), untuk mengidentifikasi trofozoit-trofozoit
protozoa manusia dan kista-kistanya, tetapi juga dapat dipakai
untuk (mengidentifikasi) telur-telur cacing.
b. Teknik pewarnaan dengan yodium dan pulasan supravital,
membantu di dalam membeda-bedakan protozoa.
c. Teknik pewarnaan feulgen, untuk mengenali asam
deoksiribonukleat (DNA).

7
d. Teknik pewarnaan dengan Hematoxylin Heidenhain, untuk
memperlihatkan struktur-struktur organism-organisme.
B. Pewarnaan Hematoxylin Heidenhain
Tujuan pewarnaan adalah untuk meningkatkan kontras alami dan
untuk lebih memperjelas berbagai unsur, dan gambaran mikroskopis telur
cacing (LEESON, C.Roland,2009).
Pada dasarnya bentuk telur cacing tidak menunjukkan kontras antara
bagian-bagiannya. Agar suspensi telur cacing dapat dipelajari strukturnya
dengan mikroskop cahaya biasa, perlu diberikan kontras melalui pewarnaan.
Metode pewarnaan telur cacing bertujuan selain agar tampak nyata, juga agar
bagian-bagian telur dapat dibedakan. Bahan pewarna secara selektif akan
mewarnai bagian-bagian telur cacing. Sebagian bahan pewarna bersifat
sebagai senyawa asam atau basa dan mempunyai kecenderungan meningkat
suspensi telur membentuk garam. Komponen telur cacing yang terwarna oleh
bahan pewarna basa disebut basofilik (bahasa yunani : senang basa) dan yang
terwarna oleh bahan pewarna asam disebut asidofilik.
Contoh bahan pewarna basa adalah toluidin blue dan methylen blue.
Hematoxylin yang umum dipakai secara rutin termasuk pewarna basa akan
mewarnai komponen telur cacing yang basofilik (mengandung bahan asam :
asam nukleat, glikosaminuglikan dan asam glikoprotein). Contoh bahan
pewarna asam : orange G, eosin, acid fuchsin, mewarnai komponen

8
asidofilik. Diantara bahan pewarna yang sering dipakai adalah kombinasi
antara hematoxylin dan eosin.
Banyak pewarna lain, seperti trichome (misalnya : metode Mallory
dan Masson) digunakan dalam prosedur yang berbeda. Bahan tersebut dapat
membantu untuk membeda-bedakan atau mengamati gambaran mikroskopis
telur cacing (Subowo, 2009).
Pewarna inti yang paling umum adalah Hematoksilin, yang sifat
memulasnya tergantung pada adanya hasil oksidasinya dalam larutan, yaitu
hematein. Bila dipulas dengan zat demikian, komponen telur cacing tampak
biru. Hematoksilin besi, yang memulas komponen menjadi biru tua atau
hitam, mempunyai aplikasi luas. Pada kebanyakan metode yang
menggunakan hematoksilin besi, seseorang memulas dengan zat itu secara
berlebihan, kemudian mengadakan diferensiasi secara regresif dalam larutan
asam lemah atau larutan garam feri.
Agar dapat memperlihatkan struktur-struktur organisme organisme,
maka perlu mewarnai mereka dengan suatu zat warna atau dengan zat-zat
warna. Zat warna yang paling baik dan paling biasa dipakai dalam karya-
karya parasitologik dan histologik adalah hematoxylin, yang diekstraksi dari
kayu gelondongan (yang berwarna coklat merah). Hematoxylin saja
mempunyai sifat-sifat mewarnai yang lemah, dan perlu dipakai suatu
mordant (bahan penajam) untuk membuatnya menjadi efektif. Banyak
formula yang berbeda-beda telah dipakai untuk membuat larutan-larutan zat
warna hematoxylin. Pada beberapa bahan mordant dicampur dengan

9
hematoxylin, sedang pada yang lain dipakai secara terpisah. Banyak
persenyawaan yang berbeda-beda dipakai sebagai mordant-mordant.
Sebagian besar berupa garam logam berat seperti misalnya besi, timah,
tembaga, coklat, tungsten, atau molybdenum. Satu dari pewarnaan
hematoxylin yang paling baik adalah Heidenhain’s iron-hematoxylin.
Pergantian bertingkat dalam konsentrasi alkohol dipakai pada semua
prosedur pewarnaan dan dehidrasi untuk mencegah distorsi (perubahan
bentuk).
Pada pewarnaan Heidenhain’s hematoxylin yang klasik, usapan-
usapan yang telah diwarnai dihilangkan warnanya dengan tawas besi. Jika
diinginkan, pemakaian mordant dan waktu pewarnaan dapat lebih lama.
Usapan-usapan itu dapat diberi mordant selama 2 jam dan diwarnai selama 4
jam, atau dapat diberi mordant selama 4 jam atau 24 jam. Waktu-waktu yang
lebih lama ini memberikan pewarnaan yang sedikit lebih baik (tepat), tetapi
tidak cukup untuk membuatnya bermanfaat untuk tujuan-tujuan rutin
(Norman, D.Levine, 1995).

10
C. Gambaran Umum Telur Cacing Ascaris lumbricoides
1. Klasifikasi Ascaris lumbricoides
Nama Latin : Ascaris lumbricoides
Phylum : Nemathelminthes
Sub Phylum : Ascaridoidea
Ordo : Ascaridida
Family : Ascaridae
Genus : Ascaris
Species : Ascaris lumbricoides
Kelas : Nematoda
Sub Kelas : Secernantea
(Arief Mansjoer, 2002)
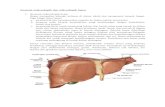
2. Morfologi Telur Ascaris lumbricoides
Ascaris lumbricoides atau yang disebut cacing gelang merupakan
salah satu infeksi cacing yang paling umum pada manusia. Cacing
berwarna merah muda atau putih kekuningan dan terlihat mengkilap.
Cacing dewasa berbentuk silindris, dengan ujung bagian depan
meruncing. Merupakan cacing nematoda terbesar yang menginfeksi
manusia. Cacing betina berukuran panjang 20-35 cm dan yang jantan 15-
31 cm, dengan ujung bagian belakang melengkung.
Telur yang telah dibuahi (fertilized) berukuran 60 mikron dan 75
mikron, sedangkan lebarnya berkisar antara 40 dan 50 mikron. Telur
cacing ini mempunyai kulit telur yang tak berwarna yang sangat kuat. Di

11
luarnya, terdapat lapisan albumin yang permukaannya berdungkul
(mamillation) yang berwarna coklat oleh karena menyerap zat warna
empedu. Di dalam kulit telur cacing masih terdapat suatu vitelline tipis,
tetapi lebih kuat daripada kulit luar. Selubung vitelline meningkatkan
daya tahan telur cacing Ascaris lumbricoides terhadap lingkungan
sekitarnya, sehingga dapat bertahan sampai 1 tahun lamanya. Telur yang
telah dibuahi ini mengandung sel telur yang tak bersegmen. Ditiap kutub
telur yang berbentuk lonjong atau bulat ini terdapat rongga udara. Telur
yang tak dibuahi (unfertilized) dijumpai di dalam tinja, bila didalam
hospes hanya terdapat cacing betina. Telur ini bentuknya lebih lonjong.
Dindingnya tipis, berwarna coklat dengan lapisan albumin yang tidak
teratur. Pada telur yang tak dibuahi tidak dijumpai rongga udara. Didalam
tinja manusia kadang-kadang ditemukan telur cacing yang telah
kehilangan lapisan albuminnya, sehingga sulit untuk menentukan
diagnosis telur cacing. Sebagai pegangan, adanya ovum yang besar di
dalam telur cacing cukup untuk menentukan jenisnya (Soedarto, 1990).
Pada pemeriksaan tinja hospes dapat ditemukan, yaitu :
a. Telur yang dibuahi, berukuran 60 x 45 ul, bulat atau oval dengan
dinding telur yang kuat, terdiri atas 3 lapis, yaitu :
1. Lapisan luar terdiri atas lapisan albuminoid dengan permukaan
tidak rata, bergerigi, berwarna kecoklat-coklatan karena pigmen
empedu.
2. Lapisan tengah merupakan lapisan chitin, terdiri atas polisakarida.

12
3. Lapisan dalam, membrane vitelline yang terdiri atas sterol yang liat
sehingga telur dapat tahan sampai satu tahun.
b. Telur yang dekortikasi adalah telur yang dibuahi akan tetapi
kehilangan lapisan albuminoidnya. Baik yang kortikasi maupun
dekortikasi, keduanya terapung di dalam larutan garam jenuh (pekat)
c. Telur yang tidak dibuahi, mungkin dihasilkan oleh betina yang tidak
subur atau terlalu cepat dikeluarkan oleh betina yang subur. Telur ini
berukuran 90 x 40 ul, berdinding tipis, akan tenggelam dalam larutan
garam jenuh
Resistensi telur sangat besar, tetapi tidak tahan terhadap
pengeringan langsung (sinar matahari langsung). Telur dapat bertahan
sampai bertahun-tahun (dalam 7 tahun yang masih survive 10%)
(Soejoto, 1996).
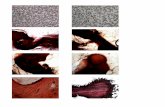
Gambar Telur cacing Ascaris lumbricoides 1. Telur yang fertilized
(telah dibuahi), 2. Telur yang unfertilized (tidak dibuahi), 3. Telur
dengan kulit luar terkelupas (Soedarto, 1990).

13
3. Siklus Hidup Ascaris lumbricoides
Telur biasanya keluar dari tubuh hospes bersama tinja dalam
keadaan belum bersegmen. Dalam tanah, apabila keadaan linkungan
cukup baik dan menguntungkan, akan menjadi telur yang bersifat
infektius dan mengandung larva yang dapat bergerak dalam waktu kira-
kira 3 minggu. Apabila telur tertelan oleh manusia bersama makanan atau
minuman, atau secara langsung melalui tangan kotor, karena kontaminasi
dengan tanah, akan menetas di dalam intestinum tenue (usus halus) dan
keluar larva. Kemudian larva ini menembus dinding usus dan masuk
saluran limfe dan darah. Mengikuti aliran darah, melalui vena portae ke
hepar, kemudian terus ke jantung kanan, ke paru-paru. Di dalam paru-
paru menembus dinding kapiler darah masuk ke dalam alveoli. Disini
tinggal sementara kemudian migrant melalui bronchiolus, bronchi, naik
sepanjang trachea sampai epiglottis lalu turun ke bawah melalui usofagus
sampai intestinum tenue dan tambah menjadi dewasa. Cacing dewasa
betina yang bertelur terjadi kira-kira 2 bulan sesudah infeksi.
Penyakit yang ditimbulkan disebut Ascariasis dan terdapat pada
manusia untuk semua umur. Bertelur sebanyak 200.000 butir/ekor/hari.
Seekor cacing mampu bertelur sampai 26 juta butir telur.