Presentasi kelompok 4 (ssa) 2013
-
Upload
edi-mikrianto -
Category
Documents
-
view
96 -
download
3
Transcript of Presentasi kelompok 4 (ssa) 2013

ANGGOTA :
AULIA PEBRINA (J1B111047)
FEBLE RIA PERTIWI (J1B111004)
RAHMIDA ULFAH (J1B111028)
SYAMSUN JAYA (J1B111012)
TRIA AGUSTINA AYU (J1B111023)
YARA TRIA (J1B111038)
PEMBIMBING MK SSA : EDI MIKRIANTO.,S.SI.,M.SI

Pada beberapa dekade terakhir, sintesis dan studi mengenai nanopartikel besi oksida khususnya magnetite (Fe3O4) menarik perhatian para ilmuwan dan engineer.
Hal ini antara lain karena sifat superparamagnetis yang dimiliki membuat nanopartikel magnetite bermanfaat dalam berbagai aplikasi. Misalnya:Bidang medisBidang teknologiMetal separator dalam pengolahan limbah cair

Magnetite (Fe3O4) merupakan salah satu bentuk oksida besi di alam selain maghemite (γ-Fe2O3) dan hematite (α-Fe2O3). Magnetite dikenal sebagai oksida besi hitam (black iron oxide) atau ferrous ferrite, yang merupakan oksida logam yang paling kuat sifat magnetisnya.

Salah satu metode sederhana yang efektif, efisien, dan ramah lingkungan yang telah dikembangkan adalah metode elektrokimia untuk mensintesis nanopartikel Magnetite (Fe3O4).
Pada metode elektrokimia digunakan elektroda, larutan elektrolit dan power supply. Beda potensial yang diberikan menyebabkan terjadinya reaksi oksidasi dan reduksi pada elektroda dan perpindahan elektron dari anoda menuju katoda. Deposisi besi oksida menempel pada bagian katoda atau anoda bergantung pada elektrolit yang digunakan.

Reaksi elektrokimia pada permukaan elektroda secara umum dipengaruhi oleh : transfer massa, transfer elektron, reaksi di permukaan elektrode, serta proses-proses permukaan seperti adsorpsi, desorpsi, kristalisasi.
Efektifitas proses tersebut diduga bergantung pada kondisi proses elektrokimia (seperti jenis dan ukuran elektrode, jenis dan konsentrasi elektrolit, rapat arus, beda potensial, suhu, dan jarak antar elektrode).

Alat dan Bahan Peralatan yang digunakan dalam penelitian ini adalah bejana acrylic berukuran 25 × 15 × 15 cm, dan 12 × 10 × 10 cm, elektroda besi berukuran 23 mm × 13 mm × 0,25 mm, power supply DC 0-30 V, HEWLETT-PACKARD DIGITAL MULTIMETER TYPE 3435A untuk amperemeter dan voltmeter, solid state relay merk OMRON type 63NA-220B dan temperatur controller merk Autonics TZN4S. Bahan kimia yang digunakan adalah demineralized water, larutan FeSO4.7H2O, dan pelat besi komersial.

1. Pelapisan BesiProses pelapisan besi menggunakan metode elektrolisis dengan elektrolit larutan FeSO4.7H2O. Lempeng besi yang akan dilapisi ditempatkan sebagai katoda sedangkan untuk anodanya dipakai elektroda inert yaitu platina. Proses pelapisan besi ini dilakukan selama 6 jam.

2. Sintesis Fe3O4
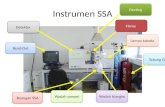
Langkah pertama yang dilakukan adalah menyusun alat percobaan seperti yang ditunjukkan pada Gambar 1.
Percobaan ini dilakukan selama 12 jam dengan tetap menjaga kestabilan arus yang mengalir. Setelah 12 jam percobaan dihentikan, kemudian produk yang berupa endapan dipisahkan, dicuci, dan dikeringkan.

Produk yang telah kering diamati warna dan kemagnetannya, diuji kelarutannya dalam air dan asam, dan dikarakterisasi dengan XRD untuk analisis kualitatif dan SEM untuk mendapatkan deskripsi morfologi dan ukuran produk.

Produk hasil elektrolisis berupa powder berwarna hitam seperti tampak pada Gambar 2, bersifat magnetik, larut dalam asam, tidak larut dalam air. Sifat-sifat ini sesuai dengan sifat Fe3O4

Analisis XRD Analisis XRD dilakukan untuk mengidentifikasi senyawa yang terkandung dalam produk elektrolisis mengacu pada pola peak standar difraksi sinar X untuk kristal Fe3O4. Sehingga dapat dikatakan bahwa Fe3O4 dapat disentesis melalui elektrokimia sederhana. Namun pada pola XRD ini ada bagian yang kurang sesuai dengan pola XRD standar pada sintesis Fe3O4, hal ini dimungkinkan terjadi karena mengandung impurities berupa FeOOH yang ditunjukkan oleh adanya puncak-puncak yang bersesuain dengan pola difraksi standar FeOOH (JCPDS 44-1415). Untuk mengatasinya sumber arus DC konstan dapat diganti dengan menggunakan pulsed DC sehingga puncak-puncak FeOOH tidak muncul.

Perbandingan Pola XRD deposit magnetite untuk Constant DC dam Pulsed DC

Secara ringkas mekanisme sintesis Fe3O4
secara elektrokimia yang diusulkan adalah:

Analisis SEMAnalisis morfologi dan ukuran partikel dilakukan dengan SEM.
Jika ditinjau dari segi ukuran, maka dapat disimpulkan bahwa nanopartikel Fe3O4
dapat disintesis dengan metode elektrokimia sederhana.

1. Nanopartikel Fe3O4 dapat disentesis dengan metode elektrokimia sederhana
2. Rapat arus berpengaruh terhadap karakter yang dihasilkan
3. Pada sintesis selama 12 jam dengan rapat arus 175 μA/cm2, 250 μA/cm2, dan 325 μA/cm2 pada 30oC masih terdapat impuritis yang diduga FeOOH