BAB II TINJAUAN PUSTAKA 2.1. Preparat Sediaan Apusan Tinjarepository.unimus.ac.id/2930/5/BAB...
Transcript of BAB II TINJAUAN PUSTAKA 2.1. Preparat Sediaan Apusan Tinjarepository.unimus.ac.id/2930/5/BAB...

7
BAB II
TINJAUAN PUSTAKA
2.1. Preparat Sediaan Apusan Tinja
Preparat adalah hasil dari tindakan atau proses pembuatan maupun penyiapan
sesuatu menjadi spesimen patologi maupun anatomi yang siap dan diawetkan untuk
penelitian dan pemeriksaan (W.A. New Dorland, 2002).
Preparat apusan tinja adalah hasil dari proses pembuatan maupun penyiapan
tinja (feses) yang dapat diperiksa secara langsung maupun diawetkan untuk
penelitian.
Dalam penyajian preparat parasitologi didasarkan atas sampel yang digunakan
dalam pembuatan preparat :
1.1. Preparat cacing, preparat yang sampelnya berupa telur cacing maupun cacing
dewasa yang didapat lewat muntahan dan feses.
1.2. Preparat protozoa, preparat yang menggunakan sampel berupa protozoa yang
ditemukan dalam feses.
1.3. Preparat entomologi, preparat yang menggunakan sampel berupa tungau, caplak,
kutu, insekta, dll.
1.4. Preparat tropozoit, preparat yang menggunakan sampel darah yang dibuat apusan
(darah tebal maupun darah tipis) untuk menemukan tropozoit, skizon dan
gametosit pada penyakit malaria (Is. Suhairiah Ismid, 2000).
http://repository.unimus.ac.id

8
2.2. Ascaris lumbricaides
2.2.1. Morfologi
Cacing jantan mempunyai panjang 10-30 cm sedangkan cacing betina 22-
35 cm. Cacing betina dapat bertelur 100 000 - 200 000 butir sehari, terdiri atas
telur dibuahi dan telur tidak dibuahi. Di tanah yang sesuai, telur yang dibuahi
tumbuh menjadi bentuk infektif dalam waktu kurang lebih tiga minggu.
Telur yang telah dibuahi berbentuk ovoid atau lonjong dengan ukuran 50-
70 x 40-50 µ. Telur ini terdiri oleh suatu membrane vetialin yang tipis untuk
meningkatkan daya tahan telur cacing tersebut dari lingkungan sekitar.
Terdapat juga membrane yang mengelilingi membrane vetialin yaitu membran
albuminoid yang pemukaannya tidak teratur atau terdapat benjolan-benjolan,
lapisan albuminoid terkadang hilang oleh karena adanya zat kimia yang
menghasilkan telur tanpa kulit (decorticated). Telur akan berwarna kecoklatan
saat berada di usus karena adanya pigmen empedu.
Telur yang tidak dibuahi (infertile) berbentuk lonjong dengan ukuran 60-
90 x 40-60 µ, memiliki dinding yang tipis, berwarna cokelat dengan lapisan
albuminnoid (Teuku Romi Imonsyah Putra, 2010).
http://repository.unimus.ac.id

9
Tabel 2.1 Karakteristik telur A. Lumbricaides (Permenkes, 2017)
FaseTelur
Ukuran Bentuk Warna KeteranganJumlah Lapisan
Gambar
Tidakdibuahi
60-90 x40-60 µ
Memanjangellipsoidal
Coklatsampaicokelattua
Lebih rampingdibanding teluryang dibuahi,bagian luar terdapattonjolon kasar danlapisan albuminois.Bagian dalam berisigranula
Dibuahi(tanpalapisanalbumin)
45-70 x35-50 µ
Oval Jernih Bentuk hampirmenyerupai telurtambang, tapidinding tebal.
Dibuahi(denganlapisanalbumin)
50-70 x40-50 µ
Lonjongatau bulat
Kuningkecoklatansampaicokelattua
Dinding tebal danberlapis. Bagianluar dilapisitonjolan-tonjolanyang bergelombang
Infektif 50-70 x40-50 µ
Lonjongatau bulat
Kuningkecokelatansampaicokelattua.
Dinding tebalberlapis 3 (fertil)atau 2(decorticated) berisi
2.2.2. Penularan
Bila telur infektif tertelan, telur akan menetas menjadi larva di usus halus.
Selanjutnya larva menembus dinding usus halus menuju pembuluh darah
atau saluran limfe, lalu terbawa aliran darah ke jantung dan paru. Di paru,
larva menembus dinding pembuluh darah, lalu dinding alveolus, masuk
rongga alveolus, kemudian naik ke trakea melalui bronkiolus dan bronkus.
Dari trakea larva menuju ke faring dan menimbulkan rangsangan di faring
http://repository.unimus.ac.id

10
sehingga penderita batuk dan larva tertelan ke dalam esofagus, lalu ke usus
halus. Di usus halus larva berubah menjadi cacing dewasa. Sejak telur
infektif tertelan sampai cacing dewasa bertelur diperlukan waktu kurang
lebih 2-3 bulan (Gambar 1).
Gambar 2.1 Siklus Masuk A. Lumbricaides Dalam Tubuh (Sumber : PermenkesNo.15, 2017)
2.3. Metode Pemeriksaan Tinja
Pemeriksaan tinja secara mikroskopis dapat dilakukan dengan beberapa teknik
dan metode sebagai berikut :
2.3.1. Pemeriksaan tinja metode langsung (Sediaan Basah)
Pemeriksaan dengan metode langsung (sedian basah) adalah
pemeriksaan kuantitatif yang bertujuan untuk mengetahui ada tidaknya telur
http://repository.unimus.ac.id

11
cacing pada tinja secara langsung dengan menggunakan larutan pewarna
Eosin 2% (dengan menggunakan kaca penutup) (Fuad, 2012).
Pemeriksaan dengan metode ini dapat dilakukan dengan 2 cara yaitu
dengan kaca penutup dan tanpa kaca penutup. Cara kerja pembuatan sediaan
langsung dengan mengambil feses sebanyak ± 2mg dengan lidi kemudian
letakkan di kaca objek dicampurkan dengan eoisn 2% hingga homogen.
Apabila terdapat bagian-bagian kasar dibuang. Lalu tutup dengan kaca slide
ukuran 20 x 20 mm, usahakan tidak terdapat gelembung-gelembung udara.
Kemudian dilakukan pengamatan di bawah mikroskop dengan perbesaran
objektif 10x dan 40x (Depkes, 2006).
2.3.2. Pemeriksaan tinja metode konsentrasi
1. Metode Sedimentasi (Metode Faust dan Russell, 1964)
Prinsip pemeriksaan dengan metode sedimentasi adalah dengan
adanya gaya sentrifugal akan memisahkan antara suspensi dan
supernatan sehingga diharapkan didapatkan telur cacing didalam
endapan (Fuad, 2012).
2. Metode Flotasi dengan NaCl jenuh (Willis, 1921)
Prinsip pemeriksaan dengan metode flotasi adalah dengan adanya
perbedaan berat jenis antara telur cacing yang lebih kecil dibanding
NaCl jenuh sehingga telur dapat mengapung (Fuad, 2012).
3. Metode Teknik Kato (Kato dan Miura, 1954)
http://repository.unimus.ac.id

12
Prinsip pemeriksaan teknik Kato adalah feses direndam dalam
larutan gliserin hijau, dikeringkan dengan kertas saring dan didiamkan
selama 20-30 menit pada inkubator dengan suhu 400C untuk
mendapatkan telur cacing dan larva (Fuad,2012).
4. Metode Teknik Modifikasi Kato Katz (Katz et al., 1972)
Prinsip pemeriksaan dengan teknik modifikasi Kato Katz adalah
feses ditutup dan diratakan di bawah cellophane tape yang direndam
dalam larutan malachite green (Depkes RI, 2006).
2.4. Pewarna Giemsa
Giemsa yang sering disebut juga sebagai pewarna Roamnowski adalah larutan
pewarna yang umumnya digunakan untuk pewarnaan pada apusan darah tepi untuk
mempelajari morfologi darah dan untuk mempelajari parasit-parasit yang
menginfeksi darah (Gandasoebrata, 2007).
Giemsa adalah larutan yang mengandung campuran dari eosin y
(Tetrabromoflurescin) yang akan memberi warna merah, methylen blue yang
berwarna biru dan metilen azur B (Trimetiltionin) yang akan memberi warna ungu.
Dalam pewarnaan giemsa, eosin akan memberi warna pada eritrosit. Perpaduan
antara eosin dan metilen azur akan memberi warna merah pada inti sel parasit dan
methylen blue akan memberi warna biru pada sitoplasma sel (Jurnal Riset Kesehatan,
2017).
http://repository.unimus.ac.id

13
Azur merupakan hasil dari oksidasi methylen blue. Berdasarkan dari 4 sifat
pewarna yang menyatakan afinitas (ikatan kimia) struktur sel oleh masing-masing zat
warna dari campuran, yaitu :
1. Afinitas untuk methylen blue.
2. Afinitas untuk Azur B dikenal dengan azurefilik, menghasilkan warna ungu.
3. Afinitas untuk eosin dikenal asdofilik (eosin bersifat asam) atau eosinifilia yang
memberi warna merah muda kekuningan.
4. Afinitas untuk komplek zat warna yang terdapat dalam campuran, secara tidak
tepat dianggap netral, dikenal nuetrofilia yang menghasilkan warna salmon-pink.
(Safar, 2009)
Berdasarkan pedoman pemakaian giemsa yang telah ditetapkan oleh Depkes RI
tahun 1993, Giemsa stock hanya boleh diencerkan menggunakan akuades, air buffer
atau air pada saat akan digunakan dengan tujuan untuk memperoleh efek pewarnaan
yang optimal. Pengambilan stok Giemsa harus menggunakan pipet khusus yang tidak
tercemar dan harus ditempatkan dalam wadah bertutup rapat karena kandungan
methanol dalam Giemsa dapat menarik air dari udara sehingga Giemsa stok akan
cepat rusak.
Aturan untuk tolak ukur pemakaian pewarna Giemsa sebagai pewarna individu
pada Giemsa stok 1 tetes ditambah pengencer 9 tetes (Giemsa 10%) atau Giemsa stok
1 tetes ditambah pengencer 19 tetes (Giemsa 5%). Dalam pengenceran Giemsa stok
air pengencer yang digunakan mempunyai pH 6,8 – 7,2 (paling ideal pH 7,2)
(Gandasoebrata, 2007).
http://repository.unimus.ac.id

14
2.5. Faktor Yang Dapat Mempengaruhi Pemeriksaan Sediaan Telur A.
lumbricaides
2.5.1. Tinja
Sampel tinja yang digunakan untuk pemeriksaan sebaiknya diperiksa
dalam keadaan segar, karena apabila terlalu lama didiamkan maka unsur-
unsur dalam tinja akan rusak. Pengiriman tinja dilakukan dengan
menggunakan wadah yang terbuat dari bahan yang tidak mudah tembus
seperti kaca atau plastik Apabila akan memeriksa tinja perlu dilakukan
pemeriksaan makroskopis untuk memilih bagian dari tinja yang memberikan
kemungkinan besar dapat ditemukannya kelainan, misalnya bercampur darah
atau lendir (Gandasoebrata, 2007).
2.5.2. Kualitas Giemsa
Kualitas Giemsa stok yang akan digunakan harus memenuhi standar
mutu antara lain tidak tercemar air dan masih aktif. Kualitas air pengencer
Giemsa harus jernih, tidak berbau, dan memiliki derajat keasaman (pH) yang
ideal berkisar 6,8 - ,7,2. Perubahan pH akan sangat berpengaruh terhadap
hasil pewarnaan.
Untuk memastikan mutu Giemsa dapat dilakukan tes menggunakan
kertas saring, dengan meneteskan 1 – 2 tetes Giemsa pada kertas saring yang
telas diletakkan di atas cawan petri. Jika Giemsa telar meresap dan melebar
diteteskan 3 – 5 tetes metil alkohol absolute tepat ditengah bulatan Giemsa
http://repository.unimus.ac.id

15
dengan satu persatu dengan jarak waktu tertentu sampai garis tengah Giemsa
menjadi 5 – 7 cm atau terbentuk bulatan biru (methylen blue) di tengah,
lingkaran cincin ungu (Azur B) di bagian luar dan lingkaran merah (eosin)
tipis di bagian pinggir. Jika warna ungu dan merak tidak tampak
menandakan Giemsa sudah rusak (Depkes, 1993).
2.5.3. Pembuatan Preparat
Pembuatan preparat dilakukan dengan meneteskan larutan atau sampel
ke atas kaca objek. Dalam pembuatan preparat ini yang harus diperhatikan
adalah pada saat penutupan sediaan dengan kaca slide (kaca penutup)
usahakan tidak boleh terdapat gelembung udara. Sediaan harus tipis, agar
unsur-unsur jelas terlihat dan dapat diidentifikasi (Gandasoebrata, 2007).
Dalam pembuatan sediaan apusan tinja, preparat sediaan dapat
dikatakan baik jika memenuhi beberapa kriteria berikut yaitu objek glass
harus bersih dan bebas kuman dan lemak, sediaan tidak terlalu tebal atau
terlalu tipis, sediaan tidak meluber keluar dari kaca objek, sediaan tidak
boleh kering, dan pada sediaan tidak terdapat gelembung udara yang dapat
mengganggu pengamatan.
http://repository.unimus.ac.id

16
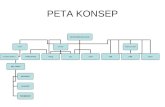
2.6. Kerangka Teori
2.7. Kerangka Konsep
2.8. Hipotesis
Terdapat perbedaan kualitas dan morfologi sediaan telur A. Lumbricoides pada
variasi konsentrasi Giemsa 3%, 4%, 5%, 6%, dan 7%.
Kualitas telur A.
lumbricaides
Kualitas
Tinja
Teknik
Pemeriksaan
Kualitas Buffer
Kualitas
Giemsa
Metode
Pemeriksaan
Sumber Daya
Manusia
Variasi konsentrasi
Giemsa 3%, 4%, 5%,
Kualitas sediaan telur A.
Lumbricaides
http://repository.unimus.ac.id