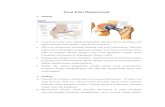
renal replacement therapy
-
Upload
herlina-rudianto -
Category
Documents
-
view
39 -
download
9
description
Transcript of renal replacement therapy
Referat nefrologi
Persiapan dan pelaksanaan renal replacement therapy pada pasien PGK
Oleh: Dr. HERLINA
Pembimbing :Dr. AUMAS PABUTI, SpA.MARS
FAKULTAS KEDOKTERAN UNIVERSITAS ANDALASRSUP Dr. M.DJAMIL PADANG2015BAB IPENYAKIT GINJAL KRONIK
Penyakit ginjal kronik (PGK) merupakan masalah kesehatan global dengan insidensi dan prevalensi yang terus meningkat, prognosis yang buruk, serta biaya perawatan yang mahal. Konsekuensi utama PGK tidak hanya progresifitas menjadi gagal ginjal terminal (end stage renal disease), tetapi juga risiko kardiovaskular yang meningkat. Kerusakan ginjal dapat berupa kelainan struktur atau fungsi ginjal dengan satu atau lebih kelainan komposisi urin atau darah, adanya kelainan dalam pemeriksaan pencitraan atau dari biopsi ginjal.1,2,3,4,5,6,7Seorang anak dikatakan menderita PGK jika terdapat salah satu dari kriteria di bawah ini:1,2,3,41. Kerusakan ginjal >3 bulan yang didefinisikan sebagai abnormalitas struktur atau fungsi ginjal dengan atau tanpa penurunan LFG yang bermanifestasi sebagai satu atau lebih gejala:a. Abnormalitas komposisi urine atau darahb. Abnormalitas pemeriksaan pencitraanc. Abnormalitas biopsi ginjal 2. LFG 3 bulan dengan atau tanpa gejala kerusakan ginjal lain yang telah disebutkan.PGK diklasifikasikan menjadi 5 derajat dengan tujuan untuk pencegahan, identifikasi awal kerusakan ginjal, dan penatalaksanaan seperti yang tercantum pada tabel 1 berikut.7Tabel 1. Klasifikasi PGK1,2,3,7
Penyebab PGK pada anak usia 5 tahun penyebab tersering PGK adalah penyakit yang diturunkan seperti penyakit ginjal polikistik atau penyakit didapat (glomerulonefritis).1,3Manifestasi klinis PGK dapat berupa peningkatan tekanan darah akibat kelebihan cairan dan produksi hormon vasoaktif (hipertensi, edema paru, dan gagal jantung kongestif), gejala uremia (letargis, perikarditis hingga ensefalopati), gangguan pertumbuhan, akumulasi kalium dengan gejala malaise hingga keadaan fatal yaitu aritmia, gejala anemia akibat sintesis eritropoeitin yang menurun, hiperfosfatemia dan hipokalsemia akibat defisiensi vitamin D3, serta asidosis metabolik akibat penumpukan sulfat, fosfat, dan asam urat.8Penderita PGK dapat mengalami eksaserbasi akut dengan perburukan fungsi ginjal yang mendadak sehingga terjadi gangguan-gangguan dalam mempertahankan homeostasis cairan tubuh, keseimbangan asam basa, elektrolit, dan eliminasi zat-zat sisa. Manifestasi eksaserbasi akut berupa gejala-gejala kelebihan cairan (gagal jantung dan/ edema paru), aritmia karena hiperkalemia atau gejala uremia, keadaan tersebut merupakan kedaruratan medis yang harus ditangani segera dengan dialisis akut. Manifestasi seperti ini susah dibedakan dengan gejala-gejala PGK derajat 5 ( gagal ginjal terminal ), perbedaannya terlihat setelah penanganan keadaan akut dengan dialisis akut. Bila setelah dialisis akut dihentikan gejala-gejala muncul kembali berarti penderita mengalami gagal ginjal terminal dan harus dilanjutkan dengan dialisis kronik sambil menunggu kemungkinan untuk dilakukan transplantasi ginjal.8Tatalaksana utama pada penderita PGK dengan eksaserbasi akut adalah dengan dialisis akut, sedangkan pada gagal ginjal terminal atau PGK derajat 5 sementara dilakukan dialisis kronik sebelum transplantasi ginjal. Tatalaksana PGK lainnya adalah dengan terapi suportif dan substitusi, meliputi tatalaksana untuk hipertensi, anemia, mengatur kadar kalsium, menjaga keseimbangan asam basa dan nutrisi.8End stage renal disease ( ESRD ) adalah keadaan klinis kerusakan ginjal yang progresif dan ireversibel yang terjadi apabila sekitar 90% dari massa nefron telah hancur, atau hanya sekitar 200.000 nefron yang masih utuh. Ditandai dengan nilai LFG < 15 ml/mn/1,73m2 dan clearance creatinin 5-10 ml/menit bahkan lebih rendah, peningkatan kreatinin serum dan kadar BUN di atas normal, urin menjadi isoosmotis dengan plasma pada berat jenis yang tetap sebesar 1,010 dan oliguri, serta kegagalan fungsi pengaturan metabolik dan cairan atau elektrolit dalam tubuh yang menyebabkan terjadinya uremia atau azotemia, sehingga apabila tidak dilakukan terapi pengganti seperti dialisis atau transplantasi ginjal dapat menyebabkan kematian.9 Insiden ESRD di USA sekitar 14 per juta populasi usia 0-19 tahun. Penyebab ESRD tersering adalah anomali perkembangan ginjal, uropati obstruktif, GSFS, nefropati refluks dan penyakit ginjal polikistik.10
Tabel 2. Penyebab tersering end stage renal disease pada populasi anak10
BAB IIRENAL REPLACEMENT THERAPY
Renal replacement therapy (RRT) adalah terapi penggantian fungsi ginjal, baik berupa transplantasi ginjal, hemodialisis atau peritoneal dialisis. Semua bentuk renal replacement therapy (RRT) berdasarkan pada prinsip transport air dan zat terlarut melewati membran semipermeabel dan kemudian membuang produk sisa. Setiap penderita PGK sebaiknya direncanakan untuk menjalani transplantasi, dan sebelum sampai pada pelaksanaan program transplantasi, penderita dipersiapkan untuk menjalani dialisis sebagai pengganti fungsi ginjal.8 Terdapat 2 kriteria yang mempengaruhi klinisi dalam pemilihan metode dialisis : indikasi dialisis dan status klinis pasien keseluruhan. Faktor lain yang memiliki peranan dalam pemilihan metode adalah usia pasien, faktor medis (peritoneum intak atau tidak), lokasi geografis pusat medis, dan adanya pengasuh yang tepat.11Indikasi absolut dialisis kronik pada anak dengan gagal ginjal:111. Hipertensi tidak terkendali, hipertensi ensefalopati2. Gagal jantung kongestif : kardiomiopati3. Perikarditis, tamponade4. Neuropati perifer : parestesi, disfungsi motorik5. Osteodistrofi ginjal : kalsifikasi tersebar, deformitas tulang6. Depresi sumsum tulang : anemia berat, leukopenia, trombositopenia.
Manajemen konservatif PGK sebelum RRTKetika anak didiagnosis penyakit ginjal kronik, harus dilakukan pemeriksaan dan tindakan untuk memperlambat progresifitas perburukan ginjal, dan mencegah serta mengobati komplikasi sebelum end stage renal disease (ESRD) atau PGK stadium V yang sudah memerlukan renal replacement therapy (RRT) berupa dialisis atau transplantasi ginjal. Persiapan yang cukup untuk renal replacement therapy (RRT) biasanya membutuhkan waktu 6 bulan sampai 1 tahun.12Untuk tata laksana yang lebih baik dalam memperlambat progresifitas gagal ginjal dan mencegah komplikasi, dibutuhkan pendekatan multi disiplin. Akan lebih baik jika pasien dirujuk ke pusat spesialisasi untuk tata laksana jika LFG sudah dibawah 40-50 ml/mnt/1,73 m2, ketika komplikasi mulai muncul dan harus cepat dilakukan tindakan untuk mengurangi tingkat progresifitas gagal ginjal. Selanjutnya dibutuhkan kerjasama yang baik antara tim kesehatan dengan pasien dan keluarga dalam perawatan jangka lama dialisis atau transplantasi ginjal. Sudah terbukti bahwa pasien yang ditatalaksana di pusat spesialisasi saat tahap awal memiliki luaran yang lebih baik.12Strategi khusus untuk memperlambat progresifitas :12 Membatasi intake protein sesuai intake harian yang direkomendasikan. Kontrol hipertensi Mengurangi proteinuria :ACEI (ramipril atau lisinopril) atau ARB (losartin) Mengurangi hiperlipidemia : diet restriksi lemak lebih dahulu sebelum mempertimbangkan penggunaan obat penurun lemak. Kontrol hiperkalsemia : mengurangi atau menghentikan suplemen kalsium dan vitamin D aktif Menjaga hidrasi dan menghindari hipotensi Menghindari bahan nefrotoksik, seperti aminoglikosida dan herbal yang tidak diketahui Menghentikan rokok Mengurangi berat badan pada anak obesitasPencegahan dan tata laksana komplikasi12 Malnutrisi dan diet Intake kalori yang cukup dengan mengacu kepada intake harian yang direkomendasikan (sesuai usia untuk mencukupi kebutuhan untuk pertumbuhan) Kandungan kalori pada makanan bisa diperkaya dengan suplementasi dalam bentuk polimer glukosa atau emulsi lemak, atau penggunaan makanan siap saji tinggi kalori seperti Nepro dan Isocal Makanan enteral untuk meningkatkan intake pada anak dengan pertumbuhan yang buruk yang tidak berhasil dengan makanan suplementasi. Intake protein yang cukup untuk pertumbuhan tetapi tidak berlebihan pada uremia, asidosis metabolik atau hiperkalemia ( menurut intake harian yang direkomendasikan untuk protein pada fungsi ginjal yang berbeda) Penilaian nutrisi berkala Nasehat untuk menghindari makanan tertentu, seperti belimbing (bisa mengendapkan hiperoksaluria sehingga memperburuk gagal ginjal) Menjaga hidrasi, keseimbangan asam basa dan elektrolit Hiperparatiroid Dimonitor dengan kadar kalsium, fosfat, alkali fosfatase, paratiroid dan rontgen lutut atau pergelangan tangan untuk melihat osteodistrofi Tata laksana dengan mengontrol hiperfosfatemia dan terapi vitamin D aktif Osteodistrofi ginjal Merupakan akibat dari hiperparatiroid dan defisiensi vitamin D aktif Anemia Terutama berhubungan dengan kekurangan sintesis eritropoeitin di ginjal Diterapi dengan human eritropoeitin. Gagal tumbuh Penyebabnya multipel, termasuk malnutrisi, dehidrasi, hiponatremia, asidosis metabolic, uremia, anemia, osteodistrofi ginjal, dan resistensi growth hormone (GH) Tata laksana adalah dengan koreksi faktor-faktor diatas dan menggunakan growth hormone Kardiomiopati Kontrol ketat hipertensi bisa mencegah atau memperlambat onset kardiomiopati Hindari hiperkalsemia dan hiperfosfatemia untuk mencegah kalsifikasi miokardium. Pemeriksaan ekokardiografi setiap tahun untuk monitoring. Ensefalopati dan neuropatiHal ini bisa dihindari dengan pelaksanaan renal replacement therapy secara optimal.
Persiapan renal replacement therapy12 Edukasi keluargaEnam sampai 12 bulan sering dibutuhkan untuk pasien dan keluarga sehingga menjadi persiapan yang lebih baik untuk dialisis atau transplantasi ginjal. Harus diberikan penjelasan tentang berbagai metode RRT kepada keluarga. Akan sangat menolong dengan memperkenalkan pasien dan keluarga kepada kelompok pasien untuk pemahaman yang lebih baik terhadap pilihan mereka. Evaluasi medisa. Untuk menilai kesesuaian dengan berbagai metode yang berbeda, termasuk ketersediaan akses vaskular dan peritoneal untuk dialisis dan sistem urologi untuk transplantasi.b. Evaluasi donor hidup potensial, termasuk kondisi medis dan kondisi psikologis. Skrining infeksia. Skrining infeksi termasuk HIV, HCV, HBV, EBV, CMV, campak, varicelab. Imunisasi : Vaksin mati atau komponen aman, vaksin virus hidup juga aman dan efektif pada anak dengan PGK atau dalam dialisis, tetapi secara umum tidak direkomendasikan setelah transplantasi. Sebaiknya mengikuti program vaksinasi primer sesuai daerah masing-masing Varicela, influenza, hepatitis B, haemophilus influenza dan streptococcus pneumonia sebaiknya juga termasuk jika tidak tersedia pada program vaksinasi primer. Evaluasi psikososial Dievaluasi oleh pekerja sosial dan psikolog Untuk mengevaluasi keluarga untuk tindakan dialisis di rumah termsuk kebutuhan dukungan sosial dan finansial Donor yang memungkinkan membutuhkan pemeriksaan psikologis Penyesuaian karir/pekerjaan kadang dibutuhkan bagi orang tua anak dengan dialisis di rumah. Untuk menilai apakah hemodialisis mempengaruhi sekolah Bantuan keuangan mungkin dibutuhkan keluarga.
Inisiasi terapi dialisis13 Dialisis sebaiknya dimulai lebih awal pada anak dengan ESRD untuk mencegah malnutrisi, gangguan pertumbuhan dan gejala uremia. Direkomendasikan oleh National Kidney Foundation Dialysis Outcome Quality Initiative (NKF-DOQI) bahwa dialisis sebaiknya dimulai ketika creatinine clearance residual turun ke nilai antara 9 dan 14 ml/mnt/1,73m2 atau urea Kt/V ginjal dibawah 2.0. Dari metode dialisis, peritoneal dialysis (PD) adalah RRT inisial yang lebih disukai pada anak (terutama sekali usia lebih muda dan berat lebih kecil). Untuk alasan teknis, PD dindikasikan pada hampir semua anak usia kurang dari 2 tahun dan 80% anak kurang dari 5 tahun.11 Keuntungan dari PD adalah lebih baik dalam memelihara fungsi ginjal residual dibanding hemodialisis (HD). PD maintenance bisa dilakukan di rumah, menghindari kebutuhan terhadap antikoagulan, dan secara hemodinamik lebih kurang merangsang stres. PD juga bisa dilakukan pada anak yang lebih muda dan restriksi diet lebih tidak terlalu ketat, sehingga nutrisi lebih baik.11 keuntungan lain dari PD adalah secara teknik lebih sederhana dan lebih mudah dikerjakan, dan merupakan pilihan yang paling tepat untuk penderita dengan keadaan hemodinamik yang tidak stabil, serta lebih murah dari segi biaya.10,14,15 Tabel 3. Perbandingan dialisis peritoneal dan hemodialisis5
PERITONEAL DIALISIS
Dialisis adalah proses pengeluaran sisa-sisa metabolisme dan kelebihan cairan dari darah melalui membran semipermeabel. Peritoneum merupakan selaput yang berfungsi sebagai membran semipermeabel yang dapat berperan dalam proses dialisis, hal ini didasarkan pertimbangan bahwa luas permukaan peritoneum kira-kira sama dengan luas permukaan seluruh kapiler glomerulus.16Metode peritoneal dialisis :17 Continuous Ambulatory Peritoneal Dyalisis (CAPD) Berbagai modifikasi Automated Peritoneal Dyalisis (APD), yaitu : Nocturnal Intermittent Peritoneal Dyalisis (NIPD)Terdiri dari pertukaran cairan (exchange) yang cepat pada malam hari dengan abdomen yang kering selama siang hari. Sesuai untuk pasien dengan fungsi ginjal residual yang baik atau pasien dengan masalah mekanik (seperti kebocoran dan hernia) Continuous Cycling Peritoneal Dyalisis (CCPD)Terdiri dari pertukaran cairan yang cepat saat malam dengan dwelling selama siang hari. Tidal PDMerupakan bentuk APD dimana hanya 50-75% dari total volume dialisat yang bertukar (exchange) pada tiap siklus. Direkomendasikan untuk pasien dengan hiperpermeabilitas peritoneal dengan gangguan ultrafiltrasi. Continuous Optimized PD (COPD)Terdiri dari pertukaran cairan yang cepat saat malam, dwelling dalam jangka lama siang hari, dan suatu pertukaran extra saat tengah hari atau satu pertukaran cairan setelah sekolah sebelum siklus malam hari. Ini dilakukan ketika dibutuhkan clearance maksimal khususnya saat sudah terjadi anuri.
Tabel 4. Perbandingan metode PD8
Prinsip transpor zat terlarut (solut) menjadi dasar semua modalitas terapi pengganti ginjal (renal replacement therapy).1. Difusi adalah pergerakan zat-zat terlarut dari larutan berkonsentrasi tinggi ke larutan berkonsentrasi rendah melalui membran semipermeabel. Mekanisme difusi dipengaruhi oleh perbedaan konsentrasi dalam kedua larutan tersebut, berat molekul zat terlarut dan resistensi membran semipermeabel.18Difusi merupakan mekanisme utama untuk mengeluarkan sisa-sisa metabolisme pada dialisis peritoneal. Pada proses difusi terjadi pertukaran solut dari dua larutan yang dipisahkan oleh membran semipermeabel, yaitu pertukaran solut yang berada dalam darah kapiler pada peritoneum dan cairan dialisat dalam rongga peritoneum. Secara mikroskopis anatomis membran peritoneum merupakan lapisan heterogen yang berupa jaringan ikat fibrosa elastik yang diliputi oleh sel mesotel, sehingga dalam proses perpindahan air dan solut dari darah ke cairan dialisat dalam rongga peritoneum harus melewati lapisan tahanan, yaitu lapisan dari selaput darah, endotel pembuluh darah, membrana basalis, jaringan interstitial, mesotel dan selaput dialisat.19
Gambar 1. Proses difusi
2. Ultrafiltrasi adalah proses perpindahan air dan zat-zat terlarut yang permeabel melalui membran semipermeabel, karena adanya perbedaan antara tekanan hidrostatik dan tekanan osmotik. Ultrafiltrasi hidrostatik. Pergerakan air terjadi dari kompartemen bertekanan hidrostatik tinggi ke kompartemen yang bertekanan hidrosatik rendah. Ultrafiltrasi hidrostatik tergantung pada tekanan transmembran (transmembrane pressure/TMP) dan koefisien ultrafiltrasi (KUF). Ultrafiltasi osmotik. Perpindahan air terjadi dari kompartemen yang bertekanan osmotik rendah ke kompartemen yang bertekanan osmotik tinggi, sampai tercapai keadaan tekanan osmotik di dalam kedua kompartemen tersebut seimbang.
Pada dialisis peritoneal yang paling berperan adalah ultrafiltrasi akibat perbedaan tekanan osmotik. Proses ini terjadi bila konsentrasi larutan di salah satu sisi membran lebih rendah, artinya molekul air lebih banyak dari molekul solut dan sisi lain membran mempunyai konsentrasi larutan lebih tinggi, artinya molekul air lebih sedikit dari molekul solut, maka air akan bergerak dari konsentrasi larutan rendah ke konsentrasi larutan tinggi. Dalam pergerakannya molekul air akan menarik solut kecil melalui membran sehingga akhirnya tercapai keseimbangan.18,19
Gambar 2. Proses ultra filtrasi
Dalam dialisis peritoneal, proses ini terjadi akibat penambahan glukosa ke dalam cairan dialisat berupa dekstrosa 1,5%, atau 2,5%, atau 4,25%. Tekanan osmotik yang disebabkan glukosa ini menyebabkan penarikan air dari darah ke dialisat. Dalam proses ini glukosa dalam dialisat diabsorpsi ke dalam darah. Dalam keadaan kelebihan cairan dipakai cairan dialisat dengan kadar glukosa 4,25% untuk menarik kelebihan cairan tersebut. Derajat penjernihan/klirens suatu zat pada dialisis peritoneal dapat ditentukan dengan rumus :20C = D__x___V P x tC : penjernihan /klirens suatu zat (ml/menit).D : konsentrasi suatu zat dari cairan dialisat yang telah dikeluarkan (mg/dl).V : volume dialisat (ml).P : konsentrasi zat dalam plasma (mg/dl).t : interval waktu.Dari variabel diatas, V dan t dapat diatur untuk menentukan C. dari hasil penelitian didapatkan bahwa bila lama cairan dialisat dalam rongga peritoneum (indwelling) 60 menit, besar difusi urea mencapai 70% dan mencapai 100% dalam 120 menit.
3. Konveksi adalah gerakan molekul-molekul lainnya akibat perbedaan tekanan hidrostatik, yang terlarut dalam air, melalui membran semipermeabel. Akibat adanya tekanan hidrostatik, molekul-molekul kecil dan besar cenderung berpindah hingga tercapai keadaan keseimbangan, sesuai dengan ukuran yang dapat dilalui oleh membran semipermeabel. Molekul besar tidak dapat berpindah.18,19
Gambar 3. Proses konveksi
Pergerakan transperitoneal dari airTenaga yang menggerakkan air, melewati membran peritoneum selama dialisis adalah glukosa yang menimbulkan derajat osmotik. Derajat osmotik glukosa dari 1 mOsm glukosa menghasilkan derajat hidrostatik sekitar 19 mmHg. Dianggap konsentrasi glukosa plasma adalah 100 mg/dl, maka derajat hidrostatik maksimal untuk ultrafiltrasi yang ditimbulkan oleh glukosa 1,5 % atau 4,25% adalah 1481 mmHg (78 mOsm) dan 4391 mmHg (231mOsm).Untuk mengukur kinetik dari pergerakan air melewati membran peritoneal dapat dilihat dengan berbagai cara, antara lain dengan cara mengukur volume dialisat setelah beberapa waktu cairan dialisat berada dalam rongga peritoneum. Pada pengukuran cairan dialisat setelah berlangsung 30 menit dari 6 anak yang ditambahkan glukosa 1,5%, 4,24% dan 2,5% didapatkan volume tambahan masing-masing 6%, 16,5% dan 13%. Hasil yang hampir sama diperoleh pada penderita dewasa.21
Gambar 4. Perubahan Volume Intraperitoneal Setelah Pemberian Cairan Dialisat Dengan Berbagai Konsentrasi Glukosa.20Ada beberapa faktor yang mempengaruhi transport dari solute air pada peritoneum, antara lain : jumlah volume dialisat; lama dari inflow, dwelling dan outflow; kadar glukosa dari dialisat; temperature dari dialisat, makin tinggi temperature dari dialisat akan meningkatkan klirens peritoneal sampai 30-35%. Proses dialisis berbanding lurus dengan keasaman. Pada pH asam akan mempengaruhi mikrosirkulasi untuk mengadakan dilatasi. Peranan asetat pada cairan dialisat mempengaruhi arteriole.19,21
Prosedur dialisis peritonealCairan dialisat yang digunakan yaitu cairan standar yang mengandung glukosa 1,5%, komposisi elektrolit yang hampir sama dengan cairan ekstraseluler tubuh, tetapi tidak mengandung kalium. Cairan yang tersedia Perisolution dari Otsuka dengan konsentrasi glukosa 1,5%, Dianeal dari Baxter dengan konsentrasi glukosa 1,5%, 2,5% dan 4,25%.22
Kateter yang digunakan:22 Rigid plastic catheter/polythelene catheter dengan stilet. Jenis ini yang tersedia di Indonesia yaitu buatan Otsuka dan Amecath (Ameco Medical Industries, Egypt). Jenis kateter ini digunakan untuk dialisa peritoneal 48-72 jam. Tenckhoff catheter dan modifikasinya. Terbuat dari silicon yang bersifat inert. Dapat dipasang untuk waktu yang lama. Untuk dialisa peritoneal akut yang diperkirakan lama dipakai jenis kateter ini.
Gambar 5. Jenis Kateter Dialisis Peritoneal
Pelaksanaan dialisis peritoneal:22 Volume cairan dialisa pada awalnya diberikan 15-20 ml/kgBB, kemudian secara bertahap dinaikkan menjadi 40-50 ml/kgBB pada bayi dan anak kecil atau menjadi 30-40 ml/kgBB pada anak yang lebih besar. Heparin 500-1000 unit/L ditambahkan ke dalam cairan dialisat dalam 3 siklus pertama dan diteruskan selama cairan dialisat berwarna merah Cairan dialisa dimasukkan ke dalam rongga peritoneum (inflow) dalam 5-10 menit, lalu dibiarkan selama 30 menit (dwelling), kemudian dikeluarkan dalam 10-20 menit (outflow). KCl ditambahkan 3-4 mEq/L pada cairan dialisa bila kadar K plasma 24 jam), pemanjangan waktu iskemia hangat, dan hipotensi perioperatif. Usia donor yang ekstrim, seperti kurang dari 2 tahun dan lebih dari 50 tahun, juga dihubungkan dengan risiko yang lebih tinggi untuk tejadinya fungsi cangkokan terlambat. Diagnosis diferensial fungsi cangkokan terlambat termsuk thrombosis arteri atau vena ginjal, fokal segmental glomerulosklerosis rekuren, sindrom hemolitik uremik, dan obstruksi atau perembesan urin.Rejeksi akutRejeksi akut terjadi dalam 3 bulan transplantasi dan secara klasik ditandai oleh demam, oliguri, hipertensi, proteinuri dan melunaknya cangkokan. Dengan adanya peningkatan surveilan laboratorium, peningkatan kreatinin asimptomatik baru-baru ini menjadi modalitas primer untuk skrining rejeksi. Rejeksi akut ditatalaksana inisial dengan steroid intravena (metilprednisolon 10-15 mg/kgBB/hari selama 3 hari). Anti thymocyte globuline biasa digunakan pada resisten steroid atau rejeksi berat (1,5 mg/kg/hari selama 5-7 hari). Untuk rejeksi diperantarai antibody, IVIG, rituximab, dan plasmaferesis mungkin dibutuhkan.Thrombosis vaskulerGagal cangkok akibat thrombosis terlihat pada 1,9% donor hidup dan 3% donor mati. Faktor risiko resipien termasuk usia lebih muda dan hiperkoagulabilitas sebelumnya. USG duple atau Doppler berwarna bisa digunakan untuk mengevaluasi dan tata laksana thrombosis atau stenosis vaskular.Komplikasi urologiKomplikasi urologi termasuk obstruksi urin, perembesan urin, refluks vesico ureter, dan urolitiasis. Insiden bervariasi antara 3% dan 15%, dan berkorelasi dengan adanya uropati obstruktif atau disfungsi vesika sebelum transplantasi. Infeksi saluran kemih rekuren setelah transplantasi bisa menjadi indikator refluks vesiko ureter dan dikonfirmasi dengan voiding uretrosistogram. Komplikasi infeksiKomplikasi infeksi setelah transplantasi dihubungkan dengan tingkat morbiditas dan mortalitas yang signifikan. Selama bulan pertama setelah transplantasi, infeksi saluran kemih, infeksi luka, dan pneumonia sering terjadi. Antara 1 bulan dan 6 bulan setelah transplantasi, infeksi jamur dan virus termasuk CMV, Epstein-Barr, herpes simpleks dan varicella zoster bisa terjadi. Setelah periode kritis ini, prevalensi infeksi sama dengan populasi umum. Vaksinasi rutin ditunda sampai 6 bulan setelah transplantasi, kecuali untuk influenza, yang bisa diberikan setelah 1 bulan. Vaksin hidup dikontraindikasikan setelah transplantasi. Anggota keluarga sebaiknya diimunisasi dengan vaksin influenza setiap tahun.KeganasanSebanyak 2,4% resipien anak mengalami keganasan. Lebih dari 50% keganasan tersebut adalah PTLD (Post Transplantation Limphoprolypherative Disorder). Keganasan non limfoproliferatif termasuk karsinoma sel skuamosa, sarcoma kaposi, melanoma, dan tumor lain yang jarang. Virus Epstein Barr umumnya diidentifikasi sebagai agen penyebab.
Evaluasi dan monitoring setelah transplantasiPasien yang selesai menjalani transplantasi akan mendapat imunosupresan sehingga harus dilakukan monitoring terhadap efek samping obat dan risiko infeksi. Untuk pemantauan jangka panjang, komplikasi seperti rejeksi, hipertensi, risiko kardiovaskuler, rekurensi penyakit ginjal primer, keganasan dan gagal cangkokan harus diawasi dan ditatalaksana. Kemungkinan non compliance (tidak patuh) juga harus dipertimbangkan terutama pada remaja.28 Monitoring bulanan28 Urinalisis Tekanan darah CaPO4, asam urat Kolesterol, trigliserida, glukosa darah puasa Monitoring efek samping obat Periksa compliance obat Mencegah dan mengatasi infeksi Monitor pertumbuhan dan perkembangan Mengawasi timbulnya rejeksi, gagal ginjal progresif, rekurensi penyakit ginjal primer, keganasan dan komplikasi lainnya. Monitoring tahunan28 Sebagai tambahan terhadap pemeriksaan diatas LFG : creatinine clearance Pemeriksaan radiologis tulang pada penurunan LFG atau kadar kalsium/fosfat/paratiroid abnormal; bone age Monitoring tekanan darah 24 jam secara rawat jalan Ekokardiogram Evalluasi pertumbuhan dan nutrisi Perkembangan seksual pada anak usia pubertas Pertimbangkan protocol biopsi ginjal setelah beberapa bulan pertama post transplantasi, atau ketika dicurigai rejeksi kronik Skrining terhadap katarak (dengan terapi steroid jangka lama) Scan ginjal DTPA
Strategi untuk memperbaiki luaran setelah transplantasiTransplantasi ginjal adalah metode RRT yang terbaik untuk ESRD. Dengan rehabilitasi dan dukungan yang baik, pasien bisa hidup normal. Akan tetapi, saat ini graft survival jangka lama hanya sekitar 10-12 tahun. Berbagai pemeriksaan harus dilakukan untuk memperbaiki luaran dan menurunkan tingkat morbiditas.28 Mengoptimalkan ginjal yang ditransplantasikanTransplantasi ginjal harus dilakukan di pusat spesialisasi sehingga keahlian bisa dikembangkan. Pemilihan ginjal dengan matching yang lebih baik, mengurangi waktu penyimpanan cangkokan, dan tehnik operasi yang baik akan mengurangi komplikasi thrombosis vaskuler dan nekrosis tubular akut. Penggunaan imunosupresanDengan imunosupresan terbaru, efek samping bisa dikurangi, dan dosis bisa disesuaikan secara individual dan digunakan secara minimal jika memungkinkan. Steroid bisa dipertahankan minimal untuk memungkinkan pertumbuhan yang lebih baik. Compliance obat sebaiknya selalu diperhatikan dan identifikasi pasien risiko tinggi. Kerjasama yang baik dengan monitoring ketat bisa membantu. Deteksi dini rejeksiKecurigaan tinggi terhadap rejeksi akut dengan tata laksana yang tepat terhadap rejeksi berguna dalam mencegah nefropati allograft kronik Mencegah infeksiPenggunaan septrin, gancyclovir profilaks, vaksin influenza dan varicella digunakan untuk pencegahan infeksi. Dalam beberapa bulan pertama post transplantasi, pasien mengalami imunocompromise berat sehingga harus menghindari infeksi dengan cara menghindari tempat yang terlalu ramai menghindari orang sakit. Melindungi ginjal memperlambat progresifitas gagal ginjalTindakan yang dilakukan antara lain kontrol agresif hipertensi, mengurangi hiperlipidemia, mengurangi proteinuria, kontrol berat badan pada obesitas, dan menghentikan rokok. Melindungi tulangOsteopenia bisa diakibatkan oleh penggunaan kortikosteroid. Bifosfonat yang menginhibisi aktifitas osteoklast, efektif untuk terapi dan ditambahkan dengan calcitriol untuk suplementasi. Pada post transplantasi lama, hipofosfatemia bisa terjadi akibat hiperparatiroid, tetapi pada insufisiensi ginjal bisa terjadi hiperfosfatemia. Suplementasi kalsium, restriksi fosfat dan penggunaan calcitriol diberikan sewajarnya. Melindungi jantungMengontrol tekanan darah dan hiperlipidemia tidak hanya memperlambat gagal ginjal, tetapi juga mengurangi risiko kardiovaskuler. Selain itu juga mengurangi berat badan pada obesitas, aktifitas fisik normal, dan menghentikan rokok juga berpengaruh. Diet sehat dan gaya hidup sehat berkontribusi terhadap luaran jangka panjang pada pasien post transplantasi. RehabilitasiAnak dan remaja sebaiknya dibantu dalam rehabilitasi baik fisik, sosial dan pendidikan sehingga mereka hidup normal dan berkualitas.28
Daftar pustaka1. Hogg RJ, Furth S, Lemley KV, Portman R, Schwartz GJ, Coresh J, et al. National kidney foundations kidney disease outcomes quality initiative clinical practice guidelines for chronic kidney disease in children and adolescents: evaluation, classification, and stratification. Pediatrics. 2003;111:1461-21.2. Levey AS, Eckardt KU, Tsukamoto Y, Levin A, Coresh J, Rossert J, et al. Definition and classification of chronic kidney disease: a position statement from kidney disease: improving global outcomes (KDIGO). Kidney International. 2005:67;2089-100.3. Sekarwana N, Rachmadi D, Hilmanto D. Gagal ginjal kronik. Dalam: Alatas H, Tambunan T, Trihono PP, Pardede SO, penyunting. Buku ajar nefrologi anak. Edisi ke-2. Jakarta:Balai Penerbit FKUI. 2002. Hal 509-30. 4. Sekarwana N. Chronic kidney disease. Dalam : Noer MS, Soemyarso NA, Subandiyah K, Prasetyo RV, Alatas H, Tambunan T, dkk, penyunting. Kompendium nefrologi anak. Jakarta:UKK Nefrologi IDAI. 2011. Hal 215-22.5. Rachmadi D, Meilyana F. Hemodialisis pada anak dengan chronic kidney disease. Majalah Kedokteran Indonesia. 2009;59:555-60.6. Fischbach M, Edefonti A, Schroder C, Watson A. Hemodialysis in children: general practical guidelines. Pediatr Nephrol. 2005;20:1054-66.7. Sudjatmiko S, Oesman O. Hemodialisis. Dalam: Alatas H, Tambunan T, Trihono PP, Pardede SO, penyunting. Buku ajar nefrologi anak. Edisi ke-2. Jakarta:Balai Penerbit FKUI. 2002. Hal 615-27.8. Sethi SK, Bunchman T, Raina R, Kher V. Unique considerations in renal replacement therapy in children: core curriculum 2014. Am J Kidney Dis. 2014;63:329-45.9. Whyte DA, Fine RN. Chronic kidney disease in children. Peds in rev. 2008;29:335-41.10. Kanitkar CM. Chronic kidney disease in children: an Indian perspective. MJAFI. 2009;65:45-49.11. Rene G, Voorde VD, Warady BA. Management of chronic kidney disease. In : Avner ED, Harmon WE. Niaudet P, Yashikawa N, editors. Pediatric nephrology. 6th ed. Berlin: Springer; 2009. pp. 1661-90.12. Tse NKC, Chiu MC. Pre-renal replacement programme : conservative management of chronic kidney disease. In : Chiu MC, Yap HK. Editors. Practical paediatric nephrology. 1st ed. Hongkong: Medcom limited; 2005.pp. 247-52.13. Lai WM, Ha IS. Chronic peritoneal dyalisis : initiation of dyalisis, peritoneal equilibration test and adequacy assessment. In : Chiu MC, Yap HK. Editors. Practical paediatric nephrology. 1st ed. Hongkong: Medcom limited; 2005.pp. 262-6.14. Verrina E. Peritoneal dialysis. In : Avner ED, Harmon WE. Niaudet P, Yashikawa N, editors. Pediatric nephrology. 6th ed. Berlin: Springer; 2009. pp. 1785-816.15. Rees L. Hemodyalisis. In : Avner ED, Harmon WE. Niaudet P, Yashikawa N, editors. Pediatric nephrology. 6th ed. Berlin: Springer; 2009. pp. 1817-34.16. Harmon WE. Pediatric kidney transplantation. In : Avner ED, Harmon WE. Niaudet P, Yashikawa N, editors. Pediatric nephrology. 6th ed. Berlin: Springer; 2009. pp. 1867-1901. 17. Ha IS, Lai WM. Continuous ambulatory peritoneal dyalisis (CAPD) and automated peritoneal dyalisis (APD). In : Chiu MC, Yap HK. Editors. Practical paediatric nephrology. 1st ed. Hongkong: Medcom limited; 2005.pp. 267-7218. Sudjatmiko S, Oesman O. Hemodialisis. Dalam: Alatas H, Tambunan T, Trihono PP, Pardede SO, penyunting. Buku ajar nefrologi anak. Edisi ke-2. Jakarta:Balai Penerbit FKUI. 2002. Hal 615-27.19. Fischbach M, Edefonti A, Schroder C, Watson A. Hemodialysis in children: general practical guidelines. Pediatr Nephrol. 2005:20;1054-66.20. Wilson Lorraine M. Gagal Ginjal Kronik. Dalam : Sylvia Anderson Price, Lorraine McCarty Wilson. alih bahasa. Brahm U. Pendit...[et. al]. editor edisi bahasa Indonesia. Huriawati Hartanto...[et. al]. Patofisiologi : Konsep Klinis Proses Proses Penyakit. Edisi 6. Volume 2. Jakarta: EGC; 2005. Hal.914 933. 21. Chan JCM, Campbell RA. Peritoneal dialysis in children: A survey of its indications and applications. Clin Ped.1973;12:131-8.22. Odel HM, Ferris DO, Power MH. Peritoneal lavage as an effective means of extrarenal excretion. A clinical appraisal. Am J Med. 1950:63-75.23. Gruskin AB, Baluarte HJ, Dabbagh S. Hemodialysis and peritoneal dialysis. Dalam: Edelmann CM, Bernstein J, penyunting. Pediatric kidney disease. Boston: Little Brown and Co; 1992. h. 827-916.24. Nolph KD. Peritoneal anatomy and transport physiology. Dalam: Maher FJ, penyunting. Replacement of renal function by dialysis: A textbook of dialysis. Edisi ke-3. Boston: Kluwer Academic; 1989. h. 516-36.25. Fine RN. Peritoneal dialysis update. The J of Ped.1982;100:1-7.26. Sharma A, Ramanathan R, Posner M, Fisher RA. Pediatric kidney transplantation : a review. Transplant Research and Risk Management 2013:5;21-31.27. Dharnidharka VR, Fiorina P, Harmon WE. Kidney transplantation in children. N Engl J Med 2014;371:549-58.28. Chiu MC. Long term post-transplant management. In : Chiu MC, Yap HK. Editors. Practical paediatric nephrology. 1st ed. Hongkong: Medcom limited; 2005.pp. 326-34.
Sumber: Harrisons Manual of Medicine 17th Edition
Description of underlying healthproblemRenal failure and reasons fortransplantationEnd-stage renal failure (ESRF) occurs when thekidneys are no longer able to function, so that thepatient would die, and necessitates lifelong and/orlife-saving intervention in the form of dialysis orkidney transplantation.1Kidney transplantation is the treatment of choicefor ESRF because, if successful, quality andduration of life are better than those achieved withlong-term dialysis.2 In 1992, the cost oftransplantation was calculated to be 11,600 forthe transplant procedure, with each subsequentyear of a successful transplant costing 4000 perannum.3 In contrast, the cost per annum fordialysis was calculated to be 21,000 in theNational Institute for Health and ClinicalExcellence (NICE) appraisal of home versushospital haemodialysis (21,000 and 22,000 forhaemodialysis in a satellite unit and hospital,respectively).4 The increased cost oftransplantation in children relates primarily to theincreased length of hospital stay. Successful kidneytransplantation is reliant on the use ofimmunosuppressant agents.Renal transplant proceduresKidney grafts can come from living or dead(cadaveric heart beating or non-heart beating)donors. Where the donor is living, both the donorand recipient are in hospitals in the same city or,in some units, in the same hospital, so thetransplant can be performed quickly afterretrieval. With a cadaveric kidney, the donor maybe several hundred miles from the recipient. Inmost transplants, the recipient receives only onekidney, but in rare circumstances, particularly ifthe donor is less than ideal, two kidneys may betransplanted.5The quality of retrieved organs is particularlyimportant because a higher quality kidney graft isassociated with increased patient survival.6 Thiscreates additional responsibility when one centre isretrieving a kidney for another. In all cases, thetime between retrieval of kidneys andtransplantation needs to be kept to a minimum.Injury to the kidney can occur during the periodof removal of the organ from the donor (warmischaemia), during storage of the organ (coldischaemia)6 or at the time of implantation(anastamosis time). The minimisation of ischaemicinjury optimises the subsequent performance ofthe transplanted kidney. Prolonged cold ischaemiais associated with reduced 5-year graft survival.7Most kidneys are now retrieved from heart beatingdonors as part of a multi-organ donorprocurement.8 Some centres in Europe areattempting to increase the number of organsavailable by retrieving from non-heart beatingdonors.9 An increasing number of reports indicatethat kidneys from this source can functionadequately but there are no plans for these organsto be routinely used for paediatric recipients.There is an increase in postoperative dialysisrequirements because of delayed graft functionand the retrieval process is more complex than isthe case with heart beating donors.10Rejection of transplanted organsRejection, acute or chronic, remains a major causeof graft dysfunction and loss. Immunosuppressiveagents therefore play a key role in the preventionof rejection.9 Rejection may occur as acuteepisodes that are managed with intensive shorttermtreatment, usually with steroids, or rejectionmay be chronic causing gradual deterioration ofthe graft.9 Some 30% of UK paediatric patientsexperience biopsy-confirmed acute rejection by1 year after renal transplantation.8Acute rejection usually occurs in the first fewweeks after transplantation. The response is cellmediated with a vascular component and leads toinjury or destruction of the transplanted organ.11In the majority of patients who experience anacute rejection, it is reversed byimmunosuppressive drugs. Acute rejectionepisodes predispose a recipient to chronicrejection and possible graft loss. Late and severeepisodes of acute rejection are particularlythreatening to the graft.12Chronic rejection [chronic allograft nephropathy(CAN)] is a gradual process with variable onsetand rate of progression. It may develop as early asa few months after transplantation or emerge afterseveral years.11 The incidence of CAN varies andapproximately 30% of renal transplant recipientsexperience this process. CAN is diagnosed byrenal transplant biopsy in a patient withprogressively worsening graft function and isnotoriously difficult to treat. In the majority ofcases, it eventually leads to complete loss offunction of the transplanted organ, necessitating areturn to dialysis or re-transplantation.12 CAN is amulti-factorial process in which tissue damageoccurs as a result of low-grade, continuousrejection exacerbated by viral infections, episodesof acute rejection and the toxic effects of certainimmunosuppressive drugs. It is characterised by aslow decline in graft function, ultimately leadingto chronic renal failure.11One-year graft survival in adults has steadilyimproved over the last two decades and is nowover 90% in low-risk patients. Impressiveimprovements in short- and long-term graftsurvival have been reported in children.13,14 Adecade ago, it was believed that children hadpoorer graft survival rates than adults;however, 1-year graft survival rates rangingfrom 89 to 96% in children after 1 year or longerhave recently been reported in North America.15Longer term graft survival appears to vary byage; those aged 10 years and under appear tohave the best 5-year graft survival (7090%)whereas those aged 1117 years have the poorest(6075%). The reasons for this decline are notentirely known, but a contributing factor may bepoor compliance with their immunosuppressiveregimens.16EpidemiologyRegistries on paediatric kidney transplantation areheld by UK Transplant (UK Renal Registry)8 andthe North American Paediatric Renal TransplantCooperative Study (NAPRTCS) (a voluntaryregistry of US and Canadian paediatric renaltransplant centres, started in 1987) and theUnited Network of Organ Sharing (UNOS)(mandatory registry of all renal transplants in theUSA started in 1987).15 The UK Renal Registrydefines the paediatric population as both infantsand children under 15 years of age plusadolescents aged between 15 and 18 years. Theremainder of this report uses the term children(or paediatric population) to include allindividuals of 18 years or less.The prevalence of ESRF in the UK paediatricpopulation varies from 13.6 per million in theunder 4-year-old population to 53.4 per million inthe under 18-year-old population. The latterfigure will almost certainly be an underestimatedue to the direct referral of young people betweenages 15 and 18 years to adult services.15 The maleto female ratio for ESRF is 1.5:1 and the take-onrate by ethnicity is 7 (whites), 21 (Asian) and 4.5(blacks) per million of the population. However, agreater proportion of Asians remain on dialysisalthough a smaller proportion of Asians undergodialysis than whites.From the 2003 Renal Registry Report,8 the totalnumber of patients being cared for in the 13 UKpaediatric units in April 2002 was 804. Of these,793 patients were below the age of 20 years, ofwhom 760 were below 18 years of age and 622were below 16 years of age.In contrast to adult practice, most children withESRF will be suitable for transplantation. Manypaediatric renal transplant centres have aminimum body weight requirement of 10 kg orminimum age of 2124 months for childrenundergoing transplantation. However, guidelinesvary and some centres will undertaketransplantation at any age.8 At the end of 2002,612 paediatric patients were in receipt of atransplant in UK.8Current service provisionCategories of immunosuppressivetherapyThe overall aim of immunosuppression therapy isto prevent mortality by prolonging graft survivalwithout exposing the patient to the risks ofexcessive immunosuppression or toxicity related tothe use of immunosuppressant therapy.15Immunosuppression treatment following kidneytransplantation can be categorised into preventionof graft rejection (initial and maintenance therapy)and the treatment of graft rejection (rescuetherapy). Initial (or induction) therapy is a short course ofintensive immunosuppression beginning beforesurgery and continued for 23 months after thetransplant operation. Maintenance therapy is the treatment that isgiven long term, for the entire duration of thesurvival of the kidney graft. Acute rejection therapies are short coursesduring maintenance where therapies areadjusted temporarily or permanently followingan episode of acute rejection (this aspect ofrenal immunosuppression is outwith thescope of this report and will not be discussedfurther).Newer immunosuppressive agentsAgents traditionally used as maintenance therapyin renal transplantation have included acombination of ciclosporin (a calcineurininhibitor), azathioprine (a DNA proliferationinhibitor) and prednisolone (a steroid) tripletherapy. During the last decade, a number of newimmunosuppressive agents have been introducedinto renal transplantation, leading to a variety ofdifferent regimens. In general, these newer agentshave more potent immunosuppressive activitythan their older counterparts. While this mayreduce the incidence of rejection, the risk ofinfection [particularly cytomegalovirus andEpsteinBarr virus (EBV)], post-transplantlymphoproliferative disease and other malignancymay also be increased.Complications of long-term immunosuppressioninclude increased risk of developing infections,cancer [post-transplant lymphoproliferativedisease (PTLD)] and specific side-effects of eachmedication. Common infections caused bysuppression of the immune system include: viral[herpes, cytomegalovirus (CMV), EBV];opportunistic protozoal; fungal; and bacterial.17 Asimmunosuppression is at its highest level in thefirst 6-months after transplantation, this is also thepeak period for infections in these patients.Nevertheless, they are at higher risk for infectionsthan the general population throughout theirpost-transplant life.18The side-effects of immunosuppressives includehigh blood pressure, excessive hair growth, handtremors, mood swings, weight gain and diabetesmellitus. Some side-effects are temporary andresolve as the body adjusts to the medication andsome will continue for as long as the medication istaken.18The newer immunosuppressive agents underconsideration in this report are tacrolimus (acalcineurin inhibitor), mycophenolate mofetil(MMF) and mycophenolate sodium (MPS) (bothDNA proliferation inhibitors), sirolimus (aproliferation signal inhibitor) and basiliximab anddaclizumab (both interleukin-2 inhibitors). Thelicense indication and dosing details of thesenewer agents are summarised in Table 1. Insummary, at present, basiliximab, daclizumab,tacrolimus and MMF are licensed in the UK foruse in children whereas sirolimus and MPS arenot. In March 2005, the US Food and DrugAdministration agreed to the use of sirolimus inchildren.Current UK practiceNICE issued guidance (No. 85) for the use of theimmunosuppressive agents in adults inSeptember 2004. However, there are currently nonationally agreed clinical guidelines on thecombination of drugs given forimmunosuppressive therapy in children. As aresult, a variety of different immunosuppressiveregimens are currently used in UK paediatricrenal transplant units. Nevertheless, the currentmainstay of therapy in children in the UK is atriple immunosuppression consisting of acalcineurin inhibitor (ciclosporin or tacrolimus), aDNA proliferation inhibitor (usually azathioprine)and steroids. Only a very small proportion (