pengujian keausan dari komposit hidroksiapatit sebagai permukaan kontak pada temporomandibular joint...
-
Upload
ridzky-zul-asdi -
Category
Documents
-
view
29 -
download
0
description
Transcript of pengujian keausan dari komposit hidroksiapatit sebagai permukaan kontak pada temporomandibular joint...

2014
Pengujian Keausan dari Komposit Hidroksiapatit sebagai Permukaan Kontak pada Temporomandibular Joint Prosthesis
Evaluasi Akhir Semester Metode Penelitan dan Komunikasi Ilmiah
RIDZKY ZUL ASDI
2114 20 5002

PENDAHULUAN
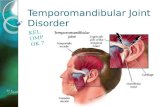
Temporomandibular Joint atau sering disingkat sebagai TMJ adalah persendian dari kondilus
mandibula dengan fossa gleinodalis dari tulang temporal. TMJ merupakan satu-satunya sendi yang
ada di kepala yang bertanggung jawab terhadap pergerakan membuka dan menutup rahang,
mengunyah serta berbicara yang letaknya dibawah depan telinga [1].
Temporomandibular joint disorder atau TMD adalah istilah medis dari kelainan pada sendi
rahang yang dapat berupa rasa sakit yang berkepanjangan atau akut terutama pada bagian otot
mengunyah serta dapat berupa peradangan. Sendi rahang sangat rawan pada kondisi abnormal
seperti ankylosis, artritis serta dislokasi sendi. Kelainan pada sendi rahang menyebabkan
terganggunya proses mengunyah serta terganggunya mekanisme buka tutup mulut yang dapat
menyebabkan rasa sakit yang luar biasa [1], [2].
Untuk beberapa kasus yang ringan, kelainan pada sendi rahang dapat diatasi dengan
perawatan tanpa proses operasi. Namun untuk penanganan kasus yang berat, proses operasi
pergantian total sendi rahang dengan sendi rahang buatan biasa dilakukan. Sendi buatan ini ditujukan
untuk menggantikan fungsi sendi yang rusak serta untuk mengurangi rasa sakit akibat kelainan atau
penyakit. Dalam ilmu medis, sendi buatan ini disebut sebagai prosthesis [2].
Prosthesis TMJ merupakan prosthesis yang digunakan untuk menggantikan fungsi sendi
rahang. Dalam perkembangannya, prosthesis TMJ dapat dibagi menjadi 3 kategori: prosthesis yang
hanya menggantikan bagian fossa, prosthesis dan plat rekonstruksi yang berfungsi untuk
menggantikan bagian condyle, serta prosthesis yang menggantikan bagian fossa dan condyle (pada
beberapa literatur disebut sebagai “total TMJ prosthesis”) [2], [3]. Sejauh yang penulis telaah, terdapat
cukup banyak variasi dari prosthesis TMJ dan masing-masing memiliki kelebihan dan kekurangan [2–
7].
Salah satu syarat desain prosthesis yang baik adalah partikel aus dari material tidak
menimbulkan reaksi alergi pada tubuh manusia. Hal ini dapat diatasi dengan penggunaan biomaterial
sebagai material utama. Biomaterial hidroksiapatit (HA) yang mempunya rumus kimia Ca10(PO4)6(OH)2
merupakan biomaterial yang sering dipakai untuk aplikasi medis. Hidroksiapatit memiliki komposisi
kimia yang sama dengan jaringan keras manusia seperti tulang dan gigi. Namun, sejauh yang penulis
teliti, belum banyak kajian tentang penggunaan hidroksiapatit sebagai material prosthesis dan
kekuatan mekanisnya [2–4], [6], [8], [9]. Kent pada tahun 1993 menggunakan hidroksiapatit sebagai
salah satu material penyusun prosthesisnya. Namun, prosthesis ini dianggap gagal karena partikel aus
dari material penyusun lainnya yaitu Proplast yang menimbulkan berbagai komplikasi pada pasien [2],
[9].
Berbagai literatur mengenai rancangan prosthesis TMJ telah penulis telaah, dan hanya ada
satu dari seluruh rancangan prosthesis TMJ tersebut yang menggunakan hidroksiapatit sebagai
material utamanya meskipun informasi yang dipaparkan sangat kurang serta tidak ada kajian tentang
kekuatan mekanisnya.
Berbagai kelebihan hidroksiapatit, membuatnya menjadi material yang cukup menjanjikan
untuk aplikasi prosthesis. Meskipun demikian, masih terdapat kekurangan seperti kekuatan mekanis
yang rendah. Dengan menggabungkan HA dengan poly(methyl methacrylate) (PMMA) diharapkan
dihasilkan material komposit yang memiliki biokompatibilitas dan kekuatan mekanis yang cukup untuk
aplikasi sebagai material prosthesis TMJ. Selain itu, harga PMMA relatif terjangkau. Pada penelitian
ini akan dilakukan eksperimen untuk mengetahui aspek tribologi dari material komposit HA+PMMA
dengan ultra-high molecular weight polyethylene (UHMWPE) sebagai permukaan kontak pada
prosthesis TMJ. Penelitian ini diharapkan dapat dijadikan sebagai referensi untuk perhitungan umur
dari material komposit HA+PMMA jika diterapkan sebagai permukaan kontak pada prosthesis TMJ.

KAJIAN PUSTAKA
Prosthesis TMJ
Penggunaan alat buatan untuk perawatan TMD secara resmi pertama kali dilakukan setelah
Perang Dunia II oleh Eggers dan Goodsell. Eggers dan Goodsell menempatkan sebuah tantalum foil
diantara persendian TMJ (antara fossa dan condyle) [2], [10]. Pada review literatur kali ini, penulis
ingin fokus pada total TMJ prosthesis, serta kekurangan dan permasalahan dari prosthesis yang sudah
ada sebagai landasan perancangan prosthesis yang lebih baik.
Total TMJ prosthesis pertama di dunia dirancang oleh Christensen pada tahun 1965, yang
dikenal dengan nama “The Christensen Prosthesis”[2], [3] (gambar 3A). Prosthesis ini dimanufaktur
dan didistribusikan oleh TMJ Inc., Golden, CO, USA. Prosthesis ini menggunakan material vitallium
(paduan 65% cobalt, 30% chromium, 5% molybdenum serta unsur-unsur lainnya) pada komponen
fossa. TMJ Inc. sebagai perusahaan penyedia prosthesis ini menyediakan 33 pilihan bentuk dan ukuran
dari komponen fossa untuk memastikan fitting yang sesuai dengan tengkorak manusia. Komponen
mandibular terbuat dari vitallium sebagai prosthetic shaft-nya serta PMMA (polymethyl methacrylate)
sebagai permukaan kontaknya [2], [3], [6], [11], [12]. Namun sejak 1997, bahan PMMA sebagai
permukaan kontak digantikan dengan vitallium karena adanya laporan terjadinya reaksi benda asing
akibat partikel aus dari PMMA [2], [12]. Perusahaan pembuat prosthesis ini menyediakan 3 pilihan
ukuran untuk komponen mandibular.
Kiehn pada tahun 1974, juga merancang sebuah prsothesis TMJ dengan menggunakan
material vitallium [2], [4]. Kiehn menggunakan semen PMMA untuk merekatkan prosthesis TMJ ke
tulang. Dalam studi follow-up 4 tahun dari prosthesis ini, tercatat dari 27 pasien, 4 prosthesis dicabut
dikarenakan terjadi infeksi, dislokasi serta skin erosion [4].
Untuk mencegah resorpsi dari glenoid fossa yang terjadi pada pasien dengan kelainan TMJ
degeneratif, Kent (1986) merancang sebuah total TMJ prosthesis. Prosthesis pada bagian glenoid fossa
memiliki material dengan tiga layer (lapisan) yang terdiri dari Proplast I (komposit PTFE-graphite) pada
lapisan pertama, Teflon FEP (fluorinated ethylene propylene) pada lapisan tengah serta Teflon PTFE
(polytetrafluoroethylene) sebagai contacting surface [4]. Kombinasi dari material logam (pada bagian
condyle) dan Teflon/Proplast pada bagian fossa ini menyebabkan terjadinya particle shedding
(pengelupasan partikel) yang menyebabkan berbagai macam komplikasi pada pasien bahkan setelah
prosthesis dilepas [2]. Hal ini menyebabkan klaim senilai jutaan dollar amerika, pencabutan ijin FDA,
serta bangkrutnya perusahaan pada tahun 1990 [2].
Pada awal tahun 1980, Sonnenburg mengembangkan sebuah sistem total TMJ prosthesis di
Jerman Timur [2]. Prosthesis ini menggunakan material polyethylene pada bagian fossa yang memiliki
kontak dengan material paduan titanium pada bagian condyle [2]. Laporan pada 12 pasien dengan
sistem ini tidak menunjukkan terjadinya komplikasi akibat fragmentasi aus dari material yang
bergesekan seperti yang terjadi pada prosthesis Kent [2].
Prosthesis Techmedica (Techmedica Inc., CA, USA), sekarang dikenal sebagai ‘TMJ Concepts
prosthesis’ (TMJ Concepts Inc., CA, USA), yang pengembangannya dimulai pada tahun 1989 didesain
untuk pasien yang telah mengalami beberapa kali operasi perbaikan dan pasien dengan anatomi TMJ
yang telah mengalami kelainan [2], [7]. Komponen bagian fossa terdiri dari dua material dasar. Bagian
fitting terbuat dari titanium sheet untuk memastikan fitting yang sesuai dengan anatomi fossa dan
articular fossa yang kemudian dilapisi dengan titanium mesh. Bagian yang mengalami kontak
(articulating surface) dengan bagian condyle terbuat dari material UHMWPE. Komponen mandibular

terbuat dari material paduan titanium untuk memastikan kekuatan mekanisnya, serta bagian condyle
(articulating surface) terbuat dari chromium-cobalt-molybdenum [7].
Bahan dasar Titanium juga digunakan sebagai bahan pada prosthesis titanium/titanium nitride
TMJ (TTN-TMJ), yang dikembangkan pada tahun 1992. Permukaan kontak pada komponen condyle
dan fossa dilapisi dengan titanium nitride untuk mengeraskan (hardening) permukaan kontak.
Kelebihan dari prosthesis TTN-TMJ ini adalah, prosthesis ini memiliki rancangan yang sangat sesuai
dengan anatomi TMJ, pergerakan translasi, termasuk pergerakan translasi medio-lateral mampu
diakomodir oleh prosthesis ini [2].
Biomet-Lorenz total TMJ prosthesis (Biomet Microfixation Inc., Jacksonville, FL, USA) mulai
dipasarkan dan FDA approved pada tahun 1995 [2]. Komponen fossa terbuat dari material UHMWPE.
Perusahaan pembuat prosthesis ini menawarkan 3 pilihan ukuran (small, medium dan large) [13].
Komponen mandibular terbuat dari vitallium (paduan Cr-Co-Mb) dengan coating dari paduan
titanium. Tersedia dalam 3 ukuran (45, 50 dan 55 mm) dan 3 bentuk (standar, narrow/sempit dan
offset) [13].
Van Loon pada tahun 1998-2000 merancang total TMJ prosthesis yang dikenal sebagai
Groningen TMJ prosthesis [14–16]. Prosthesis ini pada awalnya dirancang untuk penggunaan secara
unilateral, yaitu implant hanya dipasang pada salah satu sisi saja [14]. Van Loon menemukan bahwa
dengan memindahkan pusat putaran komponen mandibular sejauh 15 mm ke arah inferior, maka
pergerakan translasi dari sendi rahang alami dapat ditiru (gambar 2A) [15]. Pergerakan translasi inilah
yang seringkali hilang pada sistem-sistem prosthesis TMJ yang sudah ada. Dengan adanya mekanisme
pergerakan translasi pada prosthesis ini, maka distribusi beban pada prosthesis dan sendi rahang yang
alami akan lebih merata, sehingga memperpanjang usia pakai prosthesis [14–16]. Prosthesis ini
dirancang sebagai multi modular (gambar 2B) dengan material disc terbuat dari UHMWPE, condyle
headnya terbuat dari zirconium oxide, serta prosthetic shaft-nya terbuat dari paduan titanium.
Belum banyak studi yang melaporkan masalah penggunaan jangka panjang dari Groningen TMJ
prosthesis ini, sehingga belum ditemukan terjadinya komplikasi akibat penggunaan jangka panjang.
Namun, satu studi follow-up melaporkan bahwa telah terjadi dislokasi pada bagian disc di salah satu
pasien mereka yang menggunakan sistem ini [5].
Gambar 2. A.) Analisa posisi pusat perputaran mandibular. Titik analisa pusat perputaran
ditandai dengan titik 4 titik hitam (titik hitam paling atas (ditengah condyle), 10 mm, 15 mm
serta 20 mm dibawah condyle). Analisa menunjukkan bahwa dengan pusat putaran komponen
mandibular paling efektif adalah sejauh 15 mm dibawah condyle [15]. B.) Desain dari Groningen
TMJ prosthesis [14].

Gambar 3. Berbagai macam bentuk prosthesis TMJ. A.) Prosthesis rancangan Christensen [2].
B.) Prosthesis Vitek-Kent (Vitek Inc., TX, USA) [4]. C.) TMJ Concepts prosthesis (TMJ Concepts
Inc., CA, USA) [7]. D.) Biomet-Lorenz total TMJ prosthesis (Biomet Microfixation Inc., FL, USA)
[2]. E.) Groningen TMJ prosthesis [14].

Tabel 1. Kesimpulan serta komplikasi yang terjadi dari penggunaan berbagai macam tipe
prosthesis TMJ
Desain prosthesis Periode penggunaan
Material Komplikasi yang terjadi setelah penggunaan jangka panjang
Christensen [2], [8] 1965-? Fossa: Cr-Co Condyle: Cr-Co + PMMA
Reaksi alergi, ankyloses, fracture dari prosthesis bagian condyle
Kiehn [2], [4] 1974-1979 Fossa: Cr-Co Condyle: Cr-Co + PMMA
Infeksi, percutaneous erosion, pengenduran prosthesis, nyeri
Kent [2], [4] 1981-1982 Fossa: Proplast I + Teflon FEP + Teflon PTFE Condyle: Cr-Co-Mb
Infeksi, erosi, dislokasi
Kent [2], [4] 1982-1986 Fossa: Proplast II + Teflon FEP Condyle: Cr-Co-Mb
Infeksi, erosi, ankyloses, dislokasi dari TMJ natural, nyeri, kegagalan material Teflon FEP
Kent [9] 1986-1990 Fossa: Proplast hydroxyapatite + UHMWPE Condyle: Cr-Co-Mb
Ankyloses, nyeri
Sonnenburg [2] 1972-? Fossa: polyethylene Condyle: Ti-Pd
Infeksi, fitting bagian condyle yang kurang sesuai, poor shaping of prosthesis, kelumpuhan otot wajah
Techmedica/TMJ Concepts [7]
1990-sekarang
Fossa: titanium + UHMWPE Condyle: Cr-Co-Mb Mandibular shaft: titanium alloy (Ti6Al4V)
Loosening (pengenduran) pada komponen mandibular, heterotopic bone formation
Titanium/titanium nitride temporomandibular joint prosthesis (TTN-TMJ) [2]
1992-? Articulating surface: titanium nitrite
Nyeri pada daerah persendian, pergerakan rahang terbatas (dikarenakan efek dari operasi rekonstruksi sebelumnya)
Biomet-Lorenz total TMJ prosthesis [13]
1995-sekarang
Fossa: UHMWPE Condyle: Cr-Co atau titanium alloy
Terdapat kegagalan mekanis pada beberapa kasus
Groningen TMJ prosthesis [5], [14]
2001-sekarang
Fossa: UHMWPE Condyle: zirconium-oxide
Terjadi dislokasi pada satu pasien (7%)

Berbagai macam prosthesis TMJ telah dibahas dan semuanya memiliki kelebihan dan
kekurangan masing-masing. Berdasarkan hasil kajian ini, penulis merumuskan beberapa persyaratan
penting dalam perancangan prosthesis TMJ yang dapat dilihat pada Tabel 2, sebagai landasan
pengembangan sebuah prosthesis TMJ. Berdasarkan rata-rata umur pasien yang melakukan operasi
rekonstruksi TMJ yaitu berkisar 30-50 tahun [2], [5], [12–14]; maka pasien dengan prosthesis TMJ,
masih memiliki harapan hidup sekitar 20-40 tahun. Oleh karenanya, sebuah TMJ prosthesis
diharapkan memiliki usia pakai sampai 20 tahun dengan jumlah operasi revisi dibatasi hanya satu kali.
Hal ini dikarenakan, usia pakai dari prosthesis akan semakin berkurang dengan semakin banyaknya
operasi revisi [14].
Tabel 2. Persyaratan perancangan prosthesis TMJ
NO. DESKRIPSI
1. Laju keausan yang rendah 2. Partikel aus (wear debris) dapat ditoleransi oleh
tubuh 3. Memiliki kekuatan mekanis yang cukup 4. Dapat mengakomodir gerakan-gerakan
fungsional rahang 5. Memiliki fitting yang sesuai baik dengan bagian
rahang maupun tengkorak manusia 6. Sambungan prosthesis yang stabil ke struktur
tulang rahang dan tengkorak manusia
Ketahanan dari sebuah prosthesis, sangat bergantung pada laju keausan dari permukaan
kontaknya. Oleh karenanya, sebuah prosthesis TMJ harus memiliki laju keausan yang rendah
(persyaratan 1). Selain itu, partikel aus (wear debris) dari material yang bergesekan dapat
menyebabkan kegagalan penggunaan jangka panjang. Untuk itu, pemilihan material sangat perlu
dipertimbangkan, agar efek negatif dari partikel aus dapat diminimalisir (persyaratan 2). Ada kalanya
beban yang diterima prosthesis dalam penggunaannya menjadi cukup besar, oleh karenanya, material
dari prosthesis juga harus memiliki kekuatan mekanis yang cukup, untuk dapat digunakan dalam
jangka waktu yang panjang (persyaratan 3). Van Loon menunjukkan bahwa dengan terbatasnya
gerakan translasi pada rahang, mengakibatkan beban pada TMJ meningkat [14–16]. Oleh karenanya,
sebuah prosthesis TMJ juga harus dapat mengakomodir pergerakan rahang (persyaratan 4).
Permasalahan selanjutnya yang sering muncul pada prosthesis TMJ adalah fitting pada bagian rahang
dan tengkorak. Mengingat banyaknya variasi bentuk bagian tengkorak dari TMJ, maka untuk
memastikan prosthesis terpasang dengan sempurna, perlu diperhatikan bagian fitting-nya serta
sambungan antara prosthesis dan tulang (persyaratan 5 dan 6).
Hidroksiapatit
Hidroksiapatit yang memiliki rumus kimia Ca10(PO4)6(OH)2 merupakan biomaterial yang
tergolong ke dalam kalsium fosfat. Material ini diketahui memiliki sifat biokompatibel serta dapat
menyatu dengan tulang. Hidroksiapatit merupakan salah satu penyusun inorganic pada tulang dan
bentuk buatannya (HA sintetis) terbukti memiliki struktur kimia dan kristal yang sama dengan
meskipun tidak identik dengan HA yang terbentuk alami [17].

HA merupakan biomaterial dari golongan kalsium fosfat yang paling banyak diteliti dan
penggunaannya sudah dimulai sejak sejak 1970[17]. HA sintetis dapat dibuat dari berbagai macam
bahan, yaitu tulang sapi, cangkang telur, karang laut dll [17], [18].
Gambar 4. Porous HA
Pengujian Laju Keausan
Bin-Bin Jia, Tong-Sheng Li, Xu-Jun Liu dan Pei-Hong Cong pada tahun 2007 melakukan
perhitungan laju keausan dari polimer-polimer. Kombinasi polimer-polimer yang digunakan Bin-Bin Jia
dkk adalah polytetrafluoroethylene (PTFE)-PTFE; polyamide 66 (PA66)-PA66 serta polyphenylene
sulfide (PPS)-PPS. Uji keausan dilakukan dengan alat uji keausan (tribometer) tipe pin-on-disc. Sebuah
disc dengan diameter 50 mm dan tebal 5 mm berputar dengan kecepatan yang ditentukan dengan
kontak sebuah pin yang berdiameter 2,5 mm dan tebal 5 mm. Gambar 5 menunjukkan tribometer pin-
on-disc beserta letak disc dan pin serta arah putaran disc. Dengan metode ini, Bin-Bin Jia dkk. dapat
menghitung laju keausan dari beberapa polimer yang diuji. Uji keausan dilakukan pada suhu ruang
(20±5oC) dengan variasi beban dari 0,1 N sampai 5 N, variasi kecepatan dari 0,1 m/s sampai 1,2 m/s
dan dengan jarak gesekan yang tetap yaitu 1200 m. Pengujian juga dilakukan dengan dua kondisi, yaitu
dry friction dan lubricated atau dengan pelumasan. Cairan pelumasan yang digunakan adalah parrafin
cair [19].
Laju keausan dihitung berdasarkan massa yang hilang dari pin dan juga dari disc dengan
menggunakan persamaan Archard:
𝑘 =∆𝑉
𝐿𝐹
Dimana:
k = spesific wear rate (mm3/Nm)
ΔV = perubahan volume (mm3)
Δm = perubahan massa (kg)
L = jarak sliding (m)
F = gaya (N)
ρ = massa jenis (kg/mm3)

Gambar 6 menunjukkan laju keausan dari PTFE, PA66 dan PPS pada kondisi dry friction dan
lubricated. Grafik pada gambar 2.5 menunjukkan bahwa laju keausan dari PTFE merupakan yang
tertinggi diikuti dengan PA66 dan PPS yang memiliki laju keausan yang paling rendah. Dari grafik juga
terlihat pada kasus PTFE dan PPS, penambahan pelumasan dapat mengurangi laju keausan yang
terjadi.
Gambar 5. Tribometer tipe pin-on-disc.
Gambar 6. Laju keausan PTFE, PA66 dan PPS dalam keadaan kering serta lubrikasi
dengan paraffin.
Van Loon dkk. pada tahun 1998 juga melakukan uji keausan dari prosthesis TMJ
rancangannya. Van Loon menggunakan material UHMWPE dan PTFE dengan lawan kontak logam
dalam 2 keadaan lubricated, yaitu air dan serum [20].
Alat untuk menguji keausan yang digunakan Van Loon dapat dilihat pada gambar 7. alat
tersebut terdiri dari sebuah batang yang memiliki ujung berupa bola logam yang bergerak bolak balik
terhadap 2 buah cup yang menjepit bola logam. Konfigurasi tersebut ditambah dengan plastik yang
mengelilingi pangkal batang sebagai tempat untuk menambahkan cairan lubrikasi. Terdapat juga
konfigurasi untuk memberikan beban pada bagian kontak seperti terlihat pada gambar 2.9. konfigurasi
seperti ini ditujukan untuk meniru gerak rahang manusia. Material yang digunakan untuk cup
divariasikan antara UHMWPE dan PTFE. Sementara bola adalah stainless steel [20].

Gambar 7. Alat Uji Keausan yang Digunakan oleh Van Loon untuk Meniru Mekanisme
Gerak Rahang.
Gambar 8 menunjukkan hasil keausan dari PTFE dan UHMWPE. Untuk PTFE keausan yang
terjadi adalah sebesar 2,8 dan 47 mm3/106 siklus pada air dan serum. Untuk UHMWPE keausan yang
terjadi adalah sebesar 0,006 dan 0,47 mm3/106 siklus pada air dan serum. Pada air, salah satu sampel
menunjukkan terjadinya kenaikan yang signifikan setelah 3,6 juta siklus. Sedangkan pada serum, laju
keausan yang terjadi pada semua spesimen relatif sama [20].
Tabel 3 menunjukkan besar keausan yang terjadi beserta hasil perhitungan laju keausan dan
standar deviasinya. Untuk PTFE, laju keausan yang terjadi adalah sebesar 4,0 x 10-6 dan 6,8 x 10-6
mm3/Nm pada air dan serum. Sedangkan untuk UHMWPE, laju keausan yang terjadi adalah sebesar
9,2 x 10-6 dan 6,8 x 10-6 mm3/Nm. Dari hasil tersebut dapat disimpulkan bahwa untuk material PTFE,
laju keausan yang terjadi pada air lebih rendah daripada serum. Sedangkan untuk material UHMWPE
laju keausan yang terjadi pada serum justru lebih rendah dibandingkan dengan air [20].
Gambar 8. Besar keausan yang terjadi dari PTFE dan UHMWPE.
Tabel 3. Besar keausan dan laju keausan dari PTFE dan UHMWPE.
Keausan (mm3/106 siklus) Laju Keausan (mm3/Nm)
Air Serum Air Serum
PTFE 2,8 (± 0,84) 47 (± 8,8) 4,0 (± 1,2) x 10-6 6,8 (± 1,3) x 10-5
UHMWPE 0,006 (± 0,004) 0,47 (± 0,17) 9,2 (± 6,2) x 10-9 6,8 (± 2,5) x 10-7

DAFTAR PUSTAKA
[1] “TMJ.” American Association of Oral and Maxillofacial Surgeons, 2008. [2] O. Driemel, S. Braun, U. D. A. Muller-Richter, M. Behr, T. E. Reichert, M. Kunkel, and R. Reich,
“Historical Development of Alloplastic Temporomandibular Joint Replacement After 1945 and State of The Art,” International Journal of Oral and Maxillofacial Surgery, vol. 38, no. 9, pp. 909–920, 2009.
[3] J.-P. van Loon, L. G. M. de Bont, and G. Boering, “Evaluation of Temporomandibular Joint Prosthesis: Review of The Literature from 1946 to 1994 and Implications for Future Prosthesis Designs,” International Journal of Oral and Maxillofacial Surgery, vol. 53, no. 9, pp. 984–996, 1995.
[4] J. N. Kent, M. S. Block, C. A. Homsy, J. M. Prewitt III, and R. Reid, “Experience with a Polymer Glenoid Fossa Prosthesis for Partial or Total Temporomandibular Joint Reconstruction,” Journal of Oral and Maxillofacial Surgery, vol. 44, no. 7, pp. 520–533, 1986.
[5] J. M. Schuurhuis, P. U. Dijkstra, B. Stegenga, L. G. M. de Bont, and F. K. L. Spijkervet, “Groningen Temporomandibular Joint Prosthesis: An 8-Year Longitudinal Follow-Up on Function and Pain,” International Journal of Cranio-Maxillo-Facial Surgery, vol. 40, no. 1, pp. 815–820, 2012.
[6] L. M. Wolford, D. J. Dingwerth, R. M. Talwar, and M. C. Pitta, “Comparison of 2 Temporomandibular Joint Total Joint Prosthesis Systems,” Journal of Oral and Maxillofacial Surgery, vol. 61, no. 6, pp. 685–690, 2003.
[7] L. M. Wolford, M. C. Pitta, O. Reiche-Fischel, and P. F. Franco, “TMJ Concepts/Techmedica Custom-Made TMJ Total Joint Prosthesis: 5-Year Follow-Up Study,” International Journal of Oral and Maxillofacial Surgery, vol. 32, no. 3, pp. 268–274, 2003.
[8] D. C. Chase, J.-W. Hudson, D. A. Gerard, R. Russell, K. Chambers, J. R. Curry, J. E. Latta, and R. W. Christensen, “The Christensen Prosthesis: A Retrospective Clinical Study,” Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontics, vol. 80, no. 3, pp. 273–278, 1995.
[9] J. N. Kent, M. S. Block, J. Halpern, and M. G. Fontenot, “Update on the Vitek Partial and Total Temporomandibular Joint Systems,” Journal of Oral and Maxillofacial Surgery, vol. 51, no. 4, pp. 408–415, 1993.
[10] G. W. N. Eggers, “Arthroplasty of The Temporomandibular Joint in Children With Interposition of Tantalum Foil,” Journal of Bone and Joint Surgery, vol. 28, no. 3, pp. 603–606, 1946.
[11] L. G. Mercuri, “The Christensen Prosthesis,” Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology, and Endodontology, vol. 81, no. 2, pp. 134–135, 1996.
[12] N. R. Saeed, N. M. H. McLeod, and R. Hensher, “Temporomandibular Joint Replacement in Rheumatoid-Induced Disease,” British Journal of Oral and Maxillofacial Surgery, vol. 39, no. 1, pp. 71–75, 2001.
[13] R. Sanovich, U. Mehta, S. Abramowicz, C. Widmer, and M. F. Dolwick, “Total Alloplastic Temporomandibular Joint Reconstruction Using Biomet Stock Prostheses: The University of Florida Experience,” International Journal of Oral and Maxillofacial Surgery, vol. 43, no. 9, pp. 1091–1095, 2014.
[14] J.-P. van Loon, L. G. M. de Bont, B. Stegenga, F. K. Spijkervet, and G. Verkerke, “Groningen Temporomandibular Joint Prosthesis. Development and First Clinical Application,” International Journal of Oral and Maxillofacial Surgery, vol. 31, no. 1, pp. 44–52, 2002.
[15] J.-P. van Loon, C. Falkenstrom, L. G. M. de Bont, G. J. Verkerke, and B. Stegenga, “The Theoretical Optimal Center of Rotation for a Temporomandibular Joint Prosthesis: A Three-dimensional Kinematic Study,” Journal of Dental Research, vol. 78, no. 1, pp. 43–48, 1999.
[16] J.-P. van Loon, E. Otten, C. H. Falkenstrom, L. G. M. de Bont, and G. J. Verkerke, “Loading of a Unilateral Temporomandibular Joint Prosthesis: A Three-dimensional Mathematical Study,” Journal of Dental Research, vol. 77, no. 11, pp. 1939–1947, 1998.

[17] J. Vuola, “Natural coral and hydroxyapatite as bone substitutes,” Medical Faculty of the University of Helsinki, 2001.
[18] I. Hilmi, M. Rinastiti, and M. K. Herliansyah, “Synthesis of Hydroxyapatite from Local Bovine Bones for Biomedical Application,” in International Conference on Instrumentation, Communication, Information Technology and Biomedical Engineering, 2011.
[19] B.-B. Jia, T.-S. Li, X.-J. Liu, and P.-H. Cong, “Tribological Behaviors of Several Polymer–Polymer Sliding Combinations under Dry Friction and Oil-Lubricated Conditions,” Wear, vol. 262, no. 11, pp. 1353–1359, 2007.
[20] J.-P. van Loon, G. J. Verkerke, L. G. M. de Bont, and R. S. B. Liem, “Wear-testing of a Temporomandibular Joint Prosthesis: UHMWPE and PTFE Against a Metal Ball, in Water and in Serum,” Biomaterials, vol. 20, no. 16, pp. 1471–1478, 1999.