PEMBUATAN DAN KARAKTERISASI KITOSAN …repository.unair.ac.id/25759/7/KKK.compressed (1).pdfADLN...
Transcript of PEMBUATAN DAN KARAKTERISASI KITOSAN …repository.unair.ac.id/25759/7/KKK.compressed (1).pdfADLN...

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
PEMBUATAN DAN KARAKTERISASI KITOSAN-UREA
DENGAN PENAMBAHAN ASAM KLOROASETAT DAN
GLUTARALDEHID SEBAGAI ADSORBEN ION LOGAM Cu2+
MELALUI TEKNIK ADSORPSI FLUIDISASI
SKRIPSI
NOURMALASARI AISYAH
PROGRAM STUDI S-1 KIMIA
DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS AIRLANGGA
2012

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
PEMBUATAN DAN KARAKTERISASI KITOSAN-UREA
DENGAN PENAMBAHAN ASAM KLOROASETAT DAN
GLUTARALDEHID SEBAGAI ADSORBEN ION LOGAM Cu2+
MELALUI TEKNIK ADSORPSI FLUIDISASI
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar SarjanaSains
Bidang Kimia Pada Fakultas Sains dan Teknologi
Universitas Airlangga
NOURMALASARI AISYAH
080810054
Tanggal Lulus:
17 Juli 2012
Disetujui Oleh :
Pembimbing I
Dr. Ir. Suyanto, M.Si
NIP. 19520217 198203 1 001
Pembimbing II
Siti Wafiroh, S.Si, M.Si
NIP. 19681209 199411 2 001

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
LEMBAR PENGESAHAN NASKAH SKRIPSI
Judul : Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid
Sebagai Adsorben Ion Logam Cu2+ Melalui Teknik
Adsorpsi Fluidisasi
Penyusun : Nourmalasari Aisyah
NIM : 080810054
Tanggal Ujian : 17 Juli 2012
Pembimbing I
Dr. Ir. Suyanto, M.Si
NIP. 19520217 198203 1 001
Pembimbing II
Siti Wafiroh, S.Si, M.Si
NIP. 19681209 199411 2 001
Mengetahui,
Ketua Program Studi S-1 Kimia
Departemen Kimia
Fakultas Sains dan Teknologi Universitas Airlangga
Dr. Alfinda Novi Kristanti, DEA
NIP. 19671115 199102 2 001

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
PEDOMAN PENGGUNAAN SKRIPSI
Skripsi ini tidak dipublikasikan, namun tersedia di perpustakaan dalam
lingkungan Universitas Airlangga, diperkenankan untuk dipakai sebagai referensi
kepustakaan, tetapi pengutipan harus seizin penyusun dan harus menyebutkan
sumbernya sesuai kebiasaan ilmiah. Dokumen skripsi ini merupakan hak milik
Universitas Airlangga
iv

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
KATA PENGANTAR
Assalamualaikum wr.wb
Puji syukur kehadirat Allah SWT atas segala rahmat dan hidayah-Nya,
sehingga penyusun dapat menyelesaikan skripsi dengan judul Pembuatan dan
Karakterisasi Kitosan-Urea dengan Penambahan Asam Kloroasetat dan
Glutaraldehid Sebagai Adsorben Ion Logam Cu2+ Melalui Teknik Adsorpsi
Fluidisasi. Shalawat serta salam tetap tercurahkan kepada Nabi Muhammad SAW
karena berkat perjuangan beliau dan para sahabatnya, penyusun bisa menikmati
indahnya iman.
Penyusun menyadari bahwa penulisan naskah skripsi ini tidak lepas dari
bantuan berbagai pihak, untuk itu penyusun menyampaikan terima kasih kepada:
1. Bapak Dr. Ir. Suyanto, M.Si selaku pembingbing I dan Ibu Siti Wafiroh, S.Si,
M.Si selaku pembingbing II yang telah memberikan ide, saran, koreksi, doa dan
bimbingan sampai terselesaikan skripsi ini.
2. Bapak Dr. Mulyadi Tandjung, M.S selaku penguji I dan Ibu Dr. Muji Harsini,
M.Si selaku penguji II yang telah memberikan saran, doa, dan bimbingan hingga
terselesaikan skripsi ini.
3. Ibu Dr. Afaf Baktir selaku Dosen Wali yang senantiasa membimbing serta
memberikan banyak masukan selama kegiatan kuliah.
4. Ibu Dr. Alfinda Novi Kristanti, DEA selaku Ketua Departemen Kimia yang
senantiasa memberikan dukungan.
5. Seluruh staf pengajar Fakultas Sains dan Teknologi Universitas Airlangga, atas
ilmu yang telah diberikan.
6. Bapak Nono Mariyono dan Ibu Lusy Sawitri, serta kakak dan adik yang telah
memberikan kasih sayang, dukungan moral dan spiritual serta doa yang
senantiasa mengalir demi kesuksesan anak-anaknya.
v

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
7. Ardana Yudistira Aulia yang telah banyak memberikan doa dan bantuan selama
kegiatan menyelesaikan skripsi.
8. Teman-teman kimia angkatan 2008 khususnya Puji Lestari, Asri Zulchana,
Vridayani Anggi, Ryan Rachmawan, Ayu Eprilita, Yan Polan, Nadya Aisya,
Jemmy Mahesa, Reylah Mustika, Della Ratna, Laras Risqoniah, Riza Damayanti,
Siti Mariam, Wike Arnovia, Ariesta Faulina, Faiz Tamami, M.Avi, Farradhina
Choria, Ratih Kusuma.
9. Teman-teman KKN Somber khususnya Gerry Maulana, Neni Oktavia, Rara
Gendis, Darari Rahmantya, Nanda Firmanda, Isnaini Septi, Titis Rieski, dan
Wisudawan, yang banyak memberikan dukungan pada penulis selama
mengerjakan skripsi.
10. Teman-teman angkatan 2008, 2009, 2010 yang senantiasa menemani dalam
menuntut ilmu dalam perkuliahan.
11. Teman-teman yang telah membantu pada proses pembuatan kolom fluidisasi,
terimakasih untuk semangat serta saran yang telah diberikan.
Penyusun menyadari bahwa dalam penulisan naskah skripsi ini masih banyak
kekurangan, sehingga penyusun mengharapkan kritik dan saran yang membangun
demi perbaikan skripsi ini. Penyusun berharap naskah skripsi ini dapat bermanfaat dan
sedikit memberikan kontribusi dalam pengembangan ilmu pengetahuan dan teknologi
di negeri ini.
Wassalamu’alaikum wr.wb
Surabaya, Juli 2012
Penyusun,
Nourmalasari Aisyah
vi

ADLN Perpustakaan Universitas Airlangga
vii
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
Aisyah, N., 2012, Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi. Skripsi ini di bawah
bimbingan Dr. Ir. Suyanto, M.Si., dan Siti Wafiroh, S.Si, M.Si., Departemen
Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga, Surabaya
ABSTRAK
Kitosan merupakan biopolimer dengan kemampuan adsorpsi terhadap ion logam
yang sangat baik. Modifikasi kitosan banyak dilakukan sebagai upaya
meningkatkan kemampuan adsorpsi terhadap ion logam. Penelitian ini bertujuan
mengetahui pengaruh pembuatan kitosan-urea dengan penambahan asam
kloroasetat, glutaraldehid dan urea, serta kemampuan kitosan-urea dalam
mengadsorpsi ion logam Cu2+ melalui metode adsorpsi fluidisasi. Pada penelitian
ini, senyawa turunan kitosan yaitu kitosan urea disintesis melalui dua tahap, tahap
pertama o-carboksimetilasi dan modifikasi dengan penambahan glutaraldehid-
urea. Karakterisasi senyawa kitosan dan kitosan-urea dilakukan menggunakan
spektroskopi FT-IR dan pengukuran kadar ion logam Cu2+ hasil adsorpsi
dianalisis menggunakan AAS pada panjang gelombang maksimal 324.75 nm.
Proses transformasi kitosan setelah penambahan asam kloroasetat terlihat pada
perubahan struktur pada gugus hidroksil menghasilkan karboksi metil kitosan.
Penambahan glutaraldehid-urea pada karboksi metil kitosan mensubstitusi pada
gugus amina. Modifikasi kitosan menjadi kitosan-urea digunakan sebagai
adsorben ion logam Cu2+. Proses adsorpsi dilakukan menggunakan metode
adsorpsi fluidisasi dengan mengontakkan 0.5 gram adsorben kitosan-urea dengan
200 ml larutan yang mengandung ion logam Cu2+ dengan waktu kontak selama 20
hingga 100 menit. Metode adsorpsi fluidisasi lebih efektif, hal ini terlihat dari
hasil kapasitas adsorpsi kitosan pada ion logam Cu2+ sebesar 34.51 mg/g dalam
waktu adsorpsi 180 menit, dan kapasitas adsorpsi kitosan-urea sebesar 35.76 mg/g
dalam waktu adsorpsi 80 menit.
Kata kunci : kitosan, modifikasi kitosan, asam kloroasetat, glutaraldehid,
adsorpsi fluidisasi, ion Cu2+

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
Aisyah, N., 2012, Synthesize and Characterisation Chitosan-Urea With
Addition of Chloroacetic acid and Glutaraldehyde as Adsorbent Cu 2+ Ion
by Fluidization Adsorption Technique. This study is under guidance of
Dr. Ir. Suyanto, M.Si., and Siti Wafiroh, S.Si, M.Si., Department of
Chemistry, Science and Technology Faculty, Universitas Airlangga.
ABSTRACT
Chitosan is a biopolymer with the good adsorption ability of metal ions.
Modifications chitosan is widely used as an effort to improve the adsorption
ability of metal ions. This study aims to determine the effect of urea with the
addition of chloasetic acid, glutaraldehyde and urea, and the ability of chitosan-
urea adsorbed Cu2+ metal ions by fluidization adsorption method. In this study,
chitosan-urea modified chitosan derivatives were synthesizes through two steps,
o-carboxymethylated first and then modified by the addition of glutraldehyde-urea
Characterization of chitosan and chitosan-urea performed by FT-IR spectroscopy
and determination of Cu2+ metal ions adsorption results were analyzed using AAS
at wavelength of 324.75 nm. The chitosan transformation process after addition of
chloroasetic acid changes in the structure of the hydroxyl group then produce
carboxy methyl chitosan. The addition of glutaraldehyde-urea in the carboxy
methyl chitosan substituting on the amine group. Modifications chitosan into
chitosan-urea is used as adsorbent of metal ions Cu2+. The process adsorption by
fluidization adsorption method using 0.5 grams of adsorbent chitosan-urea in 200
ml solution containing metal ions Cu2+ with the contact time for 20 to 100
minutes. Fluidization adsorption method is considered as an effective method.
This is evident from the result of the adsorption capacity of chitosan on the metal
ions Cu2+ at 34.51 mg/g in the adsortption time of 180 minutes, and the adsorption
capacity of chitosan-urea of 35.76 mg/g in the adsorption time of 80 minutes.
Keywords : chitosan, modified chitosan, chloroacetic acid, glutaraldehyde,
fluidization adsorption method, ion Cu2+
viii

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
DAFTAR ISI
Halaman
LEMBAR JUDUL ..................................................................................................... i
LEMBAR PERNYATAAN....................................................................................... ii
LEMBAR PENGESAHAN ....................................................................................... iii
LEMBAR PEDOMAN PENGGUNAAN SKRIPSI ............................................... iv
KATA PENGANTAR ............................................................................................... v
ABSTRAK .................................................................................................................. vii
ABSTRACT ............................................................................................................... viii
DAFTAR ISI .............................................................................................................. ix
DAFTAR TABEL ...................................................................................................... xi
DAFTAR GAMBAR ................................................................................................. xii
DAFTAR LAMPIRAN.............................................................................................. xiv
BAB I PENDAHULUAN ........................................................................................... 1
11.1 .......................................................................................................... Latar
Belakang Permasalahan.............................................................................. 1
11.2 .......................................................................................................... Rumu
san Masalah ................................................................................................ 6
11.3 .......................................................................................................... Tujua
n Penelitian ................................................................................................. 6
11.4 .......................................................................................................... Manf
aat Peneltian ............................................................................................... 7
BAB II TINJAUAN PUSTAKA ................................................................................ 8
2.1 Kitin ............................................................................................................ 8
2.2 Kitosan........................................................................................................ 10
2.2.1 Sifat kitosan ....................................................................................... 12
2.2.2 Manfaat kitosan ................................................................................. 12
2.3 Karakterisasi Kitin dan Kitosan ................................................................. 14
2.4 Kitosan Termodifikasi ................................................................................ 18
2.5 Urea ............................................................................................................ 20
2.6 Logam Berat ............................................................................................... 21
2.7 Logam Tembaga ......................................................................................... 22
2.8 Adsorpsi...................................................................................................... 23
2.9 Teknik Adsorpsi Fluidisasi ........................................................................ 24
2.10 Spektroskopi FTIR ................................................................................... 27
2.11 AAS .......................................................................................................... 28
BAB III METODE PENELTIAN ............................................................................. 30
3.1 Tempat dan Waktu Penelitian .................................................................... 30
3.2 Bahan dan Alat Penelitian .......................................................................... 30

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ix

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
3.2.1 Bahan-bahan penelitian ..................................................................... 30
3.2.2 Alat-alat penelitian ............................................................................ 30
3.3 Diagram Kerja ............................................................................................ 31
3.4 Pembuatan Reagen ..................................................................................... 32
3.5 Prosedur Penelitian ..................................................................................... 34
3.5.1 Preparasi serbuk cangkang rajungan ................................................. 34
3.5.2 Pembuatan kitosan dari kitin ............................................................. 34
3.5.3 Karakterisasi kitin dan kitosan .......................................................... 36
3.5.4 Pembuatan kitosan-urea .................................................................... 37
3.5.5 Proses adsorpsi .................................................................................. 38
3.5.6 Penentuan kapasitas adsorpsi logam Cu2+ dalam kitosan-urea ......... 39
3.5.5 Penentuan ukuran pori adsorben kitosan-urea .................................. 40
BAB IV HASIL DAN PEMBAHASAN .................................................................... 41
4.1 Hasil Preparasi Serbuk Cangkang Rajungan .............................................. 41
4.2 Hasil Pembuatan Kitosan dari Kitin ........................................................... 41
4.2.1 Tahap isolasi kitin dari cangkang rajungan ....................................... 41
4.2.2 Hasil transformasi kitin menjadi kitosan ........................................... 44
4.3 Hasil Karakterisasi Kitin dan Kitosan ........................................................ 46
4.3.1 Hasil uji kelarutan kitosan ................................................................. 46
4.3.2 Hasil penentuan berat molekul rata-rata kitsoan ............................... 47
4.3.3 Hasil penentuan derajat deasetilasi dengan FTIR ............................. 47
4.4 Hasil Pembuatan Kitosan-urea ................................................................... 50
4.4.1 Hasil pembuatan karboksi metil kitosan ........................................... 50
4.4.2 Hasil pembuatan karboksi metil kitosan dan glutaraldehid-urea ...... 53
4.5 Hasil Proses Adsorpsi ................................................................................. 60
4.5.1 Pembuatan kurva standar Cu ............................................................. 62
4.5.2 Pengukuran kadar ion logam Cu2+ hasil adsorpsi ............................. 63
4.5.3 Hasil penentuan kapasitas adsorpsi ion logam Cu2+ dalam
kitosan-urea ....................................................................................... 66
4.5.4 Hasil analisa BET pengukuran pori kitosan-urea .............................. 68
BAB V KESIMPULAN DAN SARAN ...................................................................... 70
5.1 Kesimpulan ................................................................................................. 70
5.2 Saran ........................................................................................................... 71
DAFTAR PUSTAKA.................................................................................................. 72
LAMPIRAN ................................................................................................................ 79
x

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
DAFTAR TABEL
Nomor Judul Tabel Halaman
2.1 Komposisi cangkang rajungan ......................................... 9
4.1 Gugus fungsi dan bilangan gelombang kitin dan
kitosan .............................................................................. 48
4.2 Gugus fungsi dan bilangan gelombang senyawa
organik dan karboksi metil kitosan .................................. 53
4.3 Gugus fungsi dan bilangan gelombang senyawa
organik dan kitosan-urea .................................................. 60
4.4 Adsorpsi ion logam Cu2+ dari kitosan pada beberapa
penelitian menggunakan senyawa turunan kitosan.......... 67
4.5 Perbandingan hasil analisa BET kitosan-urea ................. 68
xi

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
DAFTAR GAMBAR
Nomor Judul Gambar Halaman
2.1 Struktur kitin ............................................................................ 8
2.2 Struktur kitosan ........................................................................ 10
2.3 Mekanisme transformasi kitin menjadi kitosan ....................... 11
2.4 Spektrum FTIR senyawa kitosan ............................................. 15
2.5 Mekanisme reaksi karboksi metil kitosan ................................ 19
2.6 Mekanisme crosslinked karboksi metil kitosan
glutaraldehid-urea .................................................................... 20
2.7 Kolom fluidisasi ....................................................................... 27
2.8 Proses atomisasi pada AAS ...................................................... 29
3.1 Kolom fluidisasi pada penelitian .............................................. 39
4.1 Serbuk cangkang rajungan ....................................................... 41
4.2 Reaksi deproteinasi .................................................................. 42
4.3 Reaksi demineralisasi ............................................................... 43
4.4 Reaksi deasetilasi ..................................................................... 45
4.5 Serbuk kitosan .......................................................................... 46
4.6 Kelarutan kitin (a) dan kitosan (b) ........................................... 47
4.7 Spektrum FT-IR kitin ............................................................... 48
4.8 Spektrum FT-IR kitosan........................................................... 49
4.9 Karboksi metil kitosan ............................................................. 51
4.10 Struktur senyawa karboksi metil kitosan ................................. 52
4.11 Spektrum FT-IR karboksi metil kitosan................................... 52
4.12 Struktur glutaraldehid............................................................... 54
4.13 Struktur urea ............................................................................. 54
4.14 Mekanisme reaksi glutaraldehid dan urea ................................ 55
4.15 Kitosan-urea ............................................................................. 56
xii

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
4.16 Mekanisme reaksi pembentukan kitosan-urea ......................... 57
4.17 Hipotesis struktur kitosan-urea ................................................ 59
4.18 Spektrum FT-IR kitosan-urea .................................................. 59
4.19 Kolom adsorpsi fluidisasi ........................................................ 61
4.20 Kurva standar Cu ..................................................................... 62
4.21 Grafik adsorpsi ion logam Cu2+ oleh kitosan........................... 63
4.22 Grafik adsorpsi ion logam Cu2+ oleh kitosan-urea .................. 64
4.23 Grafik kapasitas adsorpsi ion logam Cu2+ oleh kitosan dan
Kitosan-urea ............................................................................. 66
xiii

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
DAFTAR LAMPIRAN
Nomor Judul Lampiran
1 Data hasil perubahan massa cangkang rajungan pada proses isolasi
kitin menjadi kitosan
2 Data penentuan berat molekul kitosan rata-rata kitosan
3 Data hasil karakterisasi FTIR kitin dan kitosan organik dan
karboksi metil kitosan
4 Data hasil adsorpsi ion logam Cu2+ oleh kitosan dan kitosan-urea
5 Data hasil penentuan kapasitas adsorpsi ion
logam Cu2+ oleh kitosan dan kitosan-urea
xiv

ADLN Perpustakaan Universitas Airlangga
Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
BAB I
PENDAHULUAN
1.1 Latar Belakang Permasalahan
Logam berat di lingkungan perairan sebagian besar menyebabkan
kerusakan parah, yang berakibat pada kehidupan manusia dan lingkungan
perairan. Pencemaran logam berat dianggap sebagai bahan yang tidak dapat
didegradasi. Senyawa organik beracun dan logam berat sebagian besar berasal
dari kegiatan industri, seperti industri elektroplating, dan metalurgi (Vega et al,
2006). Toksisitas dari pencemaran yang terus menerus mencemari lingkungan
akan sangat berbahaya bagi kehidupan manusia dan lingkungan sekitarnya (Jang
et al, 2005). Oleh karena itu, logam berat harus diolah sehingga memenuhi standar
ambang batas sebelum dibuang kewilayah perairan. Tembaga (Cu2+) merupakan
ion logam yang mendapat perhatian utama sebagai bahan pencemar lingkungan,
karena secara luas digunakan dalam pembuatan pupuk, penyulingan minyak bumi,
cat dan pigmen, kertas dan pulp, pengecoran, industri elektroplating. Penyerapan
Cu2+ yang berlebihan didalam tubuh (lebih dari 1.0 mg / L pada air minum) dapat
menyebabkan anemia, hemolitik, kelainan neurologis dan kerusakan kornea
(Massaro, 2003).
Berbagai metode physico-chemical termasuk filtrasi, pertukaran osmosis
(Ning, 2002), electrochemical treatment (Chen et al, 2002), pertukaran ion,
karbon aktif (Hu et al, 2003), adsorpsi, dan teknologi membran (Reddad et al,
2003), koagulasi dan flokulasi yang digunakan untuk mengurangi dan
menghilangkan ion logam beracun. Proses koagulasi-flokulasi dapat digunakan
1

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
2
sebagai pretreatment, posttreatment atau metode utama dalam penanganan
limbah. Namun, metode ini memiliki banyak kelemahan. Sebagai contoh,
pertukaran ion adalah metode yang efisien, tetapi tidak hanya menghilangkan ion
logam berat tetapi terjadi pertukaran Ca2+ dan Mg2+ (Li et al, 2008). Beberapa
teknologi ini termasuk dalam teknologi dengan biaya yang relatif mahal. Beberapa
metode tersebut tidak efektif terutama pada ion logam berat dengan konsentrasi
yang lebih rendah dai 100 mg/L logam. Upaya pengurangan Cu2+ dari air limbah
telah banyak diselidiki. Pada berbagai penelitian telah banyak diselidiki manfaat
dari polimer sebagai bahan alternatif yang efisien dan ekonomis, serta proses
adsorpsi yang secara khusus digunakan dalam pengolahan air (Copello et al,
2008).
Adsorpsi adalah metode yang sangat efektif untuk menghilangkan limbah
beracun dari limbah yang mengandung logam berat, terutama karena kemudahan
proses dan biaya yang murah sebagai adsorben alami seperti limbah pertanian,
bahan pembuatan tanah liat, biomassa dan pengolahan limbah hasil laut.
Penggunaan biopolimer sebagai adsorben ion logam telah banyak dilakukan.
Menurut Ravi dan Muzarelli tahun 2004, kitosan adalah biopolimer yang berasal
dari kitin dan dapat diaplikasikan secara luas dalam pengolahan air limbah,
industri kimia, biomedis dan farmasi. Kitosan diperoleh dari proses deasetilasi
kitin yang memiliki manfaat lebih luas. Kitosan tidak beracun, bersifat
bioadsorben dan memiliki berbagai macam fungsi biologis termasuk
antitrombogenik, meningkatkan imunitas, homeostatik, dan penyembuhan luka
(Tang et al, 2003).

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
3
Kitosan telah digunakan secara luas sebagai adsorben untuk mengurangi
pencemaran air yang terkontaminasi logam berat. Kitosan memiliki kemampuan
mengikat logam beracun lebih dari 1 mmol / gram. Kemampuan pengikatan
kitosan terhadap logam tertentu lebih besar dibandingkan dengan karbon aktif
(Varma et al, 2004). Besarnya adsorpsi kitosan tergantung pada sumber kitosan,
derajat deasetilasi, sifat dari ion logam dan pH larutan (Cestari et al, 2005).
Biopolimer kitosan mudah diperoleh dari deasetilasi kitin, sebuah
mukopolisakarida alami yang banyak ditemukan dalam eksoskeleton serangga,
cangkang crustaceae dan dinding sel jamur (Arica et al, 2004). Rajungan sebagai
salah satu komoditas ekspor sektor perikanan Indonesia yang dijual dalam bentuk
kemasan dalam kaleng. Proses pengemasan ini menghasilkan limbah kulit
(cangkang) dalam jumlah besar, sekitar 40-60% dari total berat rajungan (Rahayu
dan Purnavita, 2004). Semakin banyak limbah rajungan yang belum dimanfaatkan
secara maksimal, perlu adanya solusi. Sehingga dapat mengurangi permasalahan
lingkungan, seperti bau dan estetika yang kurang baik, yang nantinya memberikan
nilai tambah bagi usaha pengolahan rajungan (Rahayu dan Purnavita, 2004).
Limbah cangkang rajungan masih mengandung senyawa kimia cukup
banyak yaitu protein, mineral dan kitin. Kitin adalah polimer alam yang tidak larut
dalam air, sehingga penggunaannya terbatas. Namun dengan modifikasi kimia
dapat diperoleh senyawa turunan kitin yang mempunyai sifat kimia dan efek yang
lebih baik, yaitu kitosan (Ramesh et al, 2008).
Kitosan terdiri dari β-(1,4)-2-acetamido-2-deoxy-β-D-glucose dan unit β-
(1,4)-2-amino-2-deoxy-β-D-glucose dengan gugus amino dan hidroksi yang

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
4
reaktif serta dapat menyerap ion logam pada larutan netral. Hal ini secara
signifikan mampu meningkatkan kapasitas adsorpsi secara fisik maupun kimia.
Yang termasuk dalam modifikasi kimia adalah cross-lingking (meningkatkan
stabilisasi polimer dalam larutan asam) (Piron et al, 1997), dan penambahan
gugus fungsi (memperbanyak bidang adsorpsi) (Martins et al, 2004). Modifikasi
yang banyak dilakukan para peneliti adalah dengan cara crosslinked antar rantai
atau mengubahnya dalam bentuk garam (Purwatiningsih, 2009). Beberapa macam
bahan yang digunakan untuk crosslinking adalah glutaraldehid (Wan Ngah et al,
2006), epiklorohidrin dan etilenglikol diglisidil eter (Ngah et al, 2002). Diantara
senyawa turunan kitosan, percabangan gugus fungsi karboksil mampu
meningkatkan daya adsorpsi dari kitosan. Crosslinked pada kitosan dengan
penambahan glutaraldehid mampu meningkatkan kapasitas adsorpsi dari adsorben
(Sun dan Wang, 2005). Screenivasan tahun 2009, pada penelitiannya
menggunakan kitosan tercrosslinked glutaraldehid dan epiclorohydrin yang
mampu meningkatkan penyerapan ion logam Cu2+ sebanyak 82%. Kitosan juga
memiliki kemampuan untuk menyerap ion logam Cu2+ dan Cr4+ yang terdapat
pada limbah (Schmuhl et al, 2001).
Proses adsorpsi logam berat secara umum menggunakan metode batch
atau sistem aliran silang. Metode batch memiliki beberapa kelemahan, yaitu
jumlah adsorben yang banyak akibat penampungan larutan dan adsorben dari
batch ke batch berikutnya, pemurnian yang kurang merata terhadap adsorben,
serta efisiensi terhadap waktu penyerapan logam terhadap adsorben (Crittenden,
1998). Selain metode batch, saat ini telah dikembangkan metode-metode lain pada

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
5
proses adsorpsi, diantaranya adalah teknik adsorpsi fluidisasi (fluidized bed
adsorption) yaitu teknik adsorpsi dalam media kolom dengan aliran gas secara
kontinyu melalui bed penahan adsorben. Fluidisasi digambarkan sebagai proses
kontak antara solid dengan fluid. Fluidisasi merupakan proses pengontakan bahan
padat dengan fluida sehingga sifatnya berubah menyerupai sifat fluida. Kelebihan
dari teknik adsorpsi fluidisasi adalah pergerakan adsorben dalam bagian kolom
sebagai akibat adanya proses aliran gas dalam kolom, mampu mengadsorpsi ion
logam dalam larutan secara maksimal, serta efisiensi waktu yang lebih baik
(Crittenden, 1998).
Pada penelitian sebelumnya, kitosan murni digunakan sebagai adsorben
pada ion logam Cu2+ yang menghasilkan kapasitas adsorpsi maksimal sebesar
37,88 mg/gr dan penyerapan pada ion logam Pb2+ menghasilkan kapasitas
adsorpsi maksimal sebesar 13,05 mg/g (Chen et al, 2008). Wang tahun 2010,
dalam penelitiannya menggunakan kitosan termodifikasi glutaraldehid dan tiourea
mampu mengadsorpsi ion logam Hg2+ dengan kapasitas adsorpsi sebesar 6,29
mmol/g. Chen tahun 2009, menggunakan kitosan termodifikasi glutaraldehid dan
crosslinked logam mampu mengadsorpsi ion Cu2+ dengan kapasitas adsorpsi
sebesar 33,00 mg/gr.
Pada penelitian ini akan disintesis kitin dari cangkang rajungan, melalui
tahap deproteinasi, demineralisasi dan depigmentasi. Kemudian melalui proses
deasetilasi kitin ditransformasi menjadi kitosan. Kitosan yang diperoleh
dimodifikasi menjadi kitosan-urea dengan penambahan asam kloroasetat,
glutaraldehid dan urea. Penambahan glutaraldehid sebagai agen crosslinked

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
6
diharapkan mampu meningkatkan kemampuan adsorpsi dari adsorben kitosan-
urea. Kitosan-urea yang telah disintesis digunakan sebagai adsorben ion logam
Cu2+ dengan teknik adsorpsi fluidisasi. Kitin, kitosan, dan kitosan-urea
dikarakterisasi dengan menggunakan FT-IR, larutan logam Cu2+ dianalisis
menggunakan AAS, dan adsorben kitosan-urea dianalisis menggunakan uji BET.
1.2 Rumusan Masalah
Berdasarkan latar belakang masalah tersebut di atas, maka dapat
dirumuskan masalah sebagai berikut.
1. Bagaimana mensintesis kitosan-urea dengan penambahan asam
kloroasetat dan glutaraldehid sebagai agen crosslinked ?
2. Bagaimana pengaruh variasi konsentrasi urea pada sintesis kitosan-
urea sebagai adsorben ion logam Cu2+ dari hasil kapasitas adsorpsi dan
variasi waktu kontak dalam menyerap ion logam Cu2+ melalui proses
adsorpsi fluidisasi ?
1.3 Tujuan
Tujuan penelitian ini adalah sebagai berikut.
1. Mensistesis kitosan-urea dengan penambahan asam kloroasetat dan
glutaraldehid sebagai agen crosslinked
2. Mengetahui pengaruh variasi konsentrasi urea pada sintesis kitosan-
urea sebagai adsorben ion logam Cu2+ dan variasi waktu kontak
terhadap penyerapan ion logam Cu2+ melalui proses adsorpsi fluidisasi

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
7
1.4 Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat dihasilkan suatu metode yang
efektif untuk mengurangi ion logam Cu2+ di perairan sehingga bermanfaat untuk
masyarakat secara luas.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
BAB II
TINJAUAN PUSTAKA
2.1 Kitin
Kitin disebut sebagai polisakarida linear (1,4)-2-acetamida-2-deoksi- β-D-
glukosa atau poli-(β-1,4-N-asetilglukosamin) yang merupakan polisakarida alami
dengan kelimpahan terbesar kedua setelah selulosa (Khor, 2010). Kitin dengan
rumus molekul (C8H13NO5)n tersusun atas 47% C, 6% H, 7% N dan 40%
O. Struktur kitin menyerupai selulosa dan hanya berbeda pada gugus yang terikat
di posisi atom C2. Gugus C2 pada selulosa adalah gugus hidroksil, sedangkan
pada C2 kitin adalah gugus N-asetil (-NHCOCH3, asetamida) (Kim, 2011).
Gambar 2.1 Struktur kitin
Kitin adalah senyawa yang berwarna putih, elastis, polisakarida nitrogen
dengan biodegradasi, biokompatibilitas, bersifat nontoksik, dan dapat
diaplikasikan sebagai adsorben pada adsorpsi logam (No dan Meyers, 2000).
Sumber kitin yang sangat potensial adalah kerangka luar Crustacea (seperti
udang, rajungan, dan lobster), serangga, dinding yeast dan jamur, serta mollusca
(Rinaudo, 2006).
8

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
9
Rajungan merupakan salah satu komoditas ekspor sektor perikanan
Indonesia yang dijual dalam bentuk rajungan beku atau kemasan daging dalam
kaleng. Pada proses pengambilan dagingnya, dihasilkan limbah kulit (cangkang)
cukup banyak, jumlahnya mencapai sekitar 40-60% dari total berat rajungan
(Rahayu dan Purnavita, 2004). Limbah cangkang rajungan mengandung senyawa
kimia yaitu protein, mineral dan kitin. Komposisi dari cangkang rajungan
ditunjukkan pada tabel 2.1.
Tabel 2.1 Komposisi cangkang rajungan
Komposisi Jumlah kandungan (%)
Kadar air 5,50
Kadar abu 48,43
Kadar protein 40,53
Kitin 15,04
Kadar Asetil 88,12
Sumber : Hartati (2002)
Berdasarkan sifatnya yang tidak larut dalam air, penggunaan kitin sangat
terbatas. Namun dengan modifikasi struktur kimianya kitin memiliki sifat yang
lebih baik sehingga dapat dimanfaatkan secara luas.
Menurut Khor (2010) proses isolasi kitin dan pembuatan kitosan adalah
sebagai berikut :
1. Deproteinasi
Kitin didalam cangkang luar dari crustaceae berikatan dengan kalsium
karbonat (CaCO3) dan protein. Pada cangkang mengandung 30-40% protein dari
komponen organik total. Protein terikat secara fisik dan sebagian lainnya terikat
secara kovalen. Kadar protein dari crustaceae beragam tergantung dari jenisnya.
Deproteinasi merupakan reaksi hidrolisis dalam suasana asam dan basa. Secara

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
10
umum dilakukan pada suasana basa, dengan reagen seperti NaOH, Na2CO3, KOH,
NaHSO3.
2. Demineralisasi
Kandungan mineral cangkang crustaceae umumnya sebanyak 30-50%
mineral, dengan mineral terbanyak yaitu CaCO3. Mineral lain yaitu Ca3(PO4)2
dengan kadar 8-10% dari total bahan organik. Karena garam-garam anorganik
terikat secara fisik, senyawa CaCO3 lebih mudah dipisahkan dibanding protein.
Demineralisasi secara umum dilakukan dengan larutan HCl atau asam lain seperti
H2SO4.
3. Depigmentasi
Depigmentasi adalah proses pemutihan (bleaching) pada kitin hasil
demineralisasi dan deproteinasi. Penghilangan warna dari kitin adalah dengan
menggunakan aseton.
2.2 Kitosan
Kitosan disebut juga poli(1,4)-2-amina-2-deoksi-β-D-glukosa atau poli-(β-
1,4-N-asetilglukosamine) (Khor, 2010). Kitosan merupakan senyawa kitin yang
dihilangkan gugus asetilnya dan terdeasetilasi sebanyak mungkin, secara teoritis
kandungan gugus asetil pada kitin adalah 21,2% (Sugita, 2006).
Gambar 2.2 Struktur kitosan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
11
Deasetilasi secara kimia dapat dilakukan dengan menggunakan basa kuat
NaOH dan KOH. Namun penggunaan KOH dapat memutuskan ikatan hidrogen
yang kuat antar rantai kitin (Khor, 2010).
Gambar 2.3. Mekanisme transformasi kitin menjadi kitosan
Metode penyediaan kitosan pertama kali dibuat oleh Hope Seyler pada
tahun 1894 yaitu dengan merefluks kitin dalam larutan kalium hidroksida pada
temperatur 180oC.
Senyawa kitin dan kitosan dapat dibedakan berdasarkan gugus asetamida
pada karbon kedua (C2) dalam struktur molekulnya. Pada kitosan, sebagian besar
gugus asetil digantikan dengan atom hidrogen melalui reaksi hidrolisis dengan
alkali pekat. Adanya gugus amina menjadikan kitosan bermuatan parsial positif.
Hal ini menyebabkan kitosan dapat larut dalam larutan asam hingga netral. Selain
itu, muatan positif menyebabkan kitosan dapat menarik molekul-molekul yang

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
12
bermuatan parsial negatif seperti minyak, lemak, dan protein (Puspawati dan
Simpen, 2010).
2.2.1 Sifat kitosan
Sifat fisiko-kimia kitosan yaitu berwarna putih dan berbentuk serpihan
seperti bubuk. Kitosan larut dengan baik dalam larutan asam asetat 1-2%, selain
itu kitosan larut dalam HCl encer, HNO3 encer, H3PO4 0,5% dan tidak larut dalam
asam pekat dan basa kuat. Pada suasana asam, gugus amino (-NH2) kitosan akan
menangkap H+ dari lingkungannya, sehingga gugus amino terprotonasi menjadi –
NH3+. Gugus -NH3
+ inilah yang menyebabkan kitosan bertindak sebagai garam,
sehingga dapat larut dalam air. Sebagai informasi bahwa kelarutan kitosan
bergantung pada berat molekul, derajat deasetilasi, karakteristik rantai samping.
Derajat deasetilasi dan berat molekul berperan penting dalam kelarutan kitosan,
sedangkan derajat deasetilasi menunjukkan kemampuan kitosan untuk dapat
berinteraksi isoelektrik dengan molekul lain (Wibowo, 2006).
Adanya gugus amina pada kitosan menunjukkan kapasitas dan kemampuan
adsorpsi kitosan terhadap ion logam (tembaga) dibandingkan dengan kitin. Hal ini
dikarenakan jumlah gugus amina bebas (sebanding dengan derajat deasetilasi)
kitosan yang ada untuk pengkhelatan lebih banyak dibanding pada kitin, sehingga
kemampuan kitosan dalam menyerap ion logam lebih besar dari pada kitin
(Agusnar, 2006).
2.2.2 Manfaat kitosan
Kitosan memiliki potensi besar untuk dapat diaplikasikan pada berbidang
industri maupun kesehatan, antara lain industri farmasi, biokimia, bioteknologi,

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
13
pangan, kosmetik, industri tekstil, industri kertas, dan industri elektronika.
Aplikasi khusus dari kitosan antara lain pada pengolahan limbah cair adalah
sebagai bahan bersifat resin penukar ion untuk meminimalisasi logam-logam
berat, mengkoagulasi minyak/lemak, serta pada industri pangan sebagai penstabil
minyak, rasa dan lemak (Ramesh, 2008). Kitosan tidak beracun, dengan
bifungsionalitas yang tinggi pada bidang kesehatan termasuk anti thrombogenic
dan agen penyembuh luka (Tang, et al 2003). Pada bidang kesehatan lainnya,
aplikasi kitosan adalah sebagai agen penurun kolesterol (Ormrod et al, 1998), dan
sebagai pereduksi berat badan (Ernst dan Pitler, 1998).
Kitosan telah banyak digambarkan sebagai polimer alami yang digunakan
sebagai adsorben ion logam (Volda et al, 2003). Banyaknya atom nitrogen dalam
kitosan memungkinkan penyerapan ion logam melalui berbagai mekanisme
seperti khelasi dan pertukaran ion, yang bergantung pada ion logam dan pH
larutan (Guibal, 2004). Kemampuan kitosan untuk mengikat logam dengan cara
pengkhelat adalah dihubungkan dengan kadar nitrogen yang tinggi pada rantai
polimernya. Kitosan mempunyai satu amino linier dalam setiap unit glukosa.
Kumpulan amino ini mempunyai sepasang elektron bebas yang dapat membentuk
ikatan aktif dengan kation-kation logam. Unsur nitrogen dalam pada setiap
monomer kitosan adalah sisi yang aktif dengan kation logam (Hutahahean, 2001).
Salah satu aplikasi kitosan sebagai adsorben adalah pada proses penjernihan air.
Pada proses ini diperlukan mutu kitin dan kitosan yang tinggi, sedangkan
pada bidang kesehatan diperlukan kemurnian yang tinggi. Kitosan sebagai
adsorben dapat berada dalam berbagai bentuk, antara lain bentuk butir, serpih,

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
14
hidrogel, dan membran (film). Kitosan sebagai adsorben sering dimanfaatkan
untuk proses adsorpsi ion logam berat dan beracun seperti merkuri, timah,
tembaga, dan sebagai pengikat zat warna tekstil dalam air limbah. Besarnya
afinitas kitosan dalam mengikat ion logam sangat bergantung pada karakteristik
makrostruktur kitosan yang dipengaruhi oleh sumber dan kondisi pada proses
isolasi. Perbedaan bentuk kitosan akan berpengaruh pada luas permukaannya.
Semakin kecil ukuran kitosan, maka luas permukaan kitosan akan semakin besar,
dan proses adsorpsi pun dapat berlangsung lebih baik (Purwatiningsih, 2009).
2.3 Karakterisasi Kitin dan Kitosan
1. Uji Kelarutan
Kelarutan kitin dan kitosan dapat dianalisis dengan cara melarutkan kitin
dan kitosan dalam asam asetat 0,75%. Apabila serbuk tersebut tidak larut maka
serbuk tersebut adalah kitin. Sedangkan kitosan larut dalam asam asetat encer
(Kuntoro, 2004).
2. Derajat Deasetilasi
Melalui tahap deproteinasi dan demineralisasi, kitin yang diperoleh tidak
larut dalam sebagian pereaksi kimia. Untuk memudahkan kelarutannya kitin
dideasetilasi menjadi kitosan. Bertambahnya gugus amino (NH2) pada kitosan
meningkatkan kemampuan absorpsi didalamnya. Peningkatan kelarutan
berbanding lurus dengan peningkatan derajat deasetilasi, karena pada proses
deasetilasi gugus asetil pada kitin dipotong. Ion H pada gugus amina menjadikan
kitosan mudah berinteraksi dengan air melalui ikatan hidrogen (Agusnar, 2006).

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
15
Pada penentuan derajat deasetilasi digunakan spektroskopi FTIR. Derajat
deasetilasi ditentukan dengan metode baseline, dihitung dari nilai perbandingan
pita serapan antara puncak absorbansi absorbansi gugus amida pada daerah sekitar
1655 cm-1 dan puncak absorbansi gugus hidroksi pada daerah sekitar 3450 cm-1.
Puncak tertinggi diukur dari garis dasar. Perbandingan 2 gugus fungsi tersebut
ditentukan dengan cara membuat garis lurus dari 1800 cm-1 hingga 1600 cm-1
sebagai garis dasar bagi pita gugus amida dan membuat garis lurus dari 4000 cm-1
hingga 2500 cm-1 sebagai garis dasar pita gugus hidroksil (Khopkar, 2007).
Derajat deasetilasi kitosan dapat diukur melalui beberapa metode. Metode
yang banyak digunakan adalah metode garis dasar Fourier Transform Infra Red
Spectrometry (FTIR) yang pertama kali diajukan oleh Moore dan Robert pada
tahun 1977. Keuntungan dari teknik ini adalah waktu yang relatif cepat, efisien
karena tidak perlu murni, dan dengan tingkat ketelitian yang tinggi dibandingkan
dengan teknik titrimetri atau metode spektroskopi lainnya (Khopkar, 2007).
Gambar 2.4 Spektrum FTIR senyawa kitosan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
16
Puncak tertinggi diukur dari garis dasar yang dipilih. Nilai absorbansi
dapat ditentukan dengan persamaan :
Po
dimana :
A = log ( P
) (1)
A = absorbansi cuplikan
Po = % absorbansi pada garis dasar
P = % absorbansi pada puncak minimum
Derajat deasetilasi ditentukan untuk mengetahui seberapa besar kitin yang
sudah berubah menjadi kitosan. Derajat deasetilasi kitosan ditentukan melalui
persamaan berikut :
DD = 100 – [(A1655 / A 3450 ) x 115] (2)
Nilai 115 menunjukkan rumus empiris berdasarkan data-data yang sudah
dicoba yang menyatakan hubungan yang sama untuk deasetilasi menentukan
derajat deasetilasi secara sempurna (Khan, 2002).
Semakin banyak gugus asetil yang dihilangkan, maka semakin tinggi nilai
derajat deasetilasinya. Kitosan dengan derajat deasetilasi 70-90% dinamakan
kitosan pasaran (Puspawati dan Simpen, 2010).
3. Berat Molekul Rata-rata (BM)
Metode viskosimetri adalah metode yang umum digunakan untuk
menentukan berat molekul rata-rata suatu polimer. Pengukuran berat molekul
rata-rata kitosan dilakukan dengan cara pengukuran viskositas larutan dengan
pembanding viskositas dari pelarut murni (Billmeyer, 1994). Alat yang
digunakaan adalah viskometer Ostwald yaitu dengan cara menghitung lamanya

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
17
waktu yang diperlukan cairan tertentu untuk melalui pipa kapiler dengan gaya
yang disebabkan oleh berat cairan itu sendiri, hal tersebut terjadi akibat adanya
perbedaaan tekanan antara kedua ujung pipa U yang besarnya diasumsikan
sebanding dengan berat jenis cairan (Bird, 1993). Penentuan berat molekul dapat
diketahui melalui persamaan :
η1 − η2
t − to ηsp =
η2 =
to (3)
viskositas spesifik yang diperoleh dapat digunakan untuk menentukan viskositas
intrinsik melalui persamaan Huggins (Billmeyer, 1994) sebagai berikut :
5sp = [5] + k[5′]2 (4)
C
Keterangan :
ηsp : viskositas spesifik
η1 : viskositas pelarut
η2 : viskositas larutan
t : waktu alir larutan (detik)
to : waktu alir pelarut (detik)
η’ : viskositas intrinsik
C : konsentrasi
k : konstanta
untuk menghitung berat molekul rata-rata maka viskositas intrinsic disubstitusikan
kedalam persamaan Mark-Houwink Sakurada, sebagai berikut :
[5′] = KMta (5)

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
18
Nilai K dan a untuk kitosan adalah 1,40 x 10-4 dan 0,83. Dari persamaan
Mark-Houwink Sakurada dapat diperoleh nilai massa molekul rata-rata kitosan
(Mv) (Hwang et al, 2002).
2.4 Kitosan Termodifikasi
Kitosan larut dalam larutan asam, sehingga aplikasinya terbatas, oleh
karena itu perlu adanya modifikasi dari kitosan agar tidak larut dalam media asam.
Modifikasi kitosan dapat dilakukan secara kimiawi maupun fisik. Modifikasi
dapat dilakukan melalui gabungan antara kitosan dengan beberapa polimer lain.
Polimer yang digunakan baik polimer alam maupun polimer sintetik.
Pada perkembangannya modifikasi kitosan yang telah banyak dilakukan
oleh para peneliti adalah dengan cara crosslinked antar rantai atau mengubah
dalam bentuk garamnya. Crosslinked dilakukan menggunakan senyawa dengan
minimal memiliki 2 gugus fungsi aktif. Berbagai bahan kimia yang telah banyak
digunakan sebagai agen crosslink yaitu glutaraldehid (Ruiz et al, 2000),
epiklorohidrin (Vieira dan Beppu, 2006) dan ethyleneglycol diglisidil eter (Li dan
Bai, 2006). Beberapa turunan kitosan telah diperoleh dengan cara menambahkan
gugus fungsional baru untuk membantu meningkatkan selektivitas penyerapan ion
logam. Gugus fungsional yang baru diperoleh dari poli(ethylenimine) (Chassary
et al, 2005), tiourea (Chassary et al, 2004.), melalui crosslinked kitosan.
Menurut Guibal (2004), penambahan gugus fungsional baru yaitu
meningkatkan densitas dari penyerapan logam, mengatur rentang pH, dan
meningkatkan selektivitas terhadap penyerapan logam. Beberapa tahun terakhir,
untuk meningkatkan kapasitas penyerapan logam, beberapa ligan seperti asam

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
19
ethylenediaminetetraacetic (Juang dan Ju, 1998), thicarbamonyl (Baba et al,
2002), dan L-lysine (Fujiwara et al, 2007) digunakan pada pembuatan modifikasi
kitosan crosslinked untuk menghilangkan atau mengurangi ion logam pada
larutan. Selain modifikasi kitosan dengan agen crosslinked, juga telah
berkembang modifikasi dari senyawa polimer lainnya. Salah satunya yaitu MIP
(Molecularly Imprinted Polymer). Kitosan sebagai polimer alam digunakan
dengan mensintesis kitosan dengan katalis TiO2 sebagai adsorben yang tidak
hanya mampu mendegradasi senyawa organik, tetapi juga mampu mengadsorpsi
ion logam berat (Li et al, 2008).
Senyawa turunan kitosan dapat dibuat dengan teknik modifikasi kimia,
seperti grafting (mencangkok/menambahkan gugus fungsi baru), sulfonasi,
carboxymethylation. Diantar teknik tersebut, penambahan gugus fungsi
karboksilat, glutaraldehid, dan urea dianggap menarik dan mampu meningkatkan
sifat adsorpsi dari kitosan. Karboksi metil kitosan dibuat dari reaksi antara kitosan
dengan asam kloroasetat dalam pelarut yang sesuai (Chen et al, 2003).
Gambar 2.5 Mekanisme reaksi karboksi metil kitosan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
20
Glutaraldehid adalah agen crosslinked yang paling banyak digunakan
karena dapat bereaksi dengan kitosan melalui reaksi pembentukan basa Schiff
(imina tersubstitusi, -CH=NR) antara gugus aldehid glutaraldehida dengan gugus
–NH2 kitosan. Kitosan termodifikasi glutaraldehid telah banyak digunakan
sebagai bahan penyerap berbagai logam berat (Cestari et al, 2007).
NH2
O C
N
CH
R H2C 3
O CH
O
* HO
H2C
O
O
N
CH
N
O
CH2
O
OH *
O
CH2 3
R
CH
N
C O
NH2
Gambar 2.6 Mekanisme crosslinked karboksi metil kitosan-glutaraldehid-urea
2.5 Urea
Urea merupakan padatan butiran atau prill yang diperoleh dari hasil sintesa
reaksi antara ammonia (NH3) dengan karbondioksida (CO2). Urea adalah senyawa
organik dengan rumus CON2H4 atau (NH2)2CO. Urea merupakan pupuk nitrogen
yang paling mudah dipakai. Zat ini mengandung nitrogen paling tinggi (46%) di
antara semua pupuk padat. Urea mudah dibuat menjadi butiran dan mudah
diangkut dalam bentuk curah maupun dalam kantong. Zat ini mudah larut didalam
air dan tidak mempunyai residu garam sesudah dipakai untuk tanaman. Kadang-
n

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
21
kadang zat ini juga digunakan untuk pemberian makanan daun. Disamping
penggunaannya sebagai pupuk, urea juga digunakan sebagai tambahan makanan
protein untuk hewan pemamah biak, juga dalam produksi melamin, dalam
pembuatan resin, plastik, adhesif, bahan pelapis, bahan anti kerut, tekstil, dan
resin perpindahan ion. Bahan ini merupakan bahan antara dalam pembuatan
amonium sulfat, asam sulfanat, dan ftalosianina (Austin, 1997).
Urea ditemukan pertama kali oleh Roelle pada tahun 1773 dalam urine.
Pembuatan urea dari amonia dan asam sianida untuk pertama kalinya ditemukan
oleh F.Wohler pada tahun 1828 . Namun pada saat ini pembuatan urea pada
umumnya menggunakan proses dehidrasi yang ditemukan oleh Bassarow pada
tahun 1870. Sifat fisik yang terdapat dalam urea diantaranya adalah berat molekul
sebesar 60,06, dengan berat jenis 1,355 (200C/40C), tidak bermuatan listrik, titik
leleh sebesar 132,7 oC, berbentuk butiran berwarna putih. Urea dapat dibuat dari
amoniak dan karbon dioksida menjadi amonium karbamat, dan dilanjutkan
dengan reaksi lebih lanjut amonium karbamat menjadi urea dan air (Rachman,
2006). Reaksi pembentukan urea sebagai berikut :
2 NH3 + CO2 NH4OCONH2 NH2CONH2 + H2O
(Amonium karbamat) (Urea)
2.6 Logam Berat
Logam adalah unsur alam yang dapat diperoleh dari laut, erosi batuan
tambang, vulkanisme, dan ditemukan dalam bentuk persenyawaan dengan unsur
lain. Pada kondisi suhu ruangan, unsur logam berat tidak selalu berbentuk padat
melainkan ada yang berbentuk cair, misalnya merkuri (Hg). Pada lingkungan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
22
perairan, logam pada umumnya berada dalam bentuk ion-ion, baik sebagai
pasangan ion maupun dalam bentuk tunggal, sedangkan pada lapisan atmosfer
logam ditemukan dalam bentuk partikulat (Palar, 2004). Menurut Palar (2004)
logam memiliki kerapatan yang tinggi, memiliki kemampuan sebagai penghantar
listrik dan panas, dapat membentuk alloy dengan logam yang lain serta dapat
ditempa dan dibentuk.
Dalam perairan, logam berat dapat ditemukan dalam bentuk terlarut dan
tidak terlarut. Logam berat terlarut adalah logam berat yang membentuk komplek
dengan senyawa organik dan anorganik, sedangkan logam berat tidak terlarut
merupakan partikel-partikel koloid yang tersuspensi. Menurut Darmono (2001),
permasalahan yang timbul akibat pencemaran logam berat diantaranya adalah
ancaman kehidupan bagi makhluk hidup, kerusakan ekosistem dan keterkaitan
terhadap estetika (perubahan bau, warna dan rasa air). Akan tetapi bila jumlah dari
logam berat masuk ke dalam tubuh dengan jumlah berlebih, maka akan berubah
fungsi menjadi racun bagi tubuh (Palar, 2004).
2.7 Logam Tembaga (Cu)
Tembaga dengan nomor atom 29 dalam sistem periodik unsur adalah
elemen pertama yang mengandung perak dan emas, sehingga dianggap sebagai
logam semimulia. Unsur Cu berasal dari hasil pelapukan/pelarutan mineral yang
terkandung dalam bebatuan. Kandungan Cu dalam tanahh dan perairan diperoleh
dari industry-industri tembaga, pembakaran batu bara, pembakaran kayu, minyak
bumi dan buangan di area permukiman (Lahuddin, 2007).

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
23
Tembaga (Cu2+) termasuk kedalam logam berat yang sulit untuk
didegradasi. Limbah tembaga (Cu2+) di lingkungan perairan berasal dari industri
elektroplating, industri cat dan kertas, dan industri baja. Meningkatnya kandungan
logam tembaga (Cu2+) (diatas 1.0 mg/L dalam air minum) dapat menimbulkan
gangguan kesehatan, diantaranya anemia, penyumbatan pembuluh darah, dan
kerusakan kornea (Screenivasan dan Rijith, 2009).
2.8 Adsorpsi
Adsorpsi merupakan peristiwa fisik dari permukaan suatu bahan yang
tergantung dari daya gabung antara adsorben dengan zat yang diadsorbsi.
Adsorpsi adalah peristiwa penyerapan pada permukaan suatu adsorben, zat yang
teradsorpsi disebut sebagai adsorbat dan zat pengadsorpsi disebut sebagai
adsorben (House, 2007).
Menurut Adamson (1990), Peristiwa adsorpsi pada umumnya
menggunakan adsorben berupa zat padat. Adsorpsi oleh zat padat dibedakan atas
adsorpsi fisik dan adsorpsi kimia. Adsorpsi fisik terjadi akibat oleh adanya gaya
van der Waals. Pada adsorpsi kimia, molekul-molekul yang teradsorpsi pada
permukaan bereaksi secara kimia, sehingga terjadi pemutusan dan pembentukan
ikatan. Ikatan yang terjadi antara adsorben dan adsorbat cukup kuat, karena
prosesnya bersifat irreversible dan diperlukan energi yang besar untuk melepas
ikatan tersebut. Pada peristiwa adsorpsi secara kimia, umumnya kapasitas adsorpsi
akan meningkat dengan meningkatnya temperatur. Kenaikan temperatur yang
cukup tinggi memungkinkan terjadinya perubahan adsorpsi fisik menjadi kimia.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
24
Macam-macam isoterem adsorpsi antara lain adalah isoterem Langmuir,
isoterm BET, dan isoterem Freundlich. Isoterem Langmuir lebih tepat dijelaskan
sebagai adsorpsi kimiawi, dimana sebuah ikatan kimia ionik atau kovalen
terbentuk antara adsorben dan adsorbat. Isotherm Langmuir merupakan isoterem
paling sederhana yang didasarkan pada asumsi bahwa setiap bagian tempat
adsorpsi adalah ekivalen. Pada isotherm BET, volume total yang teradsorpsi
sebanding dengan jumlah partikel yang teradsorpsi. Sedangkan pada isoterem
Freunlich menghubungkan antara jumlah bahan yang teradsorpsi dengan
konsentrasi bahan dalam larutan (House, 2007).
Faktor yang dapat mempengaruhi proses adsorpsi adalah jenis adsorben,
macam zat yang diadsorpsi, konsentrasi zat, luas permukaan adsorben, dan
temperatur saat proses berlangsung. Zat yang bersifat asam akan mudah di
adsorbs dengan adsorben basa, demikian pula sebaliknya, karena asam dan basa
akan saling tarik-menarik. Begitu juga pada konsentrasi zat, semakin tinggi
konsentrasi, makin besar adsorbat yang dapat teradsorbsi. Pada luas permukaan
adsorben yang besar maka semakin banyak adsorbat yang dapat diserap. Jenis
adsorben yang akan digunakan harus memenuhi beberapa persyaratan seperti,
berupa zat padat dengan daya serap dan luas permukaan yang besar, dan paling
utama adalah tidak larut dalam zat yang akan diadsorpsi (Crittenden, 1998).
2.9 Teknik Adsorpsi Fluidisasi
Pada perkembangan proses adsorpsi telah dikenal berbagai cara pada
proses adsorpsi. Menurut John dan Crittenden (1998) dalam bukunya menjelaskan
bahwa, teknik adsorpsi secara umum yaitu proses batch, fixed bed, dan moving

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
25
bed. Proses batch adalah proses yang banyak digunakan sebagai teknik adsorpsi.
Pada proses batch, cairan dan adsorben diletakkan dalam sebuah wadah (batch)
dengan memberikan pengadukan selama waktu tertentu pada saat proses
berlangsung. Adsorben dipisahkan dari cairan dengan cara sedimentasi atau
filtrasi. Proses batch dapat digambarkan sebagai proses sedimentasi bertingkat,
dimana pada filtrat yang telah dikontakkan dengan adsorben, dipindahkan ke
wadah (batch) lain dengan adsorben baru, sehingga adsorben dapat
menghilangkan pengotor / zat yang sengaja ingin dihilangkan dari filtrat. Proses
ini diulang beberapa kali. Teknik adsorpsi dengan metode batch memiliki
keunggulan yaitu proses pemisahannya yang sangat baik, namun proses batch
yang dilakukan memerlukan jumlah adsorben yang sangat banyak dan tidak dapat
digunakan untuk mengadsorpsi larutan dengan konsentrasi yang besar. Efisiensi
waktu dari proses sedimentasi bertingkat ini juga menjadi salah satu kekurangan
dari proses batch. Sehingga efisiensi waktu dan biaya menjadi bagian yang sangat
dipertimbangkan untuk teknik adsorpsi dengan proses batch. Teknik yang lain
yaitu fixed bed dan moving bed. Kedua teknik ini adalah dengan memberikan
bagian (bed) tetap dan berpindah dari kolom yang digunakan sebagai tempat
kontak antara adsorben dan filtrat. Secara sederhana teknik ini digambarkan
dengan adanya bagian tetap atau bergerak dari kolom yang mampu memberikan
gerakan dari adsorben dalam larutan sehingga proses adsorpsi dapat berjalan.
Kelebihan dari teknik ini sederhana dan relatif murah untuk proses pembuatannya,
karena bagian (bed) yang akan digunakan dapat diatur. Selain itu jumlah adsorben
yang digunakan tidak sebanyak yang diperlukan pada proses batch. Kekurangan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
26
dari proses fixed bed (bagian yang tetap) adalah adsorpsi yang kurang merata dari
filtrat pada seluruh bagian kolom (adsorpsi hanya terjadi pada bagian tertentu
yang dikenal sebagai zona transfer massa), sedangkan pada moving bed (bagian
yang bergerak) memerlukan desain alat yang rumit oleh karena itu diperlukan
biaya yang mahal. Teknik adsorpsi yang belum banyak dikembangkan namun
memiliki kelebihan pada prosesnya yaitu teknik adsorpsi fluidisasi (fluidized bed).
Pada proses ini adsorben dapat bergerak didalam larutan dengan adanya aliran gas
dalam kolom. Laju aliran gas yang diberikan dalam kolom untuk membantu
pergerakan adsorben dapat diatur, sehingga adsorben bergerak keseluruh bagian
kolom (Crittenden, 1998).
Fluidisasi digunakan untuk menggambarkan proses kontak antara solid
dengan fluid. Fluidisasi merupakan operasi pengontakan unggun padatan dengan
fluida sehingga sifatnya berubah menyerupai sifat fluida. Mekanisme adsorpsi
fluidisasi dilakukan dengan mengontakkan larutan limbah dengan adsorben dalam
sebuah kolom, aliran gas diberikan melalui bed distributor udara. Gas yang
dialirkan bertujuan agar butiran adsorben dapat bergerak ke atas dalam kolom
fluidisasi, sehingga logam yang terdapat dalam larutan dapat terserap. Keuntungan
dari proses fluidisasi yaitu aliran dan pertikel dapat terkontrol secara otomatis,
tercampur secara isothermal, sirkulasi padatannya besar, cocok untuk skala besar,
serta panas dan kecepatan transfer masa antar gas dan partikel sangat tinggi
(Crittenden, 1998).

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
27
Gambar 2.7 Kolom fluidisasi
2.10 Spektroskopi FTIR (Fourier Transform Infrared)
Spektrofotometer infra merah adalah suatu metode analisis untuk
mengidentifikasi suatu senyawa berdasarkan absorpsi terhadap infra merah. Pada
prinsipnya spektroskopi Fourier Transform Infrared sama dengan spektroskopi
Infra Red, hanya saja pada pada spektroskopi FTIR ditambahkan alat optic
(Fourier transform) untuk menghasilkan spektra yang lebih baik, sehingga
spektroskopi FTIR dapat menghasilkan spektra yang lebih baik dan menghasilkan
puncak yang diinginkan, dimana pada spektroskopi infra merah puncak tersebut
tidak muncul (Khan, et al, 2002).
Instrumen FTIR dapat digunakan untuk menentukan derajat deasetilasi
(DD) kitosan yang teramati pada spectrum infra merah. Derajat deasetilasi
merupakan salah satu parameter untuk mengetahui kualitas dari kitosan yang
menyatakan besarnya jumlah gugus asetil yang lepas dari kitin pada proses
deasetilasi. Spektrofotometer FTIR memiliki kelebihan dibandingkan
spektrofotometer infra merah, dimana dengan bantuan transformasi fourier akan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
28
meningkatkan sensitifitas pengukuran menjadi lebih tinggi dan waktu analisis
sampel menjadi lebih singkat.
2.11 AAS (Atomic Adsorption Spectrofotometer)
Metode AAS digunakan pada penentuan unsur-unsur logam yang
didasarkan pada penyerapan energi sinar oleh atom-atom netral dalam keadaan
gas. Pada tahun 1955, seorang ilmuwan Australia, Walsh melaporkan hasil
penelitiannya tentang penggunaan lampu katoda sebagai sumber radiasi yang
menghasilkan radiasi dengan panjang gelombang karakteristik yang sesuai dengan
SSA (Ismail, 2003).
Metode spektrometri atom yang paling banyak digunakan adalah
spektrometri serapan atom, merupakan suatu metode pengukuran unsur-unsur
logam dengan identifikasi secara kuantitatif dan kualitatif logam dalam berbagai
sampel, yang didasarkan pada jumlah radiasi yang diserap oleh atom-atom bebas
dalam keadaan gas (Mendham et al, 2000). Spektrometri serapan atom,
spektometri emisi atom dan spektrometri fluorosensi atom merupakan jenis dari
SSA. Spektrometri serapan atom terdiri dari spektrometri serapan atom nyala dan
non nyala. Karena sensitivitas yang tinggi, alat ini sering digunakan sebagai
pilihan utama dalam menganalisis unsur logam yang konsentrasinya sangat kecil.
Penggukuran AAS didasarkan pada besarnya energi radiasi yang diserap
pada panjang gelombang yang sesuai sehingga elektron terluar mengalami eksitasi
dari keadaan dasar ke keadaan tereksitasi. Pembentukan atom-atom pada keadaan
dasar atau proses atomisasi pada umumnya dilakukan dalam nyala, dimana
cuplikan sampel yang mengandung logam (M) sebagai ion M+ dalam bentuk

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
hokum Lambert-Beer yang menyatakan bahwa jumlah energi yang diserap
(absorbansi) adalah sebanding dengan konsentrasi (C) (Khopkar, 2007).
M+ + A- (larutan) M A (padat)
Mo (gas) M A (cair)
Gambar 2.8 Proses atomisasi pada AAS
M+ + A- (aerosol)
Mo + Ao (gas) M A (gas)
29
larutan garam M+ dan A- akan melalui serangkaian proses dalam nyala, sebelum
akhirnya menjadi atom logam dalam keadaan dasar (Mo). Atom-atom dalam
keadaaan dasar akan menyerap energi, sumber energi berasal dari lampu katoda
berongga dimana jumlah energi yang diserap adalah sebanding dengan
konsentrasi atom-atom dalam sampel. Penentuan konsentrasi unsur logam dalam
sampel dapat dilakukan dengan bantuan kurva kalibrasi. Hal ini sesuai dengan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Kimia Fisik, Departemen
Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga pada bulan Januari
2012 sampai dengan Juli 2012.
3.2 Bahan dan Alat Penelitian
3.2.1 Bahan-bahan penelitian
Sampel yang digunakan pada penelitian ini adalah cangkang rajungan.
Bahan lain yang digunakan berupa natrium hidroksida (NaOH) teknis (98%),
asam klorida (HCl) teknis, asam kloroasetat p.a, asam asetat teknis, aseton teknis,
glutaraldehid p.a, urea p.a, tembaga(II)sulfat (CuSO4.5H2O), etanol teknis, asam
nitrat p.a, 2-propanol p.a.
3.2.2 Alat-alat penelitian
Alat-alat yang digunakan pada penelitian ini adalah gelas beaker, labu
ukur, gelas ukur, corong Buchner, pengayak mesh, krus porselen, neraca analitik,
hotplate stirrer, kolom fluidisasi (fluidized bed), spektofotometer FT-IR, Atomic
Adsorption Spectrofotometer (AAS).
30

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
31
Uji kelarutan
Uji
deasetilasi
Penentuan
BM
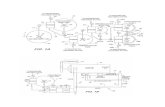
Kitin
Kitosan
1. Deproteinasi dengan larutan NaOH 3,5% pada
65oC selama 2 jam
2. Demineralisasi dengan larutan HCl 2N selama
30 menit
3. Depigmentasi dengan aseton
Deasetilasi dengan larutan NaOH 50% pada suhu
> 95oC selama 2 jam
1. 10,0 gr Kitosan dilarutkan dalam 100 ml asam
asetat 2% dan 13,5 gr NaOH direaksikan pada
suhu 50oC selama 1 jam
2. Kitosan ditambahkan 15,0 gr asam kloroasetat
dalam 20 ml isopropanol,dan direaksikan pada
suhu 50oC selama 4 jam, kemudian bilas
dengan etanol 70-90% hingga netral Karboksi metil kitosan
Analisis
dengan FT-IR
Kitosan-Urea
Uji BET
1. Larutan glutaraldehid-urea 3,0 gr urea dalam 60 ml akuades dan dilarutkan
dalam 17,1 ml glutaraldehid. Larutan
direaksikan pada 50oC selama 3 jam
2. 1,36 gr CMC dalam 30 ml akuades direaksikan
dengan larutan glutaraldehid-urea pada suhu
80oC selama 8 jam
0,5 gram kitosan-urea dalam kolom fluidisasi
dengan ditambahkan 200 ml Larutan CuSO4.5H2O
100 ppm
3.3 Diagram Kerja
Dicuci
Dikeringkan
Ditumbuk
Sampel cangkang rajungan
Adsorpsi logam dengan
metode adsorpsi fluidisasi
dengan waktu interaksi
selama 20; 40; 60; 80; 100
menit
Hasil adsorpsi Filtrat dianalisis dengan
AAS, adsorben dianalisis
dengan uji BET

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
32
3.4 Pembuatan Reagen
1. Pembuatan larutan NaOH 3.5 % (w/v) untuk proses deproteinasi
Sebanyak 43,75 gram NaOH 80% ditimbang, dan dilarutkan dengan
akuades dalam gelas beker 1000 ml. Kemudian diaduk dan ditambahkan
akuades hingga volume larutan 1000 ml.
2. Pembuatan larutan HCl 2N (v/v) untuk proses demineralisasi
Pada pembuatan larutan HCl 2N dipipet sebanyak 191,75 ml larutan HCl
32% menggunakan pipet ukur. Kemudian dilarutkan dalam gelas beker
1000 ml menggunakan akuades hingga volume larutan menjadi 1000 ml.
3. Pembuatan larutan NaOH 50 % untuk proses deasetilasi
Sebanyak 625 gram NaOH 80% ditimbang, dan dilarutkan dengan akuades
dalam gelas beker 1000 ml. Kemudian larutan dipindahkan kedalam labu
ukur 1000 ml dan diencerkan dengan menambahkan akuades sampai tanda
batas. Kocok larutan dalam labu ukur hingga larutan menjadi larutan yang
homogen.
4. Pembuatan larutan asam asetat 2 %
Sebanyak 2,02 ml larutan asam asetat 98% diambil dengan menggunakan
pipet ukur, kemudian dipindahkan kedalam labu ukur 100 ml dan
diencerkan dengan menambahkan akuades hingga tanda batas.
5. Pembuatan larutan induk Cu2+ 1000 ppm
Larutan induk 1000 ppm dibuat dengan cara menimbang sebanyak 3,9291
gram CuSO4.5H2O yang dilarutkan dengan asam nitrat pekat sebanyak

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
33
10,0 ml dalam gelas beker 100 ml. Kemudian dipindahkan dalam labu
ukur 1000 ml dan diencerkan dengan akuadem hingga tanda batas.
6. Pembuatan larutan induk Cu2+ 100 ppm
Diambil 10,0 ml larutan induk Cu2+ 1000 ppm menggunakan pipet
volume. Kemudian dipindahkan secara kuantitatif kedalam labu ukur 100
ml dan diencerkan dengan akuadem hingga tanda batas.
7. Pembuatan larutan kerja Cu2+ 10 ppm
Diambil 2,5 ml larutan induk Cu2+ 100 ppm menggunakan pipet volume.
Kemudian dipindahkan secara kuantitatif kedalam labu ukur 25 ml dan
diencerkan dengan akuadem hingga tanda batas.
8. Pembuatan larutan standar Cu2+ 2 ppm
Diambil 0,5 ml larutan kerja Cu2+ 100 ppm menggunakan pipet volume.
Kemudian dipindahkan secara kuantitatif kedalam labu ukur 25 ml dan
diencerkan dengan akuadem hingga tanda batas.
9. Pembuatan larutan standar Cu2+ 4 ppm
Diambil 1,0 ml larutan kerja Cu2+ 100 ppm menggunakan pipet volume.
Kemudian dipindahkan secara kuantitatif kedalam labu ukur 25 ml dan
diencerkan dengan akuadem hingga tanda batas.
10. Pembuatan larutan standar Cu2+ 6 ppm
Diambil 1,5 ml larutan kerja Cu2+ 100 ppm menggunakan pipet volume.
Kemudian dipindahkan secara kuantitatif kedalam labu ukur 25 ml dan
diencerkan dengan akuadem hingga tanda batas.
11. Pembuatan larutan standar Cu2+ 8 ppm

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
34
Diambil 2,0 ml larutan kerja Cu2+ 100 ppm menggunakan pipet volume.
Kemudian dipindahkan secara kuantitatif kedalam labu ukur 25 ml dan
diencerkan dengan akuadem hingga tanda batas.
12. Pembuatan larutan standar Cu2+ 10 ppm
Diambil 2,5 ml larutan kerja Cu2+ 100 ppm menggunakan pipet volume.
Kemudian dipindahkan secara kuantitatif kedalam labu ukur 25 ml.
3.5 Prosedur Penelitian
3.5.1 Preparasi serbuk cangkang rajungan
Cangkang rajungan dicuci hingga bersih dari kotoran yang menempel,
kemudian dijemur dengan tidak terkena sinar matahari langsung, yaitu dengan
cara dianginkan. Setelah kering, cangkang kepiting digiling dengan menggunakan
blender, kemudian diayak menggunakan pengayak mesh hingga diperoleh serbuk
halus.
3.5.2 Pembuatan kitosan dari kitin
Tahapan yang dilakukan pada proses isolasi kitin yaitu melalui tahap
deproteinasi, demineralisasi, depigmentasi, dan tahap transformasi kitin menjadi
kitosan melalui tahap deasetilasi.
Deproteinasi adalah tahap pemisahan protein yang terdapat pada cangkang
rajungan. Serbuk cangkang rajungan yang telah kering, diayak dengan pengayak
100 mesh, dan dimasukkan dalam gelas beaker. Kemudian ditambahkan NaOH
3,5% (b/v) dengan perbandingan 1:10 antara serbuk cangkang rajungan dengan
larutan NaOH. Kemudian diaduk mengguankan stirrer magnetic, dengan
pemanasan pada suhu 65oC selama 2 jam. Larutan disaring dengan corong

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
35
Buchner dan kertas saring sehingga diperoleh residunya. Kemudian cuci residu
dengan akuades hingga pH netral, kemudian dikeringkan dalam oven pada suhu
50oC selama 24 jam. Tahapan kedua yaitu demineralisasi, tujuan demineralisasi
adalah untuk menghilangkan mineral dari sampel. Sampel hasil deproteinasi
dimasukkan dalam gelas beaker dan ditambahkan larutan HCl 2N dengan
perbandingan 1:15 antara sampel dengan HCl. Pada proses ini dilakukan pada
suhu ruangan selama 30 menit sambil diaduk menggunakan magnetic stirrer.
Kemudian larutan disaring dan residunya dicuci dengan akuades hingga pH netral.
Residu yang diperoleh dkeringkan dalam oven pada suhu 50oC selama 24 jam.
Tahap selanjutnya pada proses pembuatan kitin adalah depigmentasi,
depigmentasi aadalah tahap penghilangan warna. Hasil sampel yang diperoleh
dari tahap demineralisasi, di rendam dalam larutan aseton dengan perbandingan
1:10 antara sampel dengan larutan aseton. Kemudian disaring dan endapan yang
diperoleh dicuci dengan akuades hingga pH netral. Sampel disaring dan
dikeringkan dalam oven pada suhu 65oC selama 24 jam. Hasil yang diperoleh
setelah melalui tiga tahapan ini adalah kitin.
Pada tahap deasetilasi, kitin yang diperoleh dimasukkan dalam gelas
beaker dan ditambahkan larutan NaOH 50% dengan perbandingan 1:10 antara
kitin dan larutan NaOH. Larutan dipanaskan pada suhu diatas 95oC selama 2 jam.
Larutan disaring dan residu yang diperoleh dicuci dengan akuades hingga pH
netral. Hasil yang diperoleh setelah tahap ini adalah kitosan.
Penentuan derajat deasetilasi (DD) kitosan dianalisis dengan menggunakan
Fourier Transformation Infra Red Spectroscopy (FT-IR).

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
36
3.5.3 Karakterisasi kitin dan kitosan
Penentuan derajat deasetilasi kitin dengan menggunakan FT-IR dan uji
kelarutan dengan cara menambahkan kitin dengan asam asetat 2%.
1. Uji kelarutan kitosan
Kelarutan kitosan dapat dianalisis dengan cara melarutkan kitosan dalam
asam asetat 2%. Apabila serbuk tersebut tidak larut maka serbuk tersebut
adalah kitin. Sedangkan kitosan larut dalam asam asetat encer (Kuntoro,
2004).
2. Penentuan berat molekul rata-rata
Metode viskosimetri adalah metode yang umum digunakan untuk
menentukan berat molekul rata-rata suatu polimer. Alat yang digunakan
adalah viskometer Ostwald yaitu dengan cara menghitung lamanya waktu
yang diperlukan cairan tertentu untuk melalui pipa kapiler. Penentuan
berat molekul rata-rata kitosan dilakukan berdasarkan metode viskosimetri
dengan menentukan waktu alir pelarut asam asetat (to) dan waktu alir
larutan kitosan (t) sehingga nilai viskositas spesifik (ηsp). Larutan kitosan
dibuat dengan cara melarutkan 0,15 gram kitosan kedalam 100 ml asam
asetat 0,75% (w/v) dan dimasukkan dalam labu ukur 100 ml, kamudian
diencerkan dengan variasi konsentrasi 0,1 ; 0,2 ; 0,3 ; 0,4 A . Kemudian
masing-masing larutan dimasukkan kedalam viskometer Ostwald
sebanyak 5,0 ml dan diukur waktu alirnya (t1). Begitu pula pada larutan
asam asetat (to). Untuk menentukan berat molekul rata-rata kitosan ( Mv )
ditentukan mengikuti persamaan Mark-Houwink Sakurada (Persamaan 5 )

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
37
dengan nilai K dan a untuk kitosan adalah 1,40 x 10-4 dan 0,83 (Hwang et
al, 2002). Dari persamaan Mark-Houwink Sakurada dapat diperoleh nilai
massa molekul rata-rata kitosan (Mv).
3. Penentuan derajat deasetilasi kitosan
Pada penentuan derajat deasetilasi digunakan spektroskopi FT-IR. Derajat
deasetilasi ditentukan dengan metode baseline, dihitung dari nilai
perbandingan pita serapan antara puncak absorbansi gugus hidroksil
disekitar 3450 cm-1 dan puncak absorbansi gugus amida pada 1655 cm-1.
Kemudian buat garis lurus dari 4000 cm-1 hingga 2500 cm-1 sebagai garis
dasar bagi gugus hidroksil dan 1800 cm-1 sampai 1600 cm-1 sebagai garis
dasar bagi gugus amida. Derajat deasetilasi ditentukan untuk mengetahui
seberapa besar kitin yang sudah berubah menjadi kitosan. Derajat
deasetilasi kitosan ditentukan melalui persamaan 2. Pada penelitian ini
derajat deasetilasi kitin dan kitosan dihitung menggunakan software DDK
project (Iflakhah, 2011).
3.5.4 Pembuatan kitosan-urea
1. Pembuatan karboksi metil kitosan
Sebanyak 10,00 gr kitosan dilarutkan dengan 100 ml asam asetat 2%, dan
ditambahkan 13,5 gram NaOH dalam gelas beaker 500 ml, kemudian
direaksikan diatas penangas air dengan suhu 50oC selama 1 jam. Setelah 1
jam, ditambahkan 15,0 gr asam kloroasetat yang telah dilarutkan dalam 20
ml isopropanol. Kemudian dicampurkan tetes demi tetes kedalam gelas
beaker yang berisi larutan kitosan. Campuran tersebut direaksikan selama

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
38
4 jam dengan suhu 50oC. Reaksi dihentikan dengan menambahkan 200 ml
etanol 70%. Kemudian dikeringkan pada suhu kamar. Hasil yang diperoleh
yaitu karboksi metil kitosan dikarakterisasi menggunakan FTIR (Chen dan
Park, 2003).
2. Pembuatan karboksi metil kitosan dan glutaraldehid-urea
Sebanyak 3,0 gram urea dilarutkan dalam 60 ml akuades, dan ditambahkan
17,1 ml 50% (v/v) glutaraldehid dalam labu alas bulat. Kemudian diaduk
dengan magnetic stirrer dan dipanaskan pada suhu 50oC selama 3 jam.
Setelah 3 jam ditambahkan 1,36 gram karboksi metil kitosan yang telah
dilarutkan dalam 30 ml akuades. Endapan yang diperoleh dibilas dengan
NaOH 0,1 M, akuades dan aseton. Residu yang diperoleh dikeringkan
pada suhu suhu 65oC selama 2 jam. Pada pembuatan kitosan-urea
diberikan variasi terhadap massa urea yang digunakan yaitu 3,0; 6,0 dan
9,0 gram urea. Sehingga diperoleh 3 variasi kitosan-urea.
Hasil yang diperoleh dikarakterisasi dengan menggunakan FT-IR dan
digunakan sebagai adsorben ion logam Cu2+ (Sun dan Wang, 2005).
3.5.5 Proses adsorpsi
Kitosan-urea digunakan sebagai adsorben logam berat melalui metode
adsorpsi fluidisasi. Pada penelitian ini kolom adsorpsi dibuat dengan skala
laboratorium dari modifikasi labu ukur 250 ml, dengan diameter kolom sebesar 5
cm dan kasa penahan butiran pada jarak 5 cm dari dasar kolom, dan aliran gas
berasal dari pompa gas akuarium.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
39
5 cm
Gambar 3.1 Kolom fluidisasi pada penelitian
Larutan logam Cu2+ 100 mg/L dan adsorben kitosan-urea sebanyak 0,5
gram dimasukkan ke dalam kolom fluidisasi. Larutan logam Cu2+ dan adsorben
kitosan-urea diinteraksikan dengan variasi waktu kontak selama 20, 40, 60, 80,
dan 100 menit. Kemudian campuran larutan logam Cu2+ dengan kitosan-urea
disaring dan konsentrasi larutan logam Cu2+ setelah proses adsorpsi di analisis
dengan AAS. Pada penentuan konsentrasi larutan logam Cu2+ dilakukan dengan
cara membandingkan larutan logam terhadap larutan standarnya.
3.5.6 Penentuan kapasitas adsorpsi logam Cu2+ dalam kitosan-urea
Kapasitas ion logam yang teradsorpsi pada saat kesetimbangan berdasarkan
neraca massa, dapat dihitung dengan persamaan berikut :
q1= V(Co – Ce) / m (6)
(Laus et al, 2005).
Keterangan :
Co : Konsentrasi awal (mg/L)
Ce : Konsentrasi akhir (mg/L)
V : volume larutan (L)
Massa : massa adsorben (gram)

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
40
3.5.7 Penentuan ukuran pori adsorben kitosan-urea
Distribusi ukuran pori dari suatu adsorben pada saat proses adsorpsi
dianalisis menggunakan BET. Analisa BET bertujuan untuk mengetahui ukuran
pori, luas area permukaan adsorben, volume total pori, dan ditribusi ukuran pori
dari adsorben.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Preparasi Serbuk Cangkang Rajungan
Cangkang rajungan perlu dipreparasi terlebih dahulu agar mempermudah
proses isolasi kitin. Cangkang rajungan diperoleh dari Pantai Ngamboh,
Lamongan. Cangkang yang diperoleh masih dalam keadaan basah, kemudian
dicuci dengan air hingga bersih dari kotoran dan sisa daging yang masih
menempel. Langkah berikutnya adalah mengeringkan cangkang rajungan di
bawah sinar matahari untuk mengurangi kandungan air sehingga menjadi awet
dan mudah disimpan. Cangkang rajungan yang telah kering kemudian digiling
dan ditumbuk. Proses penggilingan dilakukan dengan tujuan memperbesar luas
permukaan agar mudah dalam proses interaksi dengan pereaksi pada proses isolasi
kitin.
Gambar 4.1 Serbuk cangkang rajungan
4.2 Hasil Pembuatan Kitosan dari Kitin
4.2.1 Tahap isolasi kitin dari cangkang rajungan
Terdapat tiga tahapan yang dilakukan pada proses isolasi kitin dari
cangkang rajungan, yaitu deproteinasi, demineralisasi dan depigmentasi.
41

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
42
Deproteinasi adalah proses pemisahan protein melalui reaksi hidrolisis
menggunakan larutan basa, yaitu NaOH (Khor, 2010). Pada penelitian ini serbuk
cangkang rajungan direaksikan dengan larutan NaOH dengan konsentrasi 3,5%
dengan perbandingan 1:10 (w/v). Proses reaksi dilakukan pada suhu 65oC selama
2 jam sambil diaduk menggunakan pengaduk magnetik. Pada deproteinasi, protein
diubah menjadi natrium proteinat yang larut dalam air (Sugita, 2009) dan proses
deproteinasi dapat ditandai dengan terjadinya perubahan warna dari serbuk
cangkang rajungan semula berwarna putih menjadi kemerahan, hal ini akibat
adanya pelepasan pigmen cangkang rajungan (Mahmoud, 2007).
NH2 O
H OH
H O
HO
H H NH
H O C
H
O H
H
C OH
H O
NH
H + NaOH
OH O C OH OH O C OH
CH3 CH3
H OH
H O
HO
H H NH
H OH
H O
O H
H NH
+ NaO H
NH2 O
C C OH
H
OH O C OH
CH3
OH
kitin
O C OH
CH3
asam amino
Gambar 4.2 Reaksi deproteinasi
Struktur kitin dari cangkang rajungan mengandung protein, Protein
dipisahkan dengan penambahan larutan basa NaOH. Atom hidrogen (-H) dari
NaOH mensubstitusi atom oksigen pada C-6 kitin, sehingga terbentuk gugus baru
yaitu hidroksil pada C6 kitin. Senyawa yang diperoleh setelah tahap deproteinasi
merupakan crude kitin, karena kitin di dalam cangkang luar dari rajungan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
43
mengandung kalsium karbonat (CaCO3) dan protein (Khor, 2010). Dari 565 gram
serbuk rajungan diperoleh 375 gram crude kitin. Pengurangan berat pada tahap
deproteinasi ini sebesar 33,62%, hal ini disebabkan oleh lepasnya protein yang
terkandung dalam serbuk rajungan sangat banyak dan larut dalam NaOH, serta
sebagian massa crude kitin yang hilang pada proses netralisasi dan penyaringan.
Tahap kedua pada isolasi kitin adalah demineralisasi, yaitu tahap
penghilangan senyawa anorganik dan mineral yang terkandung dalam cangkang
rajungan. Mineral terbanyak berupa CaCO3 sebanyak 50% dan Ca3(PO4)2
sebanyak 10% (Khor, 2010). Senyawa CaCO3 lebih mudah dipisahkan
dibandingkan dengan protein (Sugita,2009). Tahap demineralisasi dilakukan
dengan cara mereaksikan sedikit demi sedikit crude kitin ke dalam larutan HCl
2N dengan perbandingan 1:15 (w/v) selama 30 menit. Reaksi yang terjadi adalah
sebagai berikut.
CaCO3(s) + 2HCl(aq) CaCl2(aq) + H2O(l) + CO2(g)
Ca3(PO4)2(s) + 4HCl(aq) CaCl2(aq) + Ca(H2PO4)2(l)
H OH
HO
H
H
OH
H OH
H O
O H
NH H
OH OH
C CH3
H O
NH
O C OH
CH3
+ HCl
OCaCO3
H OH
H O
HO
H H NH
H OH
H O
O H
H NH
+ CaCl2 + CO2 + H2O
OH O C OH OH O C OH
CH3 CH3
Gambar 4.3 Reaksi demineralisasi

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
44
Hasil yang diperoleh pada tahap ini disebut sebagai kitin. kitin yang
diperoleh pada tahap ini berupa serbuk berwarna coklat, sehingga dilakukan tahap
depigmentasi. Pada tahap depigmentasi, kitin ditambah dengan aseton dengan
perbandingan 1:10 (b/v) yang direaksikan pada suhu ruang selama 30 menit. Hasil
dari tahap depigmentasi diperoleh serbuk kitin yang berwarna coklat kekuningan.
Dari berat awal 375 gram crude kitin diperoleh kitin sebesar 160 gram.
Pengurangan berat yang terjadi adalah sebesar 57,33%. Hal ini disebabkan karena
mineral-mineral dari crude kitin larut dalam HCl serta hilangnya massa pada saat
netralisasi dan penyaringan.
4.2.2 Hasil transformasi kitin menjadi kitosan
Tahap transformasi kitin menjadi kitosan disebut sebagai tahap deasetilasi.
Tahap deasetilasi bertujuan untuk mengubah gugus asetamida pada kitin menjadi
gugus amina melalui proses hidrolisis. Sehingga kitosan yang terbentuk menjadi
lebih reaktif daripada kitin dan mudah larut dalam asam asetat 2% (Khor, 2010).
Pada proses deasetilasi digunakan larutan basa NaOH 50% dengan perbandingan
berat kitin dan NaOH 50% sebesar 1:10 (w/v). Menurut Khor (2010), tingginya
konsentrasi NaOH menyebabkan gugus fungsi amino (-NH2) yang mensubstitusi
gugus asetil kitin dalam larutan semakin aktif, sehingga semakin banyak gugus
asetamida yang diubah menjadi gugus amina. Deasetilasi optimum akan tercapai
pada larutan NaOH 50% dengan suhu pemanasan 95oC selama 2 jam. Mekanisme
reaksi yang terjadi pada deasetilasi kitin menjadi kitosan menggunakan NaOH
50% ditunjukkan pada Gambar 4.4.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
45
H O
H H NH
OH O C OH
H O
H H NH
OH O C OH
H O
H H NH
OH O C OH
H H OH
HO
O
+ NaOH
H OH
HO
H OH
H O
O H
H NH
CH3
CH3
CH3
OH NaO
C
CH3
OH
OH-
H OH
H O
HO
H OH
H O
H OH
H O
H OH
H O H O H
H NH HO
H NH2 H O H
OH O C OH OH OH
NaO C O
H
OH O
NH
C OH
H NH
OH OH CH3
CH3
CH3
NaO C O H CH3
H OH
HO
H H
OH
H O
NH2
OH
H OH
O H H
OH
H O
NH2
OH
O
+ H3C C
ONa
Gambar 4.4 Reaksi deasetilasi
Kitin yang mengandung gugus N-asetil (-NHCOCH3, asetamida) (Kim,
2011) digantikan dengan atom hidrogen dari basa NaOH melalui reaksi hidrolisis.
Pada awal reaksi gugus –OH dari basa NaOH menyerang atom C dari asetamida.
Atom –NH yang kurang stabil mengikat atom hidrogen sehingga terbentuk gugus
amina –NH2.
Hasil yang diperoleh dari proses deasetilasi adalah serbuk kitosan yang
berwarna putih. Dari proses ini diperoleh kitosan sebesar 55 gram dari 160 gram
kitin yang ditranformasikan menjadi kitosan. Pengurangan berat yang terjadi
sebesar 65,62% .

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
46
Gambar 4.5 Serbuk kitosan
4.3 Hasil Karakterisasi Kitin dan Kitosan
Karakterisasi kitin dan kitosan meliputi kelarutan dalam asam asetat 2%
dan analisis gugus fungsi asetamida menggunakan spektrofotometer FT-IR untuk
menentukan derajat deasetilasi (DD) kitin. Kitosan dan penentuan berat molekul
kitosan menggunakan Viscometer Ostwald.
4.3.1 Hasil uji kelarutan kitosan
Uji kelarutan kitin dan kitosan dalam larutan asam asetat 2% merupakan
uji paling sederhana. Kitosan larut sempurna dalam larutan asam asetat 2%
sedangkan kitin tidak dapat larut dalam asam asetat 2% (Kuntoro, 2004). Pada
penelitian ini hasil kitosan dilarutkan dalam asam asetat 2% dan kitosan dapat
larut dengan sempurna. Hal ini dapat terjadi akibat adanya gugus amina pada
kitosan yang dapat membentuk ikatan hidrogen antara H+ dari asam asetat dan N
dari amina yang memiliki elektron bebas. Sedangkan, pada kitin tidak dapat larut
dalam asam asetat 2%.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
47
Gambar 4.6 Kelarutan kitin (a) dan kitosan (b)
4.3.2 Hasil penentuan berat molekul rata-rata kitosan
Berat molekul rata-rata kitosan dapat diukur menggunakan metode
Viskosimetri yaitu menggunakan Viscometer Ostwald. Pengukuran dilakukan
dengan memberikan variasi konsentrasi kitosan terhadap pelarutnya, yaitu asam
asetat 2%. Kitosan dengan rumus molekul (C8H13NO5)n, dengan n berkisar antara
2000-3000 monomer (Kurita, 1998). Berdasarkan hasil perhitungan penentuan
berat molekul kitosan, diperoleh persamaan garis y = 399.8x + 8.370, sehingga
dengan menggunakan persamaan Mark Houwink-Sakurada diperoleh berat
molekul kitosan rata-rata pada penelitian sebesar 568.727,53 gr/mol. Nilai
tersebut telah memenuhi rentang berat molekul rata-rata kitosan komersil yaitu
190.000 – 700.000 gr/mol (Khor, 2010). Data perhitungan penentuan berat
molekul rata-rata kitosan ditunjukkan pada Lampiran 2.
4.3.3 Hasil penentuan derajat deasetilasi dengan spektroskopi Fourier
Transform Infra Red (FTIR)
Uji spektroskopi IR digunakan untuk menganalisa gugus fungsi dan
menentukan derajat deasetilasi (DD) dari kitin dan kitosan. Pada penelitian ini
analisa gugus fungsi menggunakan Fourier Transform Infra Red Spectrometry

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
48
Gambar 4.7 Spektrum FT-IR kitin
Tabel 4.1 Gugus fungsi dan bilangan gelombang senyawa kitin dan kitosan
(FTIR) karena lebih cepat, efisien dan memiliki ketelitian serta sensitifitas lebih
tinggi dibandingan menggunakan spektroskopi IR biasa (Khopkar, 2007).
Preparasi kitin dan kitosan dilakukan dengan cara membuat pellet KBr dengan
perbandingan 1:10 (w/w). KBr digunakan karena sel tempat cuplikan sampel
harus terbuat dari bahan yang dapat ditembus oleh sinar infra merah, seperti NaCl
dan KBr. Hasil spektrum FTIR dari senyawa kitin ditunjukkan pada Gambar 4.7.
Literatur
(Pretsch dan Buhlmann, 2006)
Penelitian
Kitin Kitosan
Gugus fungsi Bilangan
gelombang
(cm-1)
Intensitas Bilangan
gelombang
(cm-1)
Bilangan
gelombang
(cm-1)
Alkohol
O-H st
N-H st
C-O st
3650 – 3200
≈ 3300
1260 – 970
Bervariasi
Kuat
Kuat
3448.72
3271.27
1072.42
3448.72
3448.72
1087.85
Amida -C=O
HN-C=O (2o)
H2N-C=O (1o)
1655 – 1630
≈ 1530
≈ 1690
Kuat
1 peak
2 peak
1627.92
1550.77
-
1658.78
-
1658.78

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
49
Berdasarkan spektrum FTIR kitin tersebut terdapat pita tajam yang khas
untuk gugus karbonil amida (-C=O) pada bilangan gelombang 1627.92 cm-1.
Selain itu terdapat pita serapan untuk gugus hidroksi (-OH) pada bilangan
gelombang 3448.72 cm-1 , gugus nitrogen (-NH) pada 3271.27 cm-1 dan pita
serapan untuk ikatan C-O terdapat pada daerah 1072.42 cm-1.
amida (-C=O) pada bilangan gelombang 1658.78 cm-1. Pada spektrum FTIR
kitosan terdapat pita serapan amina primer (-NH2), 2 puncak pada daerah 1658.78
cm-1 . sedangkan gugus hidroksil (-OH) tetap muncul pada bilangan gelombang
3448.72 cm-1 dan pita serapan untuk ikatan C-O terdapat pada daerah 1087.85 cm-
1. Berdasarkan spektra FTIR diatas terjadi transformasi kitin menjadi kitosan
ditunjukkan hilangnya serapan gugus amida sekunder di 1560.77 cm-1 dan
Gambar 4.8 Spektrum FT-IR kitosan
Pada spektrum FTIR kitosan tidak terlihat pita serapan gugus karbonil

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
50
terdapat serapan di 1658.78 cm-1 dengan dua puncak sebagai ciri khas amida
primer.
Berdasarkan spektrum kitin dan kitosan, maka dapat ditentukan derajat
deasetilasi dari kedua senyawa menggunakan metode baseline (Khan, 2002).
Hasil perhitungan menggunakan metode baseline diperoleh derajat deasetilasi
untuk kitin sebesar 43,53% dan derajat deasetilasi kitosan sebesar 84,42%.
Menurut Puspawati dan Simpen (2010), kitosan memiliki derajat deasetilasi diatas
70%.
4.4 Hasil Pembuatan Kitosan-urea
4.4.1 Hasil pembuatan karboksi metil kitosan
Kitosan urea dibuat dengan tahapan awal yaitu pembuatan karboksi metil
kitosan. Kelarutan bergantung pada struktur molekul dan jenis pelarut yang
digunakan. Kelarutan kitosan memiliki pengaruh yang sangat penting pada
aplikasi kitosan dalam proses karboksi metilasi (Chen dan Park, 2003). Karboksi
metil kitosan merupakan senyawa turunan eter (-C-O-C-) dan mengandung gugus
–COOH serta –NH2 didalam struktur molekulnya (Chen dan Park, 2003).
Langkah pembuatan karboksi metil kitosan menurut Chen dan Park,
(2003) yaitu kitosan hasil sintesis yang dilarutkan ke dalam asam asetat 2% dan
ditambahkan dengan NaOH. Campuran larutan tersebut dipanaskan, pemanasan
dilakukan untuk mempercepat reaksi. Reaksi dihentikan dengan penambahan
etanol 70%. Kemudian ditambahkan asam kloroasetat yang telah dilarutkan dalam
isopropanol, kemudian dipanaskan dalam penangas air pada suhu 50oC.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
51
Pada penelitian Chen dan Park, (2003) menyatakan bahwa tingginya
temperatur pada preparasi karboksi metil kitosan memberikan pengaruh dari
peningkatan hasil karboksi metil kitosan yang dibuat. Residu yang diperoleh
merupakan garam Na-karboksi metil kitosan. Untuk menghilangkan kandungan
garam tersebut, ditambahkan etanol 80% dan HCl pekat 37%, sehingga diperoleh
karboksi metil kitosan dan garam NaCl. Hasil karboksi metil kitosan yang
diperoleh sebanyak 9,64 gram.
Penggunaan pelarut yang sesuai yaitu isopropanol dengan penambahan
asam kloroasetat pada temperatur reaksi yang tinggi menjadikan gugus karboksi
metil lebih banyak mensubstitusi pada atom –H dari gugus –OH pada kitosan.
Semakin tinggi substituen dari hasil karboksi metil kitosan yang diperoleh
memberikan dampak pada kelarutan karboksi metil kitosan, yaitu kelarutannya
berada pada rentang pH asam hingga netral (pH 3-7) (Chen dan Park, 2003).
Tujuan utama dari pembentukan karboksi metil kitosan adalah
memodifikasi secara kimia dengan panambahan gugus fungsi baru. Struktur
karboksi metil kitosan hasil pembuatan ditunjukkan pada Gambar 4.10.
Gambar 4.9 Karboksi metil kitosan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
52
O O O
H2 H2 H2
H O C C OH H O C C OH H O C C OH
H O H O H O
H O H
H NH2 H
OH OH OH
O H
NH2 H
OH OH
NH2
OH
Gambar 4.10 Struktur senyawa karboksi metil kitosan
Karakterisasi senyawa hasil pembuatan karboksi metil kitosan dianalisis
menggunakan FT-IR. Gambar 4.11 merupakan spektrum dari karboksi metil
kitosan.
Gambar 4.11 Spektrum FT-IR Karboksi metil kitosan
Beberapa gugus fungsi yang muncul pada spektrum FT-IR dari karboksi
metil kitosan ditunjukkan pada Tabel 4.2.
O O
n

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
53
Tabel 4.2 Gugus fungsi dan bilangan gelombang senyawa organik dan
karboksi metil kitosan
Literatur (Pretsch dan Buhlmann, 2006)
Karboksi metil kitosan pada penelitian
Gugus fungsi Bilangan
gelombang
(cm-1)
Intensitas Bilangan
gelombang
(cm-1)
Intensitas
Alkohol
O-H st
O-H polimer
N-H st
3650 – 3200
3500 – 3200
≈ 3300
Bervariasi
Melebar
Kuat
3448.72
3448.72
3417.86
Melebar
Melebar
Eter CH2-O- CH2
1150 – 1085
Lemah
1087.85
Lemah
Asam karboksilat
COOH st
C=O st
3550 – 2500
1740 – 1650
3500 – 2500
1720.50
Melebar
Nitrogen -NH2
1650 – 1590
Lemah
1635.64
Lemah
Adanya serapan gugus fungsi karboksilat (-COOH) dan gugus NH2
menunjukkan karakteristik dari karboksi metil kitosan dan menunjukkan
karboksimetilasi mensubstitusi lebih banyak pada atom –H dari –OH, terlihat
pada serapan gugus C – O – C pada 1087.85 cm-1. Serapan gugus karboksilat
(C = O) di 1720 cm-1 yang tidak terdapat pada spektra FTIR dari kitosan.
4.4.2 Hasil pembuatan karboksi metil kitosan dan glutaraldehid-urea
Kitosan-urea merupakan senyawa derivat kitosan dengan cara
memodifikasi struktur kimia dari kitosan melalui proses pengikatan silang
(crosslinked). Crosslinked dilakukan menggunakan senyawa yang minimal
memiliki 2 gugus fungsi aktif. Berbagai bahan kimia yang telah banyak digunakan
sebagai agen crosslink yaitu glutaraldehid (Ruiz et al, 2000). Glutaraldehid
dengan struktur senyawa ditunjukkan pada Gambar 4.12 memiliki 2 gugus fungsi

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
54
aktif yaitu aldehid (-COH) pada kedua ujungnya, sehingga dapat digunakan
sebagai agen crosslinked.
O O
C (CH2)3 C
H H
Gambar 4.12 Struktur glutaraldehid
Selain glutaraldehid, beberapa turunan kitosan juga dapat diperoleh
dengan cara menambahkan gugus fungsional baru untuk membantu meningkatkan
selektivitas penyerapan ion logam. Pada penelitian Chassary (2005), tiourea
digunakan sebagai bahan untuk meningkatkan selektivitas penyerapan ion logam
melalui crosslinked kitosan. Namun pada penelitian ini digunakan urea sebagai
bahan tambahan untuk meningkatkan penyerapan ion logam dari kitosan-urea
yang dibuat. Urea dengan struktur senyawa ditunjukkan pada Gambar 4.13,
dipilih karena adanya dua gugus amina. Gugus amina yang aktif dapat bereaksi
dengan kitosan dan glutaraldehid sehingga sisi-sisi aktif pengikatan ion logam
semakin banyak dan kemampuan mengikat ion logam semakin besar (Ramesh et
al, 2008).
H2N
O
C
NH2
Gambar 4.13 Struktur urea
Pada pembuatan kitosan urea, tahapan yang dilakukan adalah dengan cara
mereaksikan urea dengan glutaraldehid. Glutaraldehid dan urea digunakan pada
penelitian ini sebagai agen pengikat silang (crosslinker). Larutan glutaraldehid
dan urea direaksikan pada suhu 50oC selama 3 jam, Pemanasan bertujuan

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
55
O
mempercepat reaksi antara glutaraldehid dan urea. Pada penelitian ini, diberikan
variasi terhadap jumlah urea yang direaksikan dengan glutaraldehid. Variasi
jumlah urea dilakukan untuk mengetahui pengaruh dari pengikatan ion logam
yang akan dihasilkan pada proses adsorpsi.
O O O O O + C (CH ) C C
2 3
H H H2N NH2 C (CH2)3 C
H H C
H2N
NH2
glutaraldehid urea
O
H C (CH2)3
O H O
CH N C
H
NH2
O O H
H C (CH2)3 CH N
H
O
C NH2
O
H C (CH2)3
OH2 O
CH N C
NH2
O
H H C (CH2)3 C
O
N C NH2
Gambar 4.14 Mekanisme reaksi glutaraldehid dan urea
Reaksi antara glutaraldehid dan urea terjadi pada gugus fungsi aktif
aldehid dari glutaraldehid dan gugus amina pada urea. Kedua gugus bereaksi
dengan terbentuk ikatan baru antara atom karbon (-C) dari ujung gugus aldehid
dengan atom nitrogen pada urea.
Karboksi metil kitosan hasil sintesis pada tahap awal dilarutkan dalam
akuades dan direaksikan dengan larutan gutaraldehid-urea dari masing-masing
variasi yang telah dilakukan. Variasi diberikan dengan penambahan komposisi
urea sebanyak 3,0; 6,0; dan 9,0 gram pada saat pembuatan glutaraldehid-urea.
+

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
56
Hasil yang diperoleh berupa serbuk berwarna coklat yaitu kitosan-urea dicuci dan
dibilas dengan NaOH, akuades dan aseton. Penambahan NaOH dan akuades
bertujuan untuk menetralkan residu yang bersifat asam dan aseton berfungsi untuk
menghilangkan sisa reaktan. Terdapat 3 (tiga) macam kitosa-urea yang diperoleh
dari variasi penambahan urea, yaitu kitosan-urea (a) dengan komposisi urea
sebanyak 3,0 gram; kitosan-urea (b) dengan komposisi urea sebanyak 6,0 gram;
dan kitosan-urea (c) dengan komposisi urea sebanyak 9,0 gram.
Gambar 4.15 Kitosan-urea
Kitosan-urea yang dihasilkan yaitu kitosan-urea (a), kitosan-urea (b), dan
kitosan-urea (c) tidak terdapat perbedaan fisik. Kitosan-urea yang dihasilkan
berupa serbuk berwarna coklat.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
57
H2
C C
O O
H2
H O C C OH H
H2
O C C OH
H H
O O O
H O H O
H N H H N
OH OH
OH OH
H C
H
(CH2)3 C N
H
C N C H
(CH2)3 C H H C (CH2)3 C N
OH2 O O OH
O
H O
H2
C C OH
H O
O
H O
H N OH
OH H
H C (CH ) C 2 3
H N C N C (CH ) C 2 3 H
O
H2
H O C C OH + O O
O
O H O OH
H O H H H
O H C (CH2)3C
H O N C N C (CH2)3C H O
O
H NH2
OH OH
CMC
glutaraldehid-urea H O H H NH
OH OH
H H
H C (CH2)3 C N C N C (CH2)3 C H
O O O
O
H C N C (CH2)3 C H
O O
O O
Gambar 4.16 Mekanisme reaksi pembentukan kitosan-urea
Reaksi awal yang terjadi antara glutaraldehid dan urea terjadi pada salah
satu gugus fungsi aktif aldehid pada glutaraldehid dengan urea. Gugus fungsi aktif
aldehid yang lain berikatan dengan gugus amina yang aktif bereaksi pada C2 dari
kitosan melalui reaksi substitusi gugus hidrogen dari atom nitrogen (-NH) pada
C2 kitosan. Reaksi terjadi pada seluruh bagian dari gugus amina pada karboksi

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
58
metil kitosan, sehingga terbentuk senyawa baru yaitu kitosan-urea dengan struktur
seperti jaringan.
Kitosan berwarna putih dengan tingkat kelarutan yang baik dalam larutan
asam asetat 2%. Didalam larutan asam, kitosan yang memiliki gugus amino (-
NH2) menangkap proton menjadi NH3+ sehingga dapat berinteraksi secara
elektrostatik dengan komplek anion (Sun dan Wang, 2006). Crosslinked kitosan
dilakukan sebagai metode untuk meningkatkan stabilitas polimer dalam larutan
asam (Ruiz et al, 2000). Proses crosslinked pada kitosan terjadi pada gugus
hidroksil (-OH) dan amina (-NH2) (Wang et al, 2010). Kitosan-urea hasil
pembuatan memiliki sifat fisik yang berbeda dari kitosan, yaitu stabil dalam
suasana asam. Kitosan-urea hasil pembuatan terdiri dari susunan berulang antara
karboksi metil kitosan dengan glutaraldehid dan urea yang membentuk jaringan
dengan pengulangan struktur yang terjadi pada setiap bagian dimana kitosan-urea
merupakan senyawa polimer dengan struktur yang rumit.
Kitosan-urea dibuat dengan harapan terdapat sisi-sisi aktif yang baru pada
bagian atom nitrogen yang menyusun kitosan-urea. Sisi aktif yaitu bagian
nitrogen pada struktur penyusun kitosan-urea memiliki sepasang elektron bebas
(gambar 4.17) yang dapat berikatan dengan komplek anion, pada penelitian ini
yaitu ion logam Cu2+.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
59
H2
H O C C OH H O
H2 C C OH
H O
H2 C C OH
H O H O H O
O O
H O H O H
H N H N H N
OH OH OH OH OH OH HC HC CH
(CH2)3 (CH2)3 (CH2)3
CH CH CH
N N N
C O C O C O
N N N
HC HC HC
(CH2)3 (CH2)3 (CH2)3
CH
OH N
OH
CH
OH N
OH
CH
OH N
OH
H H H H H H
O O O O
O H O H O H
H2
HO C C O H
H2 HO C C O
H HO C H2 C O
H
n
O O O
Gambar 4.17 Hipotesis struktur kitosan-urea
O O O
Gambar 4.18 Spektrum FT-IR kitosan-urea

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
60
Tabel 4.3 Gugus fungsi dan bilangan gelombang senyawa organik dan
kitosan-urea
Literatur (Pretsch dan Buhlmann, 2006)
Kitosan-urea pada penelitian
Gugus fungsi Bilangan
gelombang Intensitas
Bilangan gelombang
Intensitas
Alkohol
O-H st
O-H polimer
3650 – 3200
3500 – 3200
Bervariasi
Melebar
3000 – 3746.62
3000 – 3746.62
Melebar
Melebar
Eter
OCH2
CH2-O- CH2
2880 – 2835 1150 – 1085
Lemah
2870.08 1056.99
Lemah
Asam
karboksilat
COOH st
C=O amida
3550 – 2500 1740 – 1650
3000 – 3746.62
Melebar dan
tajam
Amida NC=O
≈ 1650
Kuat
1658.78
Kuat
Urea
C=O
1690 – 1620
1658.78
Kuat
Gugus fungsi yang spesifik pada kitosan-urea hasil pembuatan dengan
harapan struktur adanya gugus –O- eter, –COOH dari asam karboksilat, gugus
amida, alkohol, serta gugus C = O pada urea, nampak pada spektrum FTIR
kitosan-urea dengan intensitas yang sesuai dengan literatur. Transformasi
karboksi metil kitosan menjadi kitosan-urea ditunjukkan adanya serapan ikatan
-NC = O pada 1658.78 cm-1 dengan peak yang tajam. Selain itu serapan gugus
karboksilat (C = O) yang pada karboksi metil kitosan terdapat pada 1720.50 cm-1
tidak terlihat karena tertutupi oleh serapan pada 1658.78 cm-1.
4.5 Hasil Proses Adsorpsi
Adsorpsi merupakan peristiwa penyerapan pada permukaan suatu
adsorben melalui interaksi fisik maupun kimia (House, 2007). Pada penelitian ini

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
61
zat yang diadsorpsi adalah ion logam Cu2+ dan adsorben yang digunakan adalah
kitosan-urea. Proses adsorpsi pada penelitian dilakukan menggunakan metode
adsorpsi fluidisasi. Proses adsorpsi berlangsung dalam sebuah kolom dengan
adanya aliran gas, sehingga adsorben bergerak bebas di dalam kolom.
Mekanisme adsorpsi fluidisasi dilakukan dengan mengontakkan larutan
yang mengandung ion logam Cu2+ dengan adsorben kitosan-urea dalam sebuah
kolom, aliran gas dialirkan ke kolom melalui distributor udara. Gas yang dialirkan
bertujuan agar kitosan-urea dapat bergerak bebas dalam kolom fluidisasi,
sehingga terjadi kontak antara kitosan-urea dengan ion logam Cu2+ yang terdapat
dalam larutan dapat terserap secara maksimal.
Gambar 4.19 Kolom adsorpsi fluidisasi
Menurut Agusnar (2006), kitosan memiliki kemampuan adsorpsi yang
baik karena adanya gugus -NH2 yang mampu berinteraksi dengan ion logam Cu2+.
Senyawa-senyawa turunan kitosan banyak digunakan sebagai bahan dalam
pemurnian dan pemisahan limbah logam dalam perairan (Anirudhan dan Rijith,
2009). Kitosan-urea yang merupakan senyawa turunan kitosan hasil crosslinked

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
62
antara kitosan dengan asam kloroasetat, glutaraldehid dan urea dengan struktur
senyawa yang mengandung sisi aktif pengikat logam yang lebih banyak. Sisi aktif
dari kitosan-urea pada gambar 4.17 terdapat pada atom nitrogen dimana, setiap
atom nitrogen memiliki pasangan elektron bebas dari atom nitrogen yang dapat
berinteraksi dengan ion logam Cu2+.
4.5.1 Pembuatan kurva standar Cu
Kurva standar Cu dibuat dengan tujuan untuk menentukan kadar Cu dalam
larutan. Kurva standar Cu dibuat dengan menyiapkan larutan standar Cu2+ pada
beberapa konsentrasi. Analisis kadar Cu2+ menggunakan AAS (Atomic
Adsorption Spectrofotometer) yang diukur pada panjang gelombang maksimal
324,75 nm (Laus et al,2010). Larutan standar diukur absorbansinya dengan AAS
kemudian diperoleh persamaan regresi linier yang nantinya digunakan untuk
menentukan konsentrasi akhir dari larutan. Hasil kurva standar larutan Cu2+
terdapat pada Gambar 4.20
1.6
1.4
1.2
1
0.8
0.6
0.4
0.2
0
y = 0.14161x + 0.01854
R² = 0.9993
0 5 10
konsentrasi Cu2+
Gambar 4.20 Kurva standar Cu
Absorbansi dari larutan sampel yang dianalisis dengan AAS, dapat
disubstitusi ke dalam persamaan regresi linier y = 0.14161x + 0.01854 dengan
abso
rban
si

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
63
koefisien korelasi sebesar 0.9993, dimana y adalah absorbansi dan x adalah
konsentrasi.
4.5.2 Pengukuran kadar ion logam Cu2+ hasil adsorpsi
Proses adsorpsi fluidisasi dilakukan dengan menambahkan larutan yang
mengandung ion logam Cu2+ dengan konsentrasi awal 100 mg/l, dengan jumlah
kitosan-urea sebanyak 0.5 gram. Pengukuran dilakukan dengan variasi waktu
selama 20, 40, 60, 80, dan 100 menit. Konsentrasi akhir dari larutan yang
mengandung ion logam Cu2+ dianalisis mengguanakan AAS (Atomic Adsorption
Spectrofotometer) dengan pengukuran absorbansi pada panjang gelombang
maksimal 324,75 nm. Hasil adsorpsi ion logam Cu2+ oleh kitosan dan kitosan-urea
terdapat pada Gambar 4.21 dan Gambar 4.22
22
20
18
16
14
12 0
10
0 20 40 60 80 100 120 140 160 180 200
Waktu (menit)
Gambar 4.21 Grafik adsorpsi ion logam Cu2+ oleh kitosan
Konse
ntr
asi
akhir
(m
g/l
)
20.89 20.84
21.14 19.85
14.63 14.51
13.7

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
64
60
50 41.63
40
Kitosan-urea ( a ) 30 35.08 Kitosan-urea ( b )
20 Kitosan-urea ( c )
10 10.58
0
0 20 40 60 80 100 120
Waktu (menit)
Gambar 4.22 Grafik adsorpsi ion logam Cu2+ oleh kitosan-urea
Hasil adsorpsi dari kitosan dan kitosan-urea menunjukkan perbedaan
kemampuan adsorpsi dari setiap adsorben yang digunakan. Kitosan dalam waktu
20 menit mampu mengadsorpsi ion Cu2+ dengan konsentrasi awal 100 mg/l
menjadi 21.14 mg/l dan konsentrasi ion Cu2+ menurun dengan waktu adsorpsi
yang semakin lama. Pada waktu adsorpsi ion Cu2+ selama 180 menit konsentrasi
menurun menjadi 13.70 mg/l. Pada adsorpsi menggunakan kitosan-urea dengan
variasi kitosan-urea (a), kitosan-urea (b), dan kitosan-urea (c) terdapat perbedaan
kemampuan adsorpsi dibandingkan dengan kemampuan adsorpsi pada kitosan.
Pada kitosan-urea (a) dalam waktu 20 menit dengan konsentrasi awal 100
mg/l mempu mengadsorpsi ion logam Cu2+ menjadi 12.72 mg/l. Penurunan
konsentrasi terjadi hingga rentang waktu adsorpsi selama 80 menit yaitu 10.58
mg/l. Keadaan ini tidak berlangsung selama penambahan waktu adsorpsi, karena
pada saat adsorpsi selama 100 menit konsentrasi akhir dari larutan meningkat
menjadi 11.28 mg/l dibandingkan pada saat adsorpsi selama 80 menit. Adsorpsi
Konse
ntr
asi
akhir
(m
g/l
)

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
65
kitosan-urea (a) mampu mengadsorpsi ion logam Cu2+ secara maksimal dengan
waktu adsorpsi 80 menit.
Pada kitosan-urea (b) dalam waktu adsorpsi selama 20 menit konsentrasi
larutan menjadi 39.47 mg/l, namun pada penambahan waktu adsorpsi selama 40
menit konsentrasi dari larutan menjadi 35.94 mg/l dan tidak mengalami perubahan
konsentrasi secara signifikan hingga waktu adsorpsi selama 100 menit. Hal ini
menunjukkan bahwa kemampuan adsorpsi dari kitosan-urea (b) tidak lebih baik
dari kitosan-urea (a). Hal ini menunjukkan bahwa pada waktu adsorpsi selama 40
menit adsorben ktosan-urea (b) berada pada tingkat adsorpsi maksimal (jenuh),
sehingga tidak mampu lagi menyerap ion logam Cu2+ dari larutan.
Pada kitosan-urea (c) dimana kandungan urea pada saat pembuatannya
lebih banyak dibandingkan pada pembuatan kitosan-urea (a) dan kitosan-urea (b)
menunjukkan hasil adsorpsi ion logam Cu2+ dengan konsentrasi akhir 54.30 mg/l
selama 20 menit. Pada penambahan waktu adsorpsi selama 80 menit konsentrasi
larutan menjadi 41.63 mg/l, namun pada adsorpsi selama 100 menit konsentrasi
akhir dari larutan meningkat menjadi 43.52 mg/l. Penentuan data hasil adsorpsi
ditunjukkan pada Lampiran 4.
Pada penelitian ini kitosan-urea (a) dapat mengadsorpsi secara maksimal
larutan yang mengandung ion logam Cu2+ hingga 89.42 % selama 80 menit,
sedangkan pada kitosan dengan metode adsorpsi fluidisasi yang sama
mengadsorpsi hingga 86.30 % selama 180 menit.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
66
4.5.3 Hasil penentuan kapasitas adsorpsi logam Cu2+ dalam kitosan-urea
Kapasitas adsorpsi merupakan keadaan kesetimbangan suatu adsorben
untuk menyerap ion logam secara maksimal (Wu et al, 2001).
untuk mencapai hasil kapasitas adsorpsi yang paling baik, sedangkan pada
kitosan-urea (a) pada waktu 80 menit telah mencapai hasil kapasitas adsorpsi
maksimal. Hal ini menunjukkan kesesuaian dari pengaruh adanya sisi aktif pada
kitosan yaitu gugus amina (-NH2) dan sisi aktif pada kitosan-urea (a) yang lebih
banyak (gambar 4.17). Pada kitosan-urea (b) dan kitosan-urea (c) kemampuan
adsorpsi dari kedua adsorben ini tidak lebih baik dari kitosan-urea (a) karena
produk crosslinked pada kitosan-urea (b) dan kitosan-urea (c) terjadi
40
35.7670 34.5164 35
30 32.0598
25.9646
25
20 23.3450
kitosan
kitosan-urea (a)
kitosan-urea (b)
kitosan-urea (c)
15
0 20 40 60 80 100 120 140 160 180 200
Waktu (menit)
Gambar 4.23 Grafik kapasitas adsorpsi ion logam Cu2+ oleh kitosan dan
kitosan-urea
Berdasarkan hasil penelitian penentuan kapasitas adsorpsi dari adsorben
yaitu kitosan-urea (a) lebih besar dibanding kapasitas adsorpsi dari kitosan. Pada
hasil kapasitas adsorpsi kitosan-urea (a) pada waktu 80 menit dengan hasil
kapasitas adsorpsi oleh kitosan pada waktu 80 menit, menunjukkan hasil yang
tidak terlalu jauh. Namun, pada kitosan memerlukan waktu hingga 180 menit
Kap
asit
as a
dso
rpsi
(m
g/g
r)

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
67
perbandingan stokiometri yang tidak sesuai lagi. Sehingga kitosan-urea yang
dihasilkan tidak sesuai dengan harapan. Penentuan data kapasitas adsorpsi
ditunjukkan pada Lampiran 5.
Adsorpsi fluidisasi yang digunakan pada penelitian ini memiliki
kemampuan adsorpsi yang berbeda bila dibanding dengan metode batch
(pengadukan) yang selama ini banyak digunakan sebagai metode adsorpsi.
Kelebihan dari metode adsorpsi fluidisasi pada penelitian ini dengan metode batch
pada penelitian sebelumnnya ditunjukkan pada Tabel 4.4 dan 4.5.
Tabel 4.4 Adsorpsi ion logam Cu2+ pada beberapa penelitian menggunakan
senyawa turunan kitosan
No. Parameter Laus et al
(2010) Screenivasan et al (2009)
Kitosan Penelitian
Kitosan-urea (a) Penelitian
1. Ion Logam Cu2+ Cu2+ Cu2+ Cu2+
2.
Adsorben
Kitosan-
epiklorohidrin
-triposfat
Kitosan-
glutaraldehid-
epiklorohidrin
Kitosan
Kitosan-
glutaraldehid-
urea
3. Metode Adsorpsi Batch Batch Fluidisasi Fluidisasi
4. Jumlah adsorben
(gr) 1,5 0,1 0,5 0,5
5. Jumlah larutan (ml) 200 50 200 200
6. Waktu kontak 30 jam 3 jam 180 menit 80 menit
7. Suhu (oC) 25 50 27 27
8. Konsentrasi awal
(mg/l) 100 100 100 100
9. Kapasitas Adsorpsi
(mg/g) 50.87 49.09 34.51 35.76
10. Penyerapan (%) 38.16 98.18 86.29 89.41
Kelebihan dari metode adsorpsi fluidisasi pada penelitian ini yang telah
digunakan berada pada jumlah adsorben yang dibutuhkan pada setiap proses
adsorpsi yaitu 0.5 gram kitosan-urea dan kitosan. Sedangkan pada penelitian Laus
2010, menggunakan metode batch diperlukan adsorben kitosan tercrosslinked
epiklorohidrin sebanyak 1.5 gram pada setiap proses adsorpsi dengan kapasitas

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
68
adsorpsi 50.87 mg/g dengan waktu adsorpsi selama 30 jam. Metode adsorpsi
fluidisasi menunjukkan efisiensi pada jumlah adsorben dan waktu kontak selama
proses adsorpsi dengan hasil yang baik.
4.5.4 Hasil analisa BET pengukuran pori kitosan-urea
Tabel 4.5 Perbandingan hasil analisis BET kitosan-urea
Parameter Kitosan
(Cahyaningrum,
2008)
Kitosan-urea
sebelum adsorpsi
(penelitian)
Kitosan-urea
setelah adsorpsi
(penelitian)
Spesifik Surface area ( m2/g)
0.0635 0.032 0.103
Jari-jari pori (A) 3.7070 227.984 65.99
Volume pori (cc/g) - 0.001 0.003
Berdasarkan hasil data analisa BET ditunjukkan bahwa ukuran jari-jari
pori dari kitosan-urea hasil penelitian sebelum dilakukan proses adsorpsi lebih
besar dibandingkan pada kitosan hasil penelitian Cahyaningrum, 2008. Semakin
besar ukuran jari-jari pori dari suatu adsorben, memiliki kemampuan adsorpsi
yang lebih besar dalm mengikat ion logam. Sehingga kemampuan kitosan urea
dalam menyerap ion logam Cu2+ lebih besar, Hal ini didukung oleh besarnya
kapasitas adsorpsi kitosan-urea yaitu sebesar 35.76 mg/g dengan waktu kontak
selama 80 menit, dibandingkan kapasitas adsorpsi kitosan sebesar 34.51 mg/g
dengan waktu kontak selama 180 menit.
Ukuran jari-jari pori dari kitosan-urea setelah proses adsorpsi
menunjukkan perubahan, dari semula 227.984 A, menjadi 65.99 A. Perubahan
ukuran pori menunjukkan adanya ikatan yang terjadi selama proses berlangsung
antara kitosan-urea dengan ion logam Cu2+.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
69
Pada data hasil luas permukaan kitosan-urea setelah adsorpsi meningkat
dari sebelum adsorpsi sebesar 0.032 m2/g menjadi 0.103 m2/g setelah proses
adsorpsi. Perubahan luas permukaan kitosan-urea setelah adsorpsi terjadi karena
telah terbentuknya ikatan antara kitosan-urea dengan logam Cu2+. Pada volume
pori kitosan-urea setelah proses adsorpsi menunjukan ukuran volume yang lebih
besar, keadaan ini dapat disebabkan karena adanya perubahan bentuk dari pori
sehingga terjadi perubahan ukuran volume.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian dan pembahasan yang telah dilakukan dapat
disimpulkan sebagai berikut
1. Kitosan-urea dapat disintesis dengan memodifikasi kitosan melalui
penambahan asam kloroasetat menghasilkan karboksi metil kitosan
melalui reaksi substitusi pada gugus hidroksi dari C6 pada kitosan dan
glutaraldehid sebagai agen crosslinked serta urea sebagai penambah
gugus fungsi melalui reaksi substitusi pada C2 dari karboksi metil
kitosan.
2. Variasi konsentrasi urea pada sintesis kitosan-urea mempengaruhi hasil
adsorpsi ion logam Cu2+. Hasil adsorpsi kitosan-urea (a) lebih baik
dibandingkan hasil adsorpsi oleh kitosan-urea (b) dan kitosan-urea (c)
dengan kapasitas adsorpsi kitosan-urea (a) sebesar 35.76 mg/g,
kitosan-urea (b) sebesar 25.96 mg/g, dan kitosan-urea (c) sebesar 23.34
mg/g dengan waktu adsorpsi terbaik selama 80 menit. Variasi waktu
kontak penyerapan ion logam Cu2+ melalui metode adsorpsi fluidisasi
dengan adsorben kitosan-urea penyerapan maksimal terjadi pada waktu
kontak 80 menit.
70

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
71
5.2 Saran
Perlu dikembangkan penelitian lebih lanjut terhadap adsorpsi ion logam
berat menggunakan kitosan termodifikasi dengan memberikan pengaruh suhu, pH
dan pengaruh tekanan udara pada kolom fluidisasi sehingga diperoleh kapasitas
adsorpsi ion Cu2+ yang lebih baik.

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
72
DAFTAR PUSTAKA
Adamson, A. W., 1990, Physical Chemistry of Surfaces 5th edition, John
Wiley&Sons, Inc, New York California
Agusnar, H., 2006, Penggunaan Glutaraldehid Kitosan untuk Penurunan Konsentrasi
Ion Logam Cr3+ Menggunakan Ekstraksi Fasa Padat, Disertasi USU
Anirudhan, Thayyath., Rijith, Sreenivasan, 2009, Glutaraldehyde cross-linked
epoxyaminated chitosan as an adsorbent for the removal and recovery of
copper(II) from aqueous media, Colloids and Surfaces A: Physicochem,
Engineering Aspects., 351: 52–59
Arica, YM., Yilmaz, M., Yalcin, E., Bayramoglu, G., 2004, Surface properties of
Reactive Yellow 2 Immobilised pHEMA and HEMA/chitosan
Membranes: Characterisation of Their Selectivity to Different Proteins,
Journal of Membrans Science., 240: 167-178
Austin, S., 1997, The Urea Reduction ratio and Serum Albumin Concentration
as Predictors of Hypertension, Division of Nephrology., 29: 770-775
Baba, Y., Noma, H., Nakayama, R., Matsushita, Y., 2002, Preparation of Chitosan
Derivatives Containing Methylthiocarbamoyl and Phenylthiocarbamoyl
Groups and Their Selective Adsorption of Copper(II) Over Iron(III).
Anal. Sci., 18: 359–361
Billmayer, Jr., 1994, Textbook of Polymer Science, 3th ed, John Wiley and Sons, New
York
Cestari, A.R., Vieira, E.F.S., Matos, J.D.S., 2005, Determination of Kinetic
Parameter of Cu(II) Interaction with Chemically Modified Chitin-
Chitosan Membranes, Journal Colloid Interface Science., 285: 288-295
Cestari, A.R., Vieira. E., Oliveira, Bruns, R.E., 2007, The Removal of Cu(II) and
Co(II) from Aqueous Solution Using Crosslinked Chitosan Evaluation by
The Factorial Design Methodology, Journal Hazard Mater., 143: 8-16
Chassary, P., Vincent, T., Guibal, E., 2004, Metal Anion Sorption on Chitosan and
Derivative Materials: a Strategy for Polymer Modification and Optimum
use. React. Funct. Polym., 60: 137–149

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
73
Chassary, P., Vincent, T., Marcano, J.S., Macaskie, L.E., Guibal, E., 2005,
Palladium and Platinum Recovery from Bicomponent Mixtures Using
Chitosan Derivatives. Hydrometallurgy., 76: 131–147
Chen, X., Chen, G., Yue, P.L., 2002, Novel Electrode System for Electroflotation
of Wastewater, Environomental Science Technology., 36: 778–783
Chen, A. H., Liu, S.C., Chen, C.Y., 2008, Comparative Adsorption of Cu(II),
Zn(II), and Pb(II) Ions in Aqueous solution on The Crosslinked Chitosan
with Epichlorohydrin, J.Hazard, 154: 184-191
Chen, X., Park, J.H., 2003, Chemical Characteristics of O-carboxymethyl
Chitosan related to The Preparation Conditions, Carbohydrate Polimer,
53: 355-359
Chen, A.H., Yang, C.Y., Chen, C.Y., Chen, C.W., 2009, The Chemically
Crosslinked Metal-complexed Chitosan for Comparative Adsorption of
Cu(II), Zn(II), Pb(II) ions in aqueous Medium, J.Hazard Matter, 163: 137-
149
Copello, G.J., Varela, F., Vivot, R.M., Diaz, L.E., 2008, Immobilized Chitosan as
Biosorbent for The Removal of Cd(II), Cr(III) and Cr(VI) from Aqueous
Solutions, Bioresourches Technology, 99: 6538–6544
Crittenden, Barry., Thomas, W.J., 1998, Adsorption Technology and Design, Typeset
at The Spartan Press Ltd, Great Britain, Page 96-113
Darmono, 2001, Lingkungan Hidup dan Pencemaran, UI Press., Jakarta
Ernst, E., Pittler, M., 1998, Chitosan as a Treatment for Body Weight Reduction
Meta-analysis, Perfusion, 11: 461–465
Fatmawati, 2009, Kelimpahan Relatif dan Struktur Ukuran Rajungan Di Daerah
Mangrove Kecamatan Tekolabbua Kabupaten Pangkep, Skripsi jurusan
Perikanan Fakultas Ilmu Kelautan dan Perikanan Universitas Hasanuddin,
Makassar
Fujiwara, K., Ramesh, A., Maki, T., Hasegawa, H., Ueda, K., 2007, Adsorption of
Platinum (IV), Palladium (II) and Gold (III) from Aqueous Solutions
Onto L-lysine Modified Crosslinked Chitosan Resin. Journal Hazard
Mater., 146: 39–50

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
74
Guibal, E., 2004. Interactions of Metal Ions with Chitosan-based Sorbents, a
review Sep. Purif. Technol., 38:43–74
Guibal, E., Sweeney, N.V.O., Vincenta, T., Tobinb, J.M., 2002, Sulfur Derivatives
of Chitosan for Palladium Sorption. React. Funct. Polymer.,50:149–163
Hartati, F., K, Susanto. T, Raklamadiono, S, Adi, S.L, 2002, Faktor- Faktor yang
Berpengaruh terhadap Deprotenasi Menggenakan Enzim Protease dalam
Kitin dari cangkang Rajungan (portonus Pelagicus), Biosains, Vol.2
Hutahahean, S,Ida., 2001, Pengguanan Kitosan Sebagai Penyerap Terhadap
Logam Zinkum (Zn2+) dan Logam Kromium (Cr2+) dengan Metode
Spektrofotometri Serapan Atom, Skripsi Jurusan Kimia FMIPA-USU,
Medan
Ho, Y.S., McKay, G., 2003, Sorption of Dyes and Copper Ions Onto Biosorbents,
Process Biochem, 38: 1047–1061
House, E.J., 2007, Principles of Chemical Kinetics, 2nd edition, Elsevier Inc, London,
136-142
Hu, Z., Lei, L., Li, L., Ni, Y, 2003, Chromium Adsorption on High-performance
Activated Carbons from Aqueous Solution, Purification Technology., 31:
13–18
Hwang, K.T., Jung, S.T., Lee, G.D.,Chinnan, M.S., Park, Y.S., Park, H.J., 2002,
Controlling Molecular Weight And Degree of Deacetylation of Chitosan
by Response Surface Methodology. Journal of Agricultural and Food
Chemistry., 50 (7): 1876-1882
Ismail, K., 2003, Pengantar Analisis Instrumental, Departemen Perindustrian dan
Perdagangan Pusdiklat-Indag, Bogor
Iflakhah, Dini., 2011, Otomatisasi Penentuan Derajat Deasetilasi Kitosan dari
Data Spektroskopi Inframerah, Skripsi, Departemen Kimia Fakultas Sains
dan Teknologi Universitas Airlangga, Surabaya
Jang, A., Seo, Y.W., Bishop, P.L., 2005, The Removal of Heavy Metals in Urban
Runoff by Sorption on Mulch, Environtment Pollutant., 133: 177-127
Juang, R.S., Ju, C.Y., 1998, Kinetics of Sorption of Cu(II)-
ethylenediaminetetraacetic acid Chelated Anions on Cross-linked

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
75
Polyaminated Chitosan Beads, Engineering Chemical Resources., 37: 3463–
3469
Khan, T.A., Peh, K.K., and Ching, H.S., 2002, Reporting Degree of Deacetylation
Values of Chitosan, Journal Pharmacies Pharmaceutical Science., Vol. 5(3):
205-212
Kim, Se-Kwon., 2011, Chitin, Chitosan, Oligosaccharides and Their Derivatives
Biological Activities and Applications, CRC Press Taylor & Francis Group,
United States of America., Page 12-14
Khopkar, S.M, 2007, Konsep Dasar Kimia Analitik, Universitas Indonesia Press,
Jakarta
Khor, Eugene., 2010, Chitin, Singapore, Halaman 63-69
Kolodziejska, I., Wojtasz-Pajak, A., Ogonowska, G., Sikorski, Z.E. (2000).
Deacetylation of Chitin in two-stage Chemical and Enzymatic Process.
Bulletin of Sea Fisheries Institute.. 2: 15-24
Kuntoro, Asep, 2004, Pembuatan Membran Kitosan dari Kulit Udang untuk
Proses Pengolahan Limbah Malachite Green, Skripsi, Universitas
Airlangga, Surabaya
Lahuddin, M., 2007, Aspek Unsur Mikro dalam Kesuburan Tanah, USU Press,
Medan
Laus, R., Thiago, G., Szpoganicz, B., Valfredo, T., Favere, 2010, Adsorption and
Desorption of Cu(II), Cd(II) and Pb(II) Ions using Chitosan Crosslinked
with epichlorohydrin-triphosphate as The Adsorbent, Journal of
Hazardous Materials 183:233–241
Li, N., Bai, R., 2006, Development of Chitosan-based Granular Adsorbents for
Enhanced and Selective Adsorption Performance in Heavy Metal
Removal. Water Science Techonlogy., 54: 103–113
Li, Q., Su, H., Tan, T., 2008, Synthesis of Ion-imprented Chitosan-TiO2
Adsorbent and Its Multi-functional Performance, Biochemical
Engineering Journal., 38: 212-218
Martins, A.O., Silva, E.L., Carasek, E., Gonc, N.S., Laranjeira, M.C.M., Favere,
V.T., 2004, Chelating Resin from Functionalization of Chitosan with

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
76
Complexing Agent 8-hydroxyquinoline: Application for Metal Ions on
Line Preconcentration System, Anal. Chim. Acta., 521: 157–162
Massaro, J.E., 2003, Handbook of Copper Pharmacology and Toxycology, Humana
Press, New Jersey.
Mendham, J., Denney, R.C., Barnes, J.D., Thomas, M.J.K., 2000, Vogels Text Book
of Quantitative Chemical Analysis 6th edition, Pearson Education, London
Ngah, W.S.W., Endud, C.S., Mayanar, R., 2002, Removal of Copper(II) Ions from
Aqueous Solution Onto Chitosan and cross-linked Chitosan Beads, React.
Funct. Polym. 50: 181–190
Ngah, W.S.W., Fathinathan, S., 2006, Chitosan Flakes and Chitosan–GLA Beads
for Adsorption of p-nitrophenol in Aqueous Solution, Colloid Surf. A-
Physicochem Eng Asp., 277: 214–222
Ning, R.Y., 2002, Arsenic Removal by Reverse Osmosis, Desalination, 143: 237–
241
No, H.K., Meyers, S.P., 2000, Environment Contamination Toxicology., (1): 163
Ormrod, D.J., Holmes, C.C., Miller, T.E., 1998, Dietary Chitosan Inhibits
Hypercholesterolaemia and Atherogenesis in The Apolipoprotein Edeficient Mouse Model of Atherosclerosis. Atherosclerosis.,138:329–334
Palar. H., 2004, Pencemaran dan Toksikologi Logam Berat, PT. Asdi Mahastya,
Jakarta
Piron, E., Accominoti, M., Domard, A., 1997, Interaction Between Chitosan and
Uranyl Ions Role of physical and physicochemical parameters on the
kinetics of sorption, Langmuir., 13: 1653–1658
Pretsch, E., Buhlmann, P., Affolter, C., 2006, Structure of Determination of Organic
Compounds, Tables of Spectral data, English Edition, Springer, Switzerland.,
245-303
Purwatiningsih, S., 2009, Kitosan Sumber Biomaterial Masa Depan, IPB Press,
Bandung
Puspawati, N.M., dan Simpen, I.N., (2010), Optimasi Deasetilasi Khitin dari Kulit
Udang dan Cangkang Kepiting Limbah Restoran Seafood Menjadi

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
77
Khitosan Melalui Variasi Konsentrasi NaOH, Jurnal Kimia FMIPA
Universitas Udayana, Bali. Halaman 79-90.
Rachman, Suhardi, 2006, Pengelolaan Emisi Debu Urea menuju Produksi Bersih,
Tesis, Program Magister ilmu Lingkungan, Universitas Diponegoro,
Semarang
Rahayu, L. H., dan Purnavita, S., 2004, Optimasi Proses Deproteinasi dan
Demineralisasi pada Isolasi Kitin dari Limbah Cangkang Rajungan
(Portunus pelagicus), Prosiding: Teori Aplikasi Teknologi Kelautan, ITS
Surabaya, hal. III.8 – III.11
Ramesh, A., Hasegawa, H., Sugimoto, W., Maki, T., Ueda, K, 2008, Adsorption of
Gold(III), Platinum(IV) and Palladium (II) onto glycine Modified
Crosslinked Chitosan Resin, Bioresource Technology., 99: 3801-3809
Ravi, K.M.N.V., Muzzarelli, R.A.A., Muzzarelli, C., Sashiwa, H., Domb, A.J.,
Chitosan Chemistry and Pharmaceutical Perspectives, Chem. Rev., 104:
6017-6084
Reddad, Z., Gerente, C., Andres, Y., Thibault, J.F., Cloirec, P.L., 2003, Cadmium
and Lead Adsorption by Natural Polysaccharide in MF Membrance
reactor: Experimental Analysis and Modeling, Water Researches., 37:
3983–3991
Rinaudo, M., 2006, Chitin and Chitosan: Properties and Application, Progress in
Polymer Science.,31:603-632
Ruiz, M., Sastre, A.M., Guibal, E., 2000, Palladium Sorption on Glutaraldehyde
Crosslinked Chitosan. React. Functional Polymer., 45: 155–173
Schmuhl, R., Krieg, Keizer, 2001, Adsorption of Cu(II) and Cr(IV) Ions by
Chitosan, Kinetics and Equilibrium Studies, Water SA 27
Shafaei, A., Zokaee,F, 2007, Equilibrium Studies of Hg(II) ions Onto Chitosan,
Elsevier., 133:311-316
Sreenivasan, Thayyath., Rijith, Sreenivasan, 2009, Glutaraldehyde cross-linked
epoxyaminated chitosan as an adsorbent for the removal and recovery of
copper(II) from aqueous media, Colloids and Surfaces A: Physicochem,
Engineering Aspects., 351: 52–59

Skripsi Nourmalasari Aisyah Pembuatan dan Karakterisasi Kitosan-Urea dengan
Penambahan Asam Kloroasetat dan Glutaraldehid Sebagai Adsorben Ion
Logam Cu2+ Melalui Teknik Adsorpsi Fluidisasi
ADLN Perpustakaan Universitas Airlangga
78
Sugita, P., Sjahriza, A., Rachmanita, 2006, Sintesis dan Optimalisasi Gel Kitosan
Karboksimetil Selulosa, Jurnal Alchemy., 6: 57-62
Sun, S.and Wang A., 2005, Adsorption properties of carboxymethyl-chitosan and
cross-linked carboxymethyl-chitosan resin with Cu(II) as template,
Separation and Purification Technology., 49:197–204
Susanto, B. M. Marzuki, dan I Setyadi, 2004, Pengamatan Aspek Biologi rajungan
(Portunus pelagicus) dalam Menunjang Teknik Pembenihannya, Warta
Penelitian Perikanan Indonesia., 10(1): 6-11
Tang, R., Du, Y., Fan, L., 2003, Dialdehyde Starch-crosslinked Chitosan Films
and Their Antimicrobial Effects. Journal Polymer Science Part B., 41:993–
997
Varma, A.J., Desphande, S.V., Kennedy, J.F., 2004, Metal Complexation by
Chitosan and Its Derivatives: a review, Carbohydrate Polymer., 55: 77–93
Vega, F.A., Covelo, E.F, Andrade, M.L., 2006, Competitive Sorption and
Desorption of Heavy Metals in Mine Soils : Influence of Mine Soil
Characteristics, Journal Colloid Interface Science., 298: 582-592
Vieira, R.S., Beppu, M.M., 2006, Interaction of Natural and Crosslinked Chitosan
Membranes with Hg(II) Ions, Colloids Surface A., 279: 196–207
Volda, I.M.N., Varum, K.M., Guibal, E., Smidsrod, O., 2003, Binding of Ions to
Chitosan-selectivity Studies, Carbohydrate Polymer., 54:471–477
Wang, L., Xing,R., Liu,S., 2010, Synthesis and Evaluation of a thiourea-modified
Chitosan Derivative applied for adsorption of Hg(II) from Synthetic
Wastewater, Int Journal of Biological Macromolecules., 46:524-528
Wibowo, S., 2006. Produksi Kitin Kitosan secara Komersial. Prosiding seminar
nasional Kitin-Kitosan. DTHP, Institut Pertanian Bogor
Wu, F.C., Tseng, R.L., Juang, R.S., 2001, Kinetic Modeling of Liquid-phase
adsorption of Reactive Dyes and Metal Ions on Chitosan, Water Res.
35:613–618.
Xu, WL., Fu, CL.,Li, LL., 2001, Studies On The Adsorption Capacity for
Bilirubin of The adsorbent Chitosan-β-cyclodextrin, Chinese Chemical
Letters., 12:359-362