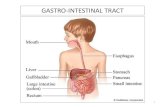
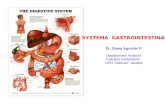
Laporan Biokimia GastroIntestinal System
-
Upload
tira-kurniati -
Category
Documents
-
view
58 -
download
1
description
Transcript of Laporan Biokimia GastroIntestinal System

LAPORAN PRAKTIKUM BIOKIMIA
BLOK GIS
Kelompok Lab: A1
Disusun oleh :
Tira Kurniati 1310211025
Mutiara Nova Pratiwi 1310211027
Iin Intansari 1310211030
Rizky Harsya Maulana 1310211032
Faiza Supraini 1310211044
FAKULTAS KEDOKTERAN
UNIVERSITAS PEMBANGUNAN NASIONAL
“VETERAN” JAKARTA
T.A 2015/2016

KATA PENGANTAR
Assalamualaikum Wr. Wb.,
Puji dan syukur kami panjatkan kehadirat Tuhan yang Maha Esa,
karena atas rahmat dan izin-Nya, kami dapat menyelesaikan makalah
Praktikum Biokimia Blok GIS dengan tepat waktu. Makalah ini kami buat
untuk memenuhi tugas yang telah diberikan kepada kami. Selain itu,
makalah ini juga dibuat agar pembaca dapat memahami bagaimana cara
kerja dan kandungan dari air liur (saliva) dan juga empedu.
Kami menyadari bahwa dalam penulisan makalah ini masih banyak
kekurangan. Untuk itu, kami sangat menerima saran dan kritik dari
pembaca sekalian demi perbaikan dalam pembuatan makalah
selanjutnya.
Demikian makalah ini kami buat, semoga makalah ini dapat
menjadi bahan pembelajaran kita semua yang membacanya.
Wassalamualaikum Wr. Wb.
Jakarta, 11 Oktober 2015

BAB I
PENDAHULUAN
1.1 LANDASAN TEORI
A. SALIVA
Merupakan cairan eksokrin yang terdiri dari 99% air, elektrolit
(sodium, potasium, kalsium, kloride, magnesium, bikarbonat, fosfat)
dan terdiri dari protein yang berperan sebagai enzim,
immunoglobulin, antimikroba, glikoprotein mukosa, albumin,
polipeptida dan oligopeptida yang berperan dalam kesehatan
rongga mulut.
Komposisi Saliva
Terdiri dari 99,5% air dan 0,5% subtansi yang larut. Komposisi
saliva antara lain :
1. Protein
Beberapa jenis protein yang terdapat didalam saliva adalah :
a) Mucoid
Merupakan sekelompok protein yang sering disebut dengan
mucin dan memberikan konsistensi mukus pada saliva.
Mucin juga berperan sebagai glikoprotein karena terdiri dari
rangkaian protein yang panjang dengan ikatan rantai
karbohidrat yang lebih pendek.
b) Enzim
Enzim yang ada pada saliva dihasilkan oleh kelenjar saliva
dan beberapa diantaranya merupakan produk dari bakteri
dan leukosit yang ada pada rongga mulut.
Beberapa enzim yang terdapat dalam saliva adalah amylase
dan lysozyme yang berperan dalam mengontrol
pertumbuhan bakteri di rongga mulut.

c) Protein Serum
Saliva dibentuk dari serum maka sejumlah serum protein
yang kecil ditemukan didalam saliva. Albumin dan globulin
termasuk kedalam serum saliva
d) Waste Products
Pada saliva juga ditemukan sebagian kecil dari waste
product pada serum, urea dan uric acid.
2. Ion-ion Inorganik
Ion-ion utama yang ditemukan dalam saliva adalah kalsium dan
fosfat yang berperan penting dalam pembentukan kalkulus. Ion-ion
lain yang memiliki jumlah yang lebih kecil terdiri dari sodium,
potasium, klorida, sulfat dan ion-ion lainnya.
3. Gas
Pada saat pertama sekali saliva dibentuk, saliva mengandung gas
oksigen yang larut, nitrogen dan karbon dioksida dengan jumlah
yang sama dengan serum. Ini memperlihatkan bahwa konsentrasi
karbon dioksida cukup tinggi dan hanya dapat dipertahankan pada
larutan yang memiliki tekanan didalam kelenjar duktus, tetapi pada
saat saliva mencapai rongga mulut banyak karbon dioksida yang
lepas.
4. Zat-zat Aditif di Rongga Mulut
Merupakan berbagai substansi yang tidak ada didalam saliva pada
saat saliva mengalir dari dalam duktus, akan tetapi menjadi
bercampur dengan saliva didalam rongga mulut. Yang termasuk
kedalam zat-zat aditif yaitu mikroorganisme, leukosit dan dietary
substance.

Volume rata-rata saliva yang dihasilkan perhari berkisar 1-1,5 liter.
Pada orang dewasa laju aliran saliva normal yang distimulasi
mencapai 1-3 ml/menit, rata-rata terendah mencapai 0,7-1 ml/menit
dimana pada keadaan hiposalivasi ditandai dengan laju aliran
saliva yang lebih rendah dari 0,7 ml/menit. Laju aliran saliva normal
tanpa adanya stimulasi berkisar 0,25-0,35 ml/menit, dengan rata-
rata terendah 0,1-0,25 ml/menit dan pada keadaan hiposalivasi laju
aliran saliva kurang dari 0,1 ml/menit.
Nilai pH saliva normal berkisar 6 – 7. Konsumsi karbohidrat padat
maupun cair dapat menyebabkan terjadinya perubahan pH saliva
dimana karbohidrat akan difermentasi oleh bakteri dan akan
melekat ke permukaan gigi. Dengan adanya sistem buffer pada
saliva, pH akan kembali netral setelah 20 menit terpapar
karbohidrat yang berkonsistensi cair dan 40-60 menit pada
karbohidrat yang berkonsistensi padat.
Fungsi Saliva
a) Sensasi Rasa
Aliran saliva yang terbentuk didalam acini bersifat isotonik, saliva
mengalir melalui duktus dan mengalami perubahan menjadi
hipotonik. Kandungan hipotonik saliva terdiri dari glukosa,
sodium, klorida, urea dan memiliki kapasitas untuk memberikan
kelarutan substansi yang memungkinkan gustatory buds
merasakan aroma yang berbeda.
b) Perlindungan Mukosa dan Lubrikasi
Saliva membentuk lapisan seromukos yang berperan sebagai
pelumas dan melindungi jaringan rongga mulut dari agen-agen
yang dapat mengiritasi. Mucinsebagai protein dalam saliva
memiliki peranan sebagai pelumas, perlindungan terhadap

dehidrasi, dan dalam proses pemeliharaan viskoelastisitas
saliva.
c) Kapasitas Buffering
Buffer adalah suatu substansi yang dapat membantu untuk
mempertahankan agar pH tetap netral. Buffer dapat
menetralisasikan asam dan basa. Saliva memiliki kemampuan
untuk mengatur keseimbangan buffer pada rongga mulut.
d) Integritas Enamel Gigi
Saliva juga memiliki peranan penting dalam mempertahankan
integritas kimia fisik dari enamel gigi dengan cara mengatur
proses remineralisasi dan demineralisasi. Faktor utama untuk
mengontrol stabilitas enamel adalah hidroksiapatit sebagai
Universitas Sumatera Utarakonsentrasi aktif yang dapat
membebaskan kalsium, fosfat, dan fluor didalam larutan dan
didalam pH saliva.
e) Menjaga Oral Hygiene
Saliva berfungsi sebagai self cleansing terutama pada saat tidur
dimana produksi saliva berkurang. Saliva mengandung enzim
lysozyme yang berperan penting dalam mengontrol pertumbuhan
bakteri di rongga mulut.
f) Membantu Proses Pencernaan
Saliva bertanggung jawab untuk membantu proses pencernaan
awal dalam proses pembentukan bolus-bolus makanan. Enzim
α-amylase atau enzim ptyalin merupakan salah satu komposisi
dari saliva yang berfungsi untuk memecah karbohidrat menjadi
maltose, maltotriose dan dekstrin.

g) Perbaikan Jaringan
Saliva memiliki peranan dalam membantu proses pembekuan
darah pada jaringan rongga mulut, dimana dapat dilihat secara
klinis waktu pendarahan menjadi lebih singkat dengan adanya
bantuan saliva.
h) Membantu Proses Bicara
Lidah memerlukan saliva sebagai pelumas selama bicara, tanpa
adanya saliva maka proses bicara akan menjadi lebih sulit.
i) Menjaga Keseimbangan Cairan
Penurunan aliran saliva akan menghasilkan adanya suatu
sensasi haus yang dapat meningkatkan intake cairan tubuh.
Faktor-Faktor yang Mempengaruhi pH Saliva
Derajat keasaman (pH) dan kapasitas buffer saliva dipengaruhi oleh
perubahan-perubahan yang disebabkan oleh irama cyrcadian, diet
dan rangsangan terhadap kecepatan sekresi saliva.
a) Irama cyrcadian
Irama cyrcadian mempengaruhi pH dan kapasitas buffer saliva.
Pada keadaan istirahat atau segera setelah bangun, pH saliva
meningkat dan kemudian turun kembali dengan cepat. Pada
seperempat jam setelah makan (stimulasi mekanik), pH saliva
juga tinggi dan turun kembali dalam waktu 30-60 menit
kemudian. pH saliva agak meningkat sampai malam, dan setelah
itu turun kembali.
b) Diet
Diet juga mempengaruhi kapasitas buffer saliva. Diet kaya
karbohidrat dapat menurunkan kapasitas buffer saliva,

sedangkan diet kaya serat dan diet kaya protein mempunyai efek
meningkatkan buffer saliva. Diet kaya karbohidrat meningkatkan
metabolisme produksi asam oleh bakteri-bakteri mulut,
sedangkan protein sebagai sumber makanan bakteri,
meningkatkan sekresi zat-zat basa seperti amonia.
B. EMPEDU
Secara fisiologi, empedu dihasilkan oleh hepatosit dan sel-sel
duktus sebanyak 500-1500 mL/ hari. Sekresi aktif garam empedu
ke dalam canaliculus bilier dipengaruhi oleh volume empedu. Na+
dan air mengalir secara pasif untuk meningkatkan isoosmolaritas.
Lechitin dan kolesterol memasuki canaliculus pada laju tertentu
yang berhubungan dengan output garam empedu. Bilirubin dan
sejumlah anion organik lainnya (esterogen, sulfobromopthalen, dll)
secara aktif disekresikan oleh hepatosit melalui sistem transport
yang berbeda dengan garam empedu. Diantara makan, empedu
disimpan di vesica biliaris, dimana empedu terkonsentrasi pada
hingga 20%/ jam. Na+ dan HCO3- atau Cl- secara aktif ditransport
dari lumennya selama absorpsi.
Ada tiga faktor yang meregulasi aliran empedu yaitu : sekresi
hepatik, kontraksi vesica biliaris, dan tahanan spincter choledochal.
Dalam keadaan puasa, tekanan di ductus choledocus adalah 5-10
cm H2O dan empedu yang dihasilkan di hati disimpan di dalam
vesica biliaris. Setelah makan, vesica biliaris berkontraksi, spincter
relaksasi dan empedu di alirkan ke dalam duodenum dengan
adanya tekanan di dalam duktus yang terjadi secara intermiten
yang melebihi tahanan spincter. Saat berkontraksi, tekanan di
dalam vesica biliaris mencapai 25 cm H2O dan di dalam ductus
choledocus mencapai 15-20 cm H2O. Cholecystokonin (CCK)

adalah stimulus utama untuk berkontraksinya vesica biliaris dan
relaksasi spincter. CCK dilepaskan ke dalam aliran darah dari
mukosa usus halus.
Gambar 3. Fisiologi Pengeluaran Empedu

Komposisi Empedu
Tabel 1. Komposisi empedu2
Komponen Dari Hati Dari Kandung
Empedu
Air 97,5 gm % 95 gm %
Garam Empedu 1,1 gm % 6 gm %
Bilirubin 0,04 gm % 0,3 gm %
Kolesterol 0,1 gm % 0,3 – 0,9 gm %
Asam Lemak 0,12 gm % 0,3 – 1,2 gm %
Lecithin 0,04 gm % 0,3 gm %
Elektrolit - -
1. Garam Empedu
Asam empedu berasal dari kolesterol. Asam empedu dari hati
ada dua macam yaitu : Asam Deoxycholat dan Asam Cholat.
Fungsi garam empedu adalah
a. Menurunkan tegangan permukaan dari partikel lemak yang
terdapat dalam makanan, sehingga partikel lemak yang
besar dapat dipecah menjadi partikel-partikel kecil untuk
dapat dicerna lebih lanjut.
b. Membantu absorbsi asam lemak, monoglycerid, kolesterol
dan vitamin yang larut dalam lemak.
Garam empedu yang masuk ke dalam lumen usus oleh kerja
kuman-kuman usus dirubah menjadi deoxycholat dan lithocholat.
Sebagian besar (90 %) garam empedu dalam lumen usus akan

diabsorbsi kembali oleh mukosa usus sedangkan sisanya akan
dikeluarkan bersama feses dalam bentuk lithocholat. Absorbsi
garam empedu tersebut terjadi disegmen distal dari ilium. Sehingga
bila ada gangguan pada daerah tersebut misalnya oleh karena
radang atau reseksi maka absorbsi garam empedu akan terganggu.
2. Bilirubin
Hemoglobin yang terlepas dari eritrosit akan pecah menjadi
heme dan globin. Heme bersatu membentuk rantai dengan
empat inti pyrole menjadi bilverdin yang segera berubah menjadi
bilirubin bebas. Zat ini di dalam plasma terikat erat oleh albumin.
Sebagian bilirubin bebas diikat oleh zat lain (konjugasi) yaitu 80
% oleh glukuronide. Bila terjadi pemecahan sel darah merah
berlebihan misalnya pada malaria maka bilirubin yang terbentuk
sangat banyak.
Metabolisme bilirubin:

1.2 TUJUAN PRAKTIKUM
1.2.1 Tujuan Umum
Mengetahui kadar pH dan ion ion yang terkandung dalam saliva (
air liur ) dan kandungan cairan empedu dengan menggunakan
reaksi biokima
1.2.2 Tujuan Khusus
1.2.2.1 Mengetahui pH saliva ( air liur )
1.2.2.2 Mengetahui adanya sulfat dalam saliva (air liur)
1.2.2.3 Mengetahui adanya fosfat dalam saliva (air liur)
1.2.2.4 Mengetahui ada tidaknya klorida dalam saliva (air liur)
1.2.2.5 Mengetahui adanya pigmen empedu
1.2.2.6 Mengetahui adanya asam empedu

BAB II
CARA KERJA
2.1 LIUR
2.1.1 PENETAPAN PH LIUR
Tujuan : untuk mengetahui pH liur
Dasar : pada kisaran pH tertentu suatu indikator akan memberikan
perubahan warna sesuai dengan H+ dalam larutan yg diperiksa
Bahan :
1. Air liur
2. pH indikator
Cara kerja : siapkan 3 ml air liur dalam tabung reaksi. Kemudian
ambil satu pH test dan masukan ke dalam tabung reaksi yang
berisi liur. Tunggu sampai ada perubahan warna. Setelah itu
bandingkan perubahan warna yang muncul dengan indikator pH.
pH liur : 8
2.1.2 UJI SULFAT
Tujuan : Untuk mengetahui adanya sulfat dalam liur
Dasar : Ion sulfat dalam suasana asam dapat diendapkan oleh
barium
Ba2+ + SO2-4 ------- BaSO4 (endapan putih) ---- (+)
Bahan :
Air liur
HCL encer / HCL 10%
BaCl2 2%

Cara kerja :
2.1.3 UJI FOSFAT
Tujuan : Untuk mengetahui adanya fosfat dalam liur
Dasar : Fosfat bereaksi dengan asam molibdat membentuk asam
fosfomolibdat, yang dapat direduksi memberikan warna biru tua
(ortofosfat)
Bahan :
Air liur
Larutan urea 10%
Pereaksi molibdat special
Larutan FeSO4 spesial
Cara kerja :
Bahan Tabung
Liur 0,5 mL
Urea 10% 0,5 mL
Molibdat special 5 mL
FeSO4 0,5 mL
Hasil Biru tua
Bahan Tabung
Liur 1 Ml
HCl 3-5 tetes
BaCl2 5-10 tetes
Hasil pengamatan Terdapat endapan
putih

2.1.4 UJI KLORIDA
Tujuan : Mengetahui ada tidaknya klorida dalam liur
Dasar : Ion klorida dalam suasana asam dapat diendapkan oleh Ag
(perak). Endapan AgCl (endapan putih) menunjukan adanya klorida
Bahan :
Liur
Asam nitrat 10%
Perak nitrat 1 %
Cara kerja :
2.2 CAIRAN EMPEDU
2.2.1 TES GMELIN
Tujuan : Untuk mengetahui adanya pigmen empedu
Dasar : Penambahan asam nitrat pada pigmen empedu akan
menghasilkan senyawa oksidasi yang berwarna.
Bahan :
1. Larutan asam empedu encer (1:5)
Bahan Tabung
Liur 1 mL
Asam nitrat 3-5 tetes
Perak nitrat 5-10 tetes
Hasil Terdapat endapan putih

2. Larutan asam nitrat pekat
Cara Kerja :
Tabung Tabung 1 Tabung 2
Cairan empedu encer 3 ml -
Aquades - 3 ml
Larutan sukrosa 5% 5 tetes 5 tetes
Asam nitrat pekat
(melalui dinding
tabung)
3 ml 3 ml
HASIL PENGAMATAN
Warna larutan
Cairan empedu
yang berwarna
hijau setelah
diteteskan asam
nitrat pekat
berubah menjadi
warna ungu tua.
Pertama-tama
hanya pada
bagian dasar,
lama kelamaan
warna ungu naik
yang
menyebabkan
warna hijaunya
semakin sedikit.
Lalu warna ungu
yg didasar
memudar,
menjadi warna
ungu muda.
Sekarang
Tidak ada perubahan
warna. Hanya bening
dan jernih.

terdapat 3 lapisan
warna (dr atas ke
bawah): hijau,
ungu, orange
muda kecoklatan.
Lalu berubah
menjadi 2 lapisan
lagi, yaitu biru dan
orange muda
kecoklatan. Lalu
terkahir sekali
berubah menjadi
1 warna yaitu,
orange muda
kecoklatan.
2.2.2 TES PETTENKOFER
Tujuan : Untuk mengetahui adanya asam empedu
Dasar : Asam-asam empedu yang terdapat dalam empedu
terutama sebagai garam empedu, yang merupakan senyawa
aromatik kompleks. Asam empedu bereaksi dengan furfural
(yang terbentuk pada penambahan asam pekat dan karbohidrat)
membentuk turunan yang berwarna.
Bahan :
1. Larutan asam empedu encer (1:5) dan akuades
2. Larutan sukrosa 5%
3. Asam sulfat pekat

Cara Kerja :
Tabung Tabung 1 Tabung 2
Cairan empedu encer 5 ml -
Aquades - 5 ml
Larutan sukrosa 5% 5 tetes 5 tetes
H2SO4 pekat (melalui
dinding tabung) 3 ml 3 ml
HASIL PENGAMATAN Terdapat perubahan
warna menjadi warna
ungu yg membentuk
cincin.
Tidak ada perubahan
warna. Hanya bening
dan jernih.
Sampel Cairan empedu Aquades
Hasil : Terdapat 4 lapisan warna (dr atas
ke bawah), yaitu hijau, ungu,
kuning dan bening. Warna ungu
tersebut membentuk suatu cincin
antara 2 lapisan warna.
Tidak ada perubahan
warna. Hanya bening
dan jernih.

BAB III
HASIL DAN PEMBAHASAN
3.1 SALIVA ( AIR LIUR )
3.1.1 Penetapan pH saliva ( air liur )
Hasil dari percobaan yaitu dengan pH 8. Dari hasil percobaan
menunjukan terdapat kenaikan pH liur melebih nilai normalnya (pH
normal saliva 6,0-7,4). Kenaikan pH tersebuh akan
mempengaruhi kerja enzim amilase, sehingga kerjanya tidak
optimal. Karena pada hakikatnya enzim amilase ini bekerja secara
optimal pada pH 6,6 (Guytondkk, 1997).
3.1.2 Uji Sulfat
Hasil : Terdapat endapan putih pada tabung
Kesimpulan : Hasil percobaan terdapat endapan putih, itu
membuktikan bahwa air liur positif mengandung sulfat. Dari hasil
pengamatan dapat dilihat bahwa pada saat air liur ditambahkan HCl
tidak terjadi perubahan (air liur tetap keruh). Warna keruh tersebut
disebabkan karena Cl berkatan dengan amilum. Sedangkan pada
saat ditambahkan dengan BaCl2 terbentuk gumpalan.
3.1.3 Uji Fosfat
Hasil : Terjadi perubahan warna menjadi biru tua
Kesimpulan : Warna larutan yang biru tua tersebut menunjukkan
bahwa air liur mengandung fosfat dalam bentuk ortofosfat.
3.1.4 Uji Klorida
Hasil : Terdapat endapan putih pada tabung
Kesimpulan : Endapan putih (AgCl) yang terbentuk pada tabung
menunjukkan bahwa klorida (Cl) yang terdapat dalam air liur dalam

suasana asam (karena penambahan asam nitrat) merupakan hasil
pengendapan yang dilakukan oleh perak ( Ag ). Hal ini sesuai
dengan teori dasarnya yaitu ion klorida dalam suasana asam dapat
diendapkan oleh Ag (perak).
3.2 CAIRAN EMPEDU
3.2.1 Test Gmelin
Hasil :
Cairan empedu Akuades
Cairan empedu yang berwarna hijau
setelah diteteskan asam nitrat pekat
berubah menjadi warna ungu tua.
Pertama-tama hanya pada bagian
dasar, lama kelamaan warna ungu
naik yang menyebabkan warna
hijaunya semakin sedikit. Lalu warna
ungu yg didasar memudar, menjadi
warna ungu muda. Sekarang terdapat
3 lapisan warna (dr atas ke bawah):
hijau, ungu, orange muda kecoklatan.
Lalu berubah menjadi 2 lapisan lagi,
yaitu biru dan orange muda
kecoklatan. Lalu terkahir sekali
berubah menjadi 1 warna yaitu,
orange muda kecoklatan.
Tidak ada perubahan
warna. Hanya bening
dan jernih.
Kesimpulan : dari hasil percobaan, terbukti bahwa cairan empedu
pada tabung I tersebut mengandung pigmen empedu, karena
didapatkan hasil positif yaitu terbentuk senyawa berwarna pada

cairan empedu yang direaksikan. Dan terdapat beberapa
perubahan warna pada reaksi tersebut.
3.2.2 Test Pettenkofer
Hasil :
Cairan empedu Akuades
Terdapat 4 lapisan warna (dr atas
ke bawah), yaitu hijau, ungu,
kuning dan bening. Warna ungu
tersebut membentuk suatu cincin
antara 2 lapisan warna.
Tidak ada perubahan
warna. Hanya bening
dan jernih.
Kesimpulan : dari hasil percobaan, terbukti bahwa cairan empedu
pada tabung I tersebut mengandung asam empedu, karena hasilter
positif yaitu dengan terjadi perubahan warna pada cairan empedu.
Perubahan warna berupa terbentuknya cincin berwarna ungu pada
cairan empedu

DAFTAR PUSTAKA
Guyton, A.C., dan Hall, J.E. 2008. Buku Ajar Fisiologi Kedokteran.
Edisi 11. Jakarta: EGC
http://repository.usu.ac.id
Sherwood, L. 2001. Fisiologi Manusia;dari Sel ke Sistem. Edisi 2.
Jakarta;EGC

LAMPIRAN
PENETAPAN PH LIUR
UJI SULFAT
UJI FOSFAT

UJI KLORIDA
TES GMELIN TES PETTENKOFER