IV. XENOTRANSPLANTASI SEL ... - repository.ipb.ac.id · umur larva berkaitan dengan perkembangan...
Transcript of IV. XENOTRANSPLANTASI SEL ... - repository.ipb.ac.id · umur larva berkaitan dengan perkembangan...
37
IV. XENOTRANSPLANTASI SEL TESTIKULAR IKAN
GURAMI PADA BERBAGAI UMUR LARVA IKAN NILA
ABSTRAK
Xenotransplantasi sel testikular merupakan suatu metode untuk melestarikan
dan mengembangkan plasma sel germinal dari ikan-ikan yang terancam punah
dan untuk produksi induk pengganti bagi ikan-ikan yang bernilai ekonomis
tinggi. Pada penelitian ini, ikan gurami digunakan sebagai model donor dan ikan
nila sebagai model resipien. Pengembangan xenotransplantasi sel testikular ini
diawali dengan penentuan umur resipien yang optimum untuk kegiatan
transplantasi sel germinal. Testis segar diisolasi dari ikan gurami ukuran 600–
800 g, lalu dicacah dalam larutan disosiasi dan selanjutnya diinkubasi pada suhu
ruang selama 3 jam untuk mendapatkan suspensi sel testikular sebagai sumber
donor. Sel donor dilabel dengan PKH 26 fluorescent dye sebelum
ditransplantasikan ke dalam rongga peritoneal larva ikan nila umur 1, 3, 5 dan 7
hari pascamenetas (hpm). Parameter yang diamati adalah sintasan larva ikan nila
24 jam pascatransplantasi (pt) dan efisiensi kolonisasi sel donor pada resipien
umur 2 dan 3 bulan pt. Hasil penelitian menunjukkan bahwa sintasan larva rata-
rata terendah adalah pada perlakuan umur larva 1 hpm (82,74±6,76%) dan
tertinggi pada larva 3 dan 5 hpm masing-masing 95,00±5,00% and 95,00±2,50%).
Efisiensi kolonisasi rata-rata tertinggi terdapat pada perlakuan umur transplantasi
larva 3 hpm (61,1±34,71% ) dan terendah pada larva umur 7 hpm
(19,43±17,33%). Dari penelitian ini dapat disimpulkan bahwa larva ikan nila
umur 3 hpm adalah resipien terbaik untuk xenotransplantasi sel testikular ikan
gurami.
Kata kunci: xenotransplantasi, sel germinal jantan, ikan gurami, ikan nila,
efisiensi kolonisasi
38
IV. XENOTRANSPLANTATION OF GIANT GOURAMI
TESTICULAR GERM CELLS INTO DIFFERENT AGE OF
NILE TILAPIA’S LARVAE
ABSTRACT
The recent study has been conducted to develop testicular germ cell
transplantation as a tool for preservation and propagation of male germ-plasm
from endangered fish species, as well as to produce surrogate broodstock of
commercially valuable fish. Giant gourami testis had been used as a model for
donor and Nile tilapia larvae as recipient. We developed testicular cell
xenotransplantation by optimizing the timing of intraperitoneal cell
transplantation to recipient larvae aged 1, 3, 5 and 7 days post hatching (dph).
Freshly isolated testis of giant gourami weighed 600–800 g were minced in
dissociation medium and then incubated for 3 hours in room temperature to
collect monodisperce cell suspension. Donor cells labeled with PKH 26 were
transplanted into the peritoneal cavity of Nile tilapia larvae using glass
micropipettes. Parameters observed were survival rate of Nile tilapia larvae at 24
hours post transplantation (pt) and colonization efficiency of donor cells at 2 and
3 months pt. The incorporated donor cells were observed under fluorescent
microscope. The result showed that the lowest survival rate at 24 hours pt was 1
dph larvae (82.74±6.76%) and the highest survival rate were 3 and 5 dph larvae
(95.00±5.00% and 95.00±2.50%, respectively). The highest colonization
efficiency was on 3 dph larvae (61.1±34.71%) and the lowest colonization
efficiency was on 7 dph larvae (19.43±17.33%). In conclusion, 3 dph Nile tilapia
larvae was the best recipient for giant gourami testicular germ cells
xenotransplantation.
Key words: xenotransplantation, testicular germ cell, giant gourami, Nile tilapia,
colonization efficiency
PENDAHULUAN
Teknologi xenotransplantasi sel testikular yang mengandung spermatogonia
pertama kali diaplikasikan pada ikan gurami (Osphronemus goramy)
menggunakan resipien larva ikan nila (Oreochromis niloticus). Pada penelitian
xenotransplantasi ini digunakan ikan gurami sebagai model donor dan ikan nila
sebagai model resipien, yang mana kedua jenis ikan ini berbeda pada tingkat
ordo. Saat ini xenotransplantasi antar dua spesies ikan yang berbeda famili telah
berhasil dilakukan. Spermatogonia ikan nibe (famili Scianidae) yang
39
ditransplantasikan ke larva ikan chub mackerel (famili Scombridae) telah berhasil
hingga tahap proliferasi sel spermatogonia ikan nibe pada gonad ikan chub
mackerel (Yazawa et al. 2010). Xenotransplantasi PGC ikan loach ke embrio
ikan zebra fase blastoderm (chimera) bahkan mampu menghasilkan spermatozoa
ikan loach yang fungsional tetapi belum mampu menghasilkan sel telur yang
fungsional (Saito et al. 2008).
Sementara itu xenotransplantasi PGC ikan pearl danio ke ikan zebra, yang
memiliki hubungan filogeni yang lebih dekat (satu genus) menghasilkan ikan
kimera pearl danio-ikan zebra. Hibrid dari kimera dan ikan zebra normal
menghasilkan individu yang normal namun sel gametnya tidak berkembang.
Fenomena ini menunjukkan bahwa terdapat mekanisme dan faktor-faktor yang
membatasi keberhasilan transplantasi antar dua spesies yang berbeda termasuk
peran imunokompetensi dari resipien terhadap sel donor, hubungan filogenetik
antar donor dan resipien, faktor intrinsik sel itu, dan peran sinyal ekstrinsik dalam
proses pertumbuhan dan perkembangan sel donor pada resipien (Saito et al.
2008). Faktor-faktor tersebut dilaporkan berbeda-beda antar spesies (Dobrinski et
al. 1999, Johnston et al. 2000).
Ketersediaan resipien yang kompeten merupakan salah satu faktor penentu
keberhasilan kegiatan transplantasi sel germinal (Honaramooz & Yang 2011).
Ikan nila telah sering dijadikan ikan model untuk penelitian biologi reproduksi,
namun penggunaannya sebagai resipien dalam kegiatan transplantasi belum
banyak dilaporkan. Selama ini hanya Lacerda et al. (2008) yang telah berhasil
melakukan uji kompetensi ikan nila sebagai resipien untuk kegiatan transplantasi
sel germinal ikan nila dan katak. Resipien yang digunakan adalah ikan nila
dewasa yang saluran reproduksinya telah disterilkan dengan busulfan, suatu
senyawa yang berfungsi untuk merusak sel endogenus Meskipun menghasilkan
sel spermatozoa yang fungsional dan sel donor katak terkolonisasi pada gonad
ikan nila namun metode ini tidak aman digunakan dalam kegiatan pembenihan
karena busulfan bersifat karsinogenik bagi manusia.
Beberapa penelitian transplantasi sel germinal telah menggunakan larva
sebagai resipien dan hasilnya menunjukkan bahwa umur resipien juga
berpengaruh terhadap keberhasilan kolonisasi (Takeuchi et al. 2003, Takeuchi et
40
al. 2009, Yazawa et al. 2010). Kemampuan lingkungan mikro somatik resipien
mengarahkan sel donor ke rongga genital semakin berkurang dengan semakin
berkembangnya gonad resipien atau dengan semakin bertambahnya umur resipien
(Okutsu et al. 2006a). Manning & Nakanishi (1996) menyatakan interval umur
resipien sebagai salah satu faktor yang mempengaruhi efisiensi kolonisasi, karena
umur larva berkaitan dengan perkembangan sistem imunodefisiensi. Sistem
imun larva yang baru menetas belum berkembang sehingga antigen atau benda
asing belum dapat terdeteksi.
Pada tahap awal larva, organ limfomieloid (limpa, timus dan darah) sebagai
organ pembentuk respons imun belum berkembang dengan sempurna. Umumnya
respon imun pada tahap larva berasal dari transfer antibodi induk dalam bentuk
maternal immunoglobulin yang terdapat pada kuning telur dan dalam limfosit
beberapa jenis ikan (Mulero et al. 2007). Pada ikan Tilapia mossambica,
jaringan limfoid mulai terbentuk pada umur 5 hari pascamenetas (Ali 1987)
sehingga diduga pada umur tersebut respons imun mulai berkembang.
Ijiri et al. (2008) menyatakan bahwa larva ikan nila umur 5 hingga 6 hari
pascamenetas (hpm) adalah titik kritis bagi gonad untuk berdiferensiasi menjadi
ovari atau testis. Hal ini menunjukkan bahwa gonad larva umur lebih dari 6 hari
yang telah terdiferensiasi dapat menciptakan penghalang (barrier) bagi sel donor
untuk terkolonisasi pada gonad yang telah terdiferensiasi. Menurut Takeuchi et
al. (2009) epitel gonad yang telah terdiferensiasi dapat menghalangi inkorporasi
sel spermatogonia A.
Fenomena respons imun dan diferensiasi kelamin tersebut menunjukkan
bahwa terdapat keterbatasan waktu yang pendek bagi sel donor untuk bermigrasi.
Keterbatasan waktu tersebut dipengaruhi oleh tahap perkembangan larva. Oleh
karena itu umur larva merupakan salah satu faktor yang perlu dikaji. Tujuan dari
penelitian ini adalah menganalisis kemampuan kolonisasi sel donor ikan gurami
pada berbagai umur larva ikan nila sebagai resipien. Untuk mendapatkan umur
resipien yang optimum digunakan empat umur larva, yaitu 1, 3, 5 dan 7 hpm.
Xenotransplantasi sel spermatogonia ikan gurami ke berbagai umur larva ikan
nila diharapkan dapat memberikan informasi mengenai kompetensi larva ikan
nila sebagai resipien untuk xenotransplantasi dengan parameter yang diamati
41
adalah sintasan larva pascatransplantasi dan kemampuan kolonisasi sel
spermatogonia ke saluran gonad resipien.
BAHAN DAN METODE
Disosiasi Jaringan Testis
Testis ikan gurami berbobot tubuh sekitar 600–800 g didisosiasi untuk
mendapatkan suspensi sel donor mengacu pada metode disosiasi yang optimum
pada bab III. Setelah dicuci dengan PBS sebanyak 2x, suspensi sel dihitung
jumlah spermatogonianya. Sel spermatogonia yang dihitung adalah yang
berdiameter ≥15 µm yang ditentukan berdasarkan kriteria yang diperoleh pada
penelitian pada bab III, dan jumlahnya dihitung menggunakan hemositometer di
bawah mikroskop CX10 (Olympus).
Pewarnaan Sel Donor
Visualisasi sel donor dilakukan dengan pewarnaan atau pelabelan
menggunakan PKH 26 fluorescent membrane dye (Sigma-Aldrich Inc., St. Louis,
MO) yang terpancar pada panjang gelombang 551–567 nm. Dalam pelabelan
ini digunakan 2 mikrotube 1,5 µL (mikrotube A dan mikrotube B). Mikrotube A
berisi diluent C (larutan iso-osmotik yang telah tersedia pada paket pewarna PKH
26) dan sel testikular, sedangkan mikrotube B berisi diluent C dan PKH 26,
dengan perbandingan volume dari mikrotube A:B = 1:1. Formulasi yang
digunakan adalah 1,5 µL PKH 26/0,1 mL diluent C untuk jumlah sel sekitar
2x106 sel testikular. Untuk melarutkan sekitar 4x10
6 sel, maka volume diluents
C yang digunakan adalah 0,2 mL (mikrotube A) dan PKH yang digunakan
sebesar 3 µL dilarutkan dalam 0,2 mL diluent C (mikrotube B). Suspensi sel
dalam mikrotube A selanjutnya dicampurkan ke dalam larutan PKH 26 di
mikrotube B dan diinkubasi selama 5 menit dalam ruang tanpa cahaya. Aktivitas
pelabelan selanjutnya dihentikan dengan penambahan medium L15 dan
diinkubasi kembali selama 2 menit. Suspensi sel disentrifugasi pada 2000 rpm
selama 10 menit, dicuci dengan medium L15 sebanyak 2 kali dan dibuat
konsentrasi suspensi sel mencapai 20.000 sel per 0,5 µL medium L15.
42
Penyiapan Resipien Ikan Nila
Resipien yang digunakan adalah larva ikan nila putih berumur 1, 3, 5, dan 7
hpm. Morfologi larva pada berbagai umur dapat dilihat pada Lampiran 4. Telur
ikan nila yang telah dibuahi diperoleh dari pemijahan massal induk nila putih di
BBPBAT Sukabumi. Telur ikan nila ditetaskan di atas saringan halus yang
ditempatkan di dalam akuarium pada suhu air 28 oC.
Transplantasi Sel Testikular ke Larva Ikan Nila
Tahap transplantasi sel donor diawali dengan persiapan mikroinjeksi yang
meliputi persiapan jarum dan mikroinjektor serta menyedot sel ke jarum. Jarum
transplantasi disiapkan dengan cara membagi dua glass capillary (GD-1,
Narishige) menggunakan alat electric puller (PC-10, Narishige). Ujung jarum
diasah dengan menggunakan mesin gurindam (EG-400, Narishige) hingga
mencapai bukaan lubang jarum 60 µm. Jarum selanjutnya dipasang pada alat
mikroinjektor. Alat mikroinjektor terdiri atas mikroinjektor yang tersambung ke
mikroskop (Olympus SZX 16). Volume sel yang disuntikkan sebanyak 0,5 µL
dengan jumlah sel testikular sekitar 20.000 sel. Larva dibius dengan fenoksietanol
(0,03-0,05%) sebelum diinjeksi. Cawan agar yang berisi agarosa 2% dikeluarkan
dari refrigerator dan didiamkan selama beberapa menit hingga gel tidak terlalu
dingin. Setelah larva pingsan, larva diletakkan di atas cawan agar. Sel
diinjeksikan secara intraperitoneal (i.p) berdasarkan metode Takeuchi et al.
(2003). Larva ikan nila hasil injeksi dan yang tidak disuntik (kontrol) dipelihara
dalam akuarium (60x60x60) cm3
hingga siap dianalisis. Penelitian transplantasi
ini diulang sebanyak 3 kali pada setiap umur resipien dengan jumlah larva yang
disuntik sebanyak 20 hingga 40 ekor per perlakuan per ulangan.
Analisis Kolonisasi Sel Donor
Analisis kolonisasi sel donor pada gonad ikan nila menggunakan dua
metode, yaitu 1) identifikasi sel germinal ikan gurami yang membawa PKH 26
fluoroscent membrane dye pada gonad ikan nila pascatransplantasi (pt), dan 2)
menggunakan marka molekular spesifik gen hormon pertumbuhan (growth
hormone, disingkat GH) ikan gurami dengan desain primer dan program PCR
merujuk pada Achmad (2009).
43
Analisis kolonisasi melalui pengamatan sel donor pada gonad resipien di
bawah mikroskop fluoresens Nikon Ellips E600 menggunakan 4 ekor resipien
ikan nila umur sekitar 2 bulan pt dari setiap perlakuan umur transplantasi (sekitar
10% dari jumlah resipien yang ditransplantasi). Sebagai kontrol digunakan ikan
nila yang tidak ditransplantasi.
Sedangkan untuk analisis kolonisasi menggunakan marka molekular GH
ikan gurami hanya dilakukan pada kelompok resipien dengan sintasan dan
efisiensi kolonisasi tertinggi. Sebanyak 15 ekor resipien ikan nila 2 bulan pt
diisolasi gonadnya dan diekstraksi DNA menggunakan kit dari Puregene (Gentra,
Minneapolis, USA). Sampel dimasukkan ke dalam 200 μL cell lysis solution
yang berisi 1,5 μL Proteinase K (20 mg/mL). Sampel diinkubasi pada suhu 55 °C
selama semalam. Setelah sel terlisis sempurna, ditambahkan 1,5 μL RNase (4
mg/mL) dan diinkubasi pada 37 oC selama 60 menit. Kemudian ke dalam tabung
sampel ditambahkan 100 μL protein precipitation solution (Gentra, Minneapolis,
USA), disentrifugasi dengan kecepatan 12.000 rpm selama 15 menit. Supernatan
dipindahkan ke dalam mikrotub yang berisikan 300 μL isopropanol. Selanjutnya
disentrifugasi dengan kecepatan 12.000 rpm selama 10 menit. Supernatan
dibuang, kemudian ditambahkan 300 μL etanol 70% dingin ke dalam mikrotub
berisi pelet DNA. Sampel disentrifugasi kembali dengan kecepatan 12.000 rpm
selama 10 menit. Supernatan dibuang, pelet DNA dikeringudarakan dan
ditambahkan 20 μL sterille destillated water (SDW).
Pereaksi PCR dibuat berdasarkan jumlah sampel yang akan diamplifikasi.
Volume total pereaksi PCR adalah 10 µL untuk setiap sampel yang terdiri atas 4
µL SDW, 1 µL masing-masing primer forward dan reverse, 1 µL dNTPs mix, 1
µL LA Taq buffer, 1 µL MgCl2, 0,05 µL LA Taq polimerase (Takara Bio, Shiga,
Japan), 1 µL DNA cetakan. Primer yang digunakan adalah GH ikan gurami dan
β-aktin ikan nila. Suhu annealing dan lama waktu ekstensi untuk primer GH dan
β-aktin masing-masing adalah 58 oC dan 45 detik untuk primer GH serta 61
oC
dan 30 detik untuk primer β-aktin. Sedangkan, suhu predenaturasi, denaturasi. dan
ekstensi akhir sama untuk kedua primer yaitu masing-masing 94 oC selama 3
menit, 94 oC selama 30 detik, dan 72
oC selama 3 menit dengan siklus amplifikasi
sebanyak 35 siklus. Hasil amplifikasi selanjutnya divisualisasikan dengan
44
elektroforesis menggunakan gel agarosa 1% dengan volume DNA sebesar 7 µL
dan loading dye (10x loading buffer, Takara bio, Japan) sebesar 3 µL. Hasil PCR
diseparasi dengan elektroforesis menggunakan gel agarosa 1 %.
Tingkat keberhasilan kolonisasi diamati dari efisiensi kolonisasi yaitu
persentase rasio antara jumlah resipien yang pada gonadnya terdapat
spermatogonia gurami+PKH26 dan total jumlah resipien yang diperiksa.
Analisis Data
Data resipien yang membawa sel donor disajikan secara deskriptif,
sedangkan data kuantitatif berupa sintasan larva ikan nila pascatransplantasi dan
efisiensi kolonisasi sel donor pada gonad resipien disajikan dalam bentuk nilai
tengah dan diuji secara statistik menggunakan ANOVA (analysis of variance). Uji
Duncan multiple range test dilakukan bilamana terdapat beda nyata antar
perlakuan. Analisis menggunakan program SPSS 17.0 for windows dan MS
Office Excell 2007.
HASIL DAN PEMBAHASAN
Pewarnaan Sel Spermatogonia Ikan Gurami dengan PKH26
Pada dekade terakhir, teknik pewarnaan atau pelabelan sel untuk mendeteksi
keberadaan sel semakin berkembang dengan semakin bertambahnya penelitian
transplantasi sel pada hewan vertebrata khususnya kelas Pisces. Penggunaan PKH
26 fluorescent membrane dye telah banyak digunakan untuk mewarnai sel
germinal beberapa ikan dari subklas teleostei (Lacerda et al. 2008, Takeuchi et al.
2009, Yazawa et al. 2010).
Testis yang digunakan sebagai sumber donor dalam penelitian ini diisolasi
dari ikan gurami dengan kisaran bobot tubuh 600-800 g per ekor dengan kisaran
indeks gonad somatik adalah 10,8x10-5–16,3x10-5. Jumlah sel yang disuntikkan
sekitar 20.000 sel dengan komposisi rata-rata spermatogonia (ø ≥15 µm ) berkisar
7–15%. Dengan volume 3 µL PKH 26 dalam 0,2 mL diluent C, PKH 26 mampu
mewarnai atau melabel sel testikular ikan gurami sebanyak 91,93±2,90%, dan
khusus sel spermatogonia sebanyak 69,44±24,53% (Gambar 6 dan Lampiran 5).
Dibandingkan dengan kemampuan PKH 26 mewarnai sel testikular ikan nibe
45
yang mencapai 96,4±1,2% dan mewarnai spermatogonia sebesar 92,3 ±1,4%,
maka pewarnaan sel testikular ikan gurami menggunakan PKH 26 dapat dikatakan
efektif karena >90% sel terwarnai oleh PKH 26.
Lensa tanpa fluoresens Lensa fluoresens
Gambar 6 Pewarnaan suspensi sel testikular ikan gurami dengan PKH 26
fluorescent membrane dye. A–D. Suspensi sel setelah pewarnaan.
E–F. Suspensi sel sebelum pewarnaan dengan. Tanda panah hitam
dan putih adalah spermatogonia yang terwarnai PKH 26, panah merah
adalah spermatogonia yang tidak terwarnai PKH 26. Sel dalam
lingkaran adalah spermatogonia A. Skala 50 µm.
Sintasan Larva Ikan Nila Pascatransplantasi
Sintasan larva ikan nila setelah transplantasi secara intraperitoneal (i.p)
dapat dilihat pada Gambar 7 dan Lampiran 6. Sintasan rata-rata terendah pada
24 jam pt dapat terlihat pada perlakuan larva ikan nila umur 1 hpm yaitu
46
82,73±6,74% dan berbeda nyata dengan larva umur 3,5,7 hari hpm dan larva
transplantasi (P<0,05). Sintasan rata-rata larva ikan nila yang berumur 3, 5, dan 7
hpm pada 24 jam pt tidak berbeda nyata dengan kontrol (P>0.05) yaitu
95,00±5,00%, 95,00±2,50% dan 94,17±5,20% (P>0.05). Sedangkan pada
pengamatan 2 bulan pt tidak terlihat perbedaan nyata antar perlakuan umur suntik
larva. Larva yang masih muda memiliki daya tahan tubuh lemah dan rentan
terhadap gangguan fisik dari luar yang dalam hal ini adalah proses injeksi.
Namun, dengan teknik penyuntikan yang tepat maka efek penyuntikan terhadap
kematian larva dapat dikurangi.
Gambar 7 Sintasan resipien ikan nila perlakuan umur 1, 3, 5, 7 hari
pascamenetas dan tanpa transplantasi (kontrol) pada 24 jam dan 2
bulan pascatransplantasi. Keterangan gambar : larva 1 hari pasca
menetas (hpm) ( ), 3 hpm ( ), 5 hpm ( ), 7 hpm ( ), kontrol
( ).
Dalam melakukan transplantasi sel germinal ke resipien berupa larva,
terdapat beberapa faktor teknis yang perlu diperhatikan diantaranya adalah teknik
dalam mempersiapkan jarum mikroinjeksi. Sudut bukaan lubang jarum atau
keruncingan dan kelenturan bahan jarum berperan dalam proses penetrasi jarum
ke jaringan target (Costa 2010). Pada penelitian ini jarum yang digunakan adalah
glass capillary needle (Narishige) dengan sudut bukaan jarum 30–35o.
Faktor teknis kedua yang dapat mengurangi tingkat kematian pada larva
adalah mengurangi motilitas larva pada saat penyuntikan berlangsung. Untuk
47
mengurangi motilitas larva, beberapa macam teknik dilakukan oleh para peneliti
di antaranya adalah menyuntik larva di atas cawan yang berisi gel agarosa yang
telah didinginkan pada suhu 4 oC selama 10 menit (Costa 2010). Takeuchi et al.
(2009) melarutkan 0,1% bovine serum albumin (BSA) dalam larutan anastesi
atau dalam medium penyimpanan larva pascapenyuntikan dan hasilnya ternyata
cenderung meningkatkan sintasan larva meskipun tidak berbeda nyata dengan
yang tanpa pemberian BSA.
Pada penelitian ini, upaya untuk mengurangi motilitas larva ikan nila adalah
dengan cara merendam larva dalam larutan anastesi fenoksietanol dengan
konsentrasi 0,03–0,05% untuk larva umur 3, 5 dan 7 hpm sehingga proses
penyuntikan tidak terganggu oleh gerakan larva. Sedangkan larva yang baru
menetas, pergerakan larva rendah sehingga tidak perlu direndam dalam larutan
fenoksietanol, melainkan hanya diletakkan di atas cawan petri berisi gel agarosa
yang agak dingin dan diupayakan tidak terendam air. Dengan teknik ini tingkat
mortalitas larva ikan nila yang diakibatkan oleh mikroinjeksi tergolong relatif
kecil.
Faktor teknis lain yang perlu diperhatikan adalah penyuntikan yang tepat
pada sasarannya. Penyuntikan yang tidak tepat sasaran akan menyebabkan organ
atau jaringan tertentu mengalami kerusakan. Di dalam rongga peritoneal larva
terdapat banyak organ-organ abdomen vital seperti saluran pencernaan dan
pembuluh darah sehingga penyuntikan yang tidak tepat akan berpeluang merusak
organ-organ vital lainnya (Costa 2010).
Ukuran larva juga berpengaruh pada proses penyuntikan. Pertumbuhan
larva akan menyebabkan organ-organ yang terdapat dalam rongga tubuh juga
semakin besar hingga memenuhi rongga peritoneal. Fujimura & Okada (2007)
menggambarkan bahwa pada larva ikan nila (Oreochromis niloticus) 7 hari
pascafertilisasi (hpf), massa kuning telur akan mulai menutupi saluran
pencernaan. Pada 8–9 hpf atau 4–6 hpm, berbagai pigmen iriodhopore ditemukan
pada permukaan tubuh yang menutupi saluran pencernaan, sehingga rongga
peritoneal tidak dapat terlihat dengan jelas. Kondisi ini juga dapat menyebabkan
penyuntikan menjadi salah sasaran. Sebaliknya ukuran resipien larva yang terlalu
kecil juga berpengaruh terhadap mortalitas larva setelah penyuntikan seperti pada
48
ikan nibe yang mortalitasnya dapat mencapai 40% (Takeuchi et al. 2009).
Rongga peritoneal yang terlalu kecil akan menyulitkan proses injeksi sel ke dalam
rongga tersebut.
Teknik yang digunakan pada penelitian ini adalah intraperitoneal yang
berarti sel disuntikkan tepat ke dalam rongga peritoneal atau rongga tubuh seperti
digambarkan oleh Takeuchi et al. (2003) pada ikan rainbow trout. Seperti
umumnya ikan teleostei, gonad ikan rainbow trout maupun gonad ikan nila
berkembang dari satu bakal gonad yang terdapat pada dinding peritoneal. PGC
endogen akan bergerak ke rongga genital tersebut melalui dinding peritoneal.
Oleh karena itu dengan penyuntikan sel germinal ikan gurami secara i.p
diharapkan dapat meningkatkan peluang migrasi sel donor bersama-sama dengan
PGC endogen ke rongga genital.
Kolonisasi Sel Donor Ikan Gurami pada Gonad Resipien Ikan Nila
Hasil identifikasi sel donor dari ikan gurami pada gonad resipien ikan nila
berumur sekitar 2 bulan pt menunjukkan bahwa efisiensi kolonisasi rata-rata pada
umur resipien 1, 3, 5,dan 7 hpm tidak berbeda nyata (P>0,05) namun cenderung
mengalami penurunan. Efisiensi kolonisasi rata-rata pada resipien tertinggi
terdapat pada perlakuan larva umur 3 hpm (61,10±34,71%), sedangkan terendah
pada perlakuan larva umur 7 hpm (19,43±17,33%) (Gambar 8). Kemampuan sel
donor terkolonisasi pada resipien diduga mulai mengalami penurunan pada
resipien umur 7 hpm. Dugaan ini didasari oleh adanya satu perlakuan
transplantasi sel dari kelompok umur suntik 7 hpm yang efisiensi kolonisasinya
0,00 % atau dengan kata lain tidak terjadi kolonisasi sel donor pada gonad
resipien (Lampiran 7).
Rendahnya efisiensi kolonisasi rata-rata pada perlakuan 7 hpm tersebut
diduga disebabkan oleh beberapa faktor. Faktor pertama adalah faktor yang
terkait dengan teknik transplantasi. Seperti yang telah dikemukakan sebelumnya
bahwa kondisi larva dapat menyebabkan penyuntikan menjadi salah sasaran.
Fujimura & Okada (2007) menyatakan bahwa larva ikan nila umur 4–6 hpm telah
mengalami proses pigmentasi permukaan tubuh. Larva ikan nila umur 7 hpm juga
telah mengalami proses pigmentasi khususnya pada permukaan tubuh yang
49
menutupi saluran pencernaan sehingga suspensi sel yang disuntikkan berpeluang
untuk tidak tepat sasaran. Profil larva 7 hpm dapat dilihat pada Lampiran 4.
Gambar 8 Efisiensi kolonisasi sel spermatogonia ikan gurami pada resipien ikan
nila perlakuan umur transplantasi 1, 3, 5 ,7 hari pascamenetas (hpm).
Faktor kedua yang dapat menyebabkan penurunan efisiensi kolonisasi
adalah terkait dengan peran sinyal kemotaktik (kemoaktraktan) yang diproduksi
oleh lingkungan mikro rongga genital resipien yang berperan dalam proses
migrasi sel donor ke bakal gonad resipien. Peran kemoatraktan ini dapat terlihat
pada beberapa penelitian transplantasi sel testikular pada ikan secara i.p.
Kemoatraktan tersebut cenderung menghilang dengan semakin bertambahnya
umur ataupun ukuran tubuh resipien. Pada transplantasi allogenik PGC ikan
rainbow trout, kemoatraktan resipien menghilang pada umur 45 hpm sehingga
pada umur tersebut tidak terjadi lagi kolonisasi sel donor pada rongga genital
resipien (Takeuchi et al. 2003). Transplantasi allogenik ikan nibe menghasilkan
kolonisasi sel donor tidak terjadi lagi pada saat resipien mencapai ukuran 6 mm
(Takeuchi et al. 2009). Demikian halnya transplantasi xenogenik ikan nibe
(donor) dan ikan mackerel (resipien) menunjukkan terjadinya penurunan efisiensi
kolonisasi pada saat ukuran ikan mackerel telah mencapai 6,9 mm (Yazawa et al.
2010). Untuk resipien ikan nila, hasil penelitian yang diperoleh menunjukkan
bahwa senyawa kemoatraktan yang berperan dalam proses migrasi sel PGC ke
50
rongga genital masih berfungsi hingga larva berumur 7 hpm walapun terlihat
adanya kecenderungan menurun.
Selain peran kemoatraktan pada rongga genital resipien, faktor ketiga yang
dapat menyebabkan rendahnya efisiensi kolonisasi adalah rongga genital resipien
yang tidak dapat lagi menampung sel donor akibat adanya proses proliferasi dari
PGC endogen. Menurut Kobayashi et al. (2000) PGC ikan nila mulai mencapai
rongga genital pada umur larva 3 hpm dan pada saat itu sel-sel somatik sudah
mulai membungkus PGC dan proses proliferasi pun mulai berlangsung. Proses
proliferasi PGC ini ditunjang oleh lingkungan mikro somatik dari rongga genital.
Semakin cepat PGC berproliferasi maka kebutuhan terhadap sel-sel somatik yang
berperan dalam proses proliferasi juga semakin besar. Schulz et al. (2005)
menyatakan bahwa proliferasi sel germinal berkorelasi positif dengan proliferasi
sel-sel sertoli. Oleh karena itu seperti yang dikemukakan oleh Takeuchi et al.
(2009), niche atau lingkungan mikro sel germinal yang terdapat di rongga genital
resipien yang berperan dalam proses proliferasi PGC endogen juga akan
memperkecil peluang sel eksogen atau sel donor terkolonisasi pada rongga
genital resipien.
Menurut Ijiri et al. (2008) larva ikan nila berumur 5–6 hpm merupakan titik
kritis atau titik awal bagi terjadinya diferensiasi gonad menjadi betina maupun
jantan. Sedangkan Takeuchi et al. (2009) menyatakan bahwa salah satu
penyebab sel donor tidak terkolonisasi karena adanya proses penolakan epitel
gonad resipien yang sedang berkembang. Jika gonad resipien telah terdiferensiasi
menjadi betina maka sel spermatogonia yang disuntikkan pada larva ikan nila
berumur 5 hpm atau lebih akan berpeluang untuk ditolak oleh epitel gonad
terdiferensiasi yang sedang berkembang. Oleh karena itu, meskipun tidak
terdapat perbedaan nyata antara efisiensi kolonisasi resipien ikan nila perlakuan
umur transplantasi 1, 3, 5 dan 7 hpm namun penggunaan larva ikan nila berumur 5
hpm atau lebih dapat memperkecil peluang sel donor terkolonisasi pada resipien.
Pada penelitian ini, tidak teramati adanya kecenderungan perbedaan
distribusi sel spermatogonia pada gonad terhadap umur transplantasi resipien
yang berbeda (Gambar 9).
51
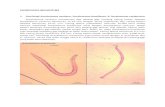
Gambar 9 Kolonisasi sel donor ikan gurami pada gonad resipien ikan nila
pascatransplantasi (pt) dengan posisi kepala di sebelah kiri
(posterior) dan ekor di sebelah kanan (anterior). A. Sel donor
(kepala panah) di bagian tengah gonad resipien 45 hari pt (perlakuan
larva 1 hari pascamenetas/hpm); B. Sel donor di bagian posterior
(dekat kepala) dari gonad resipien 72 hari pt (perlakuan larva 3
hpm); C. Sel donor di bagian tengah (di tepi pembuluh darah gonad,
panah kuning) dari gonad resipien 72 hari pt (perlakuan larva 5
hpm); D. Sel donor di bagian tengah dari gonad resipien 45 hari pt
(perlakuan larva 7 hpm), sebagian spermatogonia berada di bagian
luar gonad (panah putih); E-F. Gonad ikan nila yang tidak
ditransplantasi : tidak ada pendaran PKH 26.
Sel testikular dengan pendaran fluoresens merah umumnya terdapat di
bagian posterior hingga bagian tengah gonad 45 hari pt pada semua umur resipien.
Hasil pengamatan pada 2 ekor resipien perlakuan umur larva 7 hpm, di sekitar
gonadnya menempel beberapa sel yang berpendar yang memiliki bentuk bulat dan
52
berukuran sama besar dengan spermatogonia (Gambar 9D). Sel-sel tersebut
diduga merupakan spermatogonia yang tidak dapat bermigrasi ke rongga genital.
Keberhasilan kolonisasi sel donor ikan gurami pada gonad ikan nila juga
dibuktikan melalui metode PCR menggunakan marker GH ikan gurami. Pada
analisis kolonisasi melalui pengamatan sel donor yang dilabel pewarna fluoresens
PKH 26 tidak terdapat perbedaan efisiensi kolonisasi secara nyata antar perlakuan
umur larva. Pada penelitian ini digunakan sampel ekstraksi DNA gonad resipien
dari dua perlakuan umur resipien yaitu 3 dan 5 hpm yang diduga merupakan
resipien yang optimum untuk transplantasi berdasarkan tingkat kelangsungan
hidup atau sintasan pascatransplantasi dan efisiensi kolonisasi tertinggi. Dari
masing-masing 15 sampel gonad yang dianalisis sebanyak 26,7% (sumur c, d, f,
g) sampel gonad resipien ikan nila perlakuan 3 hpm, dan 16,7% (sumur h, j)
sampel gonad resipien ikan nila perlakuan 5 hpm yang teridentifikasi membawa
DNA ikan gurami (Gambar 10).
Gambar 10 Elektroforegram DNA produk PCR dari gonad resipien ikan nila 2
bulan pascatransplantasi menggunakan marka molekuler spesifik GH
ikan gurami dan primer β-aktin ikan nila sebagai kontrol internal.
Ket : a-g:sampel DNA nila transplantasi perlakuan 3 hari
pascamenetas (hpm), h-k:sampel DNA nila transplantasi 5 hpm, M:
marker DNA; G: DNA ikan gurami, N: DNA ikan nila,(-): kontrol
negatif bahan PCR.
Efisiensi kolonisasi menggunakan metode marka molekuler lebih rendah
dibandingkan dengan menggunakan metode pengamatan marker fluoresens PKH
26. Hal ini diduga karena jumlah sel donor yang terkolonisasi pada beberapa
gonad resipien relatif sedikit. Hasil uji sensitivitas marka molekuler GH
GH gurami
340 bp
β -aktin nila
150 bp
500 bp
bp
200 bp
bp
53
menunjukkan bahwa GH dapat mendeteksi 1 sel ikan gurami dalam 104 sel ikan
nila (Ahmad 2009). Sensitivitas marka molekuler GH diduga menjadi
penyebab sulitnya sel donor terdeteksi selama proses PCR. Menurut Kuske et al.
(1998), jumlah DNA template yang sedikit adalah salah satu faktor yang
mempengaruhi sensitivitas PCR dalam mendeteksi DNA target.
Kolonisasi Sel Donor Spermatogonia Ikan Gurami pada Ovari Ikan Nila
Hasil pengamatan dari 48 ekor jumlah sampel yang diperiksa, diperoleh 29
ekor yang berkelamin jantan dan 19 ekor berkelamin betina (rasio kelamin = 3 :
2). Sebanyak 44,90 % dari 49 ekor resipien membawa sel yang terwarnai PKH 26
dengan komposisi jantan dan betina masing-masing 50% dan 50% atau dengan
kata lain rasio kelamin jantan dan betina yang membawa sel donor adalah 1:1.
Hal ini menunjukkan bahwa sel spermatogonia ikan gurami yang diisolasi dari
gonad dewasa juga mampu terkolonisasi ke dalam jaringan gonad resipien betina
(Gambar 11).
Banyaknya jumlah ikan nila betina yang ditemukan membawa sel donor
menunjukkan bahwa sel testikular dalam penelitian ini tidak menyebabkan proses
maskulinisasi pada resipien. Yoshizaki et al. (2010) menyatakan bahwa
diferensiasi kelamin lebih banyak dipengaruhi oleh sel-sel somatik pada jaringan
gonad dibandingkan kontrol dari sel eksogen itu sendiri.
Menurut Yamamoto (1983) mekanisme yang sangat berperan dalam proses
diferensiasi kelamin pada ikan adalah kontrol dari regulasi hormon steroid yang
terdiri atas hormon androgen untuk maskulinisasi, estrogen untuk feminisasi dan
progesteron yang berhubungan dengan proses maturasi. Hormon-hormon tersebut
disekresikan oleh jaringan steroidogenik yang terdiri atas sel-sel granulosa dan
sel-sel theca pada ovari serta sel-sel Leydig dan sel-sel sertoli pada testis di bawah
pengaruh hormon gonadotropin di pituitari.
Beberapa penelitian telah menunjukkan bahwa sel spermatogonia pada ikan
rainbow trout dan ikan nibe memiliki kemampuan development plasticity yaitu
kemampuan untuk berkembang menjadi sel spermatosit dan derivatnya maupun
menjadi sel oosit dan derivatnya (Okutsu et al. 2006a, Takeuchi et al. 2009).
Kemampuan multipotensi ini umumnya dimiliki oleh sel punca dan penelitian ini
membuktikan bahwa pada sel testikular ikan gurami yang ditransplantasikan
54
masih terdapat sifat-sifat yang menyerupai sel punca yang selanjutnya
diidentifikasi sebagai spermatogonia belum terdiferensiasi atau SpA.
Lensa fluoresens Tanpa lensa fluoresens
Gambar 11 Ovari resipien ikan nila. A. Tanpa transplantasi, B. Perlakuan
umur transplantasi 1 hari pascamenetas (hpm), C. Perlakuan umur
transplantasi 3 hpm, D. Perlakuan umur transplantasi 5 hpm, E.
Perlakuan umur transplantasi 7 hpm. Kepala panah adalah sel
donor yang terkolonisasi. Skala = 100 µm.
55
Proliferasi Sel Donor pada Gonad Resipien
Dari hasil kolonisasi sel donor dengan pengamatan fluoresens, terdapat
beberapa gonad yang menunjukkan adanya indikasi proliferasi sel donor pada
gonad. Indikasi pertama adalah beberapa gonad ditemukan membawa sel donor
dalam bentuk kumpulan sel. Takeuchi et al. (2003) menggambarkan salah satu
indikasi terjadinya proliferasi adalah sel donor yang terkolonisasi membentuk
kumpulan sel (cluster) pada jaringan gonad resipien (Gambar 12). Gambar 12B
menunjukkan gonad resipien betina dengan kumpulan sel-sel yang terkolonisasi
dengan diameter yang hampir sama besar. Pada resipien jantan, kumpulan sel
donor yang terkolonisasi lebih sulit diamati morfologinya di bawah mikroskop
fluoresens yang digunakan (Gambar 12A).
Lensa fluoresens Lensa tanpa fluoresens
Gambar 12 Kumpulan sel donor ikan gurami yang terkolonisasi (kepala panah)
pada testis (A) dan ovari (B) resipien ikan nila pascatransplantasi.
Skala : 50µm.
Indikasi adanya proliferasi sel donor yang terkolonisasi pada gonad resipien
juga terlihat pada Gambar 13. Kedua gonad ini berasal dari perlakuan umur
transplantasi yang sama dan jumlah sel yang disuntikkan sama. Kedua gonad
dari resipien yang berbeda yang diisolasi dalam selang waktu 23 hari tersebut
C
D
56
terlihat memiliki perbedaan jumlah sel yang terwarnai PKH 26 sangat nyata.
Selain itu intensitas cahaya fluoresens yang dipancarkan oleh sel yang terwarnai
PKH 26 pun terlihat berbeda pada kedua gonad tersebut yang mana pada gonad
yang berumur 72 hari dengan jumlah sel yang lebih sedikit, intensitas warna sel-
selnya lebih terang dibandingkan dengan intensitas warna yang dipancarkan oleh
sel-sel pada gonad yang diisolasi pada umur 95 hari pada perlakuan yang sama.
Menurut Wallace et al. (2008) intensitas warna label pada sel dapat
menggambarkan banyaknya generasi pembelahan menggunakan metode flow
cytometry. Perbedaan intensitas warna PKH 26 pada kedua gonad tersebut
menunjukkan kemungkinan telah terjadi proses pembelahan sel (proliferasi sel).
Menurut Kobayashi et al. (2000), oogenesis pada ikan nila mulai
berlangsung pada umur 20-25 hpm dan pada umur 35 hpm tahap pembelahan
meiosis sudah terlihat (Kobayashi et al. 2010). Kumpulan sel donor pada Gambar
13 menunjukkan bahwa sel donor spermatogonia telah berproliferasi dengan cepat
dalam selang waktu 23 hari karena hampir semua bagian gonad terisi oleh sel
donor dan diduga telah terjadi proses perkembangan (diferensiasi) ditandai oleh
sebagian besar ukuran sel yang berpendar melebihi ukuran spermatogonia.
Berbeda halnya dengan ikan nila jantan, proses spermatogenesis terjadi
setelah ikan nila berumur 50 hpm (Kobayashi 2010). Pada penelitian ini,
beberapa gonad resipien yang diamati juga menunjukkan adanya kemungkinan
proliferasi sel spermatogonia ikan gurami yang ditandai dengan terdapatnya sel-
sel donor yang membentuk kumpulan sel baik pada resipien jantan berumur
sekitar 2 bulan maupun yang berumur sekitar 3 bulan. Hasil penelitian ini
menunjukkan bahwa sel spermatogonia ikan gurami kemungkinan telah
mengalami proses spermatogenesis pada umur sekitar 2 bulan. Meskipun belum
ada informasi bagaimana spermatogenesis berlangsung pada ikan gurami, namun
indikasi proliferasi sel spermatogonia pada ikan nila menunjukkan bahwa proses
proliferasi sel spermatogonia kemungkinan tidak banyak dipengaruhi oleh
mekanisme intrinsik yang berasal dari sel germinal itu sendiri melainkan
didominasi oleh peran lingkungan mikro sel germinal yaitu peran sel-sel somatik
pada gonad resipien.
57
Gambar 13 Gonad resipien ikan nila umur transplantasi 3 hari pascamenetas.
A. Resipien betina 72 hari pascatransplantasi (pt). B. Resipien
betina 95 hari pt. C,D (insersi). Pembesaran dari kotak. Kepala
panah menunjukkan kumpulan sel dengan ukuran yang sama,
indikasi terjadinya proliferasi. Skala= 100 µm.
Nagahama (1994) menggambarkan proses gametogenesis pada ikan
dikontrol oleh regulasi hormon gonadotropin yang disekresikan oleh kelenjar
pituitari. Pada ovari, hormon gonadotropin akan merangsang sel theca
memproduksi substrat androgen (testosteron). Testosteron berdifusi ke sel-sel
granulosa dan melalui aktivitas aromatase, testosterone dikonversi menjadi
estradiol 17-β (estrogen). Hormon estradiol ini kemudian merangsang sintesis
vitellogenin di hati untuk pembentukan kuning telur. Untuk proses pematangan
oosit dikatakan bahwa selain kontrol gonadotropin, terdapat pula peran kontrol
maturation-inducing hormone (MIH) dan maturation-promoting hormone (MPF).
Sedangkan pada testis, hormon gonadotropin berfungsi merangsang sel
Leydig memproduksi 11-ketotestosterone yang selanjutnya mengaktivasi sel
sertoli untuk memproduksi aktivin B. Aktivin B inilah yang selanjutnya
menginduksi proses mitosis sel spermatogonia. Untuk proses pematangan
menjadi spermatozoa diperankan oleh hormon 17α-hydroxyprogesterone pada sel-
D
58
sel somatik di bawah kontrol hormon gonadotropin (Nagahama 1994). Beberapa
hormon lain yang berperan dalam proses proliferasi dan diferensiasi oogonia dan
spermatogonia yaitu E2 dan 17,20 β-P (Young et al. 2004).
Sel spermatogonia ikan gurami diharapkan dapat berdiferensiasi menjadi sel
sperma pada jantan dan sel telur pada betina, namun sejauh mana keberhasilan
diferensiasi tersebut berlangsung juga sangat didukung oleh peran sel-sel somatik
ikan nila selama proses perkembangan sel germinal. Diferensiasi sel germinal
donor pada resipien yang jauh hubungan filogeninya membutuhkan hubungan
kerjasama yang tepat antara sel germinal donor dan sel somatik resipien seperti
misalnya sinyal-sinyal yang berperan dalam proses transfer material pembentuk
telur (Saito et al. 2008). Penelitian ini tidak akan melihat kemampuan sel donor
spermatogonia ikan gurami berdiferensiasi pada gonad resipien hingga
menghasilkan sel spermatozoa atau sel telur. Namun demikian hasil penelitian
yang menunjukkan bahwa sel spermatogonia ikan gurami mampu bermigrasi,
terkolonisasi dan kemungkinan berproliferasi merupakan awal dari
berlangsungnya spermatogenesis dan merupakan peluang bagi keberhasilan
aplikasi teknologi xenotransplantasi sel testikular ikan gurami kepada ikan nila.
KESIMPULAN
1. Umur resipien larva ikan nila yang optimum untuk transplantasi adalah 3 hari
pascamenetas.
2. Sel spermatogonia ikan gurami dapat terkolonisasi dan terdiferensiasi menjadi
sel oogonia pada gonad ikan nila betina.
3. Kumpulan sel donor ikan gurami pada gonad resipien ikan nila
mengindikasikan terjadinya proliferasi sel donor.