EFEKTIVITAS EKSTRAK PROPOLIS Trigona sp … · Antibiotik yang digunakan pada ... Penyakit...
Transcript of EFEKTIVITAS EKSTRAK PROPOLIS Trigona sp … · Antibiotik yang digunakan pada ... Penyakit...

i
EFEKTIVITAS EKSTRAK PROPOLIS Trigona sp TERHADAP
PERTUMBUHAN BAKTERI Porphyromonas gingivalis
SKRIPSI
Diajukan sebagai Salah Satu Syarat untuk Mencapai Gelar
Sarjana Kedokteran Gigi
OLEH :
HETTY NOVEILIGA CINDRAKORI
J111 12 125
BAGIAN PERIODONTOLOGI
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS HASANUDDIN
MAKASSAR
2015

ii

iii
SURAT PERNYATAAN
Dengan ini menyatakan bahwa mahasiswa yang tercantum namanya dibawah ini :
Nama : Hetty Noveiliga Cindrakori
NIM : J111 12 125
Judul Skripsi : Efektivitas Ekstrak Propolis Trigona sp terhadap Pertumbuhan
Bakteri Porphyromonas gingivalis
Menyatakan bahwa judul skripsi yang diajukan adalah judul yang baru dan tidak
terdapat di Perpustakaan Fakultas Kedokteran Gigi Universitas Hasanuddin
Makassar, September 2015
Staf Perpustakaan FKG-UH
Nuraeda A, S.Sos

iv
KATA PENGANTAR
Assalamualaikum Warahmatullahi Wabarakatuh
Alhamdulillahirabbil’alamin. Puji dan syukur penulis panjatkan kehadirat
Allah SWT atas nikmat dan karunia-Nya sehingga penulis dapat menyelesaikan
penyusunan skripsi yang berjudul “Efektivitas Ekstrak Propolis Trigona sp terhadap
Pertumbuhan Bakteri Porphyromonas gingivalis”. Skripsi ini merupakan salah satu
syarat untuk mencapai gelar Sarjana Kedokteran Gigi di Fakultas Kedokteran Gigi
Universitas Hasanuddin. Tak lupa pula penulis panjatkan shalawat dan salam kepada
nabi kita, Nabi Muhammad SAW.
Dalam penyusunan skripsi ini terdapat banyak hambatan yang dihadapi,
namun berkat bantuan dan bimbingan dari berbagai pihak sehingga penyusunan
skripsi ini dapat terselesaikan dengan baik. Oleh karena itu, pada kesempatan ini
penulis ingin menyampaikan terima kasih yang sebesar-besarnya kepada :
1. Dr. drg. Asdar Gani, M.Kes., selaku dosen pembimbing yang telah banyak
meluangkan waktu untuk memberikan pengarahan dan memberikan petunjuk serta
bimbingan bagi penulis dalam menyelesaikan penelitian dan penyusunan skripsi
ini hingga selesai.
2. Dr. drg. Bahruddin Thalib, M.Kes., Sp.Pros sebagai Dekan Fakultas
Kedokteran Gigi Universitas Hasanuddin beserta seluruh staf atas bantuannya
selama penulis mengikuti pendidikan.
3. drg. Susilowati, M.Kes., Sp.Ort selaku Penasehat Akademik atas bimbingan,
perhatian, nasehat dan dukungan bagi penulis selama perkuliahan.

v
4. Buat kedua orang tua yang tersayang dan tercinta, Ayahanda Ir. H.M. Ilyas
Timu, MM dan (Almh.) Ibu Ir. Hj. Hamsigar A. dan saudara penulis Arief
Kurniawan Ilyas serta keluarga besar penulis yang telah banyak memberikan
doa, dukungan moril dan materiil, dan terima kasih atas segala pengertian yang
telah diberikan selama proses penyusunan skripsi ini hingga selesai.
5. Teman-teman MASTIKASI 2012 terima kasih atas dukungan penuh dan
semangat yang terus diberikan kepada penulis, terima kasih atas tangis haru canda
dan tawanya selama 3 tahun, saya bangga bisa menjadi bagian dari 103 bintang.
Semoga tetap kompak dan semoga MASTIKASI sukses untuk kedepannya.
6. Sahabat penulis Nana, Kais, Ai, Keky, Lala, Kiki, Abang, Guce, Agung,
Husein, Alief terimakasih atas hiburan, liburan dan motivasinya dalam
menyelesaikan skripsi ini dan terkhusus untuk Rifdatul Ahwal Usemahu terima
kasih atas motivasi dan semangatnya, terima kasih juga atas perhatian, kasih
sayang dan kesabarannya dalam menghadapi penulis.
7. Teman skripsi bagian periodontologi Ribka, Kevin, Nuqi, Ilha, Echa, Gaby,
Wahdan, Nunu terima kasih atas ide-ide serta masukan yang diberikan kepada
penulis.
8. Saudara-saudara kesayangan Waddah, Bhollo, Opi, Iman, Ani, Sapri, Callu,
Sule, Ningsih, Mentari terima kasih banyak atas doa, dukungan, hiburan dan
liburannya disela-sela pusing dan ribetnya penelitian. Untuk Cimmi, Neno, Nina,
Muti dan Accang terima kasih atas doa dan dukungannya.
9. Kanda-kanda senior Kak Dawal, Kak Khadijah, Kak Tommy, Kak Nugi, Kak
Jojo, Kak Novi, Kanda-kanda Atrisi 2010, Kanda-kanda Oklusal 2011,

vi
Himpunan mahasiswa Islam Komisariat Kedokteran Gigi dan semua kanda-
kanda senior yang tidak bisa disebutkan satu-persatu. Terima kasih atas masukan
dan dukungannya.
10. Saudara penulis selama ber-KKN, Siti Hardiyanti Syam, Anitawati Umar,
Armi Rauf, M. Ilham Eka Putra, Wahyudi Kasrul, Wardiman Lukas,
terimakasih atas pengertian dan motivasinya selama di posko. Terima kasih juga
untuk hiburan dan liburannya.
11. Seluruh Dosen, Staf Akademik, Staf Tata Usaha, Staf Perpustakaan FKG
UNHAS dan Staf Bagian Periodontologi yang telah banyak membantu penulis.
12. Semua pihak yang tidak dapat penulis sebutkan satu persatu, terimakasih atas
bantuannya.
Dengan segala kerendahan hati, penulis memohon maaf jika terdapat kesalahan
dalam penulisan skripsi. Penulis berharap skripsi ini dapat bermanfaat bagi pembaca
dan penulis sendiri.
Wassalamualaikum Warahmatullahi Wabarakatuh
Makassar, 9 September 2015
Penulis

vii
EFEKTIVITAS EKSTRAK PROPOLIS Trigona sp TERHADAP
PERTUMBUHAN BAKTERI Porphyromonas gingivalis
Hetty Noveiliga Cindrakori
Mahasiswa Fakultas Kedokteran Gigi
Universitas Hasanuddin
ABSTRAK
Latar belakang : Penyakit periodontal disebabkan oleh berbagai faktor, deposit
bakteri berperan penting terhadap terjadinya penyakit periodontal. Salah satu bakteri
yang berperan terhadap terjadinya penyakit periodontal ialah Porphyromonas
gingivalis. Propolis merupakan bahan alami yang memiliki sifat antibakteri. Khasiat
antibakteri pada propolis berbeda bergantung pada jenis propolis. Propolis telah
digunakan untuk pengobatan apthous ulser, kandidiasis, gingivitis, periodontitis, dan
pulpitis. Tujuan : Penelitian ini bertujuan untuk mengetahui efektivitas ekstrak
propolis Trigona sp dalam bentuk gel terhadap pertumbuhan Porphyromonas
gingivalis. Metode : Jenis penelitian ini adalah eksperimental laboratorium. Uji daya
hambat dilakukan dengan metode difusi menggunakan bahan uji propolis gel dan
metronidazole gel. Zona daya hambat propolis gel terhadap Porphyromonas
gingivalis diukur menggunakan jangka sorong setelah inkubasi 1x24 jam, 2x24 jam,
dan 3x24 jam. Hasil : Zona daya hambat propolis gel terhadap Porphyromonas
gingivalis dalam pengamatan 1x24 jam, 2x24 jam, 3x24 jam berturut-turut 6.17±0.48
mm, 5.76±0.55 mm, 5.23±0.32 mm, sedangkan zona daya hambat metronidazole gel
terhadap Porphyromonas gingivalis dalam pengamatan 1x24 jam, 2x24 jam, 3x24
jam berturut-turut 13.68±1.66 mm, 13.94±2.03 mm, 12.90±1.96 mm. Adapun selisih
rerata diameter zona daya hambat antara propolis gel dan metronidazole gel pada
waktu pengamatan 1x24 jam, 2x24 jam, 3x24 jam berturut-turut 7.51 mm, 8.18 mm,
7.66 mm. Kesimpulan : Pada penelitian ini, berdasarkan uji independent t-test zona
daya hambat metronidazole gel lebih besar daripada zona daya hambat propolis gel
terhadap bakteri Porphyromonas gingivalis (p<0.05), dan berdasarkan uji repeated
Anova rata-rata zona daya hambat tidak berbeda bermakna berdasarkan waktu
pengamatan (p>0.05).
Kata Kunci : Antibakteri, propolis gel, Porphyromonas gingivalis, penyakit
periodontal

viii
EFFECTIVITY OF EXTRACT PROPOLIS Trigona sp AGAINST THE
GROWTH OF Porphyromonas gingivalis BACTERIA
Hetty Noveiliga Cindrakori
Mahasiswa Fakultas Kedokteran Gigi
Universitas Hasanuddin
ABSTRACT
Background : Periodontal disease is caused by various factors. Bacterial deposit
plays an important role against the occurrence of periodontal disease. One of the
bacterias that contribute to the occurrence of periodontal disease is Porphyromonas
gingivalis. Propolis is a natural substance contains antibacterial properties which are
different depends on the type of propolis. Propolis has been used for the treatment of
apthous ulcer, candidiasis, gingivitis, periodontitis, and pulpitis. Purpose : The
purpose of the study is determine effectivity of extract gel propolis Trigona sp
against the growth of Porphyromonas gingivalis. Methods : This research is an
experimental laboratories. Inhibition test performed a diffusion method using
propolis and metronidazole gel. Inhibition zone of propolis and metronidazole gel
against Porphyromonas gingivalis were measured using calipers after incubation
1x24 hours, 2x24 hours, and 3x24 hours. Result : The zone of propolis gel and
metronidazole gel inhibition against Porphyromonas gingivalis observed in 1x24
hours, 2x24 hours, 3x24 hours. Propolis gel consecutive are 6.17±0.48 mm,
5.76±0.55 mm, 5.23±0.32 mm, whereas metronidazole gel consecutive are
13.68±1.66 mm, 13.94±2.03 mm, 12.90±1.96 mm, and the difference of both
inhibition zone based on time 1x24 hours, 2x24 hours, 3x24 hours are 7.51 mm, 8.18
mm, 7.66 mm. Conclusion : In this study, based on independent t-test, metronidazole
gel zone of inhibition greater than propolis gel zone againsts the bacteria
Porphyromonas gingivalis (p<0.05), and the test repeated ANOVA based on average
zone of inhibition did not differ significantly by time observation (p>0.05).
Keywords : Antibacterial, propolis gel, Porphyromonas gingivalis, periodontal
disease

ix
DAFTAR ISI
HALAMAN JUDUL ....................................................................................... i
HALAMAN PENGESAHAN ......................................................................... ii
SURAT PERNYATAAN ................................................................................ iii
KATA PENGANTAR .................................................................................... iv
ABSTRAK ...................................................................................................... vii
DAFTAR ISI ................................................................................................... ix
DAFTAR GAMBAR ...................................................................................... xii
DAFTAR TABEL ........................................................................................... xiii
BAB I PENDAHULUAN
1.1. ................................................................................................. Latar
belakang ............................................................................................ 1
1.2. .................................................................................................
Rumusan masalah ............................................................................. 5
1.3. ................................................................................................. Tujuan
penelitian ........................................................................................... 5
1.4. .................................................................................................
Hipotesis penelitian ........................................................................... 5
1.5. .................................................................................................
Manfaat penelitian ............................................................................ 5
BAB II TINJAUAN PUSTAKA

x
2.1. .................................................................................................
Periodontitis ....................................................................................... 6
2.1.1. ........................................................................................ Definisi
periodontitis ............................................................................. 6
2.1.2. ........................................................................................ Etiologi
periodontitis ............................................................................. 7
2.1.3. ........................................................................................
Patogenesis periodontitis ......................................................... 8
2.1.4. ........................................................................................ Terapi
yang dapat diberikan pada periodontitis .................................. 11
2.2. ................................................................................................. Bakteri
Porphyromonas gingivalis ................................................................. 15
2.2.1. ........................................................................................
Klasifikasi dan morfologi Porphyromonas gingivalis ............ 15
2.2.2. ........................................................................................
Porphyromonas gingivalis sebagai periodontopatogen utama
pada periodontitis .................................................................... 16
2.3. .................................................................................................
Propolis .............................................................................................. 19
2.3.1. ........................................................................................ Definisi
propolis .................................................................................... 19
2.3.2. ........................................................................................
Kandungan propolis ................................................................. 21

xi
2.3.3. ........................................................................................
Manfaat propolis ...................................................................... 22
2.3.4. ........................................................................................
Aktivitas antibakteri pada propolis .......................................... 24
BAB III KERANGKA KONSEP
3.1. .................................................................................................
Kerangka konsep penelitian .............................................................. 26
3.2. ................................................................................................. Alur
penelitian ........................................................................................... 27
BAB IV METODE PENELITIAN
4.1. ................................................................................................. Jenis
penelitian ........................................................................................... 28
4.2. ................................................................................................. Rancang
an penelitian ..................................................................................... 28
4.3. ................................................................................................. Tempat
dan waktu penelitian ......................................................................... 28
4.3.1. ........................................................................................ Tempat
penelitian ............................................................................... 28
4.3.2. ........................................................................................ Waktu
penelitian ............................................................................... 28
4.4. ................................................................................................. Variabel
penelitian ............................................................................................ 28

xii
4.4.1. ........................................................................................ Variabel
menurut fungsinya ................................................................ 28
4.4.2. ........................................................................................ Variabel
menurut skala pengukurannya ............................................... 29
4.5. ................................................................................................. Definisi
operasional variabel .......................................................................... 29
4.6. ................................................................................................. Subyek
penelitian ........................................................................................... 29
4.7. ................................................................................................. Sampel
penelitian ........................................................................................... 29
4.8. ................................................................................................. Alat dan
bahan ................................................................................................. 30
4.8.1. ........................................................................................ Alat
.................................................................................................. 30
4.8.2. ........................................................................................ Bahan
.................................................................................................. 30
4.9. ................................................................................................. Prosedu
r penelitian ...................................................................................... 31
4.9.1. ........................................................................................ Prosedu
r sterilisasi alat ...................................................................... 31
4.9.2. ........................................................................................ Prosedu
r pembuatan medium MHA (Mueller Hinton Agar) .............. 31

xiii
4.9.3. ........................................................................................ Prosedu
r ekstraksi propolis ................................................................ 32
4.9.4. ........................................................................................ Prosedu
r pembuatan propolis gel ....................................................... 33
4.9.5. ........................................................................................ Uji daya
hambat ................................................................................... 33
4.9.6. ........................................................................................ Pengam
atan zona hambat ................................................................... 33
4.10. ............................................................................................... Analisis
data ................................................................................................. 33
4.10.1. ...................................................................................... Jenis
data ........................................................................................ 33
4.10.2. ...................................................................................... Pengola
han data ................................................................................. 34
4.10.3. ...................................................................................... Analisis
data ........................................................................................ 34
BAB V HASIL ................................................................................................ 35
BAB VI PEMBAHASAN ............................................................................... 40
BAB VII PENUTUP
7.1. ................................................................................................ Kesimp
ulan .................................................................................................... 45
7.2. ................................................................................................ Saran
............................................................................................................ 46

xiv
DAFTAR PUSTAKA ..................................................................................... 47
LAMPIRAN .................................................................................................... 55
DAFTAR GAMBAR
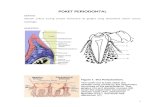
Gambar 2.1. Periodontitis ............................................................................... 6
Gambar 2.2. Porphyromonas gingivalis ......................................................... 16
Gambar 2.3. Propolis ...................................................................................... 20
Gambar 5.1. Grafik distribusi diameter zona hambat (mm) berdasarkan waktu
pengamatan pada intervensi propolis gel dan metronidazol gel 36

xv
DAFTAR TABEL
Tabel 2.1. Antibiotik yang digunakan pada terapi penyakit periodontal ........ 12
Tabel 2.2. Dosis Antibiotik yang digunakan untuk Terapi Penyakit Periodontal 14
Tabel 2.3. Komposisi Kimia Propolis ............................................................. 22
Tabel 5.1. Perbedaan rata-rata diameter zona hambat (mm) berdasarkan waktu
pengamatan pada masing-masing kelompok intervensi ................. 36
Tabel 5.2. Perbedaan rata-rata diameter zona hambat (mm) antara propolis gel dan
metronidazole gel pada waktu pengamatan 1x24 jam, 2x24 jam, dan
3x24 jam ......................................................................................... 38

1
BAB I
PENDAHULUAN
1.1...................................................................................................................... L
atar belakang
Di Indonesia penyakit periodontal menduduki urutan ke dua utama yang masih
merupakan masalah di masyarakat yaitu mencapai 96.58% (Riskesdas, 2007).
Penyakit yang menyerang gingiva dan jaringan pendukung gigi ini merupakan
penyakit infeksi yang serius dan apabila tidak dilakukan perawatan yang tepat dapat
mengakibatkan kehilangan gigi (Hinrichs, dkk., 2012). Periodontitis atau penyakit
yang menyerang gingiva menjangkit jutaan orang setiap tahun. Hal ini dilaporkan
sebagai penyakit yang paling banyak terjadi diseluruh dunia dengan perkiraan 85%.
Prevalensi penyakit periodontal adalah 24.2% sedangkan prevalensi gingivitis 19.5%
(Stein, dkk., 2008).
Penyakit periodontal dapat didefinisikan sebagai proses patologis yang mengenai
jaringan periodontal. Sebagian besar penyakit inflamatif disebabkan oleh infeksi
bakteri. Walaupun faktor-faktor lain juga dapat mempengaruhi jaringan periodontal,
penyebab utama penyakit periodontal adalah mikroorganisme yang berkolonisasi di
permukaan gigi (Fedi, dkk., 2000). Penyakit periodontal dimulai dari gingivitis yang
bila tidak terawat bisa berkembang menjadi periodontitis dimana terjadi kerusakan
jaringan pendukung periodontal berupa kerusakan fiber, ligamen periodontal dan
tulang alveolar (Wahyukundari, 2009). Beberapa kelainan sistemik juga dapat

2
berpengaruh terhadap jaringan periodontal, tetapi faktor sistemik tanpa invasi dari
plak bakteri tidak dapat menjadi pencetus terjadinya periodontitis. Mikroorganisme
yang berperan penting dalam terjadinya penyakit periodontal adalah Aggregatibacter
actinomycetemcomitans (Aa), Porphyromonas gingivalis (Pg), Prevotella intermedia
(Pi), Bacteroides forsythus (Bf), Fusobacterium nucleatum (Fn), Capnocytophaga
spp (C.sp), Campylobacter rectus (Cr). Masing-masing bakteri memiliki faktor
virulensi (komponen dari struktur sel, eksotoksin dan endotoksin) berkaitan dengan
proses penyakit periodontal. Bakteri dan produknya merangsang pembengkakan
yang menghasilkan mediator proinflamasi seperti sitokin dan prostaglandin yang
merusak jaringan periodontal (Kumar, dkk., 2003; Paster, dkk., 2006).
Diantara penyakit mulut, periodontitis merupakan penyakit yang paling lazim
pada populasi orang dewasa di seluruh dunia. Yang disebabkan oleh mikrobiota yang
kompleks, Porphyromonas gingivalis dan Aggregatibacter actinomycetemcomitans
diduga sebagai patogen yang mendominasi untuk proses inisiasi dan kerusakan dari
struktur pendukung gigi (Zambon, 1996). Kegoyangan gigi merupakan salah satu
gejala penyakit periodontal yang ditandai dengan hilangnya perlekatan serta
kerusakan tulang vertikal (Strassler, 2004).
Telah banyak dilakukan penelitian dengan memanfaatkan bahan alam yang
bertujuan untuk menghasilkan obat yang mempunyai efek samping yang tidak
merugikan, salah satunya adalah propolis (Lofty, 2006). Propolis berasal dari bahasa
Yunani, yaitu pro berarti pertahanan dan polis berarti kota, sehingga propolis dapat
diartikan sebagai pertahanan kota (Ghisalberti, 1979; Santos, dkk., 2002).

3
Propolis merupakan produk yang dihasilkan oleh serangga (lebah madu). Lebah
menghasilkan beberapa produk seperti madu, royal jeli, polen dan propolis. Propolis
merupakan bahan resin yang melekat pada bunga, pucuk dan kulit kayu. Sifatnya
pekat, bergetah, berwarna cokelat kehitaman mempunyai bau yang khas, dan rasa
pahit. Lebah menggunakan bahan propolis untuk pertahanan sarang, mengkilatkan
bagian dalam sarang dan menjaga suhu lingkungan. Bahan-bahan yang terkandung
dalam propolis sangat kompleks, dan lebih dari 200 komponen telah teridentifikasi
(Kaihena, 2013).
Lebah propolis bersifat desinfektan (antibakteri) yang dapat membunuh serangga
yang masuk ke sarang lebah, lebah juga melindungi sarangnya dengan propolis dari
virus atau bakteri. Hal ini yang mendasari propolis digunakan sebagai antibiotik.
Kelebihan propolis dibanding antibiotik lainnya adalah efek sampingnya yang kecil
dan tidak menimbulkan resistensi (Lofty, 2006). Penelitian sementara menekankan
sifat antimikroba dan antiinflamasi pada propolis. Sifat antiinflamasi pada propolis
karena adanya caffeic acid phenethyl ester (CAPE) dalam propolis. Flavonoid dan
derivat asam sinamat dianggap sebagai komponen biologis utama yang aktif dalam
propolis (Gebara, dkk., 2002; Borrelli, dkk., 2002). Disamping itu propolis juga
memiliki khasiat immunomodulator sebagai obat anti radang karena dapat
meningkatkan ketahanan tubuh alami terhadap beberapa infeksi. Propolis juga dapat
mempercepat penyembuhan luka (Castaldo, dkk., 2002). Kemampuan antimikroba
propolis ditentukan oleh flavonoid, pinocembrin, galangin dan pinobanksin
(Castaldo, dkk., 2002; Pietta, dkk., 2002). Propolis telah digunakan untuk
pengobatan apthous ulser, kandidiasis, gingivitis, periodontitis, dan pulpitis. Studi

4
mengenai penggunaan propolis telah meningkat karena sifat terapeutik dan
biologisnya (Coutinho, 2012; Gebara, dkk., 2002).
Penggunaan propolis di bidang kedokteran gigi baru dilaporkan beberapa tahun
terakhir. Hasilnya menunjukkan bahwa propolis dapat digunakan sebagai salah satu
bahan pengobatan alternatif (Scheller, dkk., 1990; Martinez-Silveira, dkk., 1988;
Murray, dkk., 1997). Penelitian sistematis pertama dibuat oleh Kivalkina pada tahun
1948, dan sejak saat itu efek antibakteri dari propolis ditunjukkan pada berbagai
macam bakteri Gram positif dan Gram negatif (Ghisalberti, 1979; Grange, dkk.,
1990).
Sejumlah studi mendokumentasikan fungsi biosidal propolis, ekstrak dan
kandungan terpenting dari propolis. Aktivitas dengan spektrum luas, dengan
melawan Gram positif dan Gram negatif batang dan kokus, yeast dan jamur
(Burdock, 1998). Salah satu keterbatasan penggunaan propolis adalah variabilitas
dalam komposisi dan kemampuannya sebagai akibat dari variasi flora daerah dimana
propolis dihasilkan. Menurut Gebara dkk, hasil penelitiannya menunjukkan bahwa
aktivitas antimikroba ekstrak propolis pada studi in vitro, tidak hanya terhadap
beberapa bakteri periodontopatik (Fusobacterium nucleatum, Porphyromonas
gingivalis, Prevotella intermedia, Prevotella melaninogenica, Aggregaibacter
actinomycetemcomitans dan Capnocytophaga gingivalis) tetapi juga terhadap
beberapa organisme yang dapat menyebabkan infeksi (Staphylococcus aureus,
Pseudomonas aeruginosa, Escherichia coli, dan Candida albicans) (Gebara,
dkk.,2002).

5
1.2...................................................................................................................... R
umusan masalah
Bagaimana efektivitas ekstrak propolis Trigona sp dalam bentuk gel terhadap
pertumbuhan bakteri Porphyromonas gingivalis pada penyakit periodontal?
1.3...................................................................................................................... T
ujuan penelitian
Untuk mengetahui efektivitas ekstrak propolis Trigona sp dalam bentuk gel
terhadap pertumbuhan bakteri Porphyromonas gingivalis pada penyakit periodontal.
1.4...................................................................................................................... H
ipotesis penelitian
Ekstrak propolis Trigona sp dalam bentuk gel efektif terhadap pertumbuhan
bakteri Porphyromonas gingivalis pada penyakit periodontal.
1.5...................................................................................................................... M
anfaat penelitian

6
Untuk menambah pengetahuan mengenai propolis sebagai bahan alami yang
dapat digunakan pada terapi penyakit periodontal.
BAB II
TINJAUAN PUSTAKA
2.1. .................................................................................................................... P
eriodontitis
2.1.1. ..................................................................................................................
Definisi periodontitis
Periodontitis didefinisikan sebagai proses inflamasi yang terjadi pada jaringan
pendukung gigi yang disebabkan karena mikroorganisme spesifik, sehingga terjadi
kerusakan yang progresif pada ligamentum periodontal dan tulang alveolar yang
ditandai dengan hilangnya perlekatan, peningkatan kedalaman poket, dan resesi
gingiva (Hinrichs, dkk., 2012).

7
Gambar 2.1. Periodontitis (Sumber : http://www.3dk.cz/en/periodontology/chronic-periodontitis/)
Peradangan kronis pada periodontitis merupakan respon terhadap bakteri pada
biofilm dalam rongga mulut. Selain kehadiran periodontopatogen seperti
Porphyromonas gingivalis, Aggregatibacter actinomycetemcomitans dan Tannerella
forsythia, faktor genetik dan lingkungan juga mampu meningkatkan kerentanan
beberapa individu pada perkembangan penyakit periodontitis (Feng, dkk., 2006).
Perkembangan penyakit ini terjadi karena kombinasi dari beberapa faktor, termasuk
adanya bakteri periodontopatik, meningkatnya proinflammatory cytokines, Matriks
metalloproteinasae (MMPs), prostaglandin E2 (PGE2), menurunnya tingkat anti-
inflammatory cytokines termasuk interleukin-10 (IL-10), transforming growth factor
(TGF-β) dan tissue inhibitors of MMPs (TIMPs) (Gemmell, dkk., 2004; Page, dkk.,
1997).
2.1.2. Etiologi periodontitis
Etiologi dari penyakit ini bisa disebabkan oleh berbagai faktor, deposit bakteri
berperan penting dalam patogenesis periodontitis. Meskipun patogenesis
periodontitis multifaktorial termasuk faktor genetik dan epigenetik, pengembangan
periodontitis dimodulasi oleh mikroba biofilm yang terbentuk pada daerah di sekitar

8
gigi, dan kemudian memunculkan reaksi inflamasi dari host (Teles, dkk., 2012;
Teles, dkk., 2010).
Bakteri yang terlibat dalam periodontitis terakumulasi dalam plak subgingiva
yang terdiri dari sebagian besar bakteri anaerob Gram negatif (Noyan, dkk., 1997)
yang dapat menimbulkan respon inflamasi gingiva, dan berlanjut ke struktur jaringan
penyangga gigi yaitu sementum, ligamentum periodontal dan tulang alveolar.
Keadaan tersebut mengakibatkan hilangnya perlekatan gingiva dan terjadinya
kerusakan tulang alveolar lebih dalam, pembentukan poket periodontal, migrasi
patologis yang menimbulkan diastema, dan kegoyangan gigi yang dapat berakibat
tanggalnya gigi (Henry, dkk., 2012). Kegoyangan gigi merupakan salah satu gejala
penyakit periodontal yang ditandai dengan hilangnya perlekatan serta kerusakan
tulang vertikal (Strassler, 2004). Kegoyangan dapat disebabkan karena adanya
kerusakan tulang yang menyangga gigi, trauma oklusi, dan adanya perluasan
peradangan dari gingiva ke jaringan pendukung yang lebih dalam, serta proses
patologik rahang (Fedi, dkk., 2000).
Secara khusus, perkembangan penyakit berhubungan dengan proliferasi dari
spesies bakteri anaerob Gram negatif seperti Porphyromonas gingivalis, Treponema
denticola, dan Tannerella forsythia (Socransky,dkk., 1998).
2.1.3. ..................................................................................................................
Patogenesis periodontitis
Periodontitis merupakan sebuah infeksi kompleks yang berasal dari bakteri
dengan beberapa faktor yang terlibat. Sebagian dari mikroorganisme tersebut dapat
menyebabkan kerusakan jaringan dengan dua cara, yaitu secara langsung, melalui

9
invasi jaringan dan produksi zat-zat berbahaya yang menyebabkan kematian sel dan
nekrosis jaringan. Secara tidak langsung, melalui aktivasi dari sel-sel inflamasi yang
dapat menghasilkan dan melepaskan mediator. Hal ini memainkan peran penting
dalam proses penghancuran jaringan periodontal, sementara beberapa bakteri
mengganggu mekanisme pertahanan host dengan menonaktifkan antibodi spesifik
atau menghambat aksi dari sel-sel fagosit (Genco, 1992; Williams, 1990).
Penyakit periodontal manusia telah dikaitkan dengan mikrobiota yang kompleks.
Komposisi dari flora subgingiva dan tingkat patogenitas mikrobiota pada setiap
orang berbeda. Bakteri Gram positif kokus berkaitan dengan kesehatan periodontal,
sedangkan penyakit periodontal dikaitkan dengan Gram negatif batang dan
spirochetes (Kesic,, dkk., 2008; Listgarten, 1976). Banyak penelitian yang
menunjukkan bahwa Aggregatibacter actinomycetemcomitans¸ Bacteroides
gingivalis (Porphyromonas gingivalis), dan Bacteroides intermedius (Prevotella
intermedia) berhubungan dengan penyakit periodontal aktif. Spesies lain yang juga
berkaitan dengan penyakit periodontal seperti Fusobacterium nucleatum, dan
Capnocytophaga sp (Dzink, dkk., 1988; Slots, dkk., 1984; Socransky, dkk., 1988;
Zambon, 1996). Berdasarkan Consensus report of the World Workshop on Clinical
Periodontitis (1996), periodontitis pada manusia dimulai dan diabadikan oleh
sekelompok bakteri yang berkolonisasi di daerah subgingiva, terutama Gram negatif,
anaerob atau bakteri mikroaerofilik. Sebagian besar kasus periodontitis pada manusia
disebabkan oleh Porphyromonas gingivalis, Bacteroides forsythus, dan
Aggregatibacter actinomycetemcomitans (Zambon, 1996). Mikroorganisme dapat

10
menghasilkan penyakit secara langsung dengan invasi pada jaringan, atau secara
tidak langsung oleh enzim bakteri dan toksin (Ezzo, dkk., 2003).
Jaringan periodontal tersusun dari komponen matriks ekstraseluler yaitu kolagen
yang berperan dalam proses regenerasi dan kerusakan jaringan. Kolagen interstisial
jaringan periodontal berfungsi untuk penyembuhan dan pembentukan jaringan baru.
Penyakit periodontal didefinisikan sebagai penyakit yang kehilangan struktur
kolagennya pada daerah yang menyangga gigi, sebagai respon dari akumulasi bakteri
pada jaringan periodontal, tapi patogenesis secara molekular masih belum jelas.
Matriks metalloproteinase (MMPs) diduga berperan secara bermakna pada penyakit
periodontal ini (DeCarlo, dkk., 1997). MMPs merupakan enzim proteolitik dimana
dalam proses proteinasenya yang diperlihatkan melalui patogen periodontal yang
terinfeksi, akan mengaktifkan MMPs inaktif sehingga terlibat dalam degradasi
makromolekul matriks ekstraseluler, termasuk juga terlibat dalam degradasi
ligamentum periodontal (Hansen, 1995). Proses penyembuhan ini secara enzimologi
bisa digambarkan dengan adanya penurunan kadar MMP-8 yang berperan aktif
dalam patogenesis periodontitis. MMP-8 dikenal predominan dan bentuk paling
umum dari penyakit periodontal (Teronen, dkk., 1997). MMP terlibat dalam
degradasi matriks kolagen interstisial ekstraseluler. MMPs yang diduga berperan
dalam banyak proses perubahan fisiologis dan patologis misalnya arthritis, invasi
kanker dan metastasis, ulser jaringan, termasuk dalam penyakit periodontal, terlibat
dalam degradasi ligamentum periodontal (DeCarlo, dkk., 1997). MMP-8 disebut juga
enzim kolagenase yaitu enzim yang dapat memecah kolagen pada peristiwa
remodeling jaringan. Enzim MMP-8 ini dihasilkan oleh bakteri penyebab kelainan

11
periodontal yang berpotensi merusak jaringan penyangga gigi dengan cara merusak
kolagen tipe I (Rams, dkk., 1996). Kolagenase merupakan suatu peristiwa untuk
memecah kolagen yang dianggap penting pada proses terjadinya penyakit
periodontal dan mengaktifkan MMPs untuk mengawali atau mempercepat degradasi
kolagen ligamentum periodontal (DeCarlo, dkk., 1997).
MMPs merupakan suatu enzim proteolitik yang mempengaruhi degradasi dari
makromolekul matriks ekstraseluler, yaitu kolagen interstisial dan kolagen
membrana basalis, fibronektin, laminin dan proteoglikan (Ingman, dkk., 1996).
MMPs disintesis dan disekresi dalam suatu bentuk proenzim inaktif. Secara alami
muncul penghambat MMPs yaitu tissue inhibitor matriks metalloproteinase (TIMP ),
kontrol yang penting terhadap setiap aksi dari MMPs. Secara fisiologis, MMP-8 dan
penghambatnya telah ada dalam jaringan periodontal, namun bila tak ada
keseimbangan antara MMP-8 dengan TIMP maka akan terjadi peristiwa patogen
pada jaringan periodontal, dimana jumlah MMP-8 akan meningkat dan terjadi
degradasi matriks ekstraseluler (Hayakawa, 1998).
2.1.4. Terapi yang dapat diberikan pada penyakit periodontal
Umumnya perawatan penyakit periodontal melibatkan terapi mekanik (non-
bedah atau debridement). Perawatan periodontal meliputi beberapa fase, antara lain
fase I (fase non-surgical) yaitu, fase terapi inisiasi meliputi kontrol plak secara
komprehensif, menghilangkan kalkulus dan plak mikroba, mengoreksi restorasi yang
rusak, perawatan lesi karies, terapi antimikroba, splinting, dan occlusal adjustment.
Prosedur ini merupakan bagian yang diperlukan pada terapi periodontal, terlepas dari
keparahan penyakit tersebut. Selanjutnya evaluasi dari fase I cek kedalaman poket,

12
inflamasi gingiva, plak, kalkulus dan karies. Kemudian pada fase II (fase surgical)
prosedur yang dilakukan pada fase ini yaitu, penempatan implan dan terapi
endodontik. Pada fase III (fase restorative) yaitu, restorasi akhir, alat prostodontik
cekat dan lepasan, evaluasi prosedur restorasi dan pemeriksaan jaringan periodontal.
Selajutnya fase IV (fase maintenance), mengecek kembali plak dan kalkulus,
keadaan poket dan inflamasi gingiva, oklusi dan mobilitas gigi, serta perubahan
patologis (Carranza, dkk., 2012).
Periodontitis merupakan penyakit infeksi dan dengan mempertimbangkan bahwa
beberapa pasien kurang merespon terapi mekanik konvensional, terkadang agen
antimikroba telah diresepkan untuk terapi periodontal. Namun, munculnya bakteri
patogen yang resisten terhadap antibiotik karena penggunaan sistemik yang tidak
tepat, telah menjadi masalah klinis yang serius (Committee on research, science and
therapy, 1996; Loesche, 1996). Menurut Gilette antibiotik harus digunakan sesuai
dengan tujuannya sehingga manfaat yang diharapkan akan lebih besar daripada risiko
yang akan didapatkan oleh pasien (Gilette, 1996). Antibiotik yang ideal untuk
digunakan dalam pencegahan dan pengobatan penyakit periodontal harus spesifik
untuk patogen periodontal, tidak beracun, substantif, tidak digunakan secara umum
untuk pengobatan penyakit lain. Kombinasi antibiotik diperlukan untuk
menghilangkan semua patogen yang diduga dari poket periodontal (Ciancio, dkk.,
2012). Pemilihan antibiotik dalam praktek klinis didasarkan pada analisis
mikrobiologi dari sampel yang diperoleh dari lokasi yang terkena. Oleh karena itu
pemilihan antibiotik secara empiris dan berdasarkan tanda-tanda klinis. Terapi
antibiotik sistemik untuk perawatan periodontal biasanya melibatkan monoterapi

13
berdasarkan metronidazole, tetracycline (tetracycline, doxycycline, minocycline),
clindamycin, ciprofloxacin dan β-lactams (amoxicillin dengan atau tanpa asam
klavulanat) (van Winkelhoff, dkk., 1996; Slots, 2004).
Tabel 2.1. Antibiotik yang digunakan pada terapi penyakit periodontal
Kategori Agen Manfaat
Penisilin* Amoksisilin Spektrum luas dari
aktivitas antimikroba;
absorpsi oral yang baik;
digunakan secara sistemik
Augmetin** Efektif terhadap
mikroorganisme yang
memproduksi
penicillinase: digunakan
secara sistemik
Tetrasiklin Minosiklin
Doksisiklin
Tetrasiklin
Efektif terhadap spektrum
luas mikroorganisme;
digunakan secara sistemik
dan diaplikasikan secara
lokal (subgingiva)
Quinolon Siprofloksasin Efektif terhadap Gram
negatif batang
Makrolida Azithromisin Konsentrasi pada daerah
yang inflamasi; digunakan
secara sistemik
Derivat Linomisin Klindamisin Digunakan pada pasien
yang alergi terhadap
penisilin; efektif terhadap
bakteri anaerob;
digunakan secara sistemik
Nitroimidazole*** Metronidazole Efektif terhadap bakteri

14
anaerob; digunakan secara
sistemik dan diaplikasikan
secara lokal (subgingiva)
*Indikasi : Localized Aggressive Periodontitis (LAP), General Aggressive Periodontitis (GAP),
Medically Related Periodontitis (MRP), Refractory Periodontitis (RP).
**Amoksisilin dan potassium klavulanat
*** Localized Aggressive Periodontitis (LAP), General Aggressive Periodontitis (GAP), Medically
Related Periodontitis (MRP), Refractory Periodontitis (RP), Necrotizing Ulcerative Periodontitis.
Penggunaan klinis antibiotik dan antimikroba lainnya, sebagai terapi untuk
periodontitis, telah banyak diteliti dalam dekade terakhir (Heasman, dkk., 1994;
Shapiro, dkk., 1994). Beberapa tahun terakhir telah banyak dilakukan penelitian
untuk obat-obatan dari bahan alami yang berasal dari tanaman herbal. Adapun
tumbuh-tumbuhan yang digunakan untuk pengobatan periodontitis adalah Acacia
catechu willd, Aloe vera (Aloe barbadensis miller), Chamomile, Azadirachta indica,
Glycyrrhiza glabra (Liquoirice root), Cinnamomum zeylanicum, Allium sativum,
Propolis, Mikania laevigata, Mikania glomerate, Droserapeltata,
Helichrysumitalicum, Coptidis rhizome, Piper cubeba, Azadirachta indica, Syzygium
aromaticum and Tea tree oil (Melaleuca alternifolia), minyak atsiri adalah
antimikroba yang digunakan dalam menangani penyakit periodontal (Neelufar,
dkk.,2014).
Tabel 2.2. Dosis Antibiotik yang digunakan untuk Terapi Penyakit Periodontal
Rejimen Dosis
Terapi Tunggal
Amoksisilin 500 mg 3 kali sehari selama 8 hari
Azithromisin 500 mg 1 kali sehari selama 4-7

15
hari
Siprofloksasin 500 mg 2 kali sehari selama 8 hari
Klindamisin 300 mg 3 kali sehari selama 10
hari
Doksisiklin / minosiklin 100 – 200 mg 1 kali sehari selama 21
hari
Metronidazole 500 mg 3 kali sehari selama 8 hari
Terapi Kombinasi
Metronidazole +
amoksisilin
250 mg 3 kali sehari selama 8 hari
Metronidazole +
siprofloksasin
500 mg 2 kali sehari selama 8 hari
Data dari Jorgensen MG, Slots J: Compend Contin Educ Dent 21: 111, 2000.
Rejimen ini diresepkan dengan review dari riwayat medis pasien, diagnosis periodontal, dan pengujian
antimikroba.
2.2. .................................................................................................................... B
akteri Porphyromonas gingivalis (Pg)
2.2.1. Klasifikasi dan
morfologi Porphyromonas ginigvalis
Klasifikasi dari bakteri Porphyromonas gingivalis ialah sebagai berikut (Boone,
dkk., 2002):
Kingdom : Bacteria
Divisi : Bacteroidetes

16
Klas : Bacteroides
Orde : Bacteroidales
Famili : Porphyromonadaceae
Genus : Porphyromonas
Species : Porphyromonas gingivalis
Porphyromonas gingivalis merupakan bakteri anaerob gram negatif, tidak
berspora, tidak mempunyai alat gerak. Kebanyakan sel di dalam media (broth),
berukuran kecil dari 0.5-0.8 hingga 1.0-1.5 μm, tetapi terkadang ada yang lebih
panjang 4-6 μm, hal ini mungkin disebabkan oleh perubahan bentuk (Mysak,
dkk.,2014).
Bakteri ini merupakan coccobacilli Gram negatif anaerob dengan panjang 0,5-2
μm, berpigmen hitam kecoklatan dan tumbuh dalam media kultur membentuk koloni
yang konveks, halus mengkilat, dan berdiameter 1-2 mm. Koloni berwarna hitam
kecoklatan. Warna gelap yang progresif pada pusatnya ini karena produksi
protoheme, suatu substansi yang bertanggung jawab terhadap tipikal warna koloni
(Kusumawardani, dkk., 2010). Pertumbuhannya dipengaruhi oleh adanya protein
hydrolysates, seperti : trypticase, proteose peptone dan ekstrak yeast (Boone, 2002).

17
Gambar 2.2. Porphyromonas gingivalis (Sumber :
http://wishart.biology.ualberta.ca/BacMap/includes/species/Porphyromonas_gingivalis.png)
2.2.2. Porphyromonas gingivalis sebagai periodontopatogen utama pada
periodontitis
Porphyromonas gingivalis adalah bakteri anaerob Gram negatif yang berada
dalam rongga mulut yang terlibat dalam patogenesis periodontitis suatu inflamasi
penyakit yang menghancurkan jaringan penyangga gigi yang akhirnya dapat
menyebabkan kehilangan gigi. Di antara lebih dari 500 spesies bakteri yang hidup di
dalam rongga mulut, bakteri kompleks yang disebut dengan “red complex” terdiri
dari Porphyromonas gingivalis, Treponema denticola, dan Tannerella forsythia yang
sangat berhubungan dengan penyakit periodontal menggunakan berbagai mekanisme
untuk mengganggu mekanisme pertahanan host (Bodet, dkk., 2007). Beberapa
penelitian mengenai Porphyromonas gingivalis sebagai periodontopatogen telah
memberikan informasi dalam hal filogenetik serta kriteria proteomik yang dapat
melebihi bakteri lainnya, seperti Bacteroides fragilis dan Bacteroides
thetaiotaomicron sebagai bakteri anaerob utama, dan merupakan patogen
oportunistik dalam bidang kedokteran gigi. Mikrobiota yang terdapat pada mukosa
mulut manusia terdiri dari berbagai spesies bakteri yang berhubungan komensalisme
dengan host. Porphyromonas gingivalis merupakan salah satu etiologi periodontitis
kronis yang terjadi pada orang dewasa dan merupakan komponen penting dari
mikrobiota dalam rongga mulut dan dapat berkolonisasi pada epitel rongga mulut
dan juga menyebabkan terjadinya resorpsi tulang alveolar (Yilmaz, 2008).

18
Lipopolisakarida Porphyromonas gingivalis tersebar secara sistemik pada lebih
dari 50% pasien penyakit periodontal dan berhubungan dengan meningkatnya MMPs
(Matriks Metalloproteinase). Lipopolisakarida sistemik yang rendah menstimulasi
terjadinya respon inflamasi pada ventrikel kiri melalui metalloproteinase yang
menyebabkan penurunan fungsi jantung (Deleon-Pennell, dkk., 2013).
Lipopolisakarida dari Porphyromonas gingivalis merupakan faktor utama terhadap
berkembangnya penyakit periodontitis. Fibroblas gingiva, yang merupakan
komponen utama dari jaringan ikat gingiva, secara langsung dapat berinteraksi
dengan Porphyromonas gingivalis dan produk yang dihasilkan oleh bakteri (Wang,
dkk., 2002). Kemampuan lipopolisakarida yang berpotensi mengaktifkan respon
pertahanan inflamasi dari host, yang memiliki fungsi sebagai molekul penting yang
memberi respon pada host jika terdapat infeksi bakteri. Lipopolisakarida juga
mengandung perbedaan struktural yang penting di antara spesies bakteri yang
berbeda yang secara signifikan dapat mengubah respon host (Bainbridge, dkk.,
2001). Plasminogen activator inhibitor tipe 1 (PAI-1) mRNA mengikat respon
protein yang meningkat pada gingiva dari pasien periodontitis (Na, dkk., 2014).
Lipopolisakarida Porphyromonas gingivalis menginduksi sitokin proinflamasi,
seperti IL-1β, IL-6, dan IL-8, yang menyebabkan kerusakan jaringan periodontal. Sel
ligamentum periodontal induk (PDLSCs) memainkan peran penting dalam regenerasi
jaringan periodontal yang diharapkan mempunyai terapi seluler untuk periodontitis
(Kato, dkk., 2014).
Protease sistein dari Porphyromonas gingivalis merupakan produk ekstraseluler
dari agen penyebab dalam penyakit periodontal. Banyak tindakan yang diamati

19
secara in vitro dari enzim ini yang merupakan target penting dari respon imun dari
individu yang terkena dan dianggap sebagai molekul yang berpotensi dalam
pendekatan terapi untuk penyakit periodontal (Curtis, dkk., 2001). Enzim ini terlibat
dalam kerusakan jaringan periodontal dan mengganggu mekanisme pertahanan host
melalui degradasi imunoglobulin dan melengkapi faktor penyebab terhadap
perkembangan penyakit (Polanowska, dkk., 1997).
Penelitian biomedis dalam beberapa dekade terakhir didapatkan bahwa
mikrobiota berkontribusi dalam pengembangan berbagai penyakit kronis pada
manusia. Ada bukti yang menunjukkan bahwa Porphyromonas gingivalis dari
biofilm rongga mulut yang paling dikenal keterlibatannya terhadap terjadinya
penyakit periodontitis. Bakteri anaerob Gram negatif dapat juga berada pada epitel
host tanpa adanya penyakit yang jelas (Atanasova, dkk., 2014).
2.3. Propolis
2.3.1. ..................................................................................................................
Definisi propolis
Kata propolis berasal dari bahasa Yunani, yaitu pro berarti pertahanan dan polis
berarti kota, sehingga propolis bermakna pertahanan kota (atau sarang lebah)
(Ghisalberti, 1979; Santos, dkk., 2002). Propolis atau lem lebah adalah nama generik

20
yang diberikan untuk bahan resin yang dikumpulkan oleh lebah madu dari berbagai
macam jenis tumbuhan, terutama dari bagian kuncup dan daun tumbuhan tersebut
(Ghisalberti, 1979; Greenway, dkk., 1990). Lebah kemudian mencampur bahan resin
ini dengan enzim yang disekresikan dari kelenjar mandibula lebah, meskipun
demikian komponen yang terdapat di dalam propolis tidak mengalami perubahan
(Chen, 1993; Ghisalberti, 1979).
Lebah menggunakan propolis sebagai: 1)
memperkuat sarang lebah; 2) bahan pelapis untuk melindungi sarangnya dari faktor
pengganggu dari luar, misalnya serangga, kumbang, atau tikus; 3) meratakan dinding
sarang lebah; 4) bahan pengisi lubang atau celah dan perekat keretakan yang terdapat
pada sarang lebah; 5) melindungi sel sarang tempat ratu lebah menetaskan telurnya
sehingga larva lebah terlindungi dari penyakit; dan 6) antibakteri (Hill, 1981; Kaal,
1991).
Sifat dari propolis telah diselidiki sebelumnya. Penelitian sementara menekankan
sifat antimikroba dan antiinflamasi pada propolis. Sifat antiinflamasi pada propolis
karena adanya caffeic acid phenethyl ester (CAPE) dalam propolis. Flavonoid dan
derivat asam sinamat dianggap sebagai komponen biologis utama yang aktif dalam
propolis (Gebara, dkk.,2002; Borrelli, dkk., 2002). Propolis telaah digunakan untuk
pengobatan apthous ulser, kandidiasis, gingivitis, periodontitis, dan pulpitis. Studi
mengenai penggunaan propolis telah meningkat karena sifat terapeutik dan
biologisnya (Coutinho, 2012; Gebara, dkk., 2002).

21
Gambar 2.3. Propolis (Sumber : http://healthymamichibi.files.wordpress.com/2012/09/propolis1.jpg)
Khasiat propolis adalah sebagai antibakteri yang mana telah banyak penelitian
yang dilakukan. Namun, bentuk kimia propolis sangat berbeda menurut iklim dan
lingkungan. Sehingga bentuk propolis sebagai obat juga berbeda, dan khasiatnya
sebagai antibakteri yang dikumpulkan dari beberapa daerah juga berbeda (Bankova,
dkk., 1999). Peran propolis sebagai antimikroba untuk melawan bakteri, jamur dan
virus telah diteliti sejak tahun 1940-an dan menunjukkan keampuhannya melawan
mikroorganisme yang berbeda (Hegazi, dkk., 1997).
Propolis tidak dapat digunakan sebagai bahan baku dan harus dipurifikasi lewat
proses ekstraksi dengan zat pelarut. Campuran ekstrak dengan etanol sangat cocok
untuk mendapatkan ekstrak propolis yang kaya dengan komponen polifenol (Pietta,
dkk., 2002). Suatu penelitian yang dilakukan oleh Tosi dkk menerangkan bahwa zat
pelarut yang dicampurkan ke dalam ekstrak propolis dapat mempengaruhi potensinya
sebagai antimikroba (Takasi, dkk., 1994).
Menurut Junior dkk., ethanolic extract of propolis (EEP) mampu meningkatkan
efek antibakteri dari berbagai antibiotik antara lain, kloramfenikol, vankomisin
terhadap Sthapylococcus aureus, dan penelitian yang dilakukan oleh Stepanovic
dkk., melaporkan bahwa EEP mampu meningkatkan efek antibakteri dari antibiotik
ampisilin, ceftriakson, doksisiklin, nalidixic acid dan trimetroprim/sulfametoksazol

22
terhadap Staphylococcus aureus yang resisten terhadap antibiotik tersebut (Junior,
dkk., 2005; Stepanovic, dkk., 2003).
2.3.2. ..................................................................................................................
Kandungan Propolis
Komposisi propolis sangat bervariasi dan erat hubungannya dengan jenis dan
umur tumbuhan di mana propolis tersebut berasal. Umumnya propolis terdiri dari:
campuran resin dan getah 39–53%, polifenol 1.2–17%, polisakarida 2–3%, lilin
(wax) 19–35%, dan bahan lain 8–12% (Chen, 1993). Komposisi propolis meliputi:
resin dan balsem ± 50%, lilin (wax) ± 30%, minyak esensial ± 10%, pollen ± 5%, dan
senyawa organik dan mineral ± 5%. Penelitian terhadap propolis yang berasal dari 15
daerah yang berbeda di Rusia menunjukkan hasil yang hampir sama, yaitu : resin 50–
55%, lilin (wax) maksimal 30%, minyak esensial ±8–10%, dan bahan padat ± 5%
(Kaal, 1991).
Jenis senyawa kimia yang terdapat pada propolis sangat kompleks. Berdasarkan
analisis dengan menggunakan metode Gas Chromatography-Mass Spectrometry
(GC-MS) yang dilakukan oleh Greenaway dkk terhadap propolis yang dihimpun oleh
lebah yang berasal dari tumbuhan poplar menunjukkan bahwa propolis mengandung
berbagai macam senyawa, yaitu: asam amino, asam alifatik dan esternya, asam
aromatik dan esternya, alkohol, aldehida, khalkon, dihidrokhalkon, flavanon, flavon,
hidrokarbon, keton, dan terpenoid (Greenway, dkk., 1990). Hasil yang hampir sama
juga diperoleh oleh Marcucci yang menemukan senyawa alkohol, aldehida, asam
alifatik dan esternya, asam amino, asam aromatik dan esternya, flavanon, keton, dan
glukosa dalam propolis (Marcucci, 1995).

23
Tabel 2.3. Komposisi Kimia Propolis
Kelas Komponen Jumlah Grup Komponen
Resin 45-55% Flavonoid, asamfenolat dan esternya
Lilin dan asam
lemak
25-53% 25-53% Sebagian besar dari lilin lebah dan
beberapa dari tanaman
Minyak essensial 10% Senyawa volatil
Protein 5% Protein kemungkinan berasal dari pollen
dan amino bebas
Senyawa organik
lain dan mineral
5% 14 macam mineral yang paling terkenal
adalah Fe dan Zn, sisanya seperti Au, Ag,
Cs, Hg, La dan Sb. Senyawa organik lain
seperti keton, laktan, kuinon, asam
benzoat dan esternya, gula, vitamin (B3)
serta gula
(Sumber : Krell 1996)
2.3.3. ..................................................................................................................
Manfaat propolis
Propolis telah digunakan sejak dahulu kala sebagai obat tradisional, yaitu sebagai
bio-kosmetik dan makanan untuk kesehatan. Penelitian di bidang kesehatan terhadap
propolis telah banyak dilakukan luar negeri, baik secara in vitro maupun in vivo.
Hasilnya menunjukkan bahwa propolis memiliki beberapa aktivitas biologis dan
farmakologis, antara lain: 1) bersifat antibakteri baik terhadap bakteri Gram positif
maupun Gram negatif; 2) bersifat anti inflamasi; 3) memiliki aktivitas anti jamur,
terutama terhadap spesies dermatofita dan kandida; 4) propolis meningkatkan
regenerasi jaringan tulang dan kartilago, dan 5) propolis bersifat antioksidan karena

24
mampu menangkap radikal bebas (Dobrowolski, dkk., 1991; Kujumgiev, dkk.,
1999).
Penggunaan propolis di bidang kedokteran gigi baru dilaporkan beberapa tahun
terakhir. Hasilnya menunjukkan bahwa propolis dapat digunakan sebagai salah satu
bahan pengobatan alternatif yakni: 1) dalam perawatan penyakit gingivitis oleh
karena mampu mencegah pembentukan plak; 2) digunakan untuk mengobati ulserasi
pada rongga mulut; 3) mencegah terjadinya karies gigi. Hal ini disebabkan karena
propolis memiliki aktivitas antibakteri, mengurangi daya adhesi bakteri rongga mulut
pada permukaan gigi, menghambat sintesis glukan yang tidak larut dalam air (water-
insoluble glucan), dan menghambat enzim glukosiltransferase; 4) meningkatkan
aktivitas mineralisasi pada permukaan email gigi; 5) mempercepat perbaikan
jaringan dan penyembuhan luka setelah prosedur bedah mulut (pasca ekstraksi
maupun terjadinya dry socket), dan 6) pada perawatan gangren pulpa serta
periodontitis (Martinez, dkk., 1988; Park, dkk., 1998; Koo., dkk 2000).
Propolis juga berfungsi memperbaiki kondisi patologi bagian tubuh yang sakit,
bekerja sebagai antioksidan dan antibiotik, serta meningkatkan sistem kekebalan
tubuh baik humoral maupun seluler karena mengandung flavonoid sekitar 15%
(Krell, 1996). Flavonoid merupakan antioksidan dan antibiotik yang berfungsi
menguatkan dan mengantisipasi kerusakan pembuluh darah dan merupakan bahan
aktif yang berfungsi sebagai antiinflamasi dan antivirus. Aktivitas antioksidan
tertinggi dihasilkan dari ekstraksi dengan menggunakan pelarut etanol. Flavonoid
yang terekstrak adalah kemferida (flavonol), akasetin (flavon) dan isoramnetin.
Propolis merupakan antibiotik karena mempunyai kandungan flavonoid, yaitu bahan

25
aktif yang berfungsi sebagai antiinflamasi dan antivirus. Ekstrak propolis dapat
memacu aktivitas makrofag sehingga meningkatkan sistem kekebalan tubuh (Kun,
dkk., 1998).
2.3.4. Aktivitas antibakteri pada propolis
Penelitian terhadap propolis telah banyak dilakukan baik secara in vitro maupun
in vivo dan hasilnya menunjukkan bahwa propolis memiliki beberapa aktivitas
biologis dan farmakologis antara lain bersifat antibakteri baik terhadap bakteri Gram
positif maupun Gram negatif. Aktivitas antibakteri propolis yang sangat bervariasi
ini bergantung pada komposisi dari propolis yang digunakan. Komposisi propolis
sangat dipengaruhi oleh jenis dan umur tumbuhan, iklim, dan waktu dimana propolis
tersebut diperoleh. Penelitian secara in vitro maupun in vivo menunjukkan salah satu
aktivitas biologis dan farmakologis dari senyawa flavonoid ialah aktivitas
antibakteri. Flavonoid merupakan salah satu senyawa fenol alami yang tersebar luas
pada tumbuhan, yang disintesis dalam jumlah sedikit (0.5-1.5%) dan dapat
ditemukan pada hampir semua bagian tumbuhan (Ghisalberti, 1979; Dobrowolski,
dkk., 1991; Grange, dkk., 1990).
Beberapa penelitian menunjukkan bahwa sifat antibakteri dari propolis tidak
hanya disebabkan karena senyawa tunggal, tetapi karena efek sinergis dari beberapa
senyawa yang ada dan memiliki daya antibakteri, yaitu flavonoid, flavon, tannin,
asam ferulat, ester asam fenol, terpenoid, asam sinamat, dan berbagai ester asam
kafeat. Sifat antibakteri yang dimiliki propolis menjadi salah satu pertimbangan
untuk menggunakan propolis sebagai bahan antibakteri (Susilo, dkk., 2009; Agarwal,
dkk., 2012).

26
Propolis yang telah diekstrak memiliki kandungan aktif saponin yang bersifat
sebagai surfaktan sehingga mampu melarutkan lemak yang merupakan salah satu
struktur dinding biofilm. Sehingga dapat melepaskan ikatan sel biofilm
Porphyromonas gingivalis (Francis, dkk., 2002). Menurut studi Koo dkk kandungan
propolis yaitu apigenin dan tt-farnesol menyebabkan penurunan jumlah polisakarida
dalam biofilm mikroorganisme. Apigenin dan tt-farnesol akan mempengaruhi salah
satu polisakarida dalam biofilm yang berfungsi untuk perlekatan pada permukaan sel,
sehingga akan menghentikan pembentukan biofilm (Koo, dkk., 2003).
BAB III

27
KERANGKA KONSEP
3.1. Kerangka konsep penelitian
: Variabel diteliti
: Variabel tidak diteliti
Gram
negatif
Periodontitis
Propolis
Propolis gel
Uji aktivitas
antibakteri
Porphyromonas
gingivalis
Flavonoid
Caffeic acid phenethyl ester (CAPE)
Polifenol
Minyak esensial
Anti-
virus
Bakteri
anaerob
Gram
positif
Anti-
inflamasi
Anti-
jamur
Anti-
bakteri
Anti-
oksidan

28
3.2. Alur penelitian
Propolis
Propolis gel
Pembuatan medium
biakan bakteri
(Mueller Hinton Agar)
Biakan murni
Porphyromonas
gingivalis
Uji daya
hambat
Pengamatan
zona hambat
Analisis data

29
BAB IV
METODE PENELITIAN
4.1. Jenis penelitian
Jenis penelitian ini ialah eksperimental laboratorium
4.2. Rancangan penelitian
Rancangan penelitian ini ialah post test only control group design
4.3. Tempat dan waktu penelitian
4.3.1. Tempat penelitian
Laboratorium Mikrobiologi Fakultas Kedokteran Universitas Hasanuddin
4.3.2. Waktu penelitian
Penelitian ini akan dilakukan pada bulan Februari – Juni 2015
4.4. Variabel penelitian
4.4.1. Variabel menurut fungsinya :
1. Variabel independen : Propolis gel
2. Variabel dependen : Zona hambat bakteri
Porphyromonas gingivalis
3. Variabel kendali : Medium biakan bakteri, suhu dan lama waktu
inkubasi

30
4.4.2. Variabel menurut skala pengukurannya :
Skala rasio untuk mengukur zona hambat ekstrak propolis terhadap bakteri
Porphyromonas gingivalis.
4.5 Definisi operasional variabel
1. Ekstrak propolis merupakan propolis dari bahan alami yang diperoleh dengan
mengekstraksi zat aktif dari propolis menggunakan etanol dengan metode
maserasi.
2. Propolis gel adalah ekstrak propolis Trigona sp yang dibuat dalam bentuk gel.
3. Zona hambat merupakan luas daerah bening pada biakan medium bakteri setelah
diinkubasi yang diukur diameternya dengan jangka sorong (mm).
4. Medium biakan bakteri yang digunakan adalah Mueller Hinton Agar (MHA)
sebagai medium pertumbuhan bakteri pada proses uji daya hambat.
4.6 Subjek penelitian
Subjek pada penelitian ini adalah biakan murni bakteri Porphyromonas gingivalis
yang tersedia di Laboratorium Mikrobiologi Fakulltas Kedokteran Universitas
Hasanuddin.
4.7 Sampel penelitian
Propolis gel

31
4.8 Alat dan bahan
4.8.1. Alat :
a. Handscoon
b. Masker
c. Alat tulis
d. Kertas label
e. Ose bulat
f. Pinset
g. Paper disc
h. Cawan petri
i. Bunsen
j. Rak tabung reaksi
k. Tabung reaksi
l. Gelas ukur
m. Labu Erlenmeyer
n. Gelas kimia
o. Kaliper
p. Inkubator
q. Autoklaf
r. GasPak
4.8.2. Bahan :
a. Propolis gel
b. Sediaan bakteri Porphyromonas gingivalis
c. Medium MHA (Muller Hinton Agar)
d. Spiritus
e. Etanol 70%
f. Metronidazole gel

31
4.9. Prosedur penelitian
Secara keseluruhan prosedur kerja dalam penelitian ini terdiri dari : sterilisasi
alat, pembuatan medium biakan bakteri, ekstraksi propolis, pembuatan propolis gel,
uji daya hambat, dan pengamatan zona hambat.
4.9.1. Prosedur sterilisasi alat
Sterilisasi alat dalam penelitian ini dilakukan dengan cara sebagai berikut :
1. Cawan petri, tabung reaksi, pinset, dibungkus dengan aluminium foil dan
disterilkan dengan autoklaf.
2. Gelas ukur dibungkus dengan kertas kemudian disterilkan pada autoklaf selama
15 menit dengan suhu 121⁰C.
3. Labu erlenmeyer diisi dengan aquades sebanyak 250 ml lalu ditutup dengan kapas
yang dipadatkan sedemikian rupa dan disterilkan dalam autoklaf pada suhu 121⁰C
selama 15 menit.
4. Bahan Mueller Hinton Agar (MHA) dimasukkan ke dalam erlenmeyer kemudian
disterilkan pada autoklaf pada suhu 121⁰C selama 25 menit.
4.9.2. Prosedur ekstraksi propolis
Metode ekstraksi yang digunakan ialah teknik maserasi. Maserasi merupakan
penyarian yang sederhana. Adapun tahap ekstraksi ialah :
1. Propolis yang sebelumnya didinginkan dalam refrigerator, dimasukkan ke
dalam oven selama tiga hari dengan suhu 40⁰C.

32
2. Propolis sebanyak 800 gram yang telah dimasukkan ke dalam oven kemudian
ditambahkan cairan etanol 70% sebanyak 2L.
3. Untuk mempercepat pelarutan, propolis dihancurkan dengan pengaduk.
4. Diamkan propolis dalam cairan etanol selama 48 jam. Selama didiamkan, aduk
setiap hari.
5. Propolis yang telah didiamkan kemudian disaring dengan penyaringan dan hasil
hasil saringan dibiarkan selama waktu tertentu untuk mengendapkan zat-zat
yang tidak diperlukan tetapi tidak ikut terlarut dalam etanol.
6. Sisa penyaringan kemudian dicampurkan kembali ke dalam larutan etanol 70%,
kemudian lakukan tahapan 3-5. Ulangi hingga tiga kali penyaringan.
4.9.3. Prosedur pembuatan propolis gel
Tahapan pembuatan propolis gel sebagai berikut :
1. Pembuatan basis gel :
a. HEC didispersikan dalam air suling dan ditambahkan zat tambahan
trietanolamin, propilenglikol, dan nipagin sambil diaduk dalam lumpang
hingga membentuk massa gel.
b. Gel ditempatkan dalam wadah kaca terlindung dari cahaya.
2. Untuk sediaan gel 10% ekstrak propolis sebanyak 10 gram ditambahkan ke
dalam basis gel HEC yang telah dilarutkan sebelumnya sambil diaduk di
lumpang membentuk massa gel 10 %.
3. Propolis gel disimpan dalam wadah kaca terlindung dari cahaya.

33
4.9.4. Prosedur pembuatan medium MHA (Mueller Hinton Agar)
Sebanyak 4.75 gram Mueller Hinton Agar dilarutkan dalam 125 ml aquades,
kemudian dipanaskan dan diaduk sampai larut. Media agar disterilkan di autoklaf
selama 15 menit pada suhu 121ºC.
4.9.5. Uji daya hambat
1. Siapkan isolat murni bakteri Porphyromonas gingivalis dan 3 cawan petri yang
berisi medium MHA (Mueller Hinton Agar)
2. Siapkan 6 paper disk untuk digunakan pada sampel yang akan diuji.
3. Masukkan 6 buah paper disk yang telah dicelupkan pada sampel uji yang akan
digunakan ke dalam cawan petri yang telah disiapkan.
4. Inkubasi dalam inkubator dengan suhu 37⁰C selama 3x24 jam, dengan
pengamatan 1x24 jam, 2x24 jam, 3x24 jam.
4.9.6. Pengamatan zona hambat
Daya hambat diketahui berdasarkan pengukuran diameter zona bening atau
hambat yang terbentuk disekitar sampel atau sumur yang telah dibuat dan diukur
dengan menggunakan jangka sorong.
4.10. Analisis Data
4.10.1. Jenis data
Jenis data yang digunakan dalam penelitian ini adalah data primer.

34
4.10.2. Pengolahan data
Pengolahan data penelitian ini dilakukan dengan perhitungan statistik
menggunakan program SPSS 18.0.
4.10.3. Analisis data
Analisis data dalam penelitian ini menggunakan uji statistik independent sample
t-test untuk melihat perbedaan diameter zona daya hambat antara propolis gel dan
metronidazole gel pada pengamatan 1x24 jam, 2x24 jam, 3x24 jam. Kemudian untuk
uji normalitas digunakan uji Shapiro-Wilk, kemudin dilakukan uji statistik
Repeated Anova untuk melihat perbedaan zona daya hambat akibat penurunan yang
terjadi pada waktu pengamatan 1x24 jam, 2x24 jam, dan 3x24 jam.

35
BAB V
HASIL PENELITIAN
Telah dilakukan penelitian mengenai efektivitas propolis gel dalam menghambat
pertumbuhan Porphyromonas gingivalis. Tujuan penelitian ini untuk mengamati luas
zona daya hambat propolis gel terhadap bakteri Porphyromonas gingivalis yang
sering menjadi penyebab periodontitis. Zona daya hambat dari propolis gel juga akan
dibandingkan dengan kontrol positif, yaitu metronidazole yang menjadi gold standar
dalam perawatan bakteri anaerob. Penelitian ini mengambil tempat di Laboratorium
Mikrobiologi Fakultas Kedokteran Universitas Hasanuddin dan dilakukan pada bulan
Februari hingga Juni 2015. Adapun, sampel dalam penelitian eksperimen laboratoris
ini merupakan biakan murni bakteri Porphyromonas gingivalis yang tersedia di
laboratorium. Jumlah sampel dalam penelitian ini ditentukan sebesar enam sampel
dan dibagi ke dalam dua kelompok dengan jumlah yang sama.
Zona daya hambat dalam penelitian ini diukur dengan satuan millimeter (mm).
Adapun, daya hambat diukur setelah perlakuan diberikan (posttest). Pengamatan
zona daya hambat diukur tiga kali, yaitu pada pengamatan 1x24 jam, 2x24 jam, dan
3x24 jam). Selanjutnya, seluruh hasil penelitian dikumpulkan, diolah, dan dianalisis
dengan program SPSS 18.0 (SPSS Inc., Chicago, IL, USA). Hasil penelitian
ditampilkan dalam tabel distribusi sebagai berikut.

36
Tabel 5.1. Perbedaan rata-rata diameter zona hambat (mm) berdasarkan waktu
pengamatan pada masing-masing kelompok intervensi (Asdar & Cindrakori, 2015)
Intervensi n (%)
Diameter Zona Daya Hambat (mm)
p-value Pengamatan
1 x 24 jam
Pengamatan
2 x 24 jam
Pengamatan
3 x 24 jam
Mean ± SD Mean ± SD Mean ± SD
Propolis gel 3 (50%) 6.17 ± 0.48a
5.76 ± 0.55a
5.23 ± 0.32a
0.111*
Metronidazole
gel 3 (50%)
13.68 ±
1.66a
13.94 ±
2.03a
12.90 ±
1.96a 0.270*
Total 6 (100%) 9.93 ± 4.25 9.85 ± 4.67 9.06 ± 4.38 aNormality test: Shapiro-Wilk test: p>0.05; data distribution is normal
*Repeated Anova test: p>0.05; not significant
Gambar 5.1. Grafik distribusi diameter zona hambat (mm) berdasarkan waktu
pengamatan pada intervensi propolis gel dan metronidazol gel (Asdar & Cindrakori,
2015)
Tabel 5.1 memperlihatkan perbedaan rata-rata diameter zona hambat (mm)
berdasarkan waktu pengamatan pada masing-masing kelompok intervensi, yaitu
propolis gel dan metronidazole gel. Hasil penelitian memperlihatkan diameter zona
daya hambat propolis gel pada pengamatan 24 jam pertama mencapai 6.17 mm.
Namun, zona daya hambat ini mengalami penurunan pada pengamatan kedua hingga
pengamatan 24 jam ketiga. Terlihat pada pengamatan 24 jam kedua, zona daya
hambat propolis rata-rata hanya mencapai 5.76 dan pada pengamatan 24 jam ketiga,

37
zona daya hambat kembali menurun menjadi 5.23 mm. Akan tetapi, berdasarkan
hasil uji statistik Repeated Anova, perbedaan zona daya hambat akibat penurunan
yang terjadi pada waktu pengamatan 1x24 jam, 2x24 jam, dan 3x24 jam tidak
bermakna secara statistik atau dengan kata lain diameter zona daya hambat dapat
dikatakan sama secara statistik. Ini diperlihatkan dari nilai p:0.111 atau p>0.05. Hal
yang berbanding terbalik diperlihatkan pada intervensi metronidazole gel pada
pengamatan 24 jam pertama ke 24 jam kedua, dimana diameter zona daya hambat
justru mengalami peningkatan, dari 13.68 mm menjadi 13.94 mm. Namun, pada
pengamatan 24 jam ketiga, diameter zona daya hambat mengalami penurunan
menjadi 12.90 mm. Hasil uji statistik juga memperlihatkan nilai p:0.270 (p>0.05),
yang berarti bahwa tidak terdapat perbedaan rata-rata diameter zona daya hambat
(mm) antara pengamatan 24 jam pertama, kedua, maupun ketiga pada kelompok
metronidazole gel (Asdar & Cindrakori, 2015).
Penelitian ini menggunakan uji parametrik, yaitu Repeated Anova (tabel 5.1) dan
Independent sample t-test (tabel 5.2), karena syarat uji parametrik dalam penelitian
ini terpenuhi. Syarat uji parametrik adalah distribusi data harus normal. Distribusi
data dalam penelitian ini diuji normalitas menggunakan uji Shapiro-Wilk yang
diperlihatkan pada tabel 5.1 dan hasilnya bahwa didapatkan nilai p>0.05 pada
seluruh kelompok data dalam penelitian ini atau dengan kata lain, distribusi data
normal. Dengan demikian, uji parametrik dapat digunakan (Asdar & Cindrakori
2015).

38
Tabel 5.2. Perbedaan rata-rata diameter zona hambat (mm) antara propolis gel dan
metronidazole gel pada waktu pengamatan 1 x 24 jam, 2 x 24 jam, dan 3 x 24 jam
(Asdar & Cindrakori, 2015)
Intervensi
Diameter Zona Daya Hambat (mm)
Pengamatan
1 x 24 jam p-value
Pengamatan
2 x 24 jam p-value
Pengamatan
3 x 24 jam p-value
Mean ± SD Mean ± SD Mean ± SD
Propolis gel 6.17 ± 0.48
0.002*
5.76 ± 0.55
0.003*
5.23 ± 0.32
0.003*
Metronidazole
gel 13.68 ± 1.66 13.94 ± 2.03
12.90 ±
1.96
Selisih
(95%CI)
7.51
(4.72 –
10.29)
8.18
(4.80 –
11.55)
7.66
(4.64 –
0.86) Total 9.93 ± 4.25 9.85 ± 4.67 9.06 ± 4.38
*Independent sample t-test: p<0.05; significant
Tabel 5.2 memperlihatkan perbedaan rata-rata diameter zona daya hambat (mm)
antara propolis gel dan metronidazole gel pada waktu pengamatan 1x24 jam, 2x24
jam, dan 3x24 jam. Hasil penelitian memperlihatkan secara keseluruhan, diameter
zona daya hambat metronidazole gel lebih tinggi daripada propolis gel, baik pada
pengamatan 24 pertama, kedua, maupun ketiga. Pada pengamatan 24 jam pertama,
terlihat diameter zona daya hambat metronidazol gel mencapai 13.68 mm, sedangkan
propolis 6.17 mm, terdapat selisih sebesar 7.51 mm. Pada pengamatan 24 jam kedua,
diameter zona daya hambat propolis gel hanya mencapai 5.76 mm, sedangkan
metronidazole gel mencapai 13.94 mm. Hal ini juga menimbulkan perbedaan selisih
sebesar 8.18 mm. Adapun, pada pengamatan 24 jam ketiga, diameter zona daya
hambat metronidazole gel sebesar 12.90 mm, namun propolis gel hanya mencapai
5.23 mm. Hasil uji statistik independent sample t-test memperlihatkan nilai p<0.05
pada pengamatan 24 jam pertama, kedua, maupun ketiga. Hal ini berarti bahwa

39
terdapat perbedaan diameter zona daya hambat antara propolis gel dan metronidazole
gel pada pengamatan 24 jam pertama, kedua, dan ketiga (Asdar & Cindrakori, 2015).

40
BAB VI
PEMBAHASAN
Penyakit periodontal adalah hilangnya struktur kolagen pada daerah penyangga
gigi, sebagai respon dari akumulasi bakteri di jaringan periodontal. Penyakit
periodontal merupakan penyakit infeksi yang menyerang gingiva dan jaringan
pendukung gigi lainnya, jika tidak dilakukan perawatan yang tepat dapat
mengakibatkan kehilangan gigi. Akumulasi bakteri plak pada permukaan gigi
menjadi penyebab utama terjadinya penyakit periodontal (Hinrichs, dkk., 2012). Di
Indonesia penyakit periodontal menduduki urutan ke dua yaitu mencapai 96.58%
(Riskesdas, 2007). Pencegahan akumulasi bakteri plak pada permukaan gigi dapat
dilakukan dengan kontrol plak, menyikat gigi, pembersihan karang gigi, serta
penggunaan obat kumur antiseptik (Harvey, 2005). Antibiotik yang dapat diberikan
pada terapi penyakit periodontal adalah metronidazole, tetracycline (doxycycline,
minocycline), clindamycin, serta ciprofloxacin (van Winkelhoff, dkk., 1996).
Beberapa tanaman herbal yang dapat digunakan untuk terapi periodontitis adalah
Aloe vera, Allivum sativum, Acacia catechu, Syzygium aromaticum, Piper cubeca,
Mikania glomerate, Drosera peltata, Helichrysumitalicum, serta propolis (Neelufar,
dkk.,2014).
Pada penelitian ini dilakukan uji efektivitas bahan propolis Trigona sp dalam
bentuk gel terhadap bakteri Porphyromonas gingivalis untuk mengetahui apakah
propolis dapat menghambat pertumbuhan bakteri Porphyromonas gingivalis yang

41
merupakan salah satu penyebab penyakit periodontal. Untuk menguji daya hambat
propolis gel terhadap bakteri Porphyromonas gingivalis dilakukan di cawan petri
yang berbeda dengan tiga replikasi. Pada penelitian ini metronidazole gel digunakan
sebagai kontrol positif. Metronidazole merupakan salah satu antibiotik yang dapat
diberikan pada terapi penyakit periodontal. Pengukuran zona hambat pada penelitian
ini menggunakan jangka sorong dengan mengukur diameter zona hambat secara
horizontal, vertikal, dan diagonal kemudian dirata-ratakan.
Beberapa penelitian yang menggunakan propolis sebagai bahan untuk uji daya
hambat yang dilakukan oleh (Poedjiono, dkk., 2014) menunjukkan bahwa ekstrak
propolis Apis mellifera 12.38% memiliki kemampuan menghambat biofilm
Porphyromonas gingivalis lebih tinggi daripada Chlorhexidine gluconate 0.2%,
penelitian yang dilakukan oleh (Agarwal, dkk., 2013) menunjukkan bahwa ekstrak
propolis China dengan rentang konsentrasi 0.1-0.0125 µg/ml dapat menghambat
bakteri Porphyromonas gingivalis. Aktivitas antimikroba pada konsentrasi 0.1
µg/ml, 0.05 µg/ml, 0.025 µg/ml, 0.0125 µg/ml zona daya hambat yang terbentuk
berturut-turut ialah 25 mm, 21 mm, 20 mm, 18 mm, sedangkan pada konsentrasi 0.1-
0.025 µg/ml dapat menghambat bakteri Aggregatibacter actinomycetemcomitans.
Aktivitas antimikroba pada konsentrasi 0.1 µg/ml, 0.05 µg/ml, 0.025 µg/ml zona
daya hambat yang terbentuk berturut-turut ialah 14 mm, 12 mm, 11 mm, penelitian
(Hasan, 2006) menunjukkan propolis hasil ekstrak etanol 70% dapat digunakan
sebagai senyawa antibakteri, baik bakteri Gram positif maupun Gram negatif.
Konsentrasi hambat tumbuh minimum dari ekstrak propolis masing-masing untuk
setiap bakteri yang diujikan adalah 0.39% terhadap Staphylococcus aureus, 0.78%

42
terhadap Bacillus subtilis, dan 0.78% terhadap Eshericia coli, hasil penelitian yang
dilakukan oleh (Prasetyorini, dkk., 2011) pada uji daya hambat ekstrak propolis
Trigona sp terhadap bakteri Eschericia coli menunjukkan bahwa semakin kecil
konsentrasi, daya hambat terhadap bakteri pun semakin kecil, dan penelitian yang
dilakukan oleh (Novilla., 2009) menunjukkan bahwa ekstrak propolis Apis mellifera
dapat menghambat bakteri Staphylococcus aureus dan Bacillus subtilis pada
konsentrasi 5%. Pada penelitian yang dilakukan oleh (Salsabila, dkk., 2013)
penghambatan Porphyromonas gingivalis harus dilakukan untuk mencegah
keparahan penyakit periodontal, pencegahannya dilakukan dengan cara pemakaian
bahan yang bersifat antibakteri. Pada penelitian tersebut digunakan ekstrak etanol
siwak, berdasarkan penelitian tentang siwak terbukti dapat menyehatkan gigi dan
gusi serta menyebabkan penurunan bakteri Gram negatif salah satunya
Porphyromonas gingivalis Uji aktivitas antibakteri ekstrak etanol siwak yang
dilakukan dengan konsentrasi sebesar 50%, 25%, 12.5%, dan 6.25% berturut-turut
menunjukkan zona daya hambat yang terbentuk sebesar 3.96±0.20 mm, 3.188±0.49
mm, 2.207±0.68 mm, 1.20±0.62 mm.
Penelitian lain menunjukkan bahwa propolis berfungsi sebagai antibakteri, anti
virus, anti jamur, antioksidan, anti peradangan serta meningkatkan sistem kekebalan
tubuh karena terdapat kandungan polifenol yang tinggi di dalam propolis (Kaihena,
2013). Kandungan flavonoid pada propolis memiliki aktivitas antibakteri melalui
hambatan fungsi DNA bakteri sehingga kemampuan replikasi dan translasi bakteri
dihambat. Aktivitas biologis senyawa flavonoid pada propolis terhadap bakteri
dilakukan dengan merusak membran sitoplasma dari bakteri. Pada penelitian yang

43
dilakukan (Hegazi, dkk., 1997) propolis memiliki efek antibakteri terhadap
Staphylococcus aureus, Escherichia coli, dan Candida albicans, efek anti bakteri
dari propolis berbeda-beda dan tergantung pada daerah asal propolis. Menurut Takasi
dkk efek antimikroba yang ditimbulkan oleh propolis dengan cara mencegah
pembelahan sel, serta propolis juga dapat merusak membran sitoplasma dan dinding
sel yang menyebabkan bacteryolisis parsial dan menghambat sintesa protein.
Mekanisme kerja propolis sangat kompleks sehingga tidak dapat dibuat bentuk klasik
sebagai antibiotik (Takasi, dkk., 1994).
Dari hasil penelitian ini memperlihatkan bahwa propolis gel dapat menghambat
pertumbuhan bakteri Porhpyromonas gingivalis. Hasil penelitian menunjukkan
bahwa daya hambat propolis gel terhadap bakteri Porphyromonas gingivalis lebih
kecil dibandingkan dengan metronidazole gel yang digunakan sebagai kontrol positif
ditunjukkan oleh hasil uji statistik independent sample t-test yang terdapat perbedaan
diameter zona daya hambat antara propolis gel dan metronidazole gel pada
pengamatan 24 jam pertama, kedua, dan ketiga.
Hasil uji efektivitas propolis gel dan metronidazole gel terhadap bakteri
Porphyromonas gingivalis pada masa inkubasi 1x24 jam sudah menunjukkan adanya
zona hambat. Pada kelompok propolis gel hasil uji statistik, Repeated Anova,
perbedaan zona daya hambat akibat penurunan yang terjadi pada waktu pengamatan
1x24 jam, 2x24 jam, dan 3x24 jam tidak bermakna secara statistik atau dengan kata
lain diameter zona daya hambat dapat dikatakan sama secara statistik, sedangkan
pada kelompok metronidazole gel hasil uji statistik memperlihatkan tidak terdapat

44
perbedaan rata-rata diameter zona daya hambat (mm) antara pengamatan 24 jam
pertama, kedua, maupun ketiga.

45
BAB VII
PENUTUP
7.1. Kesimpulan
Berdasarkan hasil penelitian uji daya hambat propolis gel terhadap bakteri
Porphyromonas gingivalis penyebab penyakit periodontal, dapat disimpulkan :
1. Terdapat perbedaan diameter zona daya hambat antara propolis gel dengan
mentronidazole gel terhadap bakteri Porphyromonas gingivalis pada
periodontitis. Hal ini dikarenakan rerata zona daya hambat yang terbentuk
pada bahan uji propolis gel lebih kecil dibandingkan dengan metronidazole
gel sebagai kontrol positif berdasarkan uji independent sample t-test.
2. Tidak terdapat perbedaan yang bermakna antara masa inkubasi 1x24 jam, 2x24
jam, 3x24 jam pada uji daya hambat propolis gel dan metronidazole gel
terhadap bakteri Porphyromonas gingivalis pada periodontitis. Hal ini
kemungkinan dikarenakan bahan uji efektif pada pengamatan 1x24 jam, dan
terjadi penurunan zona hambat pada pengamatan 2x24 jam dan 3x24 jam
tetapi dikatakan tidak bermakna secara statistik atau dengan kata lain zona
daya hambat sama secara statistik pada pengamatan 1x24 jam, 2x24 jam,
3x24 jam. Sehingga pada saat pengolahan data dengan uji repeated Anova
tidak menunjukkkan pengaruh waktu yang bermakna.

46
7.2. Saran
1. Perlu dilakukan penelitian terhadap bahan alami seperti propolis dengan jenis yang
berbeda dari jenis Trigona sp terhadap bakteri Porphyromonas gingivalis.
2. Perlu diadakan penelitian lebih lanjut mengenai kandungan yang terdapat dalam
propolis Trigonas sp yang dapat menghambat bakteri Porphyromonas gingivalis
maupun bakteri lain penyebab penyakit periodontal.

47
DAFTAR PUSTAKA
Agarwal, G., Vemanaradhya, G.G., Mehta, D.S., 2012, Evaluation of chemical
composition and efficacy of Chinese propolis extract on Porphyromonas
gingivalis and Aggregatibacter actinomycetemcomitans: An in vitro study,
Contemporary Clinical Dentistry, 3(3): 256-61.
Asdar, Cindrakori, H.N., Accepted dalam B-Dent Jurnal 2(2), Universitas
Baiturrahmah, Sumatera Barat, Desember 2015.
Atanasova, K.R., Yilmaz, O., 2014, Looking in the Porphyromonas gingivalis
cabinet of curiosities: the microbium, the host and cancer association,
Molecular Oral Microbiology.
Bainbridge B.W., Darveau, R.P., 2001, Porphyromonas gingivalis
lipopolysaccharide: an unusual pattern recognition receptor ligand for the
innate host defense system, Acta Odontologica Scandinavica, 59(3): 131-8.
Bankova, V., Bondourova-Krasteva, G., Starcin, J.M., Frete, X., Kujumgiev, A.,
1999, Phytochemical evidence for the plant origin of Brazillian propolis from
Sao Paulo State, Z. Naturforsch, 54: 401-5.
Bodet, C., Chandad, F., Grenier, D., 2007, Pathogenic potential of Porphyromonas
gingivalis, Treponem denticola, and Tannerella forsythia, the red bacterial
complex associated with periodontitis, Pathologie Biologie, 55(3-4): 154-62.
Boone, D.R., Castenholtz, R.W., 2002, Bargey’s manual of systematic bacteriology,
2nd
ed. Vol.1., Springer-Verlag, New York.
Borrelli, F., Maffia, P., Pinto, L., Ianaro, A., Russo, A., Capasso, F., et al, 2002,
Phytochemical compounds involved in the anti-inflammatory effect of propolis
extract, Fitoerapia, 73: 53-63.
Burdock, G.A., 1998, Review of the biological properties and toxicity of bee propolis
(propolis), Food Chem. Toxicol, 36: 347-63.
Carranza, F.A., Takei, H.H., 2012, The Treatment Plan, dalam dalam Newman,
M.G., Takei, H.H., Klokkevold, P.R., Carranza, F.A.: Carranza’s Clinical
Periodontology, 11th
ed., p:385, Elsevier saunders Inc., Missouri.
Castaldo, S., Capasso, F., 2002, Propolis, an old remedy used in modern medicine,
Fitoterapia, 73(1): 1-6.
Chen, Y., 1993, Apiculture in China, 1st
ed., Agricultural Publishing House. 96-7.

48
Ciancio, S., Mariotti, A., 2012, Antiinfective Therapy, dalam Newman, M.G., Takei,
H.H., Klokkevold, P.R., Carranza, F.A.: Carranza’s Clinical Periodontology,
11th
ed., pp:483-84, Elsevier saunders Inc., Missouri.
Coutinho, A., 2012, Honeybee propolis extract in periodontal treatment. A clinical
and microbiological study of propolis in periodontal treatment, Indian J Dent
Res, 23: 294-99.
Curtis, M.A., Aduse-Opoku, J., Rangarajan, M., 2001, Cysteine proteases of
Porphyromonas gingivalis, Critical Reviews in Oral Biology and Medicine,
12(3): 192-216.
DeCarlo, A.Jr., Windsor, L., Bodden, M.K., et al, 1997, Activation and novel
processing of matrix metalloproteinase by a Thiol-proteinase from the oral
anaerob Porphyromonas gingivalisí, J Dent Res 76(6): 1260-70.
Delleon-Pennell, K.Y., Bras, L.E., Lindsey, M.L., 2013, Circulating Porphyromonas
gingivalis, lipopolysaccharide resets cardiac homeostasis in mice through a
matrix metalloproteinase-9 dependent mechanism, Physiological Reports, 1(5).
Dobrowolski, J.W., Vohora, S.B., Sharma, K., Shah, S.A., Naqvi, S.A.H., Dandiya,
P.C., 1991, Antibacterial, antifungal, antiamoebic, anti-inflammatory, and
antipyretic studies on propolis bee products, J Ethno-pharmacol, 35: 77-82.
Dzink, J.L., Socransky, S.S., Haffaajee, A.D., 1988, The predominant cultivable
microbiota of active and inactive lesions of detructive periodontal diseases, J.
Clin. Periodontol., 15: 316-23.
Ezzo, P.J., Cutler, C.W., 2003, Microorganisms as risk indicators for periodontal
disease, J Periodontol 2000, 32: 24-35.
Fedi, P.F., Vernino, A.R., Gray, J.L., 2000, The Periodontic Syllabus, terj. oleh drg.
Amaliya, EGC, Jakarta, p:13, 52.
Feng, Z., Weinberg, A., 2006, Role of bacteria in health and disease of periodontal
tissues, Periodontology 2000, 40: 50-76.
Francis, G.W., Abdelrahman, H.F., Skaug, N., 2002, In vitro antimicrobial effects of
crude miswak extracts on oral pathogens, Saudi Dental J, 14(1): 26-32.
Gebara, E.C.E., Lima, L.A., Mayer, M.P.A., 2002, Propolis antimicrobial activity
against periodontopathic bacteria, Braz J Microbiol, 33(4): 365-9.
Gemmell, E., Seymour, G.J., 2004, Immunoregulatory control of Th1/Th2 cytokine
profiles in periodontal disease, Periodontol 2000, 35: 21-41.
Genco, R.J., 1992, Host responses in periodontal diseases: current concepts, J
Periodontol, 63: 338-55.

49
Ghisalberti, E.L., 1979, Propolis. A review, Bee world, 60: 59-84.
Gilette, W., 1996, Letter to the editor, J. Periodontol., 67: 726.
Grange, J.M., Davey, R.W., 1990, Antibacterial properties of propolis (bee glue), J R
Soc Med, 83: 159-60.
Greenway, W., Scaysbrook, T., Whatley, F.R., 1990, The composition and plant
origins of propolis: A report of work at Oxford, Bee World, 71:107-18.
Hansen, H.B., 1995, Proteolytic remodelling of extracellular matrix, Current opinion
of cell biology 5: 728-35.
Harvey, C.E., 2005, Management of periodontal disease: Understanding the options,
Vet Clin North Am Small Anim Pract, 35(4): 819-36.
Hasan, A.E.Z., 2006, Potensi propolis lebah madu Trigona spp. Sebagai bahan
antibakteri, Seminar Nasional HKI: Bogor.
Hayakawa, T., 1998, Matrix metallcoproteinases (MMPs) and tissue inhibitors of
metallopproteinases (TIMPs) in the development and disease of oral tissues,
Dentistry in Japan, 34: 167-173.
Heasman, P.A., Seymour, R.A., 1994, Pharmacological control of periodontal
disease. I. Antiplaque agents, J. Dent., 22: 323-35.
Hegazi, A.G., Khalifah, M.H., Tousun, E., 1997, Influence of Egyptian and Bulgari
an propolis an same biochemical changes of normal and Bacteria infected rat,
International Symposium on Apitherapy, Cairo, Egypt.
Henry, H., Takei, H.H., Carranza, F.A., 2012, Clinical Diagnosis, dalam Newman,
M.G., Takei, H.H., Klokkevold, P.R., Carranza, F.A.: Carranza’s Clinical
Periodontology, 11th
ed., p:349-50, Elsevier saunders Inc., Missouri.
Hill, R., 1981, Propolis: the natural antbiotic, 6th
ed., Thorsons Publishers Ltd,
Wellingborough, 7-8.
Hinrichs, J.E., Novak, M.J., 2012, Classification of Diseases and Conditions
Affection the Periodontium, dalam Newman, M.G., Takei, H.H., Klokkevold,
P.R., Carranza, F.A.: Carranza’s Clinical Periodontology, 11th
ed., p:41,
Elsevier saunders Inc., Missouri.
Ingman, T., Ding, et al, 1996, Matrix metalloproteinase and their inhibitors and
gingival crevicular fluid and saliva of periodontitis patients, Journal of Clinical
Periodontology, 23: 1127-32.

50
Junior A.F., Dalestrin, A.C., Betoni, J.E.C., Orsi R.O., et al., 2005, Propolis : Anti-
Staphylococcus aureus activity atid synergism with antimicrobial drugs, Mem
Inst Oswaldo Cruz, 100(5): 563-66.
Kaal, J., 1991, Natural medicine from honey bees (apitherapy), Kaal’s Printing
House, Amsterdam, 9-12.
Kaihena, M., 2013, Propolis sebagai imunostimultor terhadap infeksi Micobacterium
tuberculosis, Prosiding FMIPA Universitas Pattimura, 69-80.
Kato, H., Taguchi, K., Tominaga, K., Umeda, M., Tanaka, A., 2014, Porphyromonas
gingivalis LPS inhibits osteoblastic differentiation and promotes pro-
inflammatory cytokine production in human periodontal ligament stem cells,
Archives of Oral Biology, 59(2): 167-75.
Kesic, L., Milasin, J., Igic, M., Obradovic, R., 2008, Microbial etiology of
periodontal disease – mini review, Medicine and Biology, 15(1): 1-6.
Koo, H., Gomes, B.P.F.A., Rosalen, P.L., Ambrosano, G.M.B., Park, Y.K., Cury,
J.A., 2000, In vitro antimicrobial activity of propolis and Arnica montana
against oral patoghens, Arch Oral Biol, 45: 141-8.
Koo, H., Hayacibara, M.F., Schoel, B.D., 2003, Inhibition of Streptococcus mutans
biofilm accumulation and polysaccharide production by apigenin and tt-
farnesol, Antimicro Chemo J, 52(5): 782-89.
Krell, R., 1996, Value-added products from beekeeping, FAO Agricultural Services
Bulletin No.124 Chapter 5. http://www.fao.org/docrep/w0076e/w0076e14.htm.
Diakses tanggal 17 Februari 2015.
Kujumgiev, A., Tsvetkova, I., Serkedjieva, Y., Bankova, V., Cristov, R., Popov, S.,
1999, Antibacterial, antifungal, and antiviral activity of propolis of different
geographic origin, J Ethno-pharmacol, 64: 235-40.
Kumar, P.S., Griffen, A.L., Barton, J.A., Paster, B.J., Moeschberger, M.L., Leys,
E.J., 2003, New bacterial species associated with chronic periodontitis, J Dent
Res, 82(5): 338-44.
Kun, Y.P., Ikegaki, M., 1998, Preparation of water and ethanolic extracts of propolis
and evaluation of the preparations, Biosci. Biotechnol. Biochem, 62(11): 2230-
32.
Kusumawardani, B., Pujiastuti, P., Sandra D.S., 2010, Uji biokimiawi sistem API 20
A mendeteksi Porphyromonas gingivalis isolat klinik dari plak subgingiva
pasien periodontitis kronis, Jurnal PDGI, 59(3): 110-4.
Listgarten, M.A., 1976, Structure of microbial flora associated with periodontal
health and disease in man, J. Periodontol, 47:1-18.

51
Loesche, W.J., 1996, Antimicrobials in dentistry:With Knowledge comes
responsibility, J. Dental Res., 75: 1432-33.
Lofty, M, 2006, Biological activity of bee propolis in health and disease, Asian
Pacific Journal of Cancer Prevention, 7.
Marcucci, M.C., 1995, Propolis : chemical composition, biological properties, and
therapeutic activity, Apidologie, 26: 83-99.
Martinez-Silveria, G., Gou-Godoy, A., Ona-Torriente, R., Palmer-Ortiz, M.C.,
Falcon-Cuellar, M.A., 1988, Preliminary study of the effect of propolis in the
treatment of chronic gingivitis and oral ulceration, Rev Cubana Estomatol,
25(3): 36-44.
Murray, M.C., Worthington, H.P., Blinkhorn, A,S., 1997, A study to investigate the
effect of a propolis-containing mouthrinse on the inhibition of de novo plaque
formation, J Clin Periodontol, 24: 796-8.
Mysak, J., Podzimek, S., Sommerova, P., Lyuya-Mi, Y., Bartova, J., Janatova, T.,
2014, Porphyromonas gingivalis: Major periodontopathic pathogen overview,
Journal of Immnunology Research, 1-8.
Na, H.S., Lim, E.J., Jeong, S.Y., Ryu, M.H., Park, M.H., Chung, J., 2014,
Plasminogen activator inhibitor type 1 expression induced by
lipopolysaccharide of Porphyromonas gingivalis in human gingival fibroblast,
Journal of Microbiology, 52(2): 154-60.
Neelufar, S.S., Prasanna, K.R., Joshna, A., Lakshmi, S.T., 2014, Effect of herbs on
periodontitis – a serious gum infection, International Journal of Pharmacology
Research, 4(1): 17-22.
Novilla, A., 2010, Aktivitas antibakteri ekstrak propolis Apis mellifera terhadap
pertumbuhan Methicillin-Resistant Staphylococcus aureus (MRSA) secara in
vitro. Jurnal Kesehatan Kartika Stikes A. Yani, 9-16.
Noyan, U., Yilma, S.,Kuru, B., 1997, A clinical and microbiological evaluation of
systemic and local metronidazole delivery in adult periodontitis patients, J Clin
Periodontol, 24: 158-65.
Page, R.C., Offenbacher, S., Schroeder, H.E., Seymour, G.J., Komman, K.S., 1997,
Advances in the pathogenesis of periodontitis: summary of developments,
clinical implications and future directions, Periodontol 2000, 14: 216-48.
Park, Y.K., Koo, M.H., Abreu, J.A.S., Ikegaki, M., Cury, J.A., Rosalen, P.L., 1998,
Antimicrobial activity of propolis on oral microorganisms, Current Microbiol,
36: 24-8.

52
Paster, B.J., Olsen, I., Aas, J.A., Dewhirst, F.E., 2006, The breadth of bacterial
diversity in the human periodontal pocket and other oral sites, Periodontol
2000, 42: 80-7.
Pietta, P.G., Gardana, C., Pietta, A.M., 2002, Analytical methods or quality control
of propolis, Fitoterapia, 73(1): 7-20.
Poedjiono, E., Subiyanto, A., Widjiastuti, I., 2014, Efektivitas ekstrak propolis
12,38% dan Chlorhexidine gluconate 0,2% terhadap biofilm Porphyromonas
gingivalis, Concervative Dentistry Journal, 4(2): 11-14.
Polanowska, J., Polanowski, A., 1997, The role of Porphyromonas gingivalis
proteinases in periodontitis, Postpy Higieny I Medycyny Doswiadczalnej,
51(2): 149-69.
Prasetyorini, Hasan, A.E.Z., Siregar, R., 2011, Penerapan teknologi nanopartikel
propolis Trigona spp asal Bogor sebagai antibakteri Eschericia coli secara in
vitro, Ekologia, 11(1): 36-43.
Rams, E.T., Slots, J., 1996, Systemic and antimicrobial therapy in periodontics,
Periodontol 2000, 10: 139-154.
Riset Kesehatan Dasar (RISKESDAS), 2007, Laporan penelitian. Departemen
Kesehatan Indonesia [homepage on the internet] 2008 [cited 2013 Jan 28].
Available from URL : http://www.scribd.com/doc/82922543/laporanNasional-
Riskesdas-2007
Salsabila, V.K., Munawir, A., Dewi, R., 2013, Efek antibakteri ekstrak etanol siwak
(Salvadora persica) terhadap pertumbuhan bakteri Porphyromonas gingivalis,
Artikel Ilmiah Hasil Penelitian Mahasiswa, 1-4.
Santos, F.A., Bastos, E.M., Uzeda, M., Carvalho, M.A., Farias, L.M., Moreira, E.S.,
et al, 2002, Antibacterial activity of Brazilian propolis and fractions against
oral anaerobic bacteria, J Ethnoparmacol, 80: 1-7.
Saphiro, S., Meier, A., Guggenheim, B., 1994, The antimicrobial activity of essencial
oil components towards oral bacteria, Oral Microbiol. Immunol., 9: 202-208.
Scheller, S., Wilczok, T., Imielski, S., Krol, W., Gabrys, J., Shani, J., 1990, Free
radical scavenging by ethanol extract of propolis, Int J Radiat Biol, 57(3): 461-
5.
Slots, J., Genco, R.J., 1984, Black-pigmented Bacteroides species, Capnocytophaga
species, and Actinobacillus actinomycetemcomitans in human periodontal
disease: Virulence factors in colonization, survival and tissue destruction, J.
Dental Res., 63: 412-21.

53
Slots, J., 2004, Research, Science and Therapy Committee. Systemic antibiotic in
periodontitis, J. Periodontol, 75(11): 1553-65.
Socransky, S.S., Haffajee, A.D., Cugini, M.A., Smith, C., Kent, R.L., 1998,
Microbial complexes in subgingival plaque, J Clin Periodontol, 25(2): 134-44.
Socransky, S.S., Haffajee, A.D., Dzink, J.L., 1988, Relationship of subgingival
complexes to clinical features at the sampled sites, J. Clin. Periodontol., 15:
440-44.
Stein, J.M., Machulla, H.K., Smeets, R., Lampert, F., Reichert, S., 2008, Human
leukocyte antigen polymer-phism in chronic and aggressive periodontitis
among Caucasians: A meta-analysis, Journal of Clinical Perio-dontology, 35:
183-192.
Stepanovic, S., Antic, N., Dakic, I., Vlahovic M.S., 2003, In vitro antimicrobial
activity of propolis and synergism between propolis and antimicrobial drugs,
Microbiol. Res., 158: 353-7.
Strassler, H.E., 2004, Periodontal splinting with fiber reinforced composite resin,
Compend Contin Educ Dent, 25: 53-9.
Susilo, B., Mertaniasih, N.M., Koendhori, E.B., Agil, M., 2009, Komposisi kimiawi
dan aktivitas antimikroba propolis dari Malang Jawa Timur, J. Penelit. Med.
Eksakta, 8(1): 23-30.
Takasi, Kikuni, N.B., Schilr, H., 1994, Electron microscopic investigation of the
possible mechanism of the untibacterial action of propolis, Provenance planta
Med., 60(3): 222-7.
Teles, R.P., Sakellari, D., Teles, F.R., Konstantinidis, A., Kent, R., Socransky, S.S.,
et al, 2010, Relationships among gingival crevicular fluid biomarkers, clinical
parameters of periodontal disease, and the subgingival microbiota, J
Periodontol, 81(1): 89-98.
Teles, F.R., Teles, R.P., Uzel, N.G., Song, X.Q., Torresyap, G., Socransky, S.S., et
al, 2012, Early microbial succession in redeveloping dental biofilms in
periodontal health and disease, J Periodontal Res, 47(1): 95-104.
Teronen, Y.T., Konttnen, C.L., 1997, Human neutrophil collagenase MMP-8 in peri-
implant sulcus fluid ang its inhibition by clodronate, J Dent Res, 76(9): 1529-
37.
van Winkelhoff, A.J., Rams, T.E., Slots, J., 1996, Systemic antibiotic therapy in
periodontitis, Periodontol 2000, 10;45-78.

54
Wahyukundari, M.A., 2009, Perbedaan kadar matrix metalloproteinase-8 setelah
scalling dan pemberian tetrasiklin pada penderita periodontitis kronis, Jurnal
PDGI, 58(1): 1-6.
Wang, P.L., Ohura, K., 2002, Porphyromonas gingivalis lipopolysaccharide
signalling in gingival fibroblasts-CD14 and toll-like receptors, Critical Reviews
in Oral Biology and Medicine, 13(2): 132-42.
Williams, R.C., 1990, Periodontal disease, N Engl J Med, 373-82.
Yilmaz, O., 2008, The chronicles of Porphyromonas gingivalis: the microbium, the
human oral, epithelium and their interplay, Microbiology, 154(10): 2897-2903.
Zambon, J.J., 1996, Periodontal diseases: Microbial factors, Ann Periodontol, 1: 879-
925.
Zambon, J.J., 1996, Microbiologia da doenca periodontal, dalam Genco, R.J.,
Goldman, H.M., Cohen, D.W.: Periodontia Contemporanea, 1st ed., Livaria
editora Santos.

55
LAMPIRAN