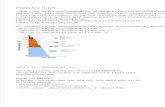
Diagram Fasa Keramik
-
Upload
aprillia-anggasari -
Category
Documents
-
view
866 -
download
59
Transcript of Diagram Fasa Keramik

DIAGRAM FASA KERAMIK
Anggota Kelompok:
1. Alfredo Ibrahim 2709 100 001
2. IGNB Dwistha Prayukti 2709 100 024
3. Aprillia Anggasari 2709 100 044
4. Saddam Husien 2709 100 094

Pengertian dan Konsep Kesetimbangan
Pengertian Diagram Fasa KeramikSuatu Diagram yang memberikan informasi mengenai :- komposisi dari setiap fasa- jumlah fasa- kuantitas fraksi setiap fasa- keadaan (cairan, larutan padat, campuran) dari
suatu sistem bahan yang berada dalam kesetimbangan

Diagram Fasa Keramik
Konsep KesetimbanganSuatu kondisi dikatakan seimbang
apabila komposisi, temperatur, tekanan dan kondisi lain yang mempengaruhi sistem tersebut berada dalam tingkat energi terendah.

Hukum Termodinamika I:
Dimana: G= Energi bebas GibssP= Tekanan sistemV= Volume sistemT= Temperatur mutlakS= Entropi µ= potensial kimia komponen ke-iX= fraksi mole komponen ke=i

Diagram Skematik Kesetimbangan
Keterangan:1.Meta Stabil2.Tidak Stabil3.Stabil

Aturan Fasa (Phase Rule)
P + V = C + 2
Keterangan :P = Jumlah Fasa yang berada dalam kesetimbangan V = Variasi atau derajat kebebasanC = Jumlah komponen penyusun sistem bahan

Teknik Pembuatan Diagram Fasa Metode Dinamik
Proses: Analisa termal Analisa perubahan fasa Analisa perubahan sifat fisik (konduktivitas
listrik, ekspansi termal dan viskositas) Kelemahan Metode Dinamik:
Tidak bisa mengetahui reaksi kimia yang terjadi secara tepat

Teknik Pembuatan Diagram Fasa Metode Statik
Proses: Memanaskan sample pada temperatur atau
pada tekanan tertentu yang diinginkan Mendinginkan secara cepat (Quenching) hingga
temperatur kamar Menguji sampel dengan menggunakan difraksi
sinar-X atau SEM untuk menganalisis perubahan fasa

Diagram Fasa Satu Komponen
• Temperatur dan Tekanan dapat menimbulkan terjadinya pembentukan fasa sekaligus dapat pula menghilangkan fasa dari keramik tersebut.
• Contoh: pada proses penguapan (cair-gas) terjadi karena adanya perubahan temperatur dan disertai tekanan
Fasa
Gas
Cair
Padat

• Hubungan antara Temperatur dan Tekanan dapat digambarkan pada diagram kesetimbangan fasa berikut:
• Titik A,merupakan titik yang menunjukkan daerah kesetimbangan dari ketiga fasa,namun setiap terjadi perubahan temperatur maupun tekanan akan menyebabkan hilangnya satu fasa
• Titik B, terletak pada garis diagram, menyatakan keadaan dimana dua fasa berada dalam kesetimbangan. P = 2 dan C = 1 sehingga V = 1. hal ini berarti bahwa baik tekanan atau temperatur tetapi tidak keduanya dapat berubah secara bebas tanpa kehilangan fasa
• Titik C,mewakili daerah satu fasa dimana P=1,C=1 dan V=2. Perubahan Temperatur dan Tekanan tidak lagi menimbulkan perubahan fasa

Untuk Keramik (contoh : SiO2) diagram fasanya dapat digambarkan sbb:

• Dari diagram tersebut dapat kita lihat pada SiO2 ketika tekanan rendah terbentuk 5 fasa padat yaitu: kuartz- ,kuartz- ,trimidit-2, kristobalit- dan silika cair.
• Pada temperatur tinggi pada silikat akan terbentuk fasa Gas (vapor)
• Pada temperatur 573°C terjadi transformasi kuartz- ke kuartz- secara cepat dan reversibel sedangkan transformasi fasa yang lain terjadi sangat lambat sehingga membutuhkan waktu yang panjang untuk mencapai kesetimbangan
Keterangan.........

Diagram Fasa Sistem Dua Komponen (Biner)
Dalam sistem dua komponen terdapat variasi menurut persamaan Gibbs adalah: Tekanan Temperatur Komposisi
Dalam bahan padat, tekanan tidak berpengaruh banyak sehingga digambarkan dengan variabel temperatur dan komposisi

Energi Bebas dalam larutan dengan 2 komposisi
Keterangan:GS = Energi bebas larutanGM = Energi bebas campuran∆HS = Entalpi larutanT = Temperatur∆ Sm = Entropi campuran

• Apabila Larutan merupakan campuran, maka ∆ Sm dan ∆HS tidak berpengaruh
Larutan Ideal

Larutan Biasa
• Dalam campuran yang biasa, semua komponen energi berpengaruh pada GS
seperti persamaan di atas. • Entalpi dapat bernilai positif atau negatif
oleh karenanya GS dapat mempunyai dua minimum.

Apabila campuran A dan B tidak bisa larut sama sekali , maka akan dapat terjadi diskontinuitas GS sehingga terjadi pemisahan fasa a dan ßLarutan padat yang tidak sempurna

Prosentase Kandungan Komposisi
Untuk menghitung prosesntase dari kandungan komposisi di setiap titik dalam menuruti prinsip lever rule fraksi a = BC fraksi ß AC Dalam hal ini kandungan di titik C merupakan campuran yang terdiri dari: fasa a = BC x 100% dan fasa ß = AC x 100%
AB AB

Phase compositions and amounts. An example.

Terima Kasih