BAB II KAJIAN PUSTAKA 2.1 Definisi Karsinoma Tiroid Papiler 2.pdfBerdasarkan WHO, tumor primer...
Transcript of BAB II KAJIAN PUSTAKA 2.1 Definisi Karsinoma Tiroid Papiler 2.pdfBerdasarkan WHO, tumor primer...
1
BAB II
KAJIAN PUSTAKA
2.1 Definisi Karsinoma Tiroid Papiler
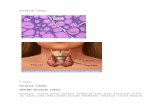
Karsinoma tiroid papiler (KTP) merupakan neoplasma ganas sel epitel folikel tiroid
yang membentuk pola pertumbuhan papiler atau disertai dengan pola folikuler dan
utamanya ditandai oleh karakteristik inti khas KTP. Gambaran inti yang khas KTP
meliputi ukuran inti membesar, berbentuk oval, mengalami elongasi, saling tumpang
tindih dengan gambaran clearing atau ground glass appearance atau dengan kontur
inti yang ireguler mencakup adanya groove dan inklusi sitoplasma intranuklear. KTP
tergolong tumor ganas tiroid yang berdiferensiasi baik (De Lellis et al., 2004).
2.2 Klasifikasi Karsinoma Tiroid
Berdasarkan WHO, tumor primer tiroid diklasifikasikan menjadi epitelial dan
nonepitelial, jinak atau ganas, dengan kategori yang terpisah untuk limfoma dan
keganasan lainnya (tabel 2.1) (De Lellis et al., 2004). Klasifikasi karsinoma tiroid
berdasarkan garis besar diferensiasinya dijabarkan menurut American Joint
Commission on Cancer (AJCC) sesuai yang dijabarkan tabel 2.2 (Rubin et al., 2012).
Penelitian ini mengacu pada sistem klasifikasi WHO dan AJCC.
2
Tabel 2.1
Klasifikasi histologik tumor tiroid berdasarkan WHO (Rubin et al., 2012)
I. Tumor epitelial
A. Jinak
1. Adenoma Folikuler
2. Lainnya
B. Ganas
1. Karsinoma Folikuler
2. Karsinoma Papiler
3. Karsinoma Meduler*
4. Karsinoma Undifferentiated (anaplastik)
5. Lainnya
II. Tumor Non-epitelial
A. Jinak
B. Ganas
III. Limfoma maligna
IV. Lainnya
V. Tumor sekunder
VI. Tumor yang tidak dapat diklasifikasikan
VII. Lesi yang menyerupai tumor
*Karsinoma sel non epitelial folikel
3
Tabel 2.2
Tipe Histopatologis Karsinoma Sel Folikel Tiroid (Rubin et al., 2012)
A. Karsinoma papiler (mencakup KTPVF)
B. Karsinoma folikuler (mencakup karsinoma sel hurtle)
C. Karsinoma poorly differentiated
D. Karsinoma undifferentiated (anaplastic)
2.3 Epidemiologi
Karsinoma tiroid merupakan keganasan tersering dari organ endokrin. Karsinoma ini
merupakan 3% dari insiden terbaru seluruh kanker yang terdiagnosis di Amerika
Serikat dan 1,7% dari insiden terbaru seluruh kasus kanker di dunia. Insiden dan
prevalen karsinoma tiroid mengalami peningkatan yang tetap selama tiga dekade
terakhir, terutama sejak pertengahan tahun 1990-an di berbagai negara di dunia. Saat
ini insiden karsinoma tiroid diperkirakan antara 5 hingga 8 kasus per 105 penduduk
per tahun di negara-negara berkembang (Frasca et al., 2008). Data lain menyebutkan
telah ditemukan lebih dari 213.000 kasus baru karsinoma tiroid di seluruh dunia pada
tahun 2008, dengan angka insiden kasar 3,1/100.000 (Cossu et al., 2013). Temuan
kasus baru meningkat lagi pada tahun 2010 berdasarkan penelitian terbaru yang
didukung oleh WHO yaitu ditemukan sekitar 44.670 kasus baru (De Matos et al.,
2012). Berdasarkan data SEER (Surveillance, Epidemiology, and End Results) di
Amerika Serikat, insiden karsinoma tiroid meningkat tiga kali lipat sejak tahun 1973,
4
dengan kecepatan pertumbuhan 2,4% per tahun antara tahun 1980 hingga 1997 dan
6,5% per tahun sejak tahun 1997 serta saat ini menduduki lima besar karsinoma yang
mengalami peningkatan insiden tercepat, baik pada pria maupun wanita. Insiden
karsinoma tiroid di seluruh dunia bervariasi pada masing-masing daerah geografis
dan secara keseluruhan lebih tinggi pada negara ekonomi berkembang (Nikiforov,
2009).
Peningkatan insiden karsinoma tiroid terutama terjadi pada KTP, sedangkan tipe
lain seperti folikuler, meduler, maupun anaplastik tidak menunjukkan perubahan
yang signifikan. KTP berjumlah sekitar 83% dari keseluruhan keganasan tiroid dan
80% dari keseluruhan tumor ganas tiroid yang berdiferensiasi baik (Nikiforov, 2009;
Meng et al., 2012; Zidan et al., 2003). Peningkatan insiden KTP mencakup KTP
klasik dan KTPVF, baik pada tumor yang berukuran <1 cm maupun >1 cm atau
bahkan >4 cm hingga 5 cm. Peningkatan temuan insiden KTP kemungkinan terkait
dengan semakin maraknya metode deteksi dini melalui pemeriksaan ultrasonografi
maupun biopsi jarum halus (FNA/ fine needle aspiration). Alasan lainnya yaitu
karena telah dikenalnya perubahan inti yang khas menjadi kriteria morfologi KTP
(Nikiforov, 2009; Kondo et al,. 2006).
Di Indonesia tidak ditemukan data khusus tentang insiden KTP, data yang
dilaporkan adalah keseluruhan kasus kanker tiroid. Menurut Registrasi Perhimpunan
Dokter Spesialis Patologi Indonesia, dari tahun 2008-2010 kanker tiroid menempati
urutan ke 5 dari 10 kanker terbanyak dan urutan ke 4 dari 10 kanker terbanyak pada
5
perempuan. Di Denpasar pada rentang tahun yang sama kanker tiroid menduduki
urutan ke 3 dari 10 kanker terbanyak dengan prevalensi secara berurutan yaitu
155/2000 kasus, 84/865 kasus, 118/1124 kasus. Diantara keseluruhan kasus tersebut,
diperkirakan sekitar 80% merupakan kasus KTP, dengan varian klasik (KTP Klasik)
sebagai subtipe KTP terbanyak (80%) dan diikuti oleh KTPVF sebagai subtipe kedua
terbanyak (9-22,5% kasus KTP) (Ditjen Yan Med, 2008-2010; Gupta et al., 2012).
0
2
4
6
8
10
2008 2009 2010
Denpasar
Gambar 2.1
Grafik prevalensi kasus karsinoma tiroid di Denpasar tahun 2008-2010
berdasarkan data registrasi kanker Perhimpunan Dokter Spesialis Patologi
Anatomi Indonesia (Ditjen Yan Med, 2008-2010).
Hingga saat ini epidemiologi KTP masih sangat menarik untuk ditelusuri.
Penelitian berbagai negara di dunia telah membandingkan insiden tumor ini pada
populasi yang tinggal di area dataran tinggi (pegunungan) dengan populasi yang
tinggal di sekitar pantai membuktikan bahwa konsentrasi asupan iodium
mempengaruhi insiden KTP bahkan pada beberapa kasus berkaitan dengan morfologi
Prev
alen
si kasu
s
Tahun
6
KTP (LiVolsi., 2011). Dilaporkan bahwa insiden KTP lebih sering pada daerah
dengan asupan iodium yang cukup, sedangkan insiden KTF berkaitan dengan
defisiensi iodium (Knobel et al., 2007).
Kasus goiter baik endemik maupun non endemik (sporadik) diyakini merupakan
prekursor perkembangan kanker tiroid. Prevalensi goiter di seluruh dunia pada
populasi umum sekitar 4-7%, dan insiden keganasan terjadi pada 10% kasus tiroid
goiter. Dilaporkan bahwa insiden karsinoma tiroid tercatat meningkat pada daerah
goiter endemik seperti Kolumbia dan Austria serta daerah non endemik seperti
Jerman. Peningkatan insiden karsinoma tiroid terkait goiter juga menjadi
permasalahan di negara Asia Tenggara termasuk Indonesia. WHO mencatat sekitar
655 juta jiwa di dunia mengalami goiter dan 27% diantaranya berada di Asia
Tenggara (Htwe, 2012). Adapun perbandingan hasil studi epidemiologi karsinoma
tiroid terkait goiter di beberapa Negara Asia Tenggara sesuai tabel 2.3.
Di RSUP Sanglah Denpasar sekitar 70% kasus KTP berasal dari nodul goiter
baik nodul soliter tunggal maupun multipel. Pada kasus tersebut umumnya secara
mikroskopis akan ditemukan adanya latar belakang gambaran goiter di sekitar area
neoplastik. Hal ini menunjukkan bahwa kasus KTP di RSUP Sanglah Denpasar juga
berkaitan dengan kasus goiter.
7
Tabel 2.3
Tabel temuan beberapa studi di Malaysia dan Myanmar tentang hubungan antara
karsinoma tiroid dan goiter (Htwe, 2012)
Studi; tahun
Sarawak;
2000–2004
Kelantan;
1994–2004
Perak;
2004–2007
Myanmar;
1996–1998
Kesimpulan dan diskusi
•Insiden secara signifikan lebih tinggi
pada pria (p=0,01)
•Prevalensi tertinggi pada rentang usia
21-40 tahun
•Tipe histologis tersering: KTP
•28,1% dari 1.480 lesi tiroid merupakan
lesi neoplastik
•Tersering adalah KTP (76,6%)
•Mayoritas kasus (59.9%) terjadi dengan
latar belakang hiperplasia noduler
•Studi menunjukkan karsinoma tiroid
yang berkembang dari MNT terbanyak
pada area defisiensi iodium
•Bukan merupakan area endemik ,
sampel sedikit tetapi Karsinoma tiroid
lebih tinggi dari daerah lain (11%) dan
KTP (57,5%)
•Rentang usia 21-60 tahun, tertinggi pada
ras malay, diikuti india kemudian china.
•Kejadian karsinoma tiroid diantara
keseluuhan kasus lebih tinggi secara
signifikan; p< 0,0001
•Frekuensi secara signifikan lebih tinggi
pada pasien usia 21-60 tahun; p < 0,008
•KTP dan adenoma folikuler secara
signifikan lebih tinggi dari tipe lainnya; p
= 0,003
•Peningkatan insiden tiap tahun;p > 0.034
8
Studi epidemiologis lain telah melaporkan kaitan KTP dengan radiasi. Pada
pertengahan abad yang lalu, karsinoma tiroid seringkali terdiagnosis pada individu
yang sebelumnya pernah menjalani terapi radiasi dosis rendah pada bagian kepala
leher untuk penyakit jinak seperti hemangioma, limfangioma, pembesaran kelenjar
tymus, pembesaran tonsil dan adenoid. Laporan selanjutnya menyebutkan KTP
dijumpai pada korban serangan bom atom di Jepang pada akhir perang dunia II
(LiVolsi., 2011). Terakhir diketahui terjadi peningkatan tajam KTP pada anak-anak
usia di bawah 15 tahun akibat bencana Chernobyl di Belarusia pada bulan april 1986
yang dikenal sebagai epidemik KTP (LiVolsi., 2011; De Lellis et al., 2004).
Tabel 2.4
Prevalensi kasus karsinoma tiroid selama 3 tahun (2008-2010) di Indonesia
berdasarkan kelompok usia
Kelompok Prevalensi (%)
Usia 2008 2009 2010
<15 1,34 1,17 1,45
15-24 10,96 8,73 7,79
25-34 20,96 18,18 18,55
35-44 22,11 23,22 23,61
45-54 20,86 23,85 24,73
55-64 12,40 13,50 12,69
65-74 7,59 6,12 8,51
≥75 1,53 2,07 1,12
Berdasarkan kelompok usia, KTP bermanifestasi pada usia dewasa antara 20-50
tahun (median usia 43 tahun) dengan rasio perbandinganan antara perempuan dan
laki-laki yaitu 4:1. Jika terjadi diatas usia 50 tahun, dominasi perempuan berkurang.
Sedangkan median usia untuk kasus KTPVF sama dengan KTP pada umumnya yaitu
9
44 tahun dengan rasio perbandingan perempuan terhadap laki-laki yaitu 6:1 (De
Lellis et al., 2004; Gupta et al., 2012; Chen et al., 2012). Sesuai tabel 2.4 di
Indonesia, selama tahun 2008-2010 lebih dari 75% kasus karsinoma tiroid terjadi
pada rentang usia 25-64 tahun, median usia yaitu 49 tahun, dengan rasio
perbandingan antara kelompok perempuan terhadap laki-laki yaitu 4:1.
Tingkat mortalitas akibat karsinoma tiroid masih rendah, namun kejadiannya
telah mengalami peningkatan sejak tahun 1992 dengan kecepatan 0,6% per tahun.
Pada tahun 2010, data terbaru WHO menyebutkan insiden mortalitas karsinoma tiroid
sebanyak 3,78%. Sedangkan untuk karsinoma berdiferensiasi baik seperti KTP, angka
harapan hidup tergolong tinggi yaitu sekitar 82-86% dan sebanding antara KTP klasik
maupun KTPVF (De Matos et al., 2012)
2.4 Faktor risiko
Terdapat beberapa faktor risiko terkait karsinoma tiroid terutama KTP, diantaranya
goiter, paparan radiasi, tiroiditis limfositik, faktor hormonal dan faktor herediter
(genetik). Goiter merupakan proliferasi kelenjar tiroid yang dapat terkait kondisi
eutiroid, hipo- maupun hipertiroid akibat penyakit primer pada tiroid maupun
rangsangan sekunder oleh faktor hormonal maupun faktor lain (Kondo et al., 2006).
Di Indonesia, beberapa wilayah masih tercatat sebagai daerah endemis goiter akibat
rendahnya asupan iodium. Adapula kasus goiter dengan etiologi yang belum jelas
diketahui, dikenal sebagai goiter sporadik diyakini berkaitan dengan faktor biologis
10
intrinsik (prevalensi goiter lima hingga sepuluh kali lipat lebih sering terjadi pada
wanita daripada laki-laki), goitrogen alami, merokok, defisiensi zinc atau selenium
dan stress emosional (Fuhrer et al., 2012).
Goiter dapat menimbulkan hiperplasia yang bersifat difusa maupun noduler
(nodul tunggal dan multipel) dan dipercaya mempengaruhi peningkatan insiden KTP.
Analisis klonal telah dimanfaatkan dalam membedakan hiperplasia dengan neoplasia,
dimana hiperplasia digolongkan sebagai proliferasi yang bersifat poliklonal
sedangkan neoplasia merupakan proliferasi monoklonal dari sel yang mengalami
transformasi genetik. Pada tiroid, ditemukan perubahan pola monoklonal pada
kelompok nodul yang sebelumnya merupakan nodul hiperplastik (Kondo et al.,
2006). Mekanisme bagaimana perubahan poliklonal menjadi monoklonal ini
merupakan interaksi antara faktor risiko goiter dan adanya predisposisi genetik yang
selanjutnya menciptakan lingkungan mutagenik yang ditandai oleh peningkatan
proliferasi sel disertai pembentukan radikal bebas yang memicu adanya mutasi
somatik tirosit. Klonal tumor terbentuk jika defek genetik tidak dapat diperbaiki.
Pada kondisi ini, mutasi merupakan pencetus proliferasi sel (Fuhrer et al., 2012).
Goiter meningkatkan risiko karsinoma tiroid sebanyak dua setengah kali lipat (Cossu
et al., 2013)
Ditemukan bahwa insiden KTF lebih tinggi terjadi pada area goiter endemik yang
berkaitan dengan rendahnya asupan iodium. Sedangkan insiden KTP lebih sering
berkaitan dengan goiter sporadik pada area dengan asupan iodium yang cukup.
11
Sebuah penelitian eksperimental pada hewan coba yang sebelumnya dengan asupan
iodium rendah kemudian diberikan suplementasi iodium didapatkan terjadinya
perubahan morfologi folikuler menjadi papiler. Hal ini menunjukkan peranan kadar
iodium lebih penting dalam memodulasi morfologi tumor daripada inisiator pada
karsinogenesis tiroid. Jika propilaksis iodium diberikan, maka terjadi penurunan rata-
rata TSH (Thyroid Stimulating Hormone) serum dan peningkatan perbandingan rasio
struktur papiler : folikuler (Kondo et al., 2006). Selain itu peningkatan iodium juga
berkaitan dengan frekuensi mutasi BRAFV600E dengan mekanisme yang belum
diketahui dan baru dibuktikan melalui beberapa studi epidemiologi (Pellegriti et al.,
2013)
Gambar 2.2
Mekanisme nodul goiter sebagai faktor risiko KTP (Fuhrer et al., 2012)
Radiasi meningkatkan risiko karsinoma tiroid hingga enam kali lipat (DeLellis et
al., 2004) Paparan radiasi menyebabkan terjadinya tata ulang kromosom yang
menghidupkan aktivitas gen secara berlebih, memicu instabilitas genomik melalui
mekanisme langsung maupun tak langsung, menyebabkan perubahan awal genetik
12
yang melibatkan jalur sinyal mitogen activated protein kinase (MAPK). Aktivasi
onkogenik sinyal MAPK selanjutnya meningkatkan instabilitas genomik, memicu
perubahan lanjut genetik yang melibatkan jalur sinyal lainnya, regulator siklus sel dan
berbagai molekul adesi. Instabilitas genomik dan perubahan genetik secara bersama-
sama memicu progresi karsinoma tiroid (Kondo et al., 2006)
Gambar 2.3
Mekanisme beberapa faktor risiko seperti radiasi dalam memicu karsinoma tiroid
(Kondo et al., 2006)
Infiltrat limfosit seringkali dijumpai pada KTP, mengindikasikan faktor
imunologis yang terlibat dalam progresi KTP. Limfositik tiroiditis seperti pada
tiroiditis Hashimoto maupun autoimun memicu KTP tidak hanya melalui peningkatan
level TSH tetapi juga dengan memproduksi berbagai sitokin proinflamasi dan tekanan
oksidatif yang meningkatkan tumorigenesis tiroid (Kondo et al., 2006). Risiko
13
terjadinya KTP akibat pengaruh imunologis sekitar satu sepertiga kali lipat
dibandingkan populasi normal (Baloch et al., 2010).
Terjadinya kasus KTP yang dua hingga empat kali lebih sering pada wanita
menunjukkan bahwa hormon pada wanita mengatur karsinogenesis tiroid. Beberapa
penelitian melaporkan bahwa reseptor estrogen diekspresikan oleh sel-sel epitel
folikel, sehingga pada pasien pemakai kontrasepsi oral maupun yang menjalani terapi
estrogen rentan mengalami karsinoma tiroid karena estrogen dapat memicu
proliferasi sel epitel folikel. Faktor lain seperti pada kehamilan terjadi peningkatan
hormon tiroid serum dan estrogen yang mendukung peranan estrogen dalam
karsinogenesis tiroid. Penelitian terbaru menyebutkan bahwa estrogen dapat
meningkatkan ekspresi reseptor estrogen α (ERα) pada sel KTP non anaplastik,
meningkatkan proliferasi sel dan menghambat ekspresi protein pro-apoptosis. Sinyal
estrogen berkaitan dengan KTP yang tidak agresif, dengan diferensiasi dan prognosis
yang baik. Hal ini terjadi karena pada mayoritas KTP, efek proliferasi ERα akan
dihambat oleh ekspresi dominan reseptor estrogen β (ERβ) (Kondo et al., 2006;
Kavanagh et al., 2010)
Risiko karsinoma tiroid meningkat hingga enam kali lipat jika orang tua atau
saudara mengalami karsinoma tiroid, hal ini menunjukkan adanya peranan faktor
herediter. Bentuk idiopatik familial non-medullary thyroid carcinoma ditemukan
pada 3,5-6,2% kasus karsinoma tiroid. Karsinoma tiroid familial berkaitan dengan
beberapa sindrom tumor seperti gen adenomatous polyposis coli (APC), Cowden
14
disease (terkait mutasi gen PTEN/ Phosphatase with tensin homology gene), sindrom
Werner (terkait mutasi gen WRN) serta karsinoma sel renal papiler (terjadi
kerentanan pada lokus 1q21) dan goiter multinoduler familial (kerentanan pada lokus
19p13.2) (Kondo et al., 2006)
2.5 Patogenesis Karsinoma Tiroid Papiler Klasik dan Varian Folikuler
Karsinoma tiroid terjadi akibat akumulasi dari sejumlah perubahan di tingkat
genomik (mutasi) yang dikenal sebagai instabilitas genomik. Berbeda dengan KTF,
pada KTP kromosom masih diploid atau mendekati diploid dengan frekuensi Loss of
Heterozygosity (LOH) yang lebih jarang. Perbedaan pola instabilitas kromosom ini
menunjukkan bahwa kedua tipe karsinoma tiroid ini melalui jalur molekuler yang
berbeda. Selanjutnya, instabilitas genomik memicu progresi neoplasma tiroid melalui
peningkatan aktivasi onkogenik hingga terhindar dari apoptosis. Serupa dengan
karsinoma di berbagai organ, proses karsinogenesis pada tiroid terjadi melalui
berbagai tahapan (multi-step) sehingga menimbulkan berbagai perubahan yang dapat
diamati secara histologik (Viglietto et al., 2012).
15
Gambar 2.4
Kaskade karsinogenesis neoplasma tiroid (Viglietto et al., 2012).
Terdapat tiga jalur utama perubahan biologi molekuler pada tumor-tumor yang
berasal dari sel epitel folikel tiroid yaitu TSH/cAMP, MAP kinase (MAPK) dan
P13K/AKT. Jalur mitogenik dan diferensiasi TSH/cAMP terlibat pada
hipertiroidisme sedangkan jalur mitogenik MAPK terlibat dalam perkembangan
karsinoma tiroid dan jalur P13K/AKT mempengaruhi perkembangan karsinoma yang
masih berdiferensiasi maupun yang berdiferensiasi buruk. Mutasi reseptor TSH
(TSHR) maupun Guanine nucleotide-binding α subunit 1 (GNAS1) memicu
proliferasi sel pada nodul hiperfungsi tiroid maupun adenoma melalui aktivasi GSα-
adnylyl cyclase-cAMP. Mutasi TSHR dan GNAS1 jarang ditemukan pada keganasan
16
tiroid, meskipun beberapa laporan kasus pernah menunjukkan adanya mutasi GNAS1
pada karsinoma tiroid berdiferensiasi baik (Kondo et al., 2006).
Gambar 2.5
Jalur sinyal sel pada neoplasia sel folikuler (Kondo et al., 2006).
Secara umum, karsinogenesis KTP terjadi melalui jalur kaskade RAS-BRAF-
MAPK. Tata ulang RET dan TRK merupakan karakteristik KTP yang berkaitan
dengan pecahnya rangkaian DNA. Sedangkan penelitian lain menemukan rendahnya
tata ulang kedua gen ini pada KTP dengan mutasi BRAF. Sehingga diketahui adanya
dua mekanisme utama pada KTP dalam aktivasi kaskade ini yaitu tata ulang RET
atau NTRK1 (Neurotrophic tyrosine kinase receptor1) dan aktivasi point mutation
pada BRAF, hanya diperlukan salah satu dari kedua mekanisme ini. Tata ulang RET
17
atau NTRK selanjutnya menyandi reseptor tirosin kinase (TRK) transmembran
(Chien et al, 2012). Sedangkan aktivasi point mutation pada BRAF, akan menjadi
komponen signaling intermediet dari jalur MAPK, hal ini terjadi terutama pada tumor
yang bersifat sporadik (Chien et al, 2012; Fuhrer et al., 2006; Viglietto et al., 2012)
Tata ulang gen RET/PTC diketahui sebagai alterasi genetik spesifik pertama pada
karsinogenesis tiroid. Gen RET mengkode reseptor tirosin kinase dari glial cell-
derived nervous growth factor dan secara endogen terekspresi pada sel
neuroendokrin. Terjadi ekspresi yang salah dari potongan gen RET pada melalui fusi
promotor pada regio N-terminal dari gen terkait (disebut PTC-1,2 dan seterusnya) dan
regio C-terminal fungsional dari gen RET (mengandung tirosin kinase). Hasilnya
adalah aktivasi RAS-RAF-MAPK signaling. Saat ini teridentifikasi lebih dari 8
protein chimera RET/PTC pada karsinoma tiroid, dimana RET/PTC-1
(inv(10)(q11.2;q21) dan RET/PTC-3 atau ELE1-RET (inv(10)(q11.2;q10) terhitung
kira-kira 80% dan merupakan fusi gen yang tersering (Chien et al, 2012). Keduanya
melibatkan inversi pada lengan panjang kromosom 10, menghasilkan perpaduan
antara RET dengan gen Histone H4 (histone protein nucleosome) pada RET/PTC-1
atau RET dengan nuclear receptor coactivator 4 (NCOA4) pada RET/PTC-3 (Chien
et al., 2012; Santoro et al., 2006).
Tata ulang gen RET/PTC spesifik untuk tumor yang memiliki arsitektur klasik
dan mikrokarsinoma dan prevalennya ditemukan lebih tinggi (30% sampai 65%) pada
keganasan yang disebabkan oleh radiasi (Chernobyl-tumor) dan lebih jarang (5%
18
sampai 15%) pada kanker yang sporadis. KTP varian klasik berkaitan dengan
RET/PTC1 (Chien et al., 2012).
Gambar 2.6
Tata ulang gen RET/PTC. A.Skema tampilan mekanisme molekuler terbentuknya
onkogen PTC. B.Perbandingan antara protoonkogen RET dan onkogen RET/PTC
(Viglietto et al., 2012)
Tata ulang gen lainnya pada KTP adalah inversi kromosom 7q menghasilkan fusi
antara BRAF dan AKAP 9 (A-kinase anchor protein 9 gene). Fusi protein ini
meningkatkan aktivitas kinase. Sepertiga sampai setengah dari kasus KTP ditemukan
gain-of-function mutation pada gen BRAF (Chien et al, 2012; Constantine et al,
2007). BRAF berlokasi pada kromosom 7q32, dan terjadi transversi thymine ke
adenine yang menyebabkan perubahan valine menjadi glutamate pada kodon 600
(BRAF V600E) (Constantine et al., 2007; Salajegheh et al., 2008). Mutasi pada BRAF
V600E dapat menyebabkan aktivasi RAF kinase dan secara in vitro dapat
menyebabkan transformasi sel dengan efikasi yang lebih tinggi daripada wild-type
A B
19
BRAF. Mutasi BRAF V600E dilaporkan sebagai defek molekular yang sering terjadi
pada KTP yang sporadis (berkisar antara 36% sampai 69%) dan pada KTP klasik
(antara 29-69%). Sementara tata ulang gen AKAP9/BRAF (inv(7)(q21-22q34) terjadi
pada radiation-induced karsinoma tiroid. Mutasi BRAF berkaitan dengan tumor yang
lebih agresif, sehingga memiliki prognosis yang buruk (Chien et al., 2012).
Seperti halnya yang sering dijumpai pada KTF, 13% KTPVF mengalami
translokasi kromosom t(2;3)(q13;p25) yang menggabungkan faktor transkripsi
khusus tiroid PAX8 ke PPARɤ, reseptor hormon inti yang secara normal terlibat
dalam diferensiasi sel berbagai jaringan. Selanjutnya ditemukan bahwa terdapat
hubungan antara adanya translokasi PAX8-PPARɤ dengan KTPVF yang multifokal
dan dengan invasi vaskuler. Sehingga tata ulangnya ini kemungkinan berperan
memicu proses metastasis (Chien et al., 2012; Salajegheh et al., 2008).
Translokasi PAX8-PPARɤ juga disertai mutasi BRAF non konvensional (K601E)
yang menimbulkan penggantian lisin oleh glutamat pada kodon 601 (BRAF K601E),
akibatnya terjadi peningkatan aktivitas kinase seperti yang terjadi pada mutasi BRAF
V600E pada KTP klasik. Namun aktivitas kinase BRAF V600E 2,5 kali lebih besar
daripada aktivitas kinase oleh BRAF K601E. Penelitian Trovisco dkk meyakinkan
bahwa mutasi BRAF K601E spesifik untuk KTPVF (Chien et al., 2012; Salajegheh et
al., 2008).
Berikutnya juga dilaporkan bahwa pola mutasi Ras pada KTF serupa dengan yang
terjadi pada sekitar 21% KTP terutama KTPVF. Hal ini menunjukkan kemungkinan
20
korelasi yang sangat kuat antara mutasi Ras dengan diferensiasi folikuler pada
karsinogenesis tiroid. Terdapat tiga protoonkogen Ras, diantaranya HRAS (pada
kromosom 11p11), KRAS (pada kromosom 12p12), dan NRAS (pada kromosom
1p13) merupakan kelompok famili besar protein yang berikatan dengan guanosin
triposfat (GTP) (Salajegheh et al., 2008). Mutasi pada karsinoma tiroid ini melibatkan
kodon 61 dari HRAS dan NRAS. Diketahui bahwa insiden mutasi Ras lebih jarang
dijumpai pada karsinoma tiroid yang berdiferensiasi baik dibandingkan dengan yang
berdiferensiasi buruk maupun yang anaplastik. Hal ini membuktikan bahwa mutasi
Ras berhubungan dengan progresi tumor (Kondo et al., 2006).
Selain keseluruhan proses intraseluler tersebut, progresi KTP berkaitan dengan
berbagai proses ekstraseluler seperti interaksi antar sel maupun interaksi sel dengan
ECM yang pada akhirnya juga mempengaruhi kondisi intraseluler (gambar 2.7).
Fibroblast growth factor (FGF) dan reseptornya (FGFR) merupakan regulator
penting dalam proses tomorigenesis maupun angiogenesis pada KTP. Pada berbagai
karsinoma tiroid akan terekspresi FGFR1, FGFR3 maupun FGFR4, sedangkan
FGFR2 hanya terekspresi pada tiroid normal dewasa. FGFR4 akan terekspresi pada
fenotip yang agresif mempengaruhi proliferasi, migrasi maupun diferensiasi sel.
Selain itu reseptor tirosin kinase MET yang merupakan reseptor untuk hepatocyte
growth factor (HGF) diketahui terekspresi kuat pada KTP (77-93%) dan berkaitan
dengan motilitas, kemampuan invasif dan memicu angiogenesis (Kondo et al., 2006).
21
Gambar 2.7
Interaksi antar sel dengan sel dan sel dengan ECM pada karsinoma tiroid (Kondo
et al., 2006).
Ligan Vascular endothelial growth factor (VEGF) seperti VEGFA, VEGFB,
VEGFC dan VEGFD berikatan dengan reseptornya dan memicu proliferasi sel
endotel dan limfatik. Ditemukan bahwa overekspresi VEGFC dan VEGFD pada KTP
berkaitan dengan densitas metastasis limfatik maupun KGB. Keseluruhan interaksi
ini juga dapat meningkatkan regulasi fibronektin pada KTP yang tidak invasif.
Fibronektin merupakan protein matriks ekstraseluler yang mengatur adesi, migrasi,
invasi tumor dan metastasis. Molekul adesi ini secara umum menghubungkan sel ke
kolagen atau substrat proteoglikan ECM lainnya. Pada kasus KTP yang invasif terjadi
penurunan ekspresi fibronektin dan kemampuan adesinya didegradasi oleh MMP
(Kondo et al., 2006).
22
2.6 Gejala klinis dan Makroskopis
Secara umum, KTP tampak sebagai massa tiroid atau cold nodule pada scan
radioaktif iodium atau seperti limfadenopati regio servikal. Pada area dengan
defisiensi iodium, KTP dapat berkembang dan tampak sebagai nodul yang berbeda
diantara goiter multinoduler. Sedangkan pada populasi dengan asupan iodium yang
cukup, KTP tampak sebagai nodul soliter yang teraba diantara kelenjar tiroid normal.
KTP seringkali ditemukan secara insidental pada nodul tiroid yang tidak teraba,
misalnya pada kasus trauma atau penyakit lainnya saat pemeriksaan imaging seperti
USG (Ultrasonografi). Nodul preklinis yang berupa fokus kecil atau fokus
mikroskopik KTP juga kadang ditemukan pada saat otopsi. Pentingnya arti klinis
karsinoma papiler yang tidak teraba tidak terlalu diperdebatkan sejak diketahui bahwa
karsinoma papiler dengan ukuran yang besar dan teraba pada pasien usia muda
memiliki harapan hidup 20 tahun sebanyak lebih dari 98% (De Lellis et al., 2004).
KTP klasik dapat menunjukkan berbagai pola makroskopis, lesi umumnya
berupa massa padat putih keabu-abuan dengan tepi yang ireguler atau kadang tampak
infiltrasi secara makroskopis ke parenkim tiroid sekitarnya. Beberapa kasus dapat
menunjukkan gambaran papil, perubahan kistik, kalsifikasi distrofik atau bahkan
pembentukan tulang. Ukuran tumor bervariasi, dari terkecil (<1 mm) hingga beberapa
sentimeter, ukuran rata-rata sekitar 2-3 cm. Tumor yang multisentrik juga sering
terjadi. Pada kasus lainnya tumor primer tampak solid meskipun metastasis ke KGB
menunjukkan gambaran kistik.
23
Gambar 2.8
Makroskopis karsinoma tiroid papiler. A. Irisan KTP klasik menunjukkan lesi dapat
bersifat multifokal, lesi terbesar berupa area kistik dengan tonjolan papiler di
dalamnya. (foto dari John Nicholls, MD, Hong Kong University) B. Lesi soliter dan
berkapsel pada KTPVF menyerupai adenoma folikuler (Baloch et al., 2011).
Karsinoma papiler juga dapat berkembang dari kista duktus tiroglosus dan dapat
menunjukkan perluasan langsung ke lemak peritiroid, otot skeletal, esofagus, larynx
dan trakea. Karsinoma papiler memiliki kemampuan menginvasi sistem limfatik
dalam kelenjar tiroid sehingga metastasis ke kelenjar getah bening sering terjadi.
Untuk KTPVF, secara makroskopis sering menyerupai adenoma folikuler
encapsulated yaitu berupa tumor cenderung soliter berbentuk bulat hingga ovoid,
dan berkapsel (De Lellis et al., 2004). Pada irisan akan tampak berwarna kuning
kecoklatan, mengkilat (glassy) karena kandungan koloid yang dimilikinya (Baloch et
al., 2010).
A B
24
2.7 Mikroskopis Karsinoma Papiler Tiroid Klasik dan Varian Folikuler
Terdapat berbagai varian/ subtipe KTP, diantaranya varian terbanyak yaitu varian
klasik yang didominasi pola pertumbuhan papiler dan varian terbanyak berikutnya
yaitu varian folikuler (KTPVF) yang didominasi dengan pola pertumbuhan folikuler.
Selain itu terdapat pula varian lain yang lebih agresif dilihat dari pola pertumbuhan,
tipe sel dan reaksi stroma seperti tall cell, columnar cell, diffuse sclerosing, clear cell
dan varian onkositik (Salajegheh et al., 2008). Secara umum, kriteria diagnosis KTP
awalnya didasarkan pada pola pertumbuhan papiler, namun saat ini sesuai ketetapan
WHO, hallmark diagnosis KTP didasarkan pada karakteristik inti (LiVolsi, 2011).
Gambaran histologi karakteristik inti KTP yaitu inti sel yang jernih, kosong, atau
Orphan Annie eye. Inti jernih ini berukuran lebih besar dengan bentuk yang lebih
ireguler dibandingkan inti sel folikel normal dan mengandung kromatin yang
hipodens. Gambaran inti yang jernih berkaitan dengan area tengah inti yang
eukromatin sedangkan area heterokromatin mayoritas terpusat di tepi inti. Anak inti
juga membenam di bagian tepi inti sehingga anak inti menjadi tidak terlihat. Inti pada
KTP ini tersusun saling tumpang tindih (overlapping) terkait dengan sitoplasma sel
epitelial folikel ganas yang terpusat di bagian apikal maupun basal sehingga inti sel
yang berdekatan tampak ramai dan saling tumpang tindih (LiVolsi, 2011). Sayangnya
gambaran inti yang jernih tidak hanya dijumpai pada KTP, tetapi juga dapat timbul
pada kasus tiroiditis autoimun khususnya tiroiditis hashimoto. Tetapi pada kasus non
neoplastik seperti tiroiditis, gambaran inti jernih bersifat fokal. Karakteristik inti
25
lainnya yaitu adanya nuclear groove yaitu gambaran inti yang terbelah seperti biji
kopi (LiVolsi, 2011; Gonzalez et al., 2011).
Pada KTP klasik, susunan sel didominasi oleh struktur papiler namun dapat
bervariasi dan bercampur dengan struktur folikuler (Gonzalez et al., 2011). Struktur
papiler umumnya kompleks dan bercabang, pada beberapa kasus papil bisa sangat
edematous. Struktur papiler ini dilapisi oleh epitel dengan polaritas yang terganggu
dan sitoplasma yang eosinofilik. Pola arsitektur lain seperti folikuler maupun solid
umumnya bersamaan dengan struktur papiler dan sangat jarang menemukan pola
petumbuhan papiler murni (Livolsi, 2011).
Papiler pada KTP harus dibedakan dengan struktur papiler yang terkadang
ditemukan pada goiter noduler atau adenoma folikuler dengan papil, dan dari lipatan
papiler pendek hiperplasia difus. Pada kondisi tersebut, inti sel epitelnya umumnya
bulat, terletak di basal dan yang terpenting tidak menunjukkan gambaran inti
karsinoma papiler atau kalaupun ada hanya dalam jumlah yang sangat sedikit (De
Lellis et al., 2004).
26
Gambar 2.9
Karakteristik inti KTP
A.Inti menggambarkan ground glass appearance (tanda panah). B.Karakeristik lain
inti KTP yaitu nuclear groove (tanda panah) (Livolsi, 2011; DeLellis et al., 2004)
Gambar 2.10
Mikroskopis KTP klasik
A. KTP dengan struktur papiler yang dominan. B. Fibrovascular core pada KTP
klasik (Gonzales et al., 2011)
A B
A B
27
Varian KTP lainnya yang sering yaitu KTPVF. Deskripsi histologik KTPVF
pertama kali diperkenalkan oleh Lindsay pada tahun 1960, diikuti oleh Chen dan
Rosai tahun 1977 dan Rosai et al tahun 1983. Sesuai dengan namanya, KTPFV
ditandai oleh gambaran inti KTP yang khas (inti jernih, groove dan pseudoinklusi)
disertai pola pertumbuhan folikuler. Pola pertumbuhan folikuler dapat dijumpai pada
KTP dengan beragam proporsi dan istilah KTPVF awalnya dipakai untuk karsinoma
invasif yang menunjukkan arsitektur histologis folikuler yang dominan. Ini berarti
bahwa KTPVF merupakan KTP dengan komponen folikuler yang dominan, dan
adanya proporsi minor dari komponen papiler masih dapat diterima. Namun
gambaran komponen papiler merupakan papiler abortif yaitu berupa tonjolan papiler
yang pendek tanpa tangkai (stalk) yang jelas, menyerupai komponen papiler pada
goiter hiperplastik (Koseoglu et al., 2006). Pada beberapa laporan, masih adanya
komponen papiler pada sekitar 20% atau bahkan 30% masih diterima sebagai KTPVF
(Kakudo et al., 2012).
28
Gambar 2.11
KTPVF yang encapsulated. KTP tersusun membentuk struktur folikuler pada
seluruh area tumor dengan inti menunjukkan karakteristik KTP (Gonzalez et al.,
2011).
KTPVF memiliki beberapa varian, diantaranya varian encapsulated,
nonencapsulated, dan difus (Gupta et al., 2012). KTPVF varian encapsulated
seringkali dikelirukan dengan adenoma folikular. Sehingga untuk menegaskan
diagnosis KTPFV pada kasus lesi tiroid berkapsel, LiVolsi and Baloch menetapkan
kriteria ditemukannya karakteristik sitologi KTP baik multifokal maupun difus pada
KTPFV yang berkapsel (Chen et al., 2012). Chan mengajukan kriteria yang lebih
ketat meliputi evaluasi gambaran mayor dan minor. Terdapat empat gambaran mayor,
antara lain: (1) inti oval hingga bulat, (2) inti yang tumpang tindih dengan polaritas
terganggu, (3) pola kromatin inti yang jernih atau pucat pada hampir seluruh lesi atau
gambaran groove yang jelas, dan (4) adanya psammoma bodies. Jika hanya ada satu
gambaran yang teridentifikasi, seluruh kriteria minor diperlukan untuk
29
menyimpulkan diagnosis. Kriteria minor tersebut mencakup: (1) adanya papil abortif,
(2) didominasi oleh folikel yang memanjang atau ireguler, (3) koloid berwarna gelap,
(4) adanya pseudoinklusi inti, dan (5) histiosit berinti banyak pada lumen folikel
(Chen et al., 2012). Selain itu, folikel neoplastik pada KTPVF umumnya dengan
bentuk yang ireguler dan ukuran yang lebih bervariasi daripada karsinoma maupun
adenoma folikuler (Baloch et al., 2011).
Gambaran psammoma bodies, kalsifikasi dan respon desmoplastik dapat
ditemukan pada KTPVF tapi cenderung lebih jarang jika dibandingkan dengan KTP
klasik. Psammoma bodies tampak sebagai “bayangan” papil yang telah mati
merupakan diferensiasi kalsifikasi distrofik terbentuk dari area infark fokal pada
ujung papil yang menarik kalsium. Infark yang terus menerus disertai deposit kalsium
menimbulkan lamelasi. Psammoma bodies biasanya tampak pada bagian sentral
tangkai, pada stroma tumor, atau pembuluh limfatik, namun tidak pernah berada di
dalam folikel neoplastik (koloid) (Livolsi 2011; De Lellis et al., 2004).
2.8 Sistem Stadium dan Pola Perluasan Karsinoma Tiroid Papiler
Klasifikasi stadium tumor tiroid sesuai sistem TNM yang didasarkan pada ukuran
tumor (T), penyebaran limfatik (N), dan metastasis jauh (M). Sistem TNM ini
disahkan oleh International Union Against Cancer (IUCC) dan American Joint
Commission on Cancer (AJCC). Berikut penjabaran klasifikasi sistem TNM
berdasarkan AJCC dalam menentukan stadium karsinoma tiroid (Rubin et al., 2012).
30
Tabel 2.5
Sistem TNM berdasarkan AJCC (Rubin et al., 2012)
Definisi TNM
Kelompok stadium
T1
Dimensi terbesar tumor ≤2
cm, terbatas pada tiroid
N0
Tanpa metastasis KGB
regional
Stadium I
T1 N0 M0
T2
Dimensi terbesar tumor >2cm tetapi ≤ 4 cm
N0
Tanpa metastasis KGB regional
Stadium II
T2N0M0
T3
Dimensi terbesar tumor >4
cm atau tumor dengan berbagai ukuran dengan
perluasan ekstratiroid
minimal (contoh: ke otot sternotiroid)
N1a
Metastasis ke level VI (KGB Pretrakea, paratrakea
dan Delphian/ Prelaringeal)
Stadium III
T3N0M0
T1N1aM0
T2N1aM0
T3N1aM0
T4a
Tumor berbagai ukuran melewati kapsel,
kejaringan subkutan, laring, trakea, esophagus
dan recurrent laryngeal
nerve.
N1b
Metastasis ke KGB
servikal unilateral, bilateral, kontralateral atau
superior mediastinum.
Stadium IVa
T4aN0M0
T4aN1aM0
T1N1bM0
T2N1bM0
T3N1bM0
T4N1bM0
T4b
Tumor menginvasi fascia
prevertebra atau menyelubungi arteri karotis
atau pembuluh darah
mediastinal
Stadium IVb
T4b berbagai N
M0
M1
Metastasis jauh
Stadum IVc Berbagai T
Berbagai N M1
31
Invasi kapsel maupun invasi intravasa merupakan faktor prediktif terjadinya
metastasis pada KTP. Selanjutnya adanya metastasis baik ke KGB maupun metastasis
jauh mempengaruhi tingginya angka kekambuhan dan mortalitas pada pasien KTP
(Gupta et al., 2012). Secara morfologi, KTPVF cenderung lebih sering berkapsel
dibandingkan KTP klasik sehingga gambaran invasi kapsel lebih sering dijumpai
pada kasus KTPVF, seperti halnya pada KTF maupun adenoma folikuler. Frekuensi
invasi kapsel pada KTPVF encapsulated lebih tinggi dibandingkan KTP klasik yaitu
65% berbanding 38% (Gupta et al., 2012; Chen et al., 2012). Pada KTPVF
encapsulated, kaskade perluasan tumor diawali dengan invasi tumor melewati
kapselnya, baik tanpa atau disertai adanya invasi vasa intra kapsuler maupun ekstra
kapsuler. Seiring dengan peningkatan ukuran tumor dan kemampuan invasifnya,
akhirnya terjadi kaskade lanjutan berupa perluasan tumor ke jaringan ekstra tiroid.
Namun proses lanjutan ini jarang terjadi pada KTPVF encapsulated, perluasan ekstra
tiroid lebih sering dijumpai pada KTPVF nonencapsulated dalam frekuensi yang
sebanding dengan KTP klasik (Chen et al., 2012; Chrisoulidou et al., 2011; Ghossein
et al., 2009). Penentuan kriteria adanya invasi kapsel pada KTPVF sama seperti
penentuan invasi kapsel pada KTF (Ghossein et al., 2009).
32
Gambar 2.12
Gambaran Skematik Interpretasi Invasi Kapsel (Ghossein et al., 2009)
Gambar 2.12 menunjukkan bahwa follicular neoplasm (oranye) yang dikelilingi oleh
kapsel fibrous (hijau). A dan B menggambarkan bagian tumor belum melewati
kapsel, C. Tumor secara total melewati kapsel, D. Tumor diliputi oleh kapsel fibrous
tipis, namun sudah meluas melampaui garis imajiner yang ditarik melalui kontur luar
kapsel, E. Satellite tumor nodule dengan arsitektur dan sitomorfologi yang sama
dengan tumor utama berada di luar kapsel, F. Folikel terletak tegak lurus pada kapsel
memberi kesan adanya invasi, G. Folikel terletak sejajar pada kapsel, H. Tumor
menyerupai gambaran mushroom, secara total melewati kapsel, I. Tumor menyerupai
gambaran mushroom, namun belum melampaui kapsel, J. Folikel neoplastik pada
kapsel fibrous disertai adanya sel limfosit dan siderofag, berkaitan dengan ruptur
kapsel karena tusukan jarum saat pemeriksaan FNAB sebelumnya. Yang digolongkan
33
telah mengalami invasi kapsel adalah C, D, E dan H sedangkan A, B, F, G, I dan J
belum dinyatakan mengalami invasi kapsel (Ghossein et al., 2009).
KTPVF merupakan varian KTP yang unik karena pola invasinya beragam, selain
menembus kapsel dan menimbulkan perluasan ke jaringan ekstratiroid, KTPVF dapat
meluas melalui vaskuler sehingga menimbulkan metastasis ke organ jauh dan dapat
pula serupa dengan KTP klasik yang melalui jalur limfonodi dan akhirnya
bermatastasis di KGB. Hal ini berkaitan dengan latar belakang molekuler KTPVF
yang dapat mengikuti pola molekuler KTP klasik maupun KTF (Chen et al., 2012;
Chrisoulidou et al., 2011; Ghossein et al., 2009).
Penentuan adanya invasi vaskuler pada KTPVF maupun KTP klasik berdasarkan
kriteria 1) adanya sel tumor pada ruang vaskuler, 2) adanya sel tumor yang menempel
di endotel vaskuler, 3) adanya sel tumor yang invasif melalui dinding pembuluh
darah dan endotel dan 4) adanya trombus yang menempel pada tumor intravaskuler
(Mete et al., 2011). Frekuensi invasi vaskuler pada KTPVF juga lebih tinggi daripada
KTP klasik yaitu 25% berbanding 5%. Pada berbagai penelitian, frekuensi terjadinya
metastasis jauh pada KTP berkisar antara 1,73-8,4% kasus yang umumnya terjadi
pada KTPVF. Dari hasil review 13 penelitian dilaporkan bahwa frekuensi metastasis
jauh tersering yaitu pada paru (49%), diikuti tulang (25%) dan pada tulang maupun
paru (5%). Sedangkan metastasis ke KGB dijumpai pada sekitar 35% keseluruhan
kasus KTP dan 70% diantaranya terjadi pada KTP klasik. Kecenderungan KTP klasik
untuk menimbulkan metastasis melalui KGB berkaitan juga dengan dasar biologi
34
molekulernya yaitu adanya perubahan genetik akibat mutasi BRAF dan tata ulang
RET/PTC (Chen et al., 2012; Chrisoulidou et al., 2011; Ghossein et al., 2009;
NCNN, 2012).
2.9 Penanganan Karsinoma Tiroid Papiler
Penanganan pasien dengan KTP secara umum terdiri dari empat komponen utama
diantaranya ekstirpasi pembedahan yang adekuat, ablasi RAI (Radioactive Iodine)
tambahan pada kasus tertentu, supresi TSH, dan surveillance. Keseluruhan strategi
terapi tergantung pada temuan preoperatif dan intraoperatif sesuai klasifikasi TNM
serta evaluasi postoperatif yang berkaitan dengan perangai biologis tumor (Cooper et
al., 2006; NCCN, 2012). Penelitan sebelumnya menunjukkan perangai KTPVF
varian encapsulated berbeda dengan KTP klasik, terkait tingkat mutasi BRAF V600E
dan metastasis KGB yang lebih rendah. Berbeda dengan KTPVF non encapsulated
yang perangai biologisnya menyerupai KTP klasik, dengan tingkat mutasi BRAF
V600E dan metastasis KGB yang secara signifikan lebih tinggi. Namun penelitian
terbaru menemukan bahwa perangai kedua varian KTPVF ini tidak menunjukkan
perbedaan yang bermakna, sehingga penentuan agresivitas kasus KTPVF dari
berbagai aspek sangat penting untuk ketegasan penentuan terapi karena kasus yang
agresif memerlukan tiroidektomi total, radical neck dissection (RND) dan ablasi RAI
(Constantine et al., 2007; Chang et al., 2006; Xing et al., 2005)
35
Pilihan terapi untuk reseksi tumor primer tiroid sering diperdebatkan, apakah
harus memilih lobektomi atau tiroidektomi total atau near-total (mendekati total).
Hingga saat ini masih diperdebatkan luas tiroidektomi yang harus dilakukan,
terutama untuk KTP yang berukuran kecil, intratiroid, berisiko rendah dan
berdiferensiasi baik. Beberapa memaparkan bahwa terapi lobektomi tidak
memberikan keuntungan harapan hidup dibandingkan tiroidektomi yang lebih luas
namun bisa mengurangi risiko terjadinya komplikasi cedera RLN (Recurrent
Laryngeal Nerve) dan hipoparatiroidisme permanen (Cooper et al., 2006; Bilimoria et
al., 2007)
Pendapat yang mendukung tiroidektomi total meliputi laporan bahwa tiroidektomi
yang lebih luas mengurangi risiko kekambuhan dan memberikan keuntungan untuk
harapan hidup dibandingkan lobektomi. Demikian pula di tangan ahli bedah endokrin
yang berpengalaman, tingkat komplikasi antara tiroidektomi total sebanding dengan
lobektomi. KTP bersifat multifokal pada 80% kasus dan bilateral pada 60% kasus,
dan pilihan untuk menghilangkan seluruh kelenjar tiroid memfasilitasi kegunaan RAI
postoperatif untuk menangani sisa tumor yang tampak secara mikroskopik atau lesi
metastatik, serta mendukung kegunaan tiroglobulin (Tg) postoperatif sebagai marker
sensitif dalam mengetahui kekambuhan. Pedoman konsensus menganjurkan
tiroidektomi total atau yang mendekati total sebagai pilihan terapi awal pada pasien
KTP dengan indikasi absolut meliputi riwayat paparan radiasi, kanker tiroid familial,
tumor ukuran lebih dari 4 cm, adanya perluasan ekstratiroid, adanya metastasis
36
limfonodi atau metastasis jauh, atau varian histologis KTP bersifat agresif (Toniato et
al., 2008; Haigh et al., 2005)
Metastasis KGB pada kasus KTP sering ditemukan, melalui tindakan diseksi
leher propilaktik didapatkan prevalensi 33-63% untuk metastasis KGB leher sentral
(pre-atau paratrakea/ level VI), dan prevalensi 57-64% untuk metastasis KGB leher
lateral (level II, III, dan IV) yang sebelumnya tidak terdeteksi melalui pemeriksaan
ultrasonografi preoperatif. Diseksi limfonodi yang berorientasi pada terapeutik
kompartemen diindikasikan bagi metastasis limfonodi servikal yang sudah diketahui.
Meskipun jumlah ini tinggi, namun arti pentingnya metastasis limfonodi masih belum
jelas karena beberapa studi menunjukkan bahwa metastasis limfonodi tidak
berpengaruh pada keseluruhan harapan hidup, terutama pada pasien yang berusia
dibawah 45 tahun (Shindo et al., 2006; Ito et al., 2006; Pereira et al., 2005)
Kegunaan limfadenektomi propilaktik dalam terapi kasus KTP masih kontroversi.
Kelompok pendukung RND berpendapat bahwa metastasis limfonodi regional sering
terjadi dan berkaitan dengan tingginya tingkat kekambuhan dan kematian. Sedangkan
kelompok yang menetang berpendapat bahwa metastasis limfonodi tidak berpengaruh
pada keseluruhan harapan hidup, dan prosedur ini justru meningkatkan risiko
komplikasi dengan dilaporkannya 2-7% kasus paralisis vocal cord sementara, 14-
60% hipoparatiroidisme sementara dan 2-5% hipoparatiroidisme permanen. American
Thyroid Association Guidelines (ATA) 2009 memberi rekomendasi untuk tindakan
elektif (propilaksis) diseksi kompartemen sentral leher pada pasien dengan tumor
37
primer bersifat lanjut (T3 atau T4) meskipun secara klinis tidak ditemukan
keterlibatan limfonodi sentral leher (Ito et al., 2012). Disisi lainnya, pedoman NCCN
(National Comprehensive Cancer Network) tidak menganjurkan tindakan diseksi
leher sentral rutin, kecuali jika pada pemeriksaan palpasi atau biopsi limfonodi positif
menunjukkan lesi metastasis (Ito et al., 2012; Pereira et al., 2005).
Komponen kedua pada strategi penanganan global pasien KTP adalah ablasi RAI
yang diberikan pada 4-12 minggu setelah tindakan pembedahan, bertujuan untuk
menghancurkan sisa jaringan tiroid setelah tiroidektomi dan menangani lesi
metastasis yang masih tersembunyi ataupun telah diketahui. Kontroversi tindakan
ablasi RAI timbul karena meskipun dapat mengurangi tingkat kekambuhan dan
mortalitas, beberapa studi justru menunjukkan tidak ada keuntungan, terutama bagi
pasien yang masuk dalam kelompok risiko rendah. Baik pedoman ATA maupun
NCCN menganjurkan ablasi RAI untuk seluruh pasien KTP kecuali pasien stadium 1
yang memiliki risiko kekambuhan sangat rendah (pasien dengan diferensiasi baik,
unifokal, tumor berukuran lebih kecil dari 1 cm, tanpa perluasan ekstratirod atau
invasi vaskuler, dan tanpa metastasis limfonodi maupun jauh (Sawka et al., 2004).
Komponen ketiga untuk strategi penanganan global kasus KTP adalah pemberian
hormon tiroid dosis suprafisiologis dalam bentuk levotiroksin (LT4) dengan harapan
dapat menekan TSH yang diketahui menjadi stimulator proliferasi sel tiroid.
Penelitian retrospektif maupun prospektif menunjukkan bahwa pasien dengan terapi
LT4 mengalami penurunan risiko efek samping klinis mayor terutama pada kelompok
38
pasien risiko tinggi. Pedoman ATA menganjurkan penekanan TSH dibawah 0.1
mIU/mL untuk kelompok risiko tinggi dan antara 0.1-0.5 mIU/mL untuk kelompok
risiko rendah (McGriff et al., 2004).
Komponen terakhir pada strategi penanganan global kasus KTP adalah surveilens.
Lonjakan terjadinya tumor dipantau secara periodik oleh klinisi yang berpengalaman.
Pengukuran TSH, Tg dan anti-TG serum, USG servikal dan scan RAI sensitif untuk
adanya lesi sisa atau kekambuhan (Cooper et al., 2006).
Terapi terbaru untuk pasien dengan KTP lanjut dan metastatik meliputi pemberian
agen rediferensiasi, dimana agen tersebut memiliki target pada jalur RAS, BRAF,
VEGF dan reseptornya, jalur reseptor EGF dan jalur angiogenik lain dengan agen
seperti thalidomide dan proteasome (Xing et al., 2005; Ito et al., 2007).
2.10 Struktur, Jenis dan Fungsi Umum Matriks Metalloproteinase (MMP)
MMP merupakan famili endopeptida yang tergantung pada zinc. MMP sering disebut
sebagai kelompok protease metzincin karena selalu menyediakan corak pengikat zinc
yang tersimpan ada bagian katalitik aktifnya. MMP pertama kali ditemukan oleh
Jerome Gross dan Charles Lapiere pada tahun 1962 ketika mengetahui adnya
aktivitas enzimatik selama metamorfosis ekor kecebong. Mereka menemukan bahwa
triple helix kolagen didegradasi jika ekor kecebong ditempatkan pada matriks
kolagen kecebong yang bermetamorfosis (Ansari et al., 2013; Loffek et al., 2011).
39
MMP dilepaskan sebagai proenzim yang tidak aktif, tetapi selanjutnya diaktifkan
oleh berbagai faktor yang dikendalikan oleh TIMP (tissue inhibitors of matrix
metalloproteinases). Kelompok/ famili TIMP dibentuk oleh empat enzim. Kondisi
patologis akan timbul jika terjadi ketidakseimbangan tingkat MMP dan TIMP.
Berbagai penelitian juga melaporkan bahwa peningkatan ekspresi MMP memicu
berbagai penyakit inflamasi, keganasan dan degeneratif. Disinilah pentingnya
aktivitas penghambat MMP dalam terapi (Ansari et al., 2013). Seperti yang tampak
pada gambar 2.13, MMP memiliki tiga domain utama, yaitu:
1) Pro-peptida yang berperan menjaga enzim dalam bentuk tidak aktif. Domain
ini mengandung “Cystein switch” yakni residu cystein unik dan selalu terjaga,
yang berinteraksi dengan zinc pada bagian aktif. Saat aktivasi enzim, bagian
ini akan dipecah secara proteolitik oleh furin secara intraseluler atau MMP
lainnya dan protease serin secara ekstraseluler.
2) Domain katalitik yang menjadi penanda struktural corak pengikat zinc. Ion
Zn2+, diikat oleh tiga residu histidin membentuk area aktif. Area aktif ini
berjalan secara horizontal melewati molekul sebagai celah dangkal dan
berikatan dengan substrat.
3) Bagian penghubung (hinge region) merupakan sebuah jembatan lentur atau
bagian penghubung yang terbuat dari 75 rantai asam amino berfungsi untuk
menghubungkan domain katalitik dengan domain terminal-C. Bagian ini
sangat penting untuk menjaga stabilitas enzim.
40
4) Domain terminal-C yang menyerupai hemopexin merupakan domain yang
rangkaiannya menyerupai protein serum hemopexin. Rantai polipeptida
domain ini tersusun dalam empat lembaran β yang simetris. Permukaan datar
yang disediakan oleh struktur ini dipercaya terlibat dalam interaksi antar
protein dan merupakan penentu spesifisitas substrat, contohnya: TIMP
berinteraksi pada area ini.
Gambar 2.13
Struktur Matriks Metaloproteinase (MMP) (Ansari et al., 2013)
Kemampuan MMP dalam menghancurkan berbagai komponen matriks
ekstraseluler (ECM) menunjukkan bahwa berperan utama dalam remodeling ECM
yang signifikan selama perkembangan embryogenik karena remodeling ECM
merupakan bagian penting dalam pertumbuhan dan morfogenesis jaringan. Ini juga
didukung oleh penelitian terbaru yang menunjukkan peranan penting MMP sebagai
jaringan sinyal pengatur komponen ekstraseluler yang mempengaruhi kondisi seluler
41
(Loffek et al., 2011). Secara sistematis, beberapa fungsi seluler MMP selama
perkembangan dan fisiologis normal, yaitu (sesuai gambar 2.15) (Ansari et al., 2013):
1) Membantu migrasi sel melalui degradasi molekul ECM
2) Mengubah perangai seluler dengan mengubah lingkungan mikro ECM
3) Membantu aktivitas molekul aktif secara biologis dengan pemecahan
langsung, pelepasan dari simpanan, atau memodulasi aktivitas
penghambatnya.
Gambar 2.14
Fungsi seluler MMP selama perkembangan dan fisiologis normal.
Berdasarkan spesifisitas MMP terhadap komponen ECM, MMP dibagi menjadi
kelompok kolagenase, gelatinase, stromelysin dan matrilysin. Sedangkan diantara
42
delapan kelas struktural MMP, 5 disekresikan dan 3 lainnya merupakan MMP tipe
membran (MT-MMP) (Ansari et al., 2013).
Tabel 2.6
Jenis Matriks Metaloproteinase (Ansari et al., 2013)
Jenis MMP Kelas struktural Nama umum MMP-1 Simple hemopexin domain Kolagenase-1, interstitial Kolagenase, fibroblast
kolagenase, tissue kolagenase
MMP-2 Gelatin-binding Gelatinase A, 72-kDa gelatinase, 72-kDa typeIV
kolagenase, neutrophil gelatinase
MMP-3 Simple hemopexin domain Stromelysin-1, transin-1, proteoglikanase, protein
pengaktivasi prokolagenase
MMP-7 Minimal domain Matrilysin, matrin, PUMP1, small uterine
metalloproteinase
MMP-8 Simple hemopexin domain Kolagenase-2, kolagenase neutrophil, kolagenase
PMN, kolagenase granulosit
MMP-9 Gelatin-binding Gelatinase B, gelatinase 92-kDa, kolagenase 92-
kDa tipe IV
MMP-10 Simple hemopexin domain Stromelysin-2, transin-2 MMP-11 Furin-activated
dan Stromelysin-3
MMP-12 Simple hemopexin domain Metalloelastase, elastase makrofag, metalloelastase
makrofag
MMP-13 Simple hemopexin domain Kolagenase-3
MMP-14 Transmembrane MT1-MMP, MT-MMP1
MMP-15 Transmembrane MT2-MMP, MT-MMP2
MMP-16 Transmembrane MT3-MMP, MT-MMP3
MMP-17 GPI-linked MT4-MMP, MT-MMP4
MMP-18 Simple hemopexin domain Kolagenase-4 (Xenopus)
MMP-19 Simple hemopexin domain RASI-1, MMP-18
MMP-20 Simple hemopexin domain Enamelysin
MMP-21 Vitronectin-like insert Homolog dari Xenopus XMMP
MMP-22 Simple hemopexin domain CMMP (pada ayam)
MMP-23 Type II transmembrane Cysteine array MMP (CA-MMP), femalysin,
MIFR,MMP-21/MMP-22
MMP-24 Transmembrane MT5-MMP, MT-MMP5
MMP-25 GPI-linked MT6-MMP, MT-MMP6, leukolysin
MMP-26 Minimal domain Endometase, matrilysin-2
MMP-27 Simple hemopexin domain
MMP-28 Furin-activated and secreted Epilysin
Tanpa nama Simple hemopexin domain Mcol-A (pada tikus)
Tanpa nama Simple hemopexin domain Mcol-B (pada tikus)
Tanpa nama Gelatin-binding Gelatinase 75-kDa (pada ayam)
43
Dalam proses keganasan, peranan MMP juga menyerupai yang terjadi dalam
proses fisiologis namun terjadi ketidakseimbangan dengan aktivitas penghambatnya.
Terjadi degradasi komponen ECM pada membran basalis dan jaringan ikat interstisial
yang tersusun atas kolagen, glikoprotein dan proteoglikan. Suatu karsinoma pertama-
tama harus menembus membran basalis dibawahnya, kemudian melintasi jaringan
ikat, dan secara cepat mencapai sirkulasi dengan cara menembus membran basalis
pembuluh darah. Proses ini berulang lagi jika emboli sel tumor mengalami
ekstravasasi ke tempat jauh. Invasi melalui ECM mengawali kaskade metastasis dan
merupakan proses aktif yang melibatkan beberapa tahap, diantaranya perubahan
interaksi antara sel tumor dengan sel, degradasi ECM, perlekatan ke komponen
terbaru ECM dan migrasi sel tumor (Kumar et al., 2010).
MMP terlibat dalam tahap kedua proses invasi yaitu degradasi lokal membran
basalis dan jaringan ikat interstisial. Sekresi MMP tersebut dapat berasal langsung
dari sel tumor atau dari induksi terhadap sel stroma (seperti fibroblast dan sel
inflamasi). Protease lain yang juga disekresikan yaitu cathepsin D dan urokinase
plasminogen activator. MMP mengatur invasi tumor tidak hanya dengan cara
mengubah komponen yang tidak larut pada membran basalis dan matriks interstisial,
tetapi juga dengan pelepasan growth factor yang disimpan ECM (Kumar et al., 2010;
Bouchet et al., 2014).
44
2.11 Fungsi Matriks Metaloproteinase 9 (MMP-9/Gelatinase)
Diantara seluruh MMP, salah satu kelompok gelatinase yaitu MMP-9 (gelatinase B)
mendapat perhatian pada beberapa penelitian dalam memahami sifat invasif dan
metastatik tumor terkait kemampuannya dalam mendegradasi kolagen IV, komponen
utama dari membran basalis epitel dan vaskuler. Hubungan antara komponen radang,
stroma dan tumor mempengaruhi aktivasi dan produksi MMP-9/ gelatinase B. Gen
MMP-9/ gelatinase B berlokasi pada kromosom 20q11.2-q13.1, terdiri dari 7.654
basa dan ditranskripsikan sebagai 2.4 kb mRNA tunggal (Bouchet et al., 2014;
Marecko et al., 2014).
Protein MMP-9 merupakan enzim metallo-multidomain, dengan catalytic site
tersusun atas domain pengikat logam yang dipisahkan dari active site oleh ulangan
tiga fibronektin yang memfasilitasi degradasi substrat besar seperti elastin dan
penghancuran kolagen. Dalam regio ini, asam amino Asp309, Asn319, Asp232,
Tyr320 dan Arg3076 penting untuk pengikat gelatin. Catalytic site tetap
dipertahankan dalam bentuk tidak aktif oleh amino-terminal pro-peptide PRCGXPD,
dengan koordinasi cysteine bersama katalitik Zn2+. Ujung terminal COOH dari
MMP-9 mengandung domain hemopexin yang mengatur ikatan dengan substrat,
berinteraksi dengan inhibitor dan membantu ikatan ke permukaan sel. Domain O-
glycosylated sentral memberikan fleksibilitas molekuler, mengatur spesifisitas
substrat MMP-9 invasi yang bergantung MMP-9, interaksi dengan TIMP dan
lokalisasi permukaan sel. Domain ini membantu pergerakan MMP-9 sepanjang
45
substrat makromolekuler dan melepaskan ikatan kolagen sebelum dipecahkan oleh
enzim lainnya (Farina et al., 2014; Loffek et al., 2011).
Keterangan:
Gambar 2.15
Struktur MMP-9 (Gelatinase B) (Loffek et al., 2011)
MMP-9 dihasilkan oleh sel tubuh manusia, seperti sel fibroblast stroma, sel
endotelial, sel polimorfonuklear (PMN), keratinosit, makrofag dan beberapa sel
epitel. Aktivitas enzimatik MMP-9 dihambat oleh inhibitor protease sistemik α2-
makrogloblin, anggota famili TIMP dan antagonis terhadap domain hemopexinnya
sendiri. MMP-9 mendapat perhatian khusus karena ekspresi basalnya rendah secara
normal, sedangkan pada kondisi kanker MMP-9 terekspresi kuat akibat respon
terhadap berbagai faktor pertumbuhan dan sitokin. Melalui penelitian eksperimental
terhadap tikus dengan defisiensi MMP-9 menunjukkan kegagalan metastasis dan
pertumbuhan tumor (Farina et al., 2014).
Peranan proonkogenik MMP-9 telah dilaporkan, diantaranya berkaitan dengan
transformasi neoplastik, inisiasi dan promosi tumor dan instabilitas genetik. MMP-9
46
dapat menempati inti sel, meskipun memiliki sinyal lokalisasi inti klasik yang rendah
dan aktivitas gelatinase inti menyatu dengan peningkatan fragmentasi DNA.
Gelatinase inti ini mendegradasi matriks protein inti yaitu PARP (poly-ADP-ribose-
polymerase), menghindarkannya dari proses perbaikan DNA (Farina et al., 2014).
Gambar 2.16
Peranan MMP-9 yang bebas TIMP yang berasal dari sel radang PMN sel tumor
maupun stroma dalam inisiasi tumor dan promosi instabilitas genetik. Melalui
degradasi matriks ekstraseluler (ECM), dan aktivitas kemokin, sitokin dan growth
factor (Farina et al., 2014).
Peningkatan aktivitas MMP-9 yang ditunjang oleh PMN neutrofil selanjutnya
juga meningkatkan penarikan neutrofil melalui degradasi yang dimediasi MMP-9 dan
superaktivasi IL-8, meningkatkan istabilitas genetik. Selanjutnya MMP-9 terlibat
dalam ekspansi klonal yang merupakan tahap penting pada progresi tumor dengan
melibatkan keseimbangan antara proliferasi, apoptosis dan angiogenesis. Transisi
epitelial menjadi mesenkimal (EMT) merupakan kemampuan perubahan sel epitel
yang awalnya tidak dapat bergerak menjadi sel progenitor mesenkimal yang dapat
47
bergerak. Mekanisme ini penting untuk perkembangan (tipe 1), proses penyembuhan
normal atau fibrosis patologis (tipe 2) dan transformasi metastatik sel kanker (tipe 3).
EMT tipe 3 sangat fundamental pada progresi tumor untuk bermetastasis, dan baik sel
kanker yang mengalami reaktivasi ataupun dediferensiasi atau teraktivasi ini akan
terinduksi menjadi fenotip yang invasif dan memiliki kemampuan motilitas. MMP-9
merupakan protein penting yang berkaitan dan bahkan penyebab EMT (Antonietta et
al, 2014).
Gambar 2.17
Transisi epitelial menjadi mesenkimal (EMT) yang dipicu MMP-9 (Farina et al.,
2014)
Neovaskularisasi tumor merupakan proses penting untuk ekspansi tumor primer,
progresi metastatik dan pertumbuhan metastatik, terjadi melalui beberapa proses
meliputi permulaan angiogenesis, vaskulogenesis, gabungan intersusepsi dan/atau
menyerupai vaskuler. Tidak seperti pembuluh darah normal, pembuluh darah pada
tumor bersifat abnormal dan imatur. MMP-9/ gelatinase B merupakan molekul
proangiogenik dan memicu aktivasi angiogenik pada pembuluh darah tua dengan cara
48
mengatur proliferasi perisit, apoptosis dan penarikan perisit selama angiogenesis serta
memobilisasi perekrutan prekursor angiogenik sumsum tulang ke stroma tumor untuk
meningkatkan proses angiogenik dan vaskulogenik tumor. MMP-9 juga memicu
aktivasi angiogenik dengan memobilisasi mitogen angiogenik seperti FGF and
VEGF. Selain itu hipoksia karena tumor merupakan stimulus angiogenesis dan
berperan meningkatkan ekspresi MMP-9 vaskuler (Farina et al., 2014).
Gambar 2.18
Peranan MMP-9 bebas TIMP dari sel radang PMN, MMP-9 tumor/ stroma onkogen
dan hipoksia dalam mengaktifkan angiogenesis (Farina et al., 2014)
Sedangkan keterlibatan MMP-9 dengan proses metastasis merupakan kolaborasi
proses ekspansi, EMT dan angiogenesis. Khusus mengenai invasi ke limfonodi
dikaitkan dengan keterlibatan interaksi antara kemokin dengan reseptor kemokin
49
CCR7 yang sebelumnya berfungsi meningkatkan ekspresi MMP-9 (Farina et al.,
2014).
Gambar 2.19
Kaitan MMP-9 dengan kemampuan metastasis tumor (Farina et al., 2014)
2.12 Peranan Matriks Metaloproteinase 9 (MMP-9)/Gelatinase B pada
Karsinoma Tiroid Papiler
Berbagai landasan teoritis telah memaparkan bahwa MMP-9 mempengaruhi sifat
invasif, kemampuan progresi dan kemampuan bermetastasis tumor sehingga dapat
menjadi acuan bahwa MMP-9 layak menjadi salah satu marka atau penanda
agresivitas tumor. Sebuah penelitian menemukan bahwa terdapat hubungan yang
bermakna antara ekspresi MMP-9 dengan stadium IUCC dan metastasis ke
limfonodi. Penelitian lainnya membuktikan perbedaan ekspresi MMP-9 yang sangat
bermakna antara karsinoma tiroid, adenoma tiroid dan goiter multinoduler. Hal ini
50
menunjukkan bahwa MMP-9 memiliki peranan kunci dalam transformasi onkogenik
tumor tiroid. Adapula penelitian yang menyebutkan bahwa ekspresi MMP-9 secara
bermakna berkaitan dengan ukuran tumor selain stadium UICC dan adanya
metastasis ke limfonodi maupun metastasis jauh. Namun ekspresi MMP-9 tidak
berkorelasi dengan jenis kelamin dan usia pasien. Hasil penelitian ini mendukung
teori mengenai kaitan MMP-9 dengan progresi, kemampuan invasi dan metastasis
tumor. Temuan ini kemudian menjadi landasan bahwa tingginya ekspresi MMP-9
dapat menjadi marker diagnostik yang berguna dan mungkin juga merupakan target
yang potensial pada terapi karsinoma tiroid (Marecko et al., 2008).
Bahkan temuan terbaru membuktikan BRAFV600E yang merupakan marka spesifik
penentu agresivitas KTP terlebih dahulu perlu menginduksi MMP untuk memunculan
sifat invasif dan kemampuan metastasis tumor. Hal ini tampak setelah dilakukan
pemeriksaan imunohistokimia pada enam puluh kasus KTP klasik baik antibodi anti
MMP-2 maupun MMP-9, didapatkan MMP-2 terdeteksi pada 32 spesimen (53.3%),
sedangkan MMP-9 pada 52 spesimen (86.7%). Pada analisis univariat, terdapat
korelasi yang signifikan antara positivitas BRAFV600E dengan hasil IHK MMP-2 atau
MMP-9 atau keduanya (PZ 0.028). Adanya ekspresi MMP-2 maupun MMP-9 secara
signifikan juga berkaitan dengan perluasan ekstratiroid (PZ 0.030). Temuan ini
menegaskan bahwa ekspresi MMP-9 merupakan marka atau penanda yang sinergis
dengan ekspresi BRAFV600E Akhirnya disimpulkan bahwa MMP merupakan mediator
efek BRAF pada sifat invasif tumor (Frasca et al., 2008).
51
Diketahui pula bahwa P53 yang merupakan guardian of genome dapat mengatur
ekspresi MMP secara kompleks, dengan memicu peningkatan ekspresi MMP-2 dan
DDR1 namun menghambat ekspresi MMP-1 dan MMP-9. Sehingga adanya mutasi
P53 secara tidak langsung akan meningkatkan ekspresi MMP-9. Mutasi P53
berkaitan dengan sifat agresivitas tumor dan penanda prognosis yang buruk.
Mengingat keterkaitan mutasi P53 dengan peningkatan ekspresi MMP-9 maka
ekspresi MMP-9 merupakan marker yang relevan dalam menentukan agresivitas
tumor, khususnya pada KTP (Powell et al., 2014).
Penelitian terbaru lainnya membuktikan bahwa imunoekspresi MMP-9 aktif
berkorelasi positif dengan usia pasien, adanya metastasis ke limfonodi, adanya invasi
ekstratiroid dan derajat infiltrasi tumor. Penelitian ini agak berbeda dengan penelitian
sebelumnya karena menemukan bahwa ukuran tumor tidak terkait dengan tingkat
ekspresi MMP-9 aktif. Hasil yang masih serupa yaitu memaparkan bahwa jenis
kelamin juga tidak berhubungan dengan ekspresi MMP-9. Temuan ini kembali
memaparkan bahwa MMP-9 bersifat aktif pada sel tumor dan hal ini mempengaruhi
perangai agresif pada KTP (Ansari et al., 2013).
Sel yang mengekspresikan MMP-9 akan tampak berwarna coklat pada sitoplasma
sel epitel ganas maupun stroma. Penilaian ekspresi MMP-9 dibuat berdasarkan
analisis persentase sel tumor yang positif dan intensitas pewarnaannya (Meng et al.,
2012; Marecko et al., 2014).
52
Gambar 2.20
Pulasan MMP-9 pada KTP. A.Hasil pulasan IHK MMP-9 total pada kasus KTP
encapsulated yang menunjukkan gambaran difus sedang. B. Hasil IHK MMP-9 aktif
dengan gambaran negatif pada sampel yang sama. C. Pulasan MMP-9 yang positif
kuat dan difus pada kasus KTP dengan invasi ekstratiroid. D. Pulasan MMP-9 yang
juga positif kuat pada KTP dengan invasi ekstratiroid (Marecko et al., 2014).